研究背景
結(jié)直腸癌(CRC)是全球第三大常見(jiàn)癌癥,盡管免疫療法的進(jìn)步給癌癥治療帶來(lái)了革命性變化,但其在CRC中的有效性仍然有限。已有研究表明APC驅(qū)動(dòng)的多克隆性顯著增強(qiáng)了致瘤潛力,但APC突變?cè)诮閷?dǎo)免疫逃避中的作用仍知之甚少。近期南方醫(yī)科大學(xué)周偉杰團(tuán)隊(duì)在Cell Research (IF 25.9)上發(fā)表文章“Targeting PTPN13 with 11-amino-acid peptides of C-terminal APC prevents immune evasion of colorectal cancer”,揭示了一種以前未知的APC/PTPN13/STAT1依賴的腫瘤免疫抑制機(jī)制。
 維真助力 - 腺病毒·
維真助力 - 腺病毒·
病毒產(chǎn)品 Ad-Cre、Ad-GFP
實(shí)驗(yàn)細(xì)胞 Apcfl/fl /LSL-KrasG12D/p53fl/fl小鼠腸道類器官
結(jié)果展示
1. APC缺失損害IFNγ-STAT1-IRF1信號(hào)傳導(dǎo)并抑制抗原呈遞
作者發(fā)現(xiàn)APC缺失損害CD8+T細(xì)胞浸潤(rùn)誘導(dǎo)CRC的免疫逃避,提高CRC模型對(duì)免疫檢查點(diǎn)封鎖的抵抗力,且PTPN13介導(dǎo)APC缺失驅(qū)動(dòng)的CRC免疫逃避。作者通過(guò)RNA-seq研究了CRC中APC缺失誘導(dǎo)的免疫逃避所涉及的信號(hào)通路,發(fā)現(xiàn)APC敲低與II型干擾素和JAK-STAT信號(hào)通路反應(yīng)的抑制有關(guān),Apc敲低顯著降低了IFNγ誘導(dǎo)的STAT1磷酸化和IRF1上調(diào),而JAK1磷酸化保持不受影響,表明APC在該通路中在JAK1下游和STAT1上游發(fā)揮作用。作者還探究了APC缺失對(duì)抗原呈遞和CD8+T細(xì)胞功能的影響,發(fā)現(xiàn)Apc敲低后抗原呈遞受損,抗原特異性CD8+T細(xì)胞顯著減少。機(jī)制研究發(fā)現(xiàn)Stat1R274Q和Irf1的過(guò)度表達(dá)顯著抑制WT Balb/c小鼠皮下移植的CT26-shApc細(xì)胞的生長(zhǎng),并增強(qiáng)CD8+T細(xì)胞浸潤(rùn),這些結(jié)果表明,APC丟失通過(guò)抑制STAT1/IRF1信號(hào)傳導(dǎo)促進(jìn)免疫逃避,而恢復(fù)該通路可有效抵消腫瘤免疫抵抗。
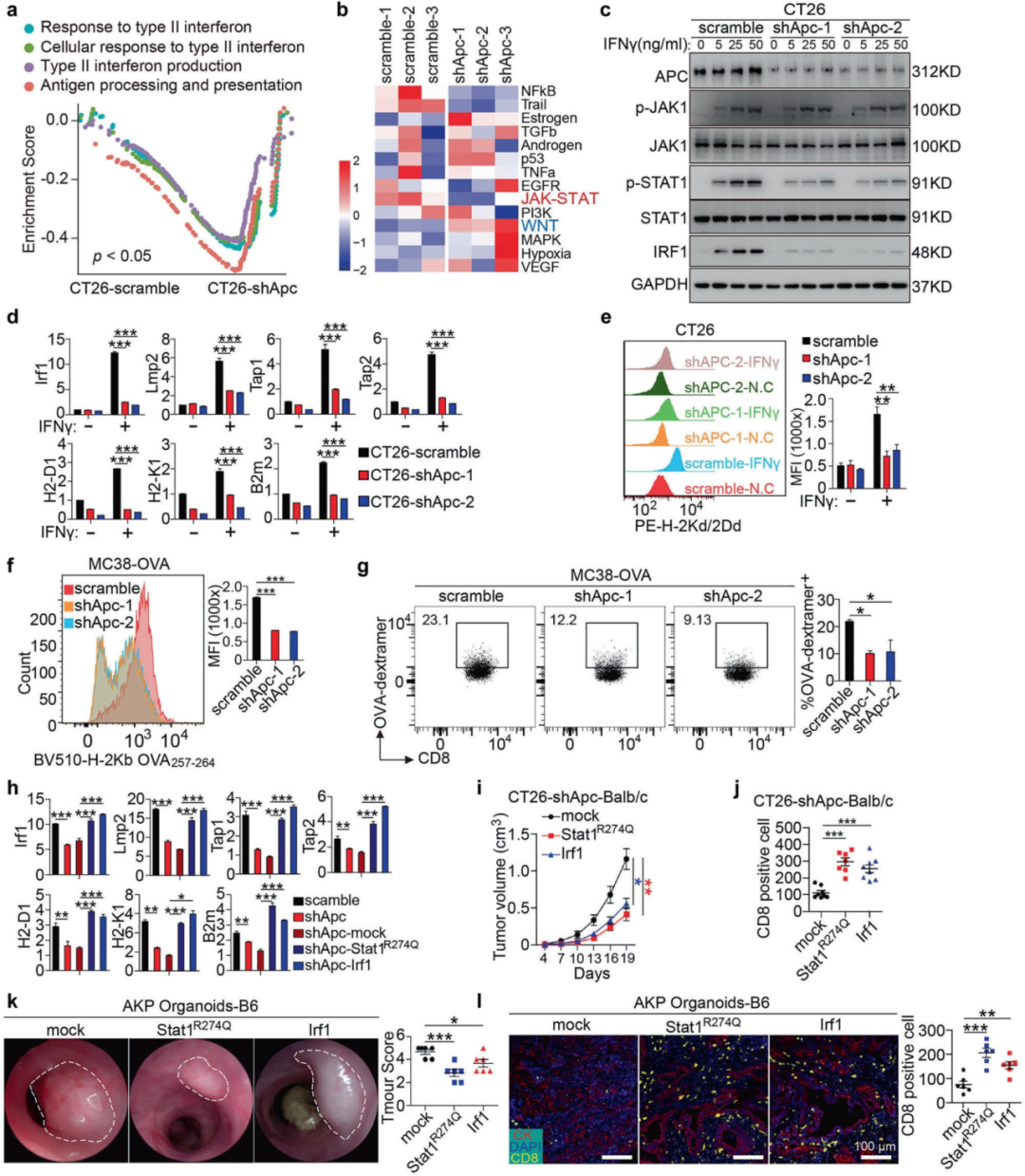
圖1 APC缺失使IFNγ-STAT1-IRF1-MHC-I抗原呈遞信號(hào)失活
2. PTPN13與STAT1的直接相互作用和去磷酸化
已有研究表明PTPN13參與了STAT家族成員的去磷酸化,作者通過(guò)免疫共沉淀確認(rèn)STAT1–PTPN13存在相互作用,并證實(shí)STAT1直接結(jié)合到PTPN13的PDZ2a結(jié)構(gòu)域。體外PTPase測(cè)定表明STAT1是PTPN13的直接底物,PTPN13使STAT1去磷酸化。免疫共沉淀還表明APC-PTPN13存在相互作用,并且IFNγ刺激增強(qiáng)了該復(fù)合物的形成,因此作者假設(shè)APC阻斷STAT1-PTPN13相互作用,這一觀點(diǎn)在Apc敲除細(xì)胞中增強(qiáng)的PTPN13-STAT1相互作用所證實(shí)。進(jìn)一步研究發(fā)現(xiàn)APC的C端纈氨酸對(duì)于其與PTPN13的相互作用至關(guān)重要,并且這種相互作用對(duì)于調(diào)節(jié)CRC的免疫逃避至關(guān)重要。
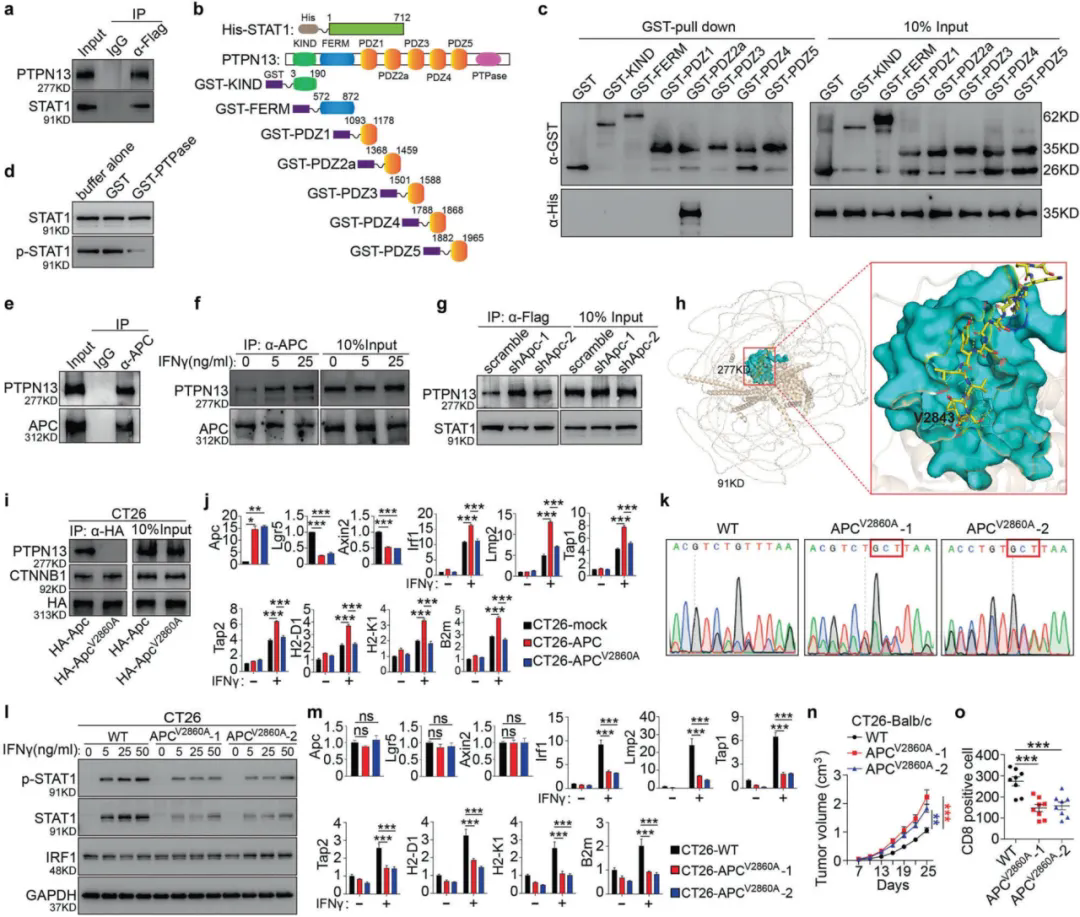
圖2 APC的C端纈氨酸對(duì)于CRC中PTPN13的結(jié)合和免疫逃避至關(guān)重要
3. APC11抑制腫瘤生長(zhǎng)并增強(qiáng)抗PD1治療的反應(yīng)
作者發(fā)現(xiàn)APC11(APC的C端最后11個(gè)氨基酸)有效阻斷PTPN13/STAT1相互作用,恢復(fù)APC缺失引起的IFNγ-STAT1-IRF1-MHC-I抗原呈遞途徑失活。TAT綴合APC11肽(TAT-APC11)治療顯著提高了腫瘤小鼠的生存率。為了提高溶解度和穩(wěn)定性,作者將TAT-APC11與PEG綴合,評(píng)估了PEG-TAT-APC11的治療潛力,發(fā)現(xiàn)在腫瘤小鼠模型中,抗PD1單一療法并未提高生存率,而PEGTAT-APC11則延長(zhǎng)了生存率。PEG-TAT-APC11和抗PD1的組合進(jìn)一步改善了生存結(jié)果。為了進(jìn)一步優(yōu)化腫瘤靶向,作者開(kāi)發(fā)了基于APC11的納米顆粒(NP-APC11)并與腫瘤穿透肽iRGD34綴合以提高選擇性,發(fā)現(xiàn)NP-APC11顯著抑制腫瘤生長(zhǎng)并增加CD8+T細(xì)胞浸潤(rùn)。作者還評(píng)估了NP-APC11與抗PD1聯(lián)合治療腫瘤的療效,發(fā)現(xiàn)NP-APC11顯著抑制腫瘤生長(zhǎng),NP-APC11與抗PD1聯(lián)合治療比抗PD1單一療法具有更有效的治療效果。這些結(jié)果證明了APC11單獨(dú)或與抗PD1組合作為治療APC缺陷的CRC的有效治療策略的潛力。
圖3 APC11抑制腫瘤生長(zhǎng)并增強(qiáng)抗PD1治療的反應(yīng)
實(shí)驗(yàn)結(jié)論
本研究發(fā)現(xiàn)PTPN13是APC驅(qū)動(dòng)的免疫逃避的關(guān)鍵介質(zhì),在機(jī)制上APC直接與PTPN13相互作用,阻斷其與STAT1的相互作用,進(jìn)而抑制腫瘤進(jìn)展。APC11可以有效阻斷PTPN13-STAT1相互作用,恢復(fù)STAT1磷酸化并重新激活針對(duì)腫瘤的免疫反應(yīng),APC11與抗PD1療法結(jié)合時(shí),觀察到更好的腫瘤抑制效果,這為開(kāi)發(fā)CRC患者抗腫瘤藥物提供了新的思路。
