2024年5月,中南大學(xué)湘雅二醫(yī)院金鑫聯(lián)合華中科技大學(xué)同濟醫(yī)學(xué)院附屬協(xié)和醫(yī)院江科/唐露團隊在Nature Communications上在線發(fā)表了文章“ZDHHC20-mediated S-palmitoylation of YTHDF3 stabilizes MYC mRNA to promote pancreatic cancer progression”。研究發(fā)現(xiàn)KRAS上調(diào)的蛋白ZDHHC20在胰腺癌中異常過表達,預(yù)示著不良預(yù)后;ZDHHC20通過Cys474的棕櫚酰化抑制YTHDF3的溶酶體定位和降解,從而通過m6A修飾進一步調(diào)節(jié)MYC mRNA的穩(wěn)定性,促進癌癥細胞的惡性表型。本研究確定了ZDHHC20-YTHDF3-MYC軸以棕櫚酰化依賴的方式促進胰腺癌進展的機制。

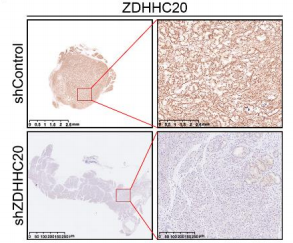
AAV-shControl和AAV-shZDHHC20感染KPC小鼠腫瘤組織的免疫組化染色
研究背景
胰腺導(dǎo)管腺癌(Pancreatic ductal adencarcinoma, PDAC)是一種致死性實體腫瘤,在世界范圍內(nèi)發(fā)病率較高。由于PDAC缺乏早期診斷,且有轉(zhuǎn)移和耐藥傾向,因此PDAC的死亡率與發(fā)病率幾乎相等。研究表明,KRAS突變是胰腺腫瘤發(fā)生的起始事件,常見的突變是KRAS G12D,發(fā)生在90%以上的胰腺上皮內(nèi)瘤變(PanINs)中。在KRAS信號的背景下,PDAC中惡性轉(zhuǎn)化和腫瘤維持的遺傳控制在很大程度上仍未被探索。
研究結(jié)果
1、KRAS突變通過STAT3誘導(dǎo)ZDHHC20在胰腺癌中積累
作者發(fā)現(xiàn)ZDHHC20在胰腺癌細胞系中的表達明顯高于正常胰腺上皮組織,與其他胰腺癌細胞系相比,ZDHHC20在無KRAS突變的胰腺癌細胞系BxPC-3中的表達水平相對較低。此外,TIMER數(shù)據(jù)庫分析顯示,在KRAS突變的胰腺癌患者的腫瘤組織中,ZDHHC20的表達水平高于沒有KRAS突變的胰腺癌患者。為了進一步研究KRAS突變是否導(dǎo)致ZDHHC20在胰腺癌組織中高表達,作者利用KRAS G12D抑制劑處理胰腺癌細胞,發(fā)現(xiàn)KRAS G12D抑制劑處理可顯著下調(diào)胰腺癌細胞中ZDHHC20的表達。進一步研究KRAS調(diào)控ZDHHC20表達的機制,發(fā)現(xiàn)外源KRAS G12D的表達導(dǎo)致ZDHHC20顯著上調(diào)。利用KnockTF平臺分析發(fā)現(xiàn)STAT3對ZDHHC20具有顯著調(diào)節(jié)作用,ChIP-qPCR結(jié)果表明STAT3可以結(jié)合到ZDHHC20的啟動子區(qū)。此外,KRAS G12D的外源表達增強了ZDHHC20啟動子區(qū)域STAT3的富集。以上表明KRAS突變是胰腺癌中STAT3-ZDHHC20軸過度激活的主要致病因素之一。
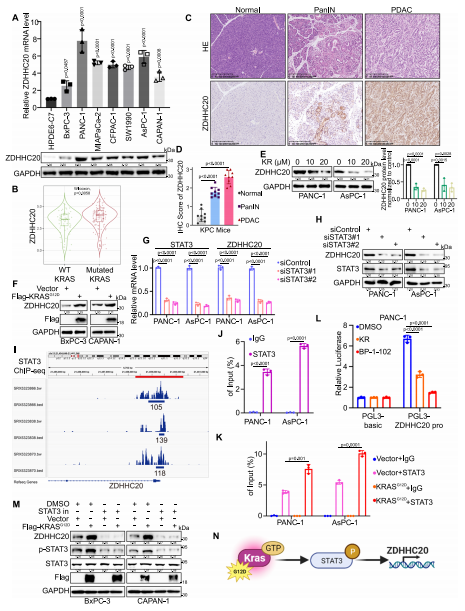
圖1.KRAS突變通過STAT3誘導(dǎo)ZDHHC20在胰腺癌中積累
2、ZDHHC20以棕櫚酰化依賴的方式促進胰腺癌進展
接下來,作者探究了ZDHHC20在胰腺癌細胞中的生物學(xué)功能。在PANC-1和AsPC-1細胞中特異性敲低ZDHHC20,發(fā)現(xiàn)ZDHHC20沉默可顯著降低這些胰腺癌細胞株的增殖、侵襲和遷移。此外,通過細胞源異種移植(CDX)模型,發(fā)現(xiàn)ZDHHC20的敲低抑制了腫瘤的生長。作者利用AAV8-shZDHHC20在KPC小鼠中敲低ZDHHC20,發(fā)現(xiàn)在KPC小鼠中敲低ZDHHC20導(dǎo)致腫瘤重量降低,胰腺腫瘤病變面積減小,值得注意的是,小鼠存活時間延長,表明ZDHHC20在胰腺癌中作為腫瘤啟動子起作用。考慮到ZDHHC20作為棕櫚酰酰基轉(zhuǎn)移酶的功能,作者探究了ZDHHC20的致癌能力是否依賴于其棕櫚酰化活性,構(gòu)建了兩個沒有明顯催化活性的ZDHHC20突變體(C156S和F171A),發(fā)現(xiàn)這兩個突變體的過表達顯著降低了ZDHHC20的棕櫚酰化催化活性,抑制了胰腺癌細胞的增殖和侵襲。表明ZDHHC20可能以部分依賴于棕櫚酰化的方式促進胰腺癌的進展。
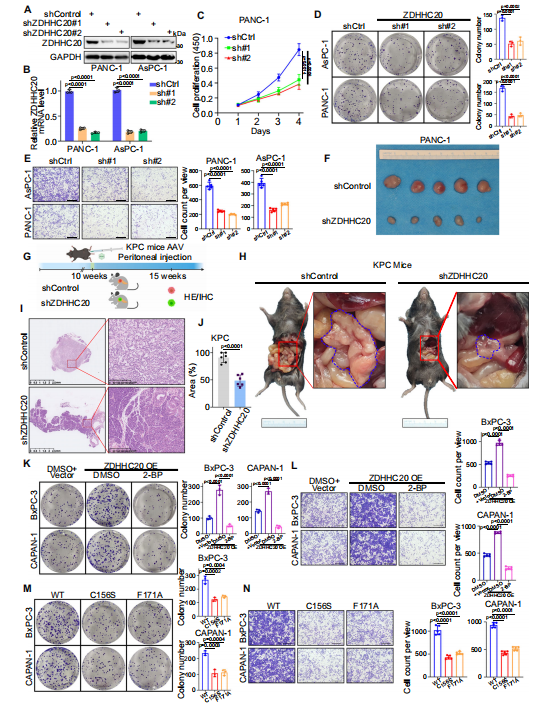
圖2. ZDHHC20以棕櫚酰化依賴的方式促進胰腺癌的進展
3、ZDHHC20通過Cys474上的棕櫚酰化抑制YTHDF3的降解
作者進一步研究發(fā)現(xiàn)ZDHHC20是YTHDF3棕櫚酰化酶,ZDHHC20介導(dǎo)的YTHDF3在Cys474上的棕櫚酰化促進了胰腺癌的進展。為了更全面地了解YTHDF3棕櫚酰化,作者評估了YTHDF3棕櫚酰化修飾對其亞細胞定位的潛在影響。核/胞質(zhì)分離實驗表明,YTHDF3主要定位于細胞質(zhì)中,這與之前的報道一致。下調(diào)ZDHHC20只降低了YTHDF3的蛋白水平,并沒有改變YTHDF3的mRNA水平。作為一種可逆的翻譯后修飾,棕櫚酰化調(diào)節(jié)蛋白質(zhì)的運輸、相互作用和降解。接下來,作者評估了ZDHHC20棕櫚酰化是否調(diào)節(jié)YTHDF3降解,發(fā)現(xiàn)ZDHHC20介導(dǎo)的YTHDF3-Cys474棕櫚酰化抑制了HSC70對YTHDF3的識別,從而通過CMA途徑抑制了其隨后的溶酶體降解。
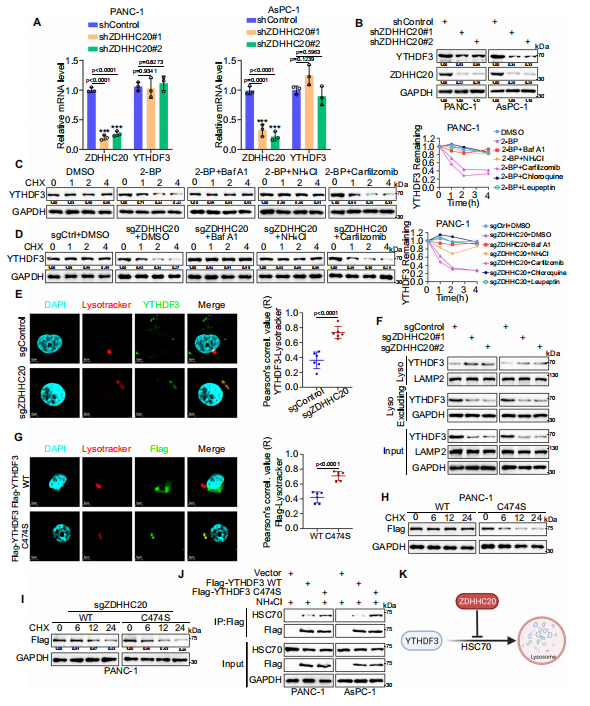
圖3.ZDHHC20通過Cys474上的棕櫚酰化抑制YTHDF3的降解
4、ZDHHC20介導(dǎo)的YTHDF3-Cys474棕櫚酰化穩(wěn)定MYC mRNA水平
作者探究了ZDHHC20-YTHDF3軸促進胰腺癌進展的機制,發(fā)現(xiàn)YTHDF3棕櫚酰化與MYC表達密切相關(guān)。作為m6A的主要讀取器之一,YTHDF3可識別m6A修飾的RNA,隨后調(diào)控其穩(wěn)定性和翻譯,機制研究發(fā)現(xiàn)YTHDF3以依賴m6A的方式穩(wěn)定MYC mRNA。接下來,作者探究了ZDHHC20是否通過影響MYC的生物學(xué)功能來促進胰腺癌的進展,評估2-BP處理和敲除ZDHHC20對MYC mRNA穩(wěn)定性的影響,發(fā)現(xiàn)阻斷YTHDF3 Cys474棕櫚酰化可降低MYC mRNA的半衰期。WB結(jié)果表明,異位表達ZDHHC20上調(diào)MYC的表達,這一作用可被YTHDF3敲除阻斷。MYC沉默在體外和體內(nèi)逆轉(zhuǎn)了異位ZDHHC20表達對PDAC的促進作用。以上結(jié)果表明,ZDHHC20介導(dǎo)的YTHDF3-Cys474棕櫚酰化調(diào)節(jié)MYC mRNA的穩(wěn)定性,促進PDAC的進展。治療性阻斷ZDHHC20-YTHDF3相互作用可抑制胰腺癌進展。

圖4. ZDHHC20介導(dǎo)的YTHDF3-Cys474棕櫚酰化穩(wěn)定MYC mRNA水平
小結(jié)
綜上,KRAS上調(diào)的ZDHHC20在胰腺癌患者中異常過表達并與不良預(yù)后相關(guān)。ZDHHC20表達失調(diào)以棕櫚酰化依賴的方式促進胰腺癌的進展,ZDHHC20通過Cys474的S-棕櫚酰化抑制伴侶蛋白介導(dǎo)的YTHDF3自噬,導(dǎo)致致癌產(chǎn)物MYC的異常積累,從而促進癌細胞的惡性表型。以上發(fā)現(xiàn)還確定了YTHDF3作為m6A讀取器的致癌作用,并強調(diào)了靶向ZDHHC20-YTHDF3-MYC信號軸在胰腺癌中的治療潛力。
