2024年2月,中國科學院大學陸忠兵教授聯合北京朝陽醫院張敏醫生和美國密西西比大學醫學中心陳英杰教授團隊在Redox Biology(IF 11.4)上發表了題為“DDAH1 recruits peroxiredoxin 1 and sulfiredoxin 1 to preserve its activity and regulate intracellular redox homeostasis ”的論文。研究表明,DDAH1可以招募PRDX1和SRXN1在氧化應激條件下維持其活性/表達和氧化還原穩態,提示靶向DDAH1-PRDX1-SRXN1可能成為氧化應激相關肝臟疾病的一種新型治療方法。


01 研究背景
氧化應激是由活性氧(ROS)的過量產生和抗氧化系統的損傷引起的,可引發各種生化反應,如脂質過氧化、DNA損傷和蛋白質氧化修飾或錯誤折疊。越來越多的證據表明,氧化應激在包括非酒精性脂肪性肝病(NAFLD)在內的許多疾病的發病機制中起著重要作用,二甲基精氨酸二甲胺水解酶(DDAH1)是降解不對稱二甲基精氨酸(ADMA)的關鍵酶,與多種疾病發展過程中的氧化應激密切相關。然而,DDAH1調節細胞內氧化還原狀態的潛在機制尚不清楚。
02 研究結果
1、PRDX1可以防止H2O2誘導的DDAH1下調
研究人員發現PRDX1與DDAH1相互作用,為闡明DDAH1-PRDX1相互作用對細胞氧化還原穩態的影響,在HepG2細胞中敲低PRDX1。結果發現,在H2O2處理(150 μM, 24 h)下,PRDX1敲低導致細胞活力下降,細胞內ADMA、ROS和超氧化物水平增加;H2O2處理顯著降低GSH/GSSG比值,PRDX1基因敲低加重了這一作用。另一方面,過表達PRDX1 降低了對照細胞內ADMA和ROS水平;在H2O2處理的細胞中,PRDX1過表達增加細胞活力,降低細胞內ADMA、ROS和超氧化物水平。WB結果顯示PRDX1敲低增加了對照細胞中氧化PRDXs (PRDX-SO3)和SRXN1的表達,加劇了H2O2誘導的DDAH1下調和PRDX-SO3上調;PRDX1過表達降低了基礎條件下PRDX-SO3的表達,顯著減弱H2O2誘導的DDAH1和SRXN1的下調。進一步研究發現PRDX1可以在氧化應激條件下保持DDAH1的表達和活性。
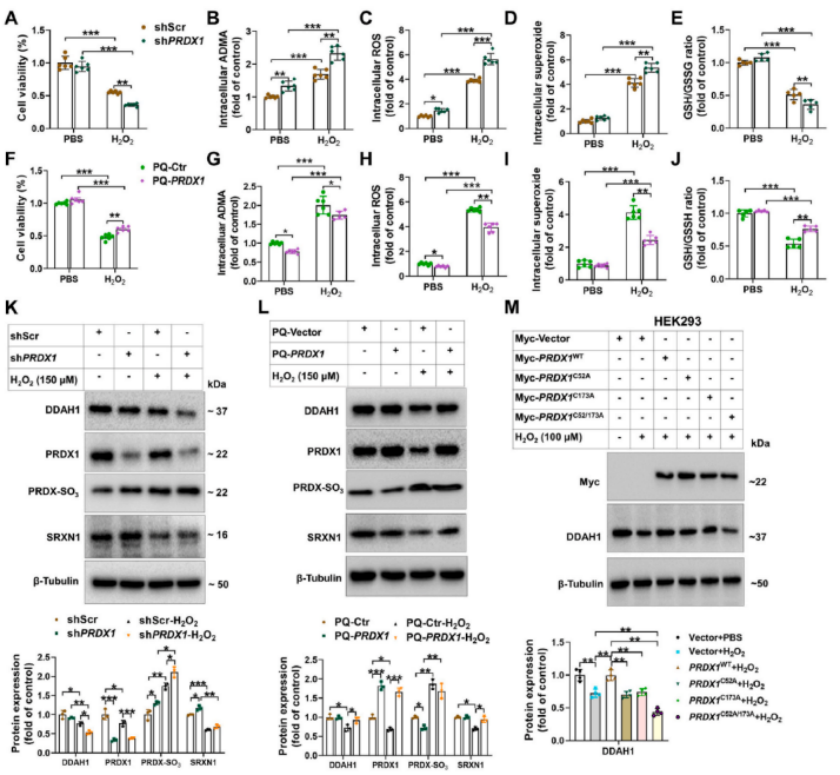
圖1. PRDX1在H2O2處理的細胞中保持細胞活力、DDAH1表達和氧化還原穩態
2、SRXN1與DDAH1相互作用并保護其表達和活性
研究人員進一步研究發現SRXN1與DDAH1相互作用并保護其表達和活性,并且STRING數據庫的結果表明PRDX和SRXN1在蛋白水平上相互作用。研究人員利用Myc-DDAH1構建體轉染HEK293細胞,并進行co-IP分析,結果表明,SRXN1存在于Myc-DDAH1免疫沉淀中,且隨著H2O2處理(150μM, 2 h),SRXN1含量增加,表明SRXN1與DDAH1存在直接相互作用,且氧化應激可增強這種相互作用。研究人員通過進一步的實驗確定了SRXN1會影響DDAH1的表達和活性。表明SRXN1不僅作為氧化PRDXs的還原酶,而且在氧化應激條件下維持DDAH1的表達和活性。
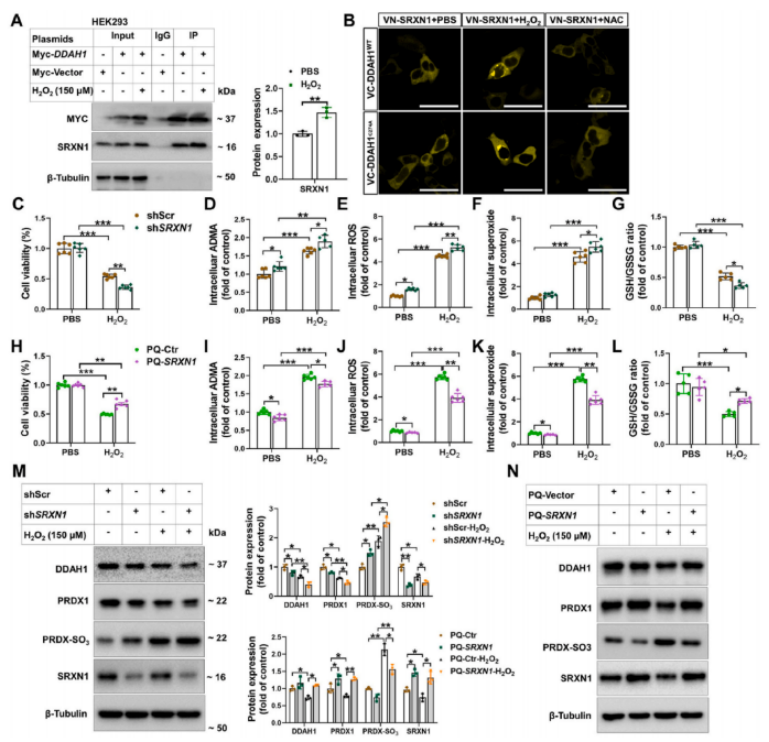
圖2. SRXN1與DDAH1相互作用
3、肝細胞特異性的DDAH1缺失加劇了CCl4誘導的肝毒性和PRDX1的下調
DDAH1可改善CCl4誘導的肝損傷、氧化應激和細胞死亡,為闡明肝DDAH1是否影響CCl4和PRDX1/SRXN1通路的肝毒性,研究人員用CCl4處理Ddah1HKO和Ddah1f/f小鼠,結果發現Ddah1HKO小鼠的AST和ALT水平高于Ddah1f/f小鼠,CCl4減弱了Ddah1HKO小鼠在基礎條件下的血清ADMA水平高于Ddah1f/f小鼠的差異。染色結果顯示,CCl4對Ddah1HKO小鼠的肝損傷、纖維化、超氧化物生成和凋亡細胞的影響大于Ddah1f/f小鼠。WB分析顯示,肝細胞特異性缺失DDAH1加劇了CCl4處理小鼠肝臟中PRDX1和Bcl-2的下調以及PRDX-SO3和Bax的上調,減弱了SRXN1和PRDX4的上調。
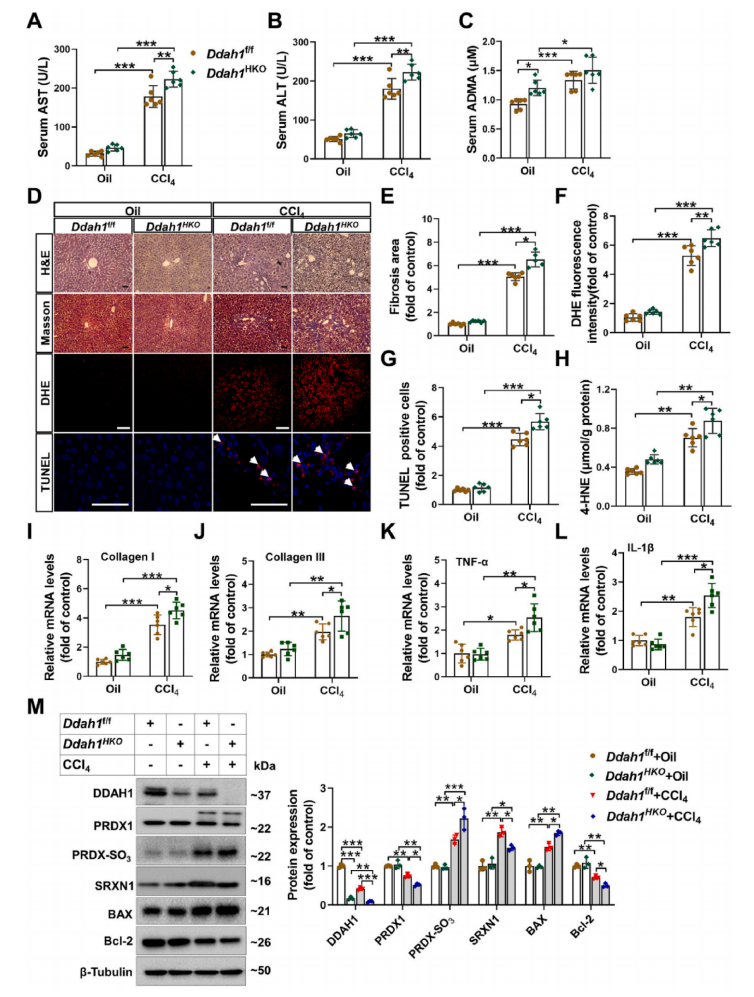
圖3. 肝臟Ddah1缺乏加重了CCl4處理小鼠的肝功能障礙、氧化應激和細胞凋亡
4、肝臟過表達PRDX1可減輕CCl4誘導的肝毒性,降低Ddah1缺乏的影響
為確定肝細胞特異性過表達PRDX1是否能在體內維持DDAH1的表達和活性,研究人員通過尾靜脈注射AAV8-Prdx1治療CCl4處理的WT和Ddah1-/-小鼠,以注射AAV8-GFP的WT小鼠為對照。PRDX1過表達降低了WT和Ddah1-/-小鼠血清AST和ALT水平的差異,此外,PRDX1過表達改善了CCl4誘導的WT和Ddah1-/-小鼠肝臟的病理改變、纖維化、超氧化物生成和凋亡。PRDX1過表達降低了CCl4處理小鼠肝臟中3′-NT和4-HNE水平以及I型膠原、III型膠原、TNF-α和IL-1β mRNA水平。WB結果表明,過表達PRDX1可提高DDAH1、SRXN1、Bcl-2和PRDX4的表達,而降低PRDX-SO3和Bax的表達。
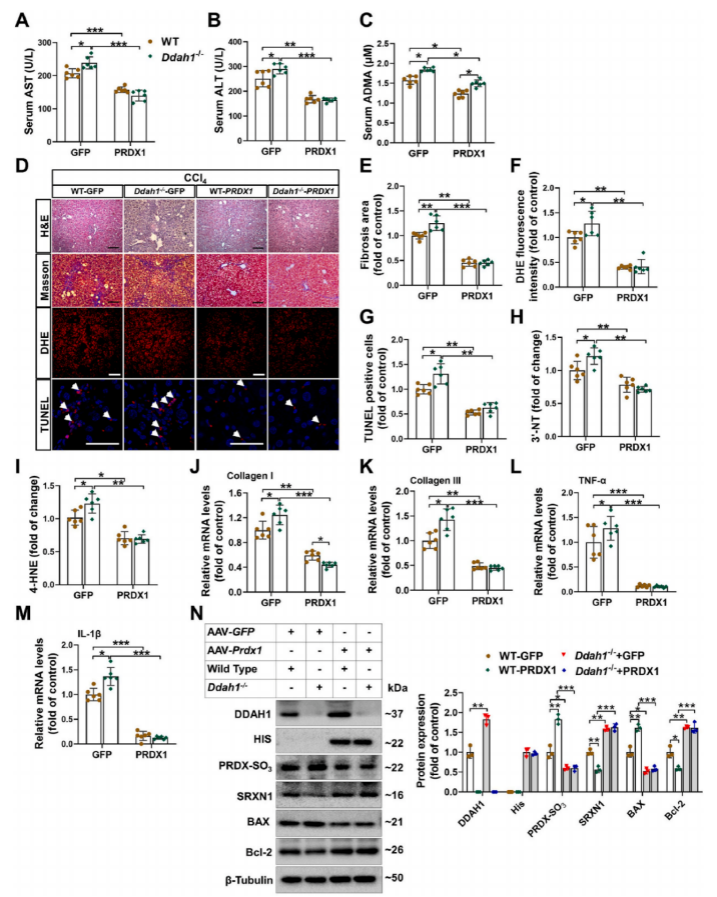
圖4.PRDX1過表達可改善CCl4誘導的肝損傷、氧化應激和細胞凋亡
03 小結
本研究首次提供了直接證據,證明DDAH1可以招募PRDX1和SRXN1在氧化應激條件下維持其活性/表達和氧化還原穩態;靶向DDAH1-PRDX1-SRXN1相互作用可能是與氧化應激相關的肝臟疾病的一種新的治療方法。
