血管損傷誘導的再狹窄是冠心病患者長期預后不良的重要原因,盡管乙醛脫氫酶2(ALDH2)缺乏與冠心病患者預后不良有關(guān),但ALDH2影響血管損傷誘導的再狹窄的確切機制仍不清楚。2025年10月,山東大學齊魯醫(yī)院陳玉國/徐峰教授團隊在Metabolism(IF11.9)發(fā)文“ALDH2 deficiency aggravates vascular injury-induced restenosis by enhancing vascular smooth muscle cell proliferation through SLC38A2-mediated upregulation of glutamine uptake”,研究結(jié)果闡明了ALDH2 缺陷會通過增加谷氨酰胺攝取來促進血管平滑肌細胞增殖,進而加劇新生內(nèi)膜形成,這一發(fā)現(xiàn)為預防血管損傷誘導的再狹窄提供了一種具有潛力的轉(zhuǎn)化策略。

· 維真助力 ·
In vivo
基因信息
ALDH2:乙醛脫氫酶2
SLC38A2:溶質(zhì)載體家族38成員2
實驗動物
8周齡雄性ALDH2flox和ALDH2ΔSMC小鼠;C57BL/6小鼠
病毒產(chǎn)品
AAV2-SM22α-GFP-mir30-sh-SLC38A2、 AAV2-sh-Scramble;
AAV2-SM22α-GFP-ALDH2、AAV2-GFP
病毒用量
5×1011
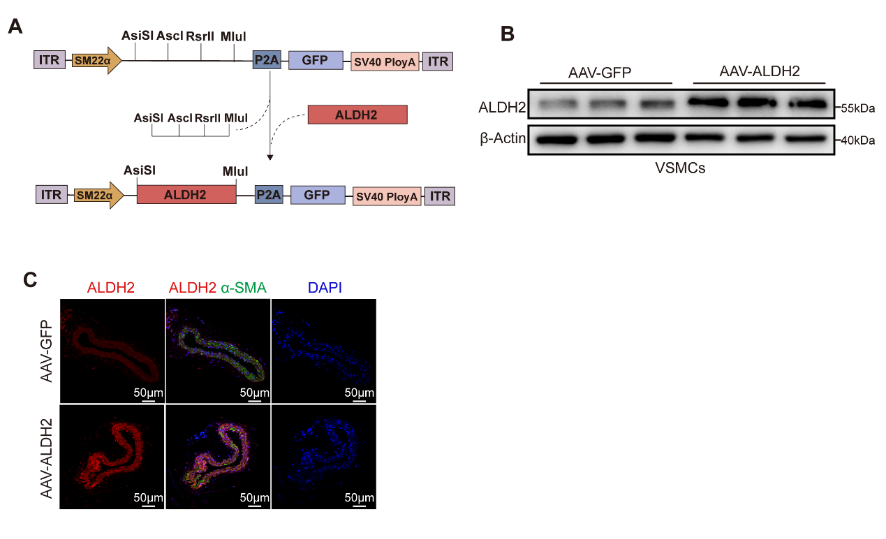
SMC特異性ALDH2過表達AAV的構(gòu)建與轉(zhuǎn)染效率驗證
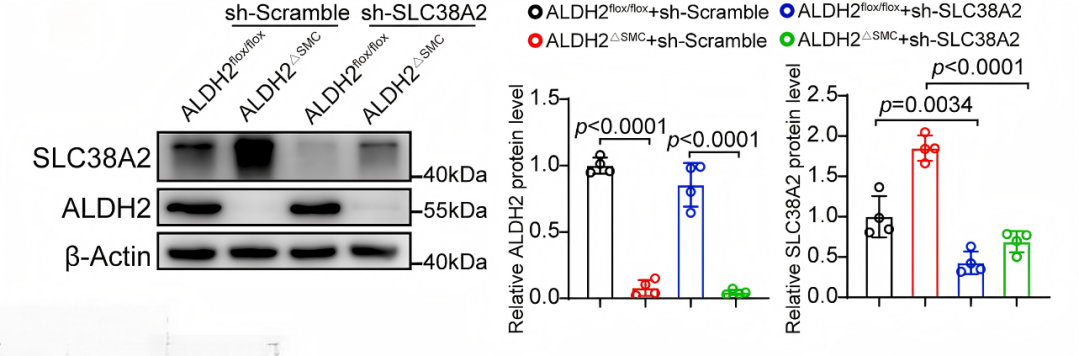
蛋白質(zhì)印跡證實MASMC中SLC38A2表達被顯著抑制
In vitro
病毒產(chǎn)品
Lv-shALDH2、Lv-Control
感染細胞
原代小鼠主動脈平滑肌細胞MASMCs
研究結(jié)果
1.ALDH2缺陷促進新生內(nèi)膜形成
研究團隊發(fā)現(xiàn)在人狹窄冠狀動脈組織的新生內(nèi)膜區(qū)域、小鼠股動脈導絲損傷模型及頸動脈結(jié)扎模型的損傷血管VSMCs中,ALDH2顯著下調(diào)。在體內(nèi)實驗中,全身性ALDH2敲除與VSMC特異性ALDH2敲除均會促進血管損傷后的新生內(nèi)膜形成。研究人員使用攜帶SM22α啟動子的AAV2在小鼠血管平滑肌細胞中特異性過表達ALDH2,以AAV-GFP組作為對照。通過Western blot和免疫熒光染色證實,AAV-ALDH2組小鼠血管中的ALDH2蛋白表達水平顯著高于對照組。與對照組相比,ALDH2過表達顯著減輕兩種模型中的新生內(nèi)膜形成,并有效抑制損傷動脈中的VSMC增殖。隨后研究人員從ALDH2基因敲除小鼠和野生型小鼠中分離原代小鼠主動脈平滑肌細胞,探索ALDH2在PDGF-BB中的潛在作用,結(jié)果表明ALDH2敲除細胞遷移及增殖能力增強,使用siRNA敲低MASMCs中的ALDH2,同樣可以增強PDGF-BB誘導的VSMC增殖和遷移。作為反向驗證,研究人員在MASMCs中通過慢病毒載體過表達ALDH2,證實VSMC遷移和增殖受到抑制。
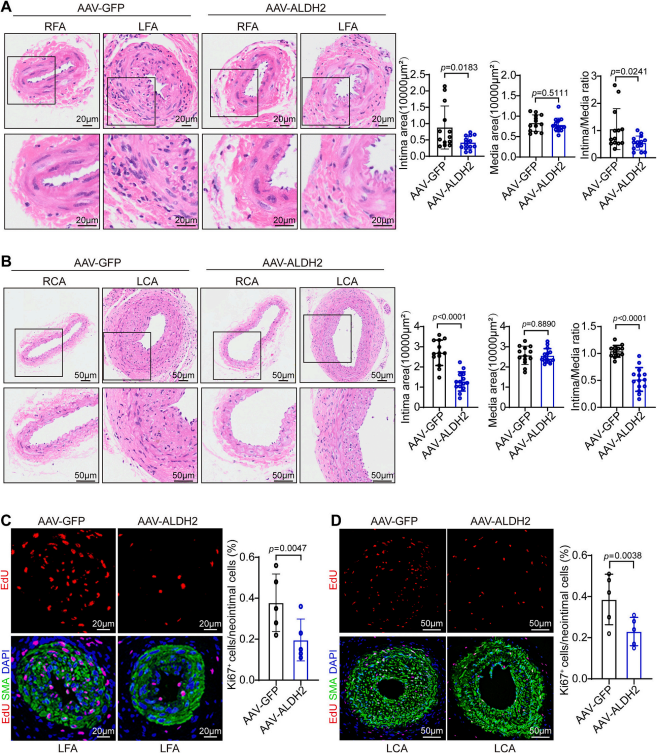
ALDH2過表達通過抑制VSMCs增殖減少新生內(nèi)膜形成
2.ALDH2缺陷通過上調(diào)SLC38A2的表達促進VSMC增殖
mRNA測序和代謝組學分析顯示,在ALDH2敲除的VSMCs中,谷氨酰胺和谷胱甘肽的水平顯著升高,并且谷胱甘肽代謝通路被富集。對谷氨酰胺轉(zhuǎn)運蛋白進行篩選后發(fā)現(xiàn),SLC38A2在mRNA和蛋白水平上均被ALDH2缺陷特異性上調(diào),而其他轉(zhuǎn)運蛋白未受影響。在VSMCs中過表達SLC38A2,能夠模擬ALDH2敲除的表型,即促進PDGF-BB誘導的細胞增殖、遷移并激活mTORC1信號通路。在ALDH2敲低的VSMCs中,使用siRNA敲低SLC38A2,可以有效逆轉(zhuǎn)由ALDH2缺陷引起的mTORC1信號激活、細胞增殖和遷移增強。研究團隊探索了ALDH2上調(diào)SLC38A2表達的分子機制,通過mRNA-seq數(shù)據(jù)與Jaspar數(shù)據(jù)庫預測的轉(zhuǎn)錄因子進行交叉比對,篩選出13個潛在調(diào)控SLC38A2的轉(zhuǎn)錄因子。其中,激活轉(zhuǎn)錄因子4(ATF4)表達量最高,且實驗證實ALDH2敲低會顯著上調(diào)ATF4的表達水平。進一步的研究發(fā)現(xiàn)ALDH2缺陷激活轉(zhuǎn)錄因子ATF4,使其與SLC38A2基因啟動子的結(jié)合增加,從而驅(qū)動SLC38A2的轉(zhuǎn)錄,體外數(shù)據(jù)表明ATF4是ALDH2-SLC38A2介導的谷氨酰胺攝取和VSMC增殖所必需的。
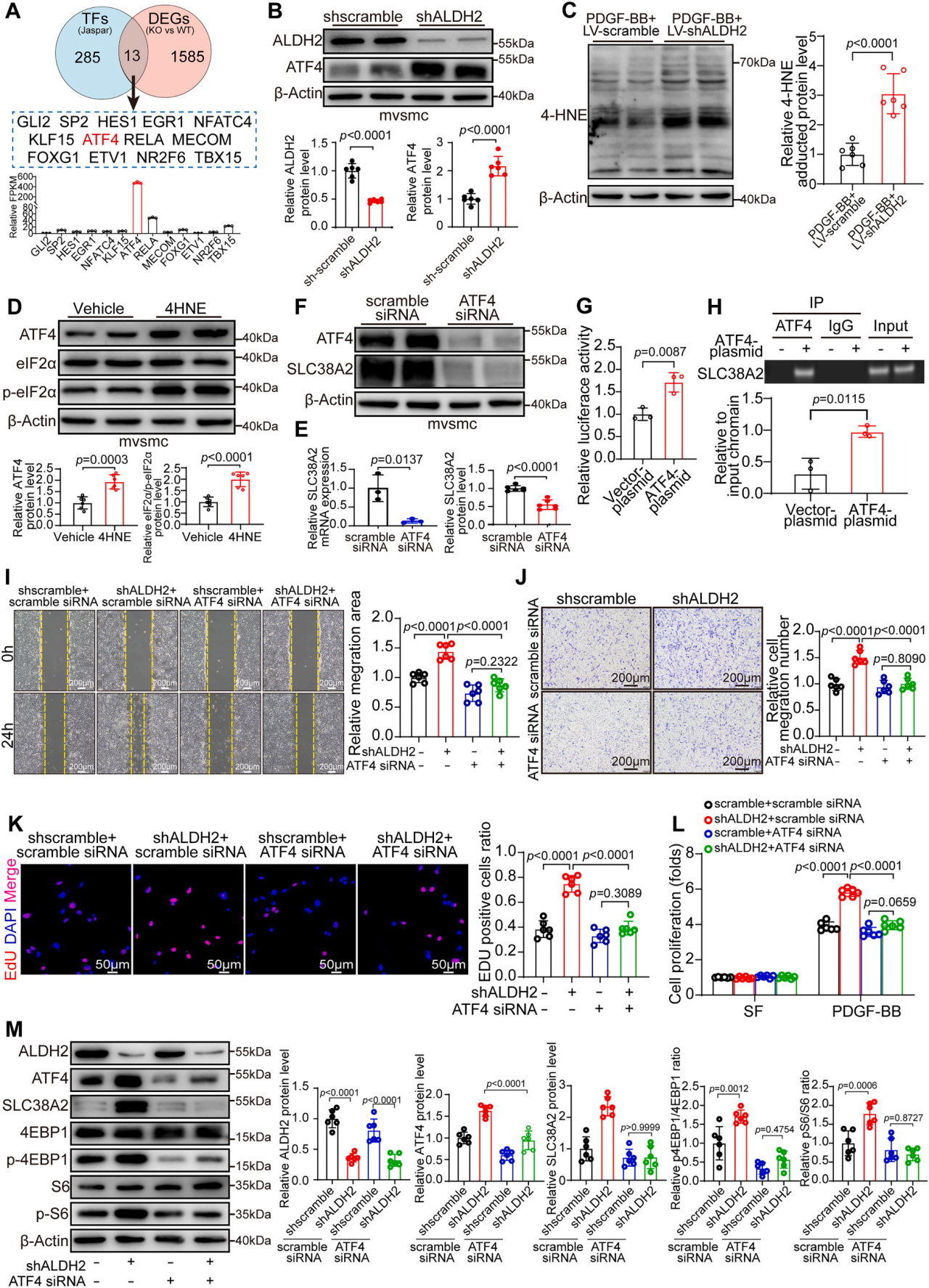
ALDH2缺失上調(diào)SLC38A2并通過ATF4介導的轉(zhuǎn)錄激活促進VSMCs增殖和遷移
3.SLC38A2是ALDH2調(diào)控新生內(nèi)膜形成的下游關(guān)鍵執(zhí)行者
使用AAV2-SM22α-shSLC38A2注射VSMC特異性ALDH2敲除小鼠及其對照小鼠中,實現(xiàn)VSMC特異性SLC38A2敲低,四周后對小鼠進行股動脈導絲損傷和頸動脈結(jié)扎手術(shù),以誘導血管新生內(nèi)膜形成。研究數(shù)據(jù)顯示,ALDH2敲除小鼠新生內(nèi)膜面積和內(nèi)膜/中膜面積比顯著增加,敲低SLC38A2明顯減輕上述新生內(nèi)膜形成。Ki67免疫熒光染色顯示,在VSMC特異性ALDH2缺失組中,損傷動脈內(nèi)增殖的Ki67陽性細胞數(shù)量的增加,可被SLC38A2缺失所消除。這些結(jié)果證明,ALDH2缺陷通過SLC38A2促進血管平滑肌細胞增殖及損傷誘導的新生內(nèi)膜形成。進一步探究發(fā)現(xiàn)ALDH2的酶活性是其發(fā)揮保護作用的核心,其功能喪失會直接加劇疾病。

VSMC特異性SLC38A2敲低減少了ALDH2缺失引起的新生內(nèi)膜形成
研究結(jié)論
本研究闡明了一種新機制:ALDH2通過激活溶質(zhì)載體家族38成員2(SLC38A2)-谷氨酰胺攝取軸,調(diào)控血管平滑肌細胞增殖與新生內(nèi)膜形成。ALDH2-ATF4-SLC38A信號通路的發(fā)現(xiàn),不僅加深了對ALDH2介導細胞行為的分子機制的理解,也為治療血管損傷誘導的再狹窄提供了潛在的靶點。
