01研究背景
肝細胞癌(HCC)是全球第四大癌癥死亡原因,泛素-蛋白酶體系統、NF-κB通路、自噬等細胞信號通路都參與了HCC的發生發展。TRAF2作為銜接蛋白和泛素E3連接酶,在介導TNFα-NFκB信號通路中發揮重要作用,并在多種人類癌癥中表達失調,但TRAF2是否調節肝癌細胞的生長尚不清楚。
2023年, 浙江大學醫學院第一附屬醫院鄭敏、趙永超團隊在“Cell Death and Differentiation (IF 12.067)”上發表文章“The TRAF2-p62 axis promotes proliferation and survival of liver cancer by activating mTORC1 pathway”,發現TRAF2通過促進p62多泛素化來增強其與Raptor-RagC的結合,導致mTORC1激活,進而促進肝癌的發展,表明TRAF2是肝癌治療的潛在靶點。
· 維真助力 ·
維真生物提供文中所用慢病毒載體:pLent-shRNA-p62
02部分結果展示
1. TRAF2負調控p62蛋白水平和自噬通量
作者發現HCC細胞系和HCC臨床組織中TRAF2 mRNA水平高于正常肝臟細胞和鄰近非腫瘤組織,同時還與HCC患者預后不良高度相關。為了探索TRAF2促進肝癌進展的機制,作者通過串聯親和純化和質譜分析,發現p62是TRAF2結合的候選蛋白。結構域分析發現,TRAF2的TRAF結構域和p62的TB結構域介導了TRAF2-p62的結合。為了探討TRAF2對p62的影響,作者研究了TRAF2是否影響HCC細胞系中p62蛋白的表達,發現敲低TRAF2顯著增加了HepG2和Huh7細胞中的p62蛋白水平,TRAF2過表達以劑量依賴的方式降低內源性p62水平。p62參與自噬調控,作者進一步研究了TRAF2對自噬的影響,發現TRAF2敲低會破壞HCC細胞的自噬通量。
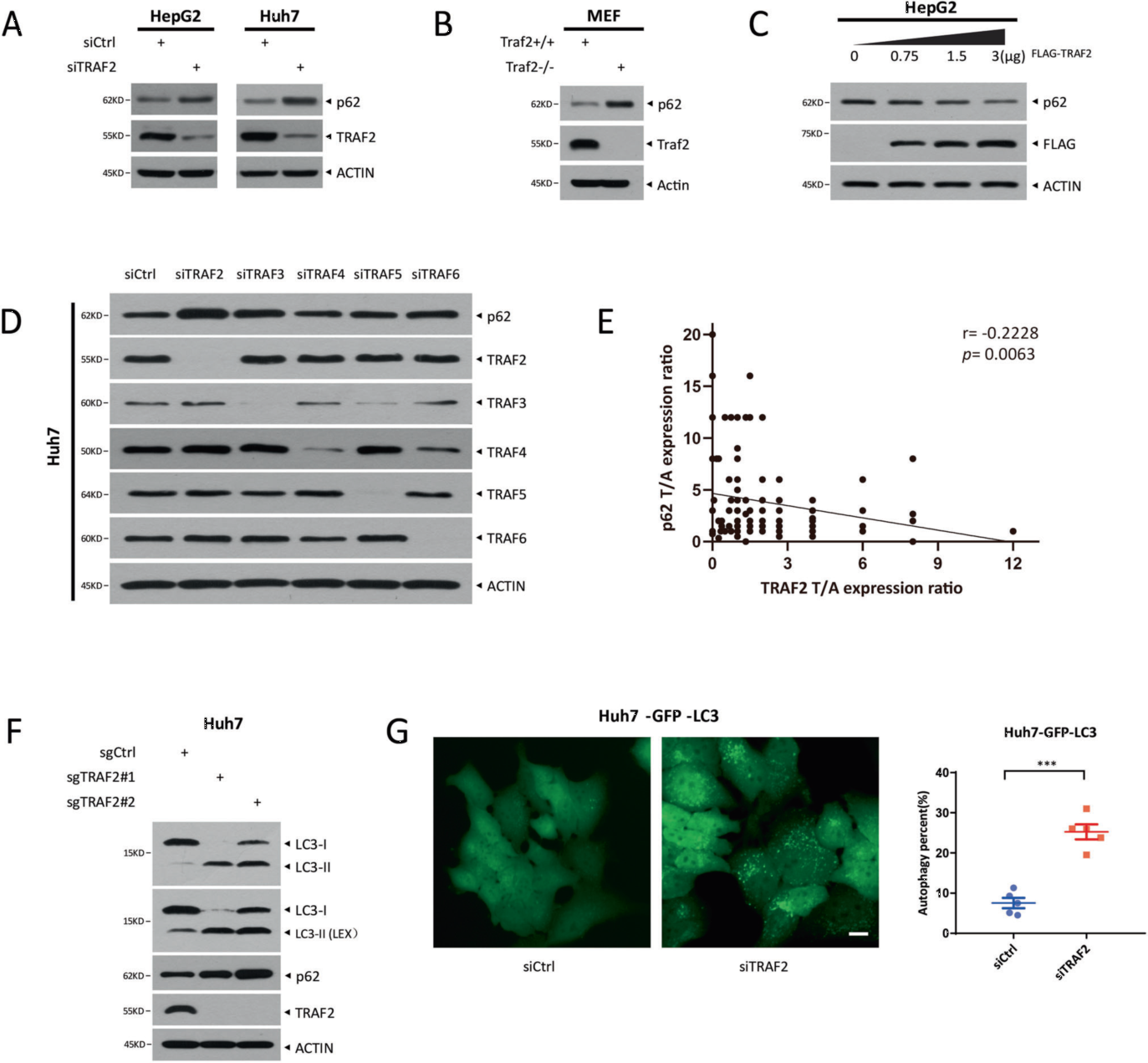
圖1. TRAF2負調控p62蛋白水平和自噬
2. TRAF2促進p62的k63連接的多泛素化和溶酶體依賴性降解
由于TRAF2與p62相互作用并負向調節p62蛋白水平,作者假設TRAF2介導p62的降解。為了驗證這一假設,作者先研究了TRAF2對p62蛋白半衰期的影響,發現TRAF2敲低后p62的半衰期延長。之后作者研究了p62是否受到TRAF2誘導的多泛素化,發現TRAF2顯著促進p62多泛素化,進一步研究發現TRAF2促進p62在420賴氨酸殘基上的k63連接的多泛素化,且p62的降解是通過溶酶體介導的,而不是蛋白酶體系統。
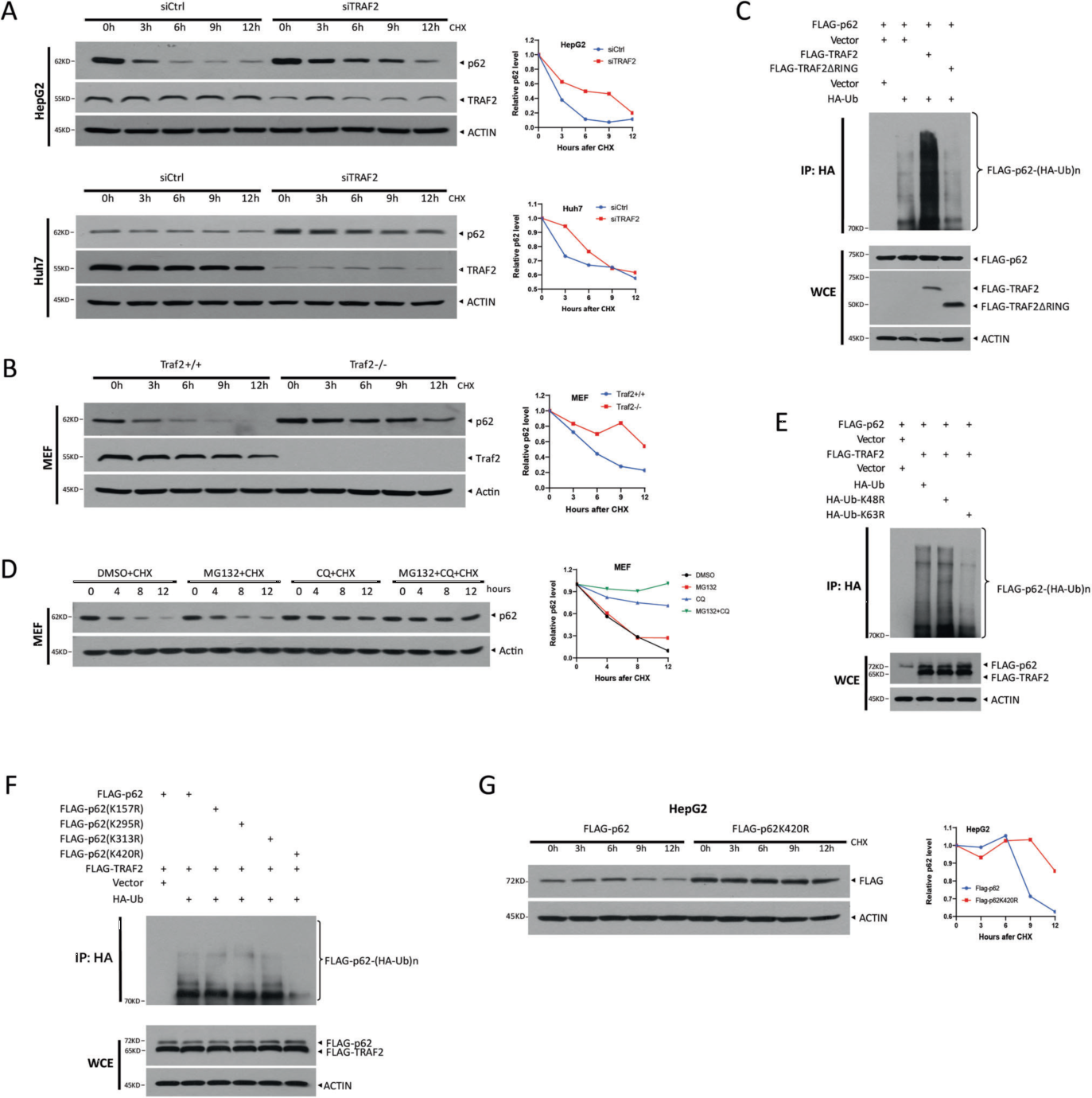
圖2. TRAF2促進p62的k63連鎖多泛素化和溶酶體依賴性降解
3. TRAF2在體外和體內以p62依賴的方式促進腫瘤生長
由于p62是TRAF2的底物,作者接下來研究了p62在TRAF2敲除肝癌細胞中的作用機制,發現在TRAF2缺失的細胞中,p62的敲低促進了肝癌細胞的生長和存活,表明p62起抑制生長的作用。之后作者用小鼠異種移植腫瘤模型驗證了這一結果,將表達p62 shRNA的慢病毒轉染到TRAF2缺失的Huh7細胞中,擴增后接種裸鼠,發現p62敲低顯著逆轉TRAF2敲低對腫瘤生長的抑制作用,腫瘤體積和重量增加。進一步研究發現,p62敲低通過激活mTORC1活性,在體外和體內挽救了TRAF2敲低對腫瘤生長抑制。
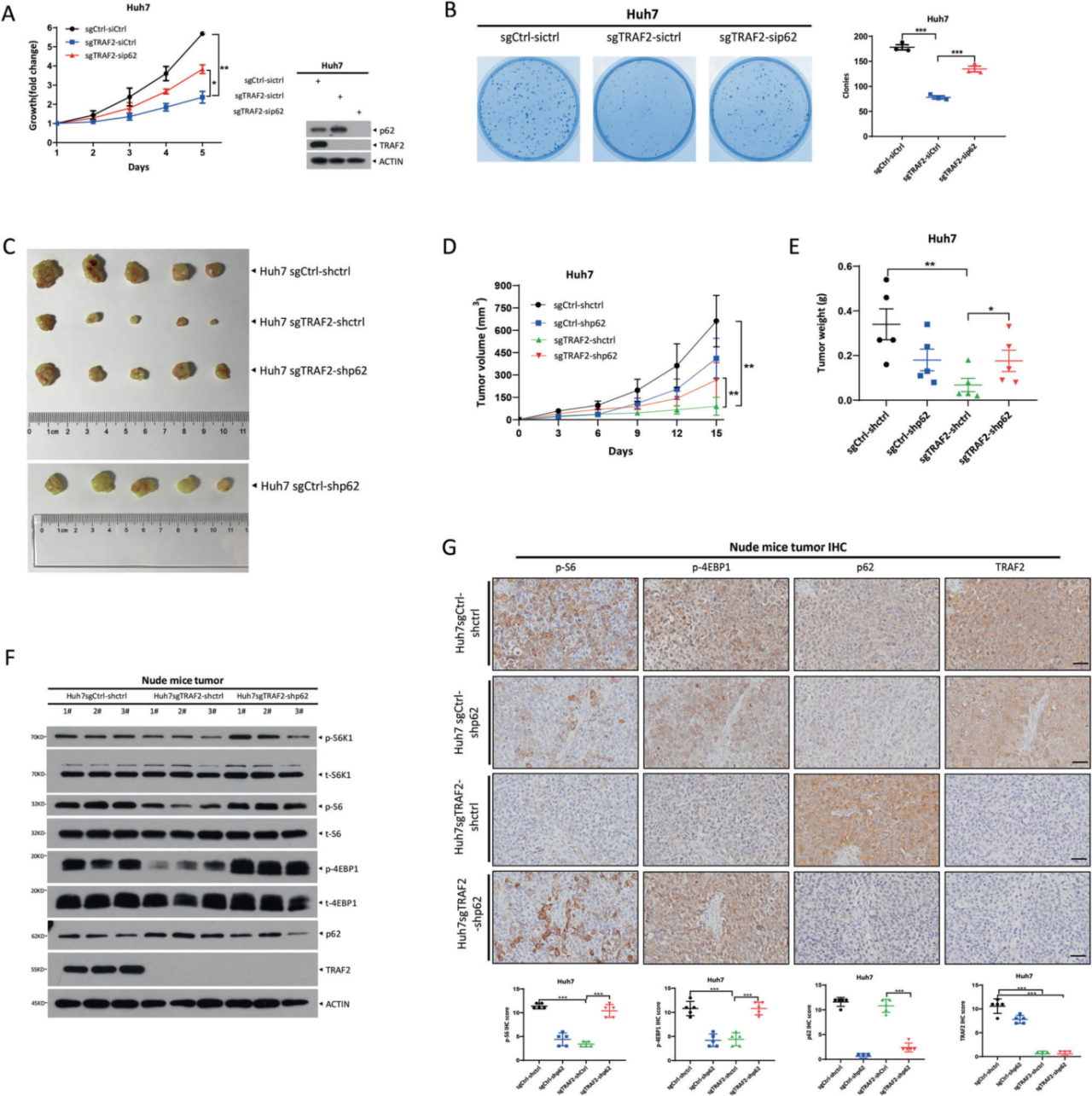
圖3. TRAF2在體外和體內以p62依賴的方式促進腫瘤生長
4. TRAF2泛素化p62促進mTOR激活
由于p62敲低挽救了TRAF2敲除對生長的抑制,作者假設泛素化的p62可能是調控HCC生長的主要作用形式。為了驗證這一假設,作者將p62與其泛素死亡突變體重新轉染到p62缺失的Huh7細胞中,發現p62能顯著促進細胞和裸鼠異種移植模型的生長,并重新激活了腫瘤組織中的mTORC1活性,但p62泛素死亡突變體無上述功能。之后作者研究了p62泛素化調控mTORC1活性的機制,發現與p62相比,突變體抑制Raptor和RagC的結合,并導致mTOR與LAMP2的共定位減少,表明mTORC1的再激活減少。綜上所述,泛素化p62似乎是mTORC1激活的原因,mTORC1激活進一步促進了肝癌細胞的生長。
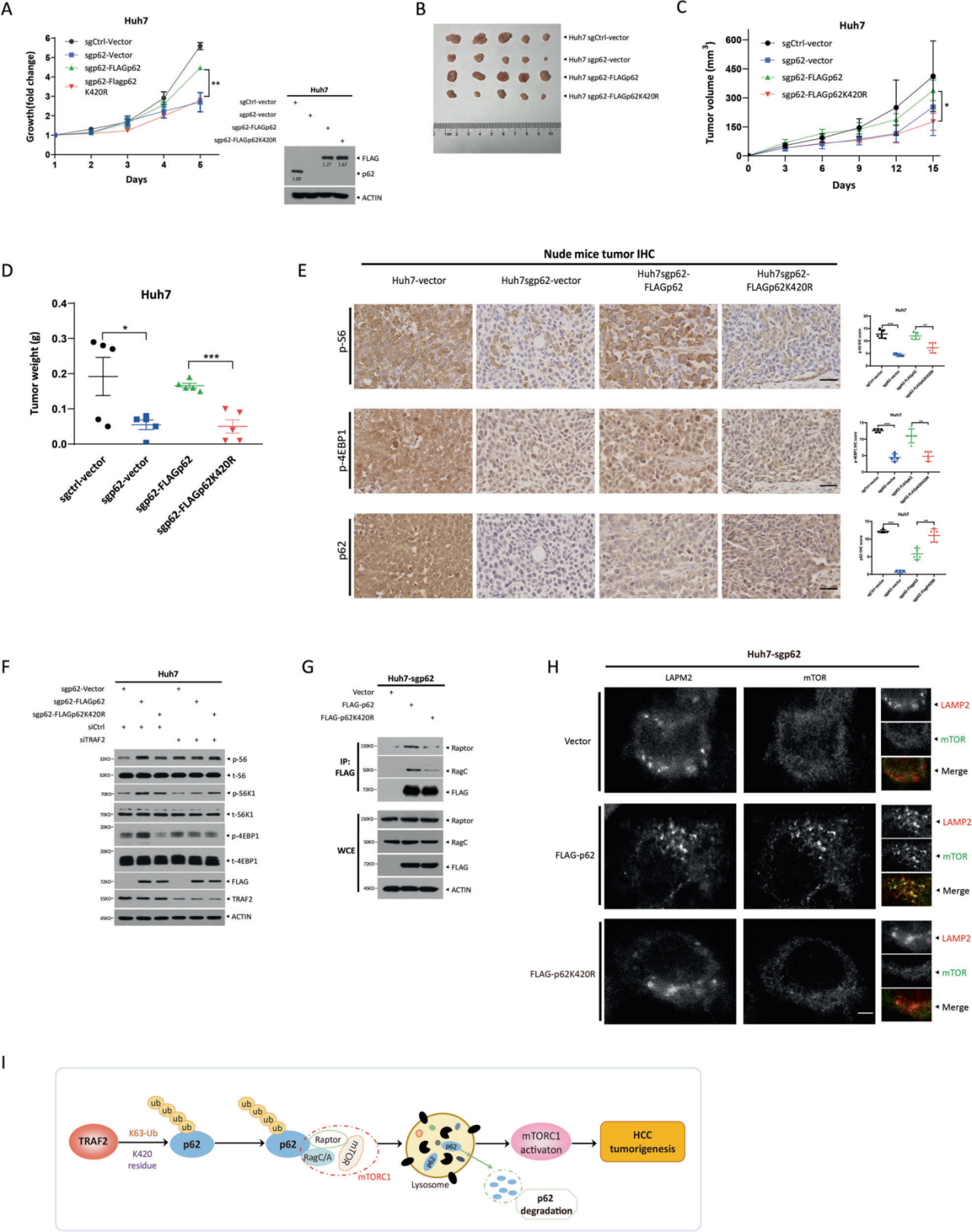
圖4. TRAF2泛素化p62促進mTOR激活
03實驗結論
本研究發現TRAF2促進肝癌細胞生長和存活。從機制上講,TRAF2通過促進p62多泛素化來增強其與Raptor-RagC的結合,從而導致mTORC1激活,進而促進了肝癌細胞的生長,表明TRAF2是肝癌治療的潛在靶點。
