重復(fù)使用生物制劑后產(chǎn)生的抗藥抗體(ADAs)是導(dǎo)致生物療法出現(xiàn)耐藥性的主要原因,尤其是在酶替代療法和腺相關(guān)病毒(AAV)基因療法中。ADAs會(huì)導(dǎo)致藥物清除加快、療效降低和不良反應(yīng),幾乎影響所有生物藥物,現(xiàn)有應(yīng)對(duì)策略效果不佳,雷帕霉素雖可調(diào)節(jié)免疫,但傳統(tǒng)使用方式存在問題。近期,沈陽藥科大學(xué)劉洪卓/王永軍教授團(tuán)隊(duì)在ACS Nano(IF 15.8)上發(fā)表了題為“Lipid-Rapamycin Nanovaccines Overcome the Antidrug Antibody Barrier in Biologic Therapies”的文章,研究開發(fā)了一種基于脂質(zhì)-雷帕霉素(Rapa)的納米疫苗,可恢復(fù)對(duì)生物制劑的免疫耐受,克服ADAs帶來的挑戰(zhàn),為解決生物療法的耐藥問題提供了新途徑。
· 維真助力 - AAV ·
基因信息
Luciferase:熒光素酶;GFP:綠色熒光蛋白;
SEAP:分泌型胚胎堿性磷酸酶
實(shí)驗(yàn)動(dòng)物
雄性C57BL/6小鼠
病毒產(chǎn)品
AAV8-CMV-luciferase;AAV8-CAG-GFP;AAV8-CMV-SEAP
注射劑量
4 × 1012 vg/kg
注射方式
靜脈注射
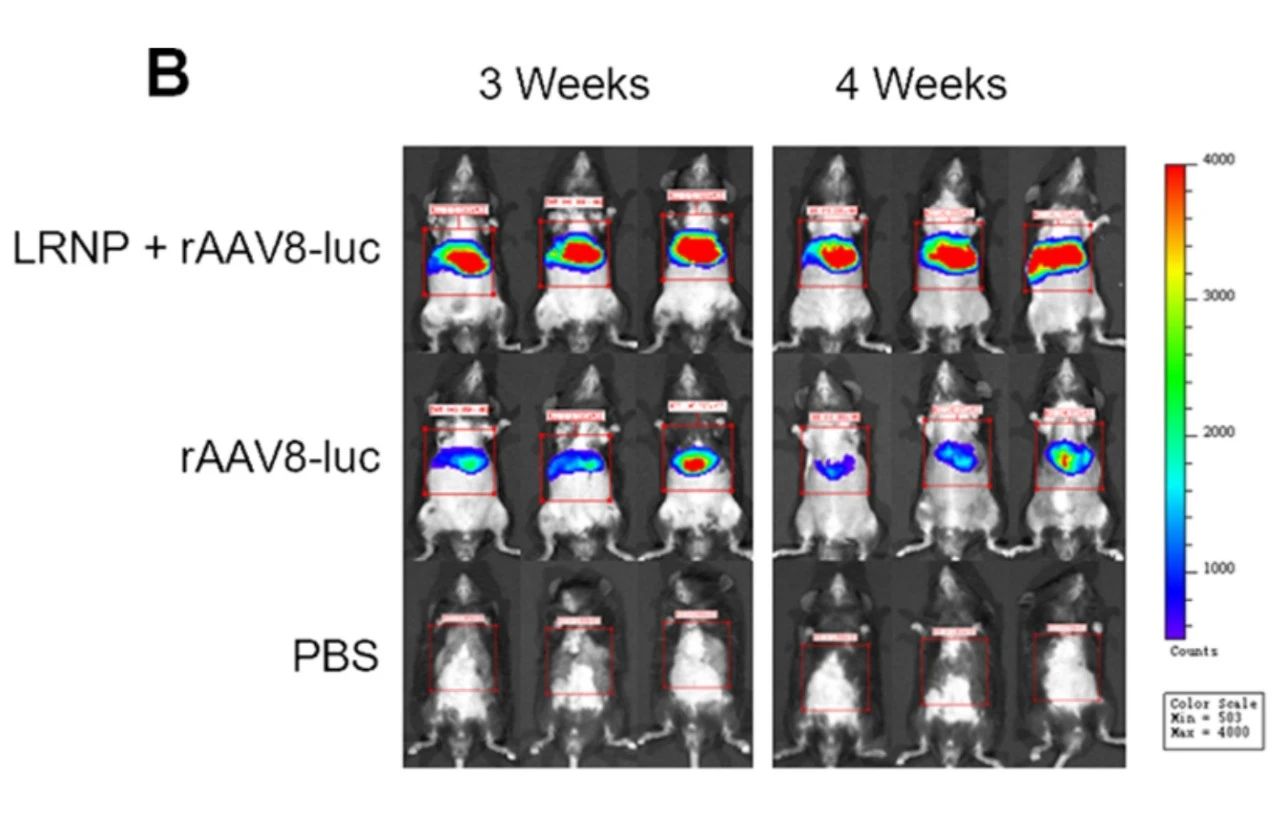
注射AAV8-luc后小鼠熒光素酶表達(dá)的熒光圖像
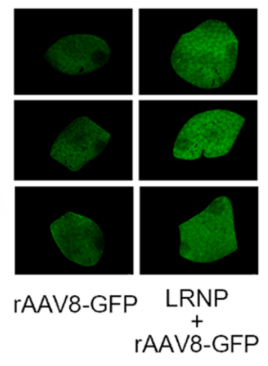
注射AAV8-GFP后小鼠肝臟GFP表達(dá)的熒光圖像
01研究結(jié)果
1. 納米疫苗的設(shè)計(jì)與合成
研究人員設(shè)計(jì)了兩類脂質(zhì)-雷帕霉素(Rapa)結(jié)合物,分別通過可裂解和不可裂解的連接子將脂質(zhì)部分連接到雷帕霉素的42-羥基位置。將含有溶解在甲醇或乙醇中的脂質(zhì)Rapa的有機(jī)相加入蒸餾水中,在DSPE-PEG2000的幫助下自發(fā)形成納米顆粒(NPs)。隨后通過蒸發(fā)去除有機(jī)溶劑,產(chǎn)生脂質(zhì)Rapa納米顆粒(LRNPs)。研究人員進(jìn)一步證明了NP對(duì)有效耐受的必要性。實(shí)驗(yàn)表明,LRNPs能夠顯著降低抗藥抗體的產(chǎn)生,在小鼠模型中,LRNPs與KLH聯(lián)合使用后,小鼠體內(nèi)的KLH特異性IgM和IgG抗體水平顯著降低。此外,LRNPs還能夠在多次挑戰(zhàn)后維持低水平的抗體反應(yīng),表明其能夠誘導(dǎo)長期的免疫耐受。

圖1. LRNPs與游離抗原聯(lián)合預(yù)防性給藥可誘導(dǎo)抗原特異性免疫耐受
2. LRNPs聯(lián)合治療增加AAV8載體轉(zhuǎn)基因表達(dá)
為了確定LRNPs是否可以阻斷抗衣殼抗體的產(chǎn)生并提高AAV8載體在體內(nèi)的轉(zhuǎn)基因效率,研究人員在有或沒有LRNPs的情況下在小鼠中靜脈注射表達(dá)熒光素酶的AAV8。發(fā)光成像顯示,與單獨(dú)用AAV8-luc治療的小鼠相比,在給藥后3周和4周,與LRNP聯(lián)合治療的小鼠肝臟區(qū)域的螢光素酶信號(hào)明顯更高,且轉(zhuǎn)基因表達(dá)持續(xù)時(shí)間更長,并再次利用AAV8-GFP驗(yàn)證了這一結(jié)果。表明與LRNP聯(lián)合治療可減少意外的免疫反應(yīng),并在再次給藥后提高AAV基因治療的療效。
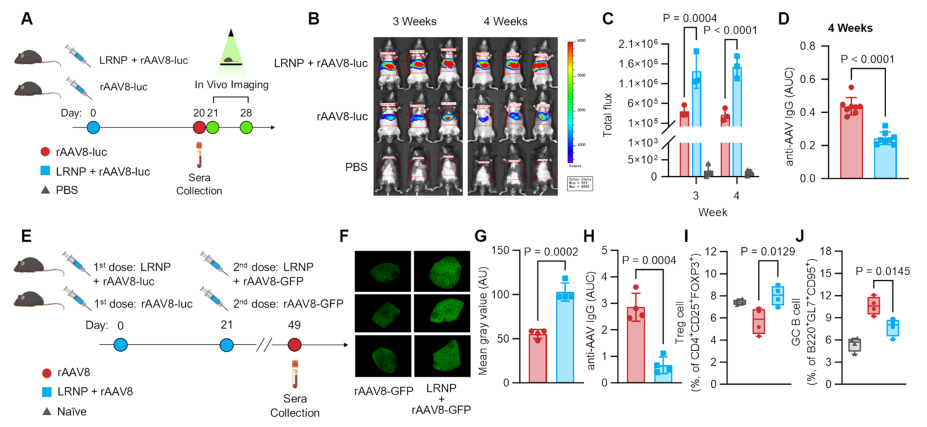
圖2. LRNP共處理增加AAV8載體轉(zhuǎn)基因表達(dá)
3. 納米疫苗的優(yōu)化與改進(jìn)
研究人員進(jìn)一步優(yōu)化了LRNPs的設(shè)計(jì),發(fā)現(xiàn)使用甘露糖修飾的LRNPs(MLRNPs)是緩解免疫反應(yīng)的較優(yōu)選擇,適用于真實(shí)生物制劑的進(jìn)一步挑戰(zhàn)。研究發(fā)現(xiàn)MLRNPs增強(qiáng)了肝APCs的耐受性,并誘導(dǎo)了更多的免疫調(diào)節(jié)性DN T細(xì)胞。MLRNPs在肝臟APCs中的攝取增加,進(jìn)一步增強(qiáng)了其對(duì)生物制劑的免疫耐受效果。
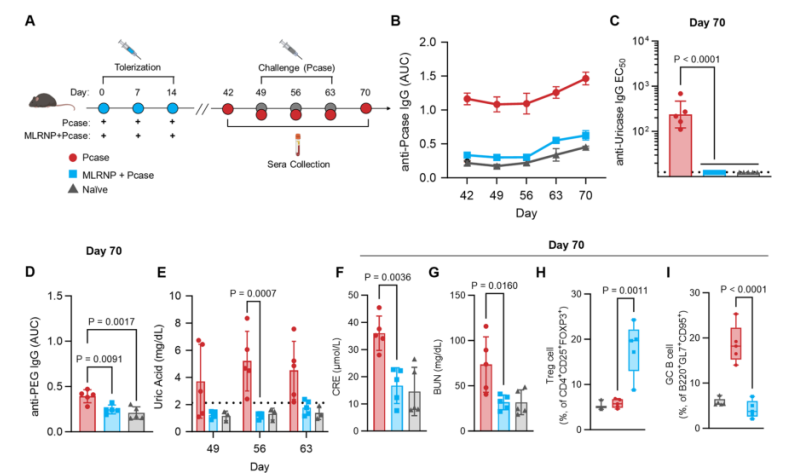
圖3. MLRNPs提高了聚乙二醇化尿酸酶治療的長期有效性
4. MLRNPs使AAV8載體重新給藥成為可能
為了確定甘露糖修飾的納米疫苗是否能夠成功地重新給藥AAV,研究人員首先將AAV8-Luc注射到小鼠體內(nèi),3周后將AAV8-SEAP注射到相同的動(dòng)物體內(nèi)。在單次注射AAV后,單獨(dú)治療的AAV組的所有小鼠在第7天都產(chǎn)生了衣殼特異性IgM。雖然未修飾的納米疫苗治療產(chǎn)生了IgM,但與單獨(dú)的AAV治療相比,增加的幅度顯著降低。在MLRNP組中,在八只小鼠中只有四只檢測(cè)到抗包膜IgM,表明降低了不必要的免疫反應(yīng)發(fā)生率。在AAV8-SEAP給藥后,觀察到IgM的AUC增加。然而,接受納米疫苗的小鼠IgM量明顯減少,特別是在MLRNP組中。進(jìn)一步研究發(fā)現(xiàn)納米疫苗和AAV8共給藥后,幾乎檢測(cè)不到抗體水平,這是由于肝臟中的APCs誘導(dǎo)耐受,然后是免疫調(diào)節(jié)DN T細(xì)胞和Tregs阻斷B細(xì)胞活化,但該策略在較長時(shí)間和較高劑量AAV治療下的轉(zhuǎn)基因效率仍有待闡明。
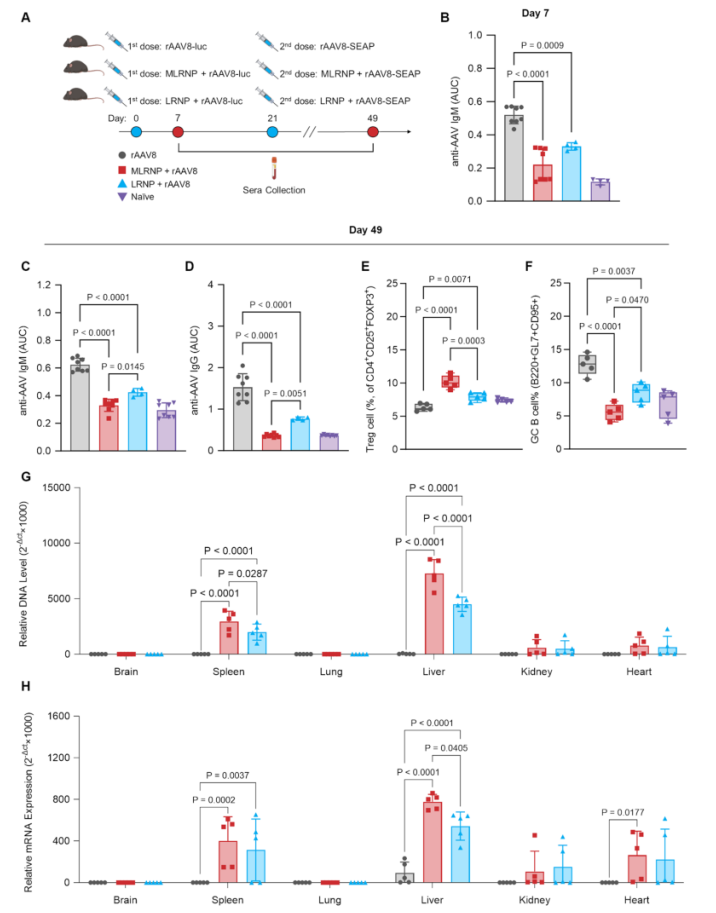
圖4. MLRNPs使AAV8載體重新給藥
02總結(jié)
這項(xiàng)研究成功開發(fā)了一種基于脂質(zhì)-雷帕霉素的納米疫苗,能夠有效克服生物療法中的抗藥抗體屏障。通過誘導(dǎo)免疫耐受,這種納米疫苗不僅能夠延長生物制劑的療效,還為AAV基因療法的重復(fù)給藥提供了可能。未來,這種納米疫苗有望在酶替代療法和基因治療中得到廣泛應(yīng)用,為患者帶來更持久的治療效果。
