回顧2025年,中喬新舟產(chǎn)品在科研領(lǐng)域影響力持續(xù)增強(qiáng),全年被SCI文獻(xiàn)引用的頻次穩(wěn)步攀升,平均影響因子達(dá)到6.61,實(shí)現(xiàn)了引用數(shù)量與學(xué)術(shù)質(zhì)量的雙重突破。產(chǎn)品所支持的研究覆蓋腫瘤學(xué)、分子生物學(xué)、免疫學(xué)、再生醫(yī)學(xué)、生物材料、組織工程及轉(zhuǎn)化醫(yī)學(xué)等多個(gè)前沿?zé)狳c(diǎn)領(lǐng)域,已成為國(guó)內(nèi)高校與科研機(jī)構(gòu)開(kāi)展高水平研究的信賴之選。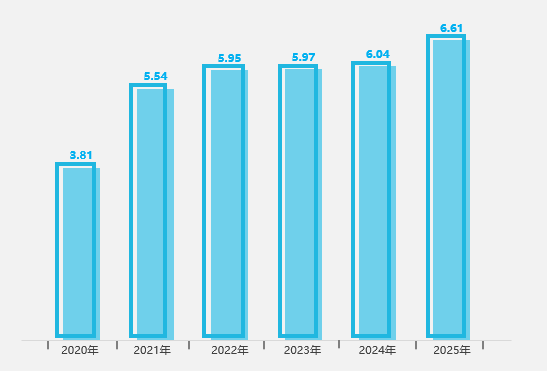
近6年度平均影響因子變化
2025年度國(guó)內(nèi)高分文獻(xiàn)前10及單位
| 標(biāo)題 | 發(fā)表時(shí)間 | DOI | 影響因子 | 單位 | |
 |
Magnetically actuated multimode... | 2025-09-05 | 10.1038/s41563-025-02340-5 | 38.5 | 中山大學(xué) |
 |
Macrophage PD-1 regulates ene... | 2025-12-10 | 10.1016/j.cmet.2025.11.009 | 30.9 | 哈爾濱醫(yī)科大學(xué)附屬第一醫(yī)院 |
 |
Zwitterionic Brush-Grafted Interf... | 2025-04-30 | 10.1002/adma.202501137 | 26.8 | 復(fù)旦大學(xué)附屬中山醫(yī)院 |
 |
Programmable Bacterial Architec... | 2025-05-22 | 10.1002/adma.202504206 | 26.8 | 西安電子科技大學(xué) |
 |
Engineering Highly Aligned and ... | 2025-01-15 | 10.1002/adma.202419380 | 26.8 | 西安交通大學(xué) |
 |
A Promising Biomimetic Hydrog... | 2025-09-28 | 10.1002/adma.202510602 | 26.8 | 西安電子科技大學(xué) |
 |
A chemical agonist and the Golg... | 2025-12-05 | 10.1016/j.jmmuni.2025.11.004 | 26.3 | 清華大學(xué) |
 |
N6-methyladenosine-regulated ... | 2025-05-15 | 10.1002/cac.2.70034 | 24.9 | 山東大學(xué)齊魯醫(yī)院 |
 |
NAT10 regulates tumor progress... | 2025-06-20 | 10.1002/cac.2.70045 | 24.9 | 江南大學(xué)附屬醫(yī)院 |
 |
Ultrasound-driven in situ self-ass... | 2025-12-16 | 10.1016/j.mattod.2025.12.006 | 22.0 | 蘇州大學(xué) |
本期精選十二月內(nèi)引用喬新舟產(chǎn)品的高質(zhì)量文獻(xiàn),并概述其核心研究?jī)?nèi)容,旨在為科研同仁呈現(xiàn)相關(guān)領(lǐng)域的前沿動(dòng)態(tài),助力把握最新研究進(jìn)展。精彩不容錯(cuò)過(guò)!
題目一
巨噬細(xì)胞 PD-1 介導(dǎo)免疫檢查點(diǎn)阻斷治療中能量代謝的消耗與功能紊亂調(diào)控
Macrophage PD-1 regulates energy expenditure and metabolic dysfunction under immune checkpoint blockade
期刊:Cell Metabolism|影響因子:30.9
DOI:10.1016/j.cmet.2025.11.009
發(fā)表時(shí)間:2025-12-10
發(fā)表單位:哈爾濱醫(yī)科大學(xué)
文章摘要
免疫檢查點(diǎn)抑制劑(ICI)療法會(huì)增加代謝綜合征的風(fēng)險(xiǎn);其基本機(jī)制仍然難以捉摸。我們表明,抗PD-1抗體針對(duì)巨噬細(xì)胞PD-1,降低能量消耗而不影響食物攝入,增強(qiáng)小鼠對(duì)高脂飲食(HFD)誘發(fā)的肥胖和系統(tǒng)性代謝疾病的易感性。從機(jī)制上講,脂多糖(LPS)激活Unc-51樣自噬,激活激酶1(ULK1),以一種依賴?yán)撩顾兀╩TOR)的哺乳動(dòng)物靶點(diǎn)。活化的ULK1磷酸化Thr250上的PD-1,通過(guò)破壞FBXO38-PD-1結(jié)合,抑制FBXO38介導(dǎo)的PD-1泛素化和降解。磷酸化的PD-1與肌醇需求酶1α(IRE1α)相互作用,并削弱IRE1α自磷酸化,以抑制內(nèi)質(zhì)網(wǎng)(ER)壓力介導(dǎo)的炎癥反應(yīng)。抑制IRE1α可緩解巨噬細(xì)胞特異性PD-1敲除小鼠中高血衰竭引起的代謝障礙,從而減少能量消耗。我們的發(fā)現(xiàn)凸顯了巨噬細(xì)胞PD-1在免疫檢查點(diǎn)阻斷、能量消耗和代謝功能障礙交匯處的關(guān)鍵作用。巨噬細(xì)胞PD-1的“兼職”功能可能為對(duì)抗ICI治療和高脂飲食引起的代謝疾病提供新的依據(jù)。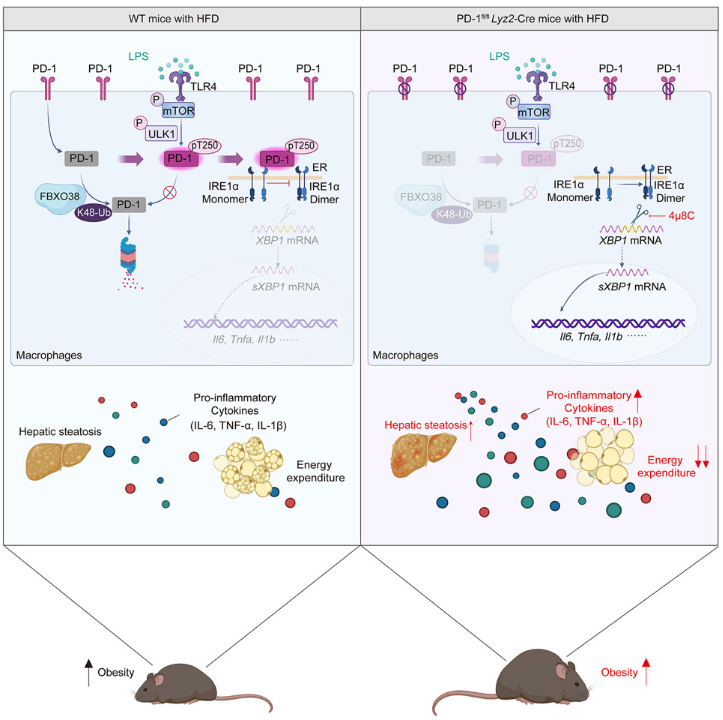
研究示意圖
Raw264.7小鼠單核巨噬細(xì)胞白血病細(xì)胞(貨號(hào):ZQ0098 )參與了該項(xiàng)研究。
題目二
化學(xué)激動(dòng)劑與高爾基體駐留脂質(zhì)PI4P通過(guò)誘導(dǎo)跨膜螺旋重排激活STING蛋白。
A chemical agonist and the Golgi-resident lipid PI4P activate STING by inducing transmembrane
 |
helix rearrangement期刊:IMMUNITY |影響因子:26.3
DOI:10.1016/j.immuni.2025.11.004
發(fā)表時(shí)間:2025-12-05
發(fā)表單位:清華大學(xué)
文章摘要
環(huán)狀GMP-AMP合成酶(cGAS)干擾素基因刺激因子(STING)信號(hào)通路在先天免疫中至關(guān)重要。最新研究強(qiáng)調(diào)了磷脂酰肌醇4-磷酸(PI4P)信號(hào)在高爾基體中對(duì)STING激活的重要性。然而,PI4P調(diào)控STING的具體分子機(jī)制仍不明確。本文報(bào)告了由PI4P和化學(xué)STING激動(dòng)劑GNE-6468觸發(fā)的STING激活機(jī)制。利用低溫電子顯微鏡,我們確定GNE-6468結(jié)合STING跨膜(TM)結(jié)構(gòu)域內(nèi)的一個(gè)特殊囊袋,促進(jìn)STING TM3螺旋向外運(yùn)動(dòng),而不改變配體結(jié)合域的構(gòu)象。值得注意的是,我們提供了STING結(jié)合PI4P和GNE-6468的結(jié)構(gòu)洞見(jiàn),這些結(jié)合共同誘導(dǎo)了STING寡聚化和STING介導(dǎo)的免疫反應(yīng)。功能性檢測(cè)進(jìn)一步證實(shí),STING、PI4P和GNE-6468之間的相互作用對(duì)STING激活至關(guān)重要。綜合來(lái)看,這些結(jié)果表明PI4P和GNE-6468能夠協(xié)同結(jié)合STING激活其信號(hào)傳導(dǎo),凸顯其治療潛力。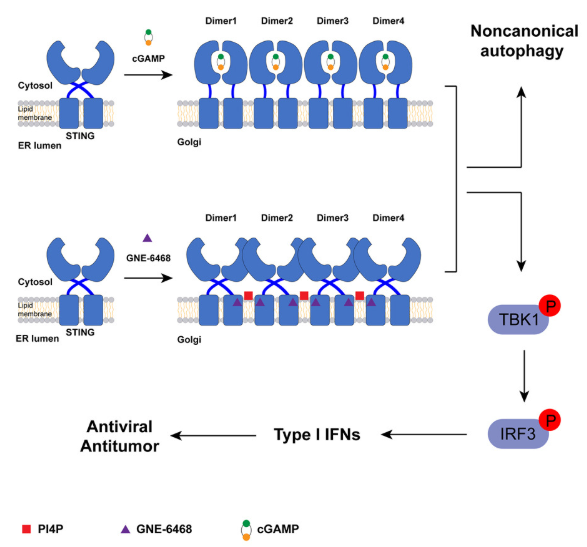
研究示意圖
中喬新舟生物的產(chǎn)品原代人外周血單核細(xì)胞(貨號(hào):PRI-H-00052)參與了該項(xiàng)研究。
題目三
超聲驅(qū)動(dòng)藥物水凝膠的原位自組裝用于增強(qiáng)肝動(dòng)脈灌注化療
Ultrasound-driven in situ self-assembly of drug hydrogel for enhanced hepatic artery infusion chemotherapy
期刊:Materials Today |影響因子:22
DOI:10.1016/j.mattod.2025.12.006
發(fā)表時(shí)間:2025-12-16
發(fā)表單位:江蘇大學(xué)
文章摘要
肝動(dòng)脈輸注化療(HAIC)為肝癌治療提供高濃度局部藥物,但面臨導(dǎo)管相關(guān)并發(fā)癥和全身毒性等挑戰(zhàn)。為此,我們開(kāi)發(fā)了Mel-gel,這是一種完全由化療劑Melphalan(Mel)形成的超聲驅(qū)動(dòng)水凝膠系統(tǒng),且未經(jīng)過(guò)化學(xué)修飾。在超聲波下,Mel從球形轉(zhuǎn)變?yōu)槿湎x(chóng)狀聚集體,通過(guò)非共價(jià)相互作用迅速形成基于納米纖維的水凝膠。這一創(chuàng)新系統(tǒng)實(shí)現(xiàn)了持續(xù)的藥物釋放、優(yōu)異的生物利用度和更優(yōu)的生物安全特性。Mel-gel使得導(dǎo)管拔除更快,降低全身毒性,提高局部藥物濃度,并延長(zhǎng)藥物與細(xì)胞的相互作用時(shí)間。與傳統(tǒng)HAIC系統(tǒng)相比,Mel-gel獨(dú)特的原位形成最大化了藥物遞送,并在復(fù)雜血管結(jié)構(gòu)中實(shí)現(xiàn)了更優(yōu)越的靶向。在大鼠正位肝癌模型中,Mel凝膠輔助HAIC展現(xiàn)出顯著療效,腫瘤抑制率達(dá)98.09%,激活抗腫瘤免疫反應(yīng),并治愈了60%的治療大鼠。這種新型超聲響應(yīng)水凝膠代表了肝癌治療的有前景進(jìn)展,提供了更高的精準(zhǔn)度、療效和安全性。此外,Mel-gel多樣化的藥物遞送能力可能提升多種藥物的藥代動(dòng)力學(xué),并支持協(xié)同療法。這種新型水凝膠系統(tǒng)為肝炎治療帶來(lái)了有前景的進(jìn)步,旨在優(yōu)化治療效果并擴(kuò)大其在其他治療藥物中的應(yīng)用。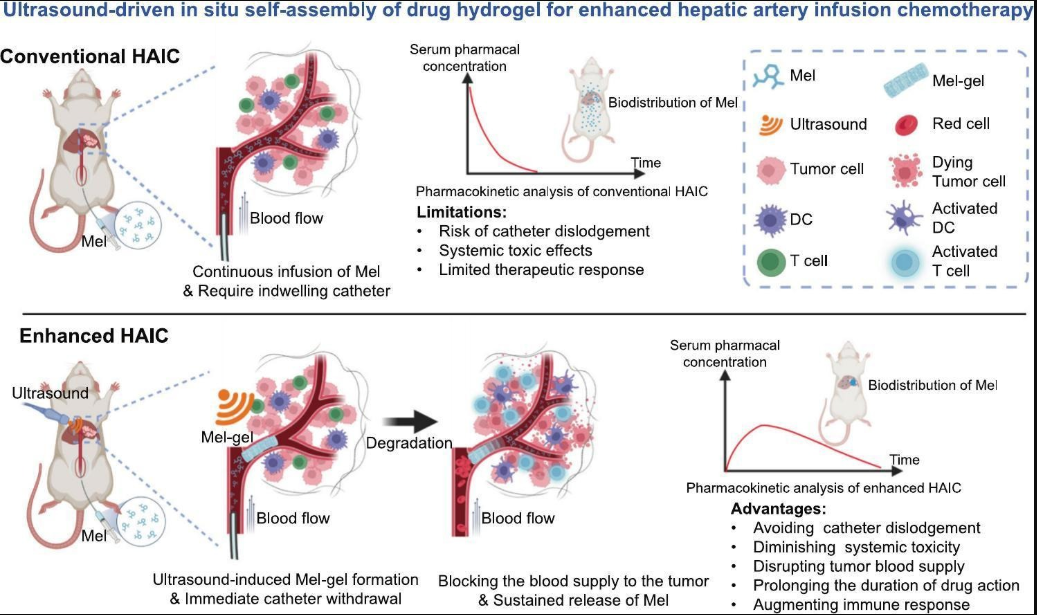
研究示意圖
中喬新舟生物的產(chǎn)品H22小鼠肝癌細(xì)胞系肌成纖維細(xì)胞永生化(貨號(hào):ZQ0109 )參與了該項(xiàng)研究。
題目四
代謝支持可保護(hù)黏膜免受放射性黏膜炎中的鐵死亡損傷
Metabolic support protects mucosa from ferroptosis in radiation-induced mucositis
期刊:Nature Communications|影響因子:15.7
DOI:10.1038/s41467-025-67214-5
發(fā)表時(shí)間:2025-12-08
發(fā)表單位:第四軍醫(yī)大學(xué),陜西
文章摘要
電離放療在治療癌癥方面有效,但會(huì)對(duì)黏膜造成顯著損傷,從而增加患者的不適,延遲治療,并提高死亡風(fēng)險(xiǎn)。這種損傷的根本機(jī)制仍然不清楚,目前的治療大多是姑息性的。本研究確定鐵磷遁是導(dǎo)致輻射誘導(dǎo)口腔黏膜上皮細(xì)胞耗盡的主要細(xì)胞死亡方式。值得注意的是,在輻射暴露后的早期階段還發(fā)現(xiàn)了代償期,在此期間成纖維細(xì)胞提供關(guān)鍵的代謝支持。具體來(lái)說(shuō),成纖維細(xì)胞提供多胺,這些多胺能被基底上皮細(xì)胞迅速吸收,保護(hù)其免受鐵剝蝕。補(bǔ)充多氨類藥物被發(fā)現(xiàn)能有效預(yù)防黏膜損傷。這些發(fā)現(xiàn)凸顯了成纖維細(xì)胞介導(dǎo)的代謝支持在保護(hù)口腔黏膜免受輻射損傷中的關(guān)鍵作用,并為增強(qiáng)身體內(nèi)在保護(hù)機(jī)制免受輻射相關(guān)疾病的啟示提供了見(jiàn)解。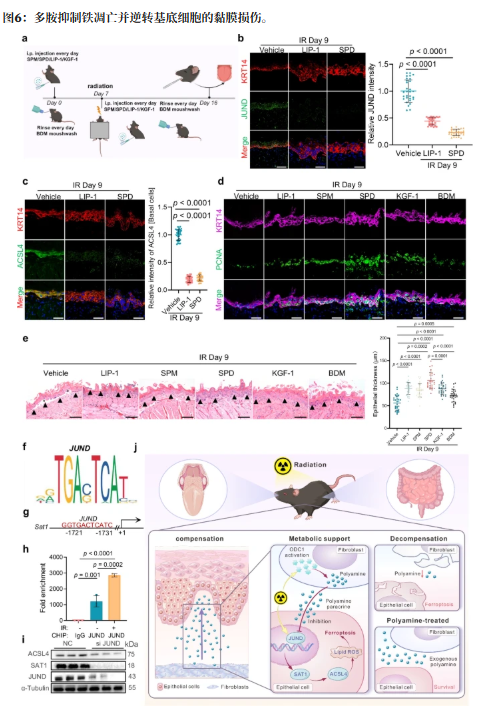

中喬新舟生物的產(chǎn)品原代人口腔角質(zhì)形成細(xì)胞(貨號(hào):PRI-H-00140 )參與了該項(xiàng)研究。
題目五
內(nèi)體-吞噬體連接組裝體介導(dǎo)膜蛋白/胞外蛋白降解
Endosome-phagophore linking assemblies for the degradation of membrane/extracellular proteins
期刊:Nature Communications|影響因子:15.7
DOI:10.1038/s41467-025-67805-2
發(fā)表時(shí)間:2025-12-22
發(fā)表單位:蘇州大學(xué)
文章摘要
溶酶體靶向嵌合體特異性降解膜/細(xì)胞外蛋白,其特異性和效力高度依賴于溶酶體靶向受體的表達(dá)模式和動(dòng)力學(xué)。本文描述一種內(nèi)體-吞噬連接組裝(EPLA),該組裝體通過(guò)將目標(biāo)蛋白(POI)的特定配體連接到由pH值較低的插入肽和噬噬結(jié)合元件組成的內(nèi)核體表面錨定吞噬蛋白(ES-PTP)構(gòu)成。EPLA通過(guò)與POI結(jié)合、內(nèi)化到內(nèi)體、插入內(nèi)體膜、將針對(duì)吞噬的基部錨定在內(nèi)體表面,從而觸發(fā)內(nèi)體與吞噬體的空間接近來(lái)降解蛋白質(zhì)。我們通過(guò)降解膜結(jié)合的PD-L1、RAGE、GRP94、PSMA、ICAM-1、p32、VCAM-1和LRP1,以及細(xì)胞外淀粉樣蛋白β和tau,展示了EPLA技術(shù)的模塊化性和通用性。我們的研究結(jié)果為膜/胞外POIs的自噬降解奠定了技術(shù)基礎(chǔ),這可能對(duì)生化研究和臨床治療產(chǎn)生廣泛影響。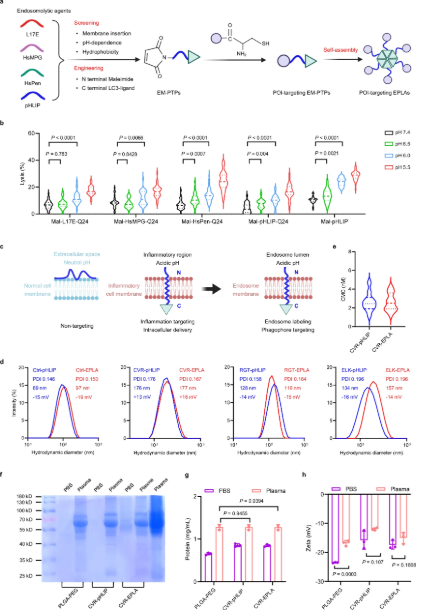
研究示意圖
中喬新舟生物的產(chǎn)品293T人胚腎細(xì)胞(貨號(hào):ZQ0033 )參與了該項(xiàng)研究。