頂刊高光?輝煌里程碑
中喬新舟助力成果榮登國際頂刊,影響因子 42.5 再創(chuàng)新高!熱烈祝賀!
l 文獻(xiàn)標(biāo)題:Hijacking ERAD for targeted degradation of transmembrane proteins
l 研究單位:復(fù)旦大學(xué)發(fā)表
l 期刊:CELL
l 影響因子:42.5

期刊名稱:《CELL》
靶向蛋白降解(TPD)技術(shù)為藥物發(fā)現(xiàn)提供了巨大機(jī)遇,但降解跨膜(TM)靶點(diǎn)仍然充滿挑戰(zhàn)。由于TM蛋白在內(nèi)質(zhì)網(wǎng)膜上規(guī)范地折疊,我們假設(shè)利用ER相關(guān)降解(ERAD)可能實(shí)現(xiàn)TM蛋白的高效降解。在此,我們建立了一種TPD技術(shù),將其命名為ERAD結(jié)合嵌合體(ERADECs),能夠高效降解TM靶點(diǎn)。我們鑒定了地奈德是SYVN1的結(jié)合劑,SYVN1是一種介導(dǎo)ERAD的ER E3連接酶。我們通過將去sonide與已知的PD-L1配體連接,設(shè)計了針對程序性死亡配體1(PD-L1)的ERADECs,并以高效能觀察到SYVN1和ERAD依賴的PD-L1降解。在功能上,這些ERADEC在腫瘤抑制和PD-L1降低作用上表現(xiàn)得比臨床使用的PD-L1抗體更為顯著。ERADEC的概念也可擴(kuò)展到其他膜靶點(diǎn)。我們共同建立了一種平臺技術(shù),利用ERAD以極高的效率選擇性降解TM靶點(diǎn)。
我們榮幸地向長期使用中喬新舟細(xì)胞以及專用培養(yǎng)基的合作伙伴致以熱烈祝賀由復(fù)旦大學(xué)研究團(tuán)隊(duì)完成的成果《Hijacking ERAD for targeted degradation of transmembrane proteins》發(fā)表于國際知名期刊《CELL》(IF=42.5)。在該研究中,作者團(tuán)隊(duì)選用了中喬新舟提供的A-375人惡性黑色素瘤細(xì)胞專用培養(yǎng)基(貨號:ZM0042),NCI-H1975人肺腺癌細(xì)胞專用培養(yǎng)基(貨號:ZM0395),MDA-MB-231人乳腺癌細(xì)胞(貨號:ZQ0118),NCI-H1975人肺腺癌細(xì)胞(貨號:ZQ0395),A375人惡性黑色素瘤細(xì)胞(貨號:ZQ0042)用于關(guān)鍵細(xì)胞模型的培養(yǎng)。
 A-375人惡性黑色素瘤細(xì)胞專用培養(yǎng)基(買二送一,三瓶到手678)
A-375人惡性黑色素瘤細(xì)胞專用培養(yǎng)基(買二送一,三瓶到手678)
中喬新舟®貨號:ZM0042
 NCI-H1975人肺腺癌細(xì)胞專用培養(yǎng)基
NCI-H1975人肺腺癌細(xì)胞專用培養(yǎng)基
中喬新舟®貨號:ZM0395
A375人惡性黑色素瘤細(xì)胞(STR鑒定)
[細(xì)胞+500ml專培套餐促銷]:980¥
中喬新舟®貨號:ZQ0042
MDA-MB-231人乳腺癌細(xì)胞(STR鑒定)
[細(xì)胞+500ml專培套餐促銷]:980¥
中喬新舟®貨號:ZQ0118
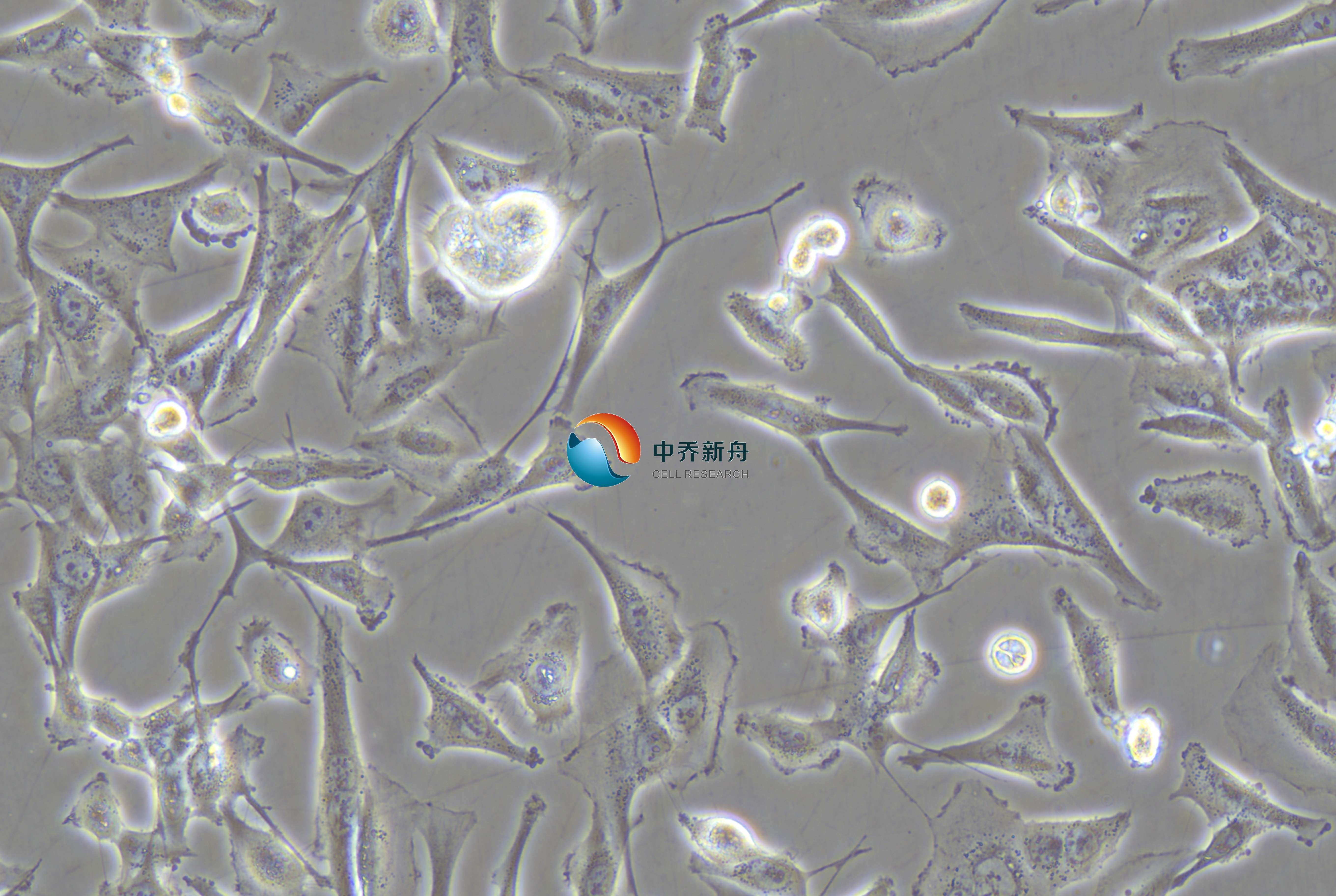
NCI-H1975人肺腺癌細(xì)胞(STR鑒定)
[細(xì)胞+500ml專培套餐促銷]:980¥
中喬新舟®貨號:ZQ0395
一、研究背景與科學(xué)問題
靶向蛋白降解(TPD)技術(shù),如蛋白水解靶向嵌合體(PROTACs),劫持細(xì)胞內(nèi)降解機(jī)制以選擇性降解目標(biāo)蛋白,并為藥物發(fā)現(xiàn)提供了有前景的新途徑。同時,這些方法在降解大多數(shù)跨膜(TM)蛋白方面面臨挑戰(zhàn),因?yàn)檫@些蛋白在很大程度上無法被這些TPD策略所啟動的降解機(jī)制接觸到。由于TM蛋白的重要性,科學(xué)家們已建立了幾種針對它們的TPD策略,例如溶酶體靶向嵌合體(LYTACs)、共價工程化納米抗體嵌合體(GlueTACs)、和轉(zhuǎn)鐵蛋白受體靶向嵌合體(TransTACs)等,它們開辟了前所未有的機(jī)會。同時,所有這些技術(shù)都依賴于內(nèi)體-溶酶體途徑,因此受到回收內(nèi)體的影響,這些內(nèi)體傾向于將TM目標(biāo)回收回去,從而降低它們的降解效率。此外,這些目標(biāo)蛋白還會不斷被內(nèi)含新合成蛋白的細(xì)胞內(nèi)囊泡補(bǔ)充。最后,大多數(shù)TPD策略使用大分子生物物質(zhì)如抗體,而小分子化合物可能提供若干優(yōu)越特性,如更易遞送、更低成本、多用途應(yīng)用途徑、長儲存穩(wěn)定性,且通常不具有免疫原性。因此,建立能夠高效降解TM目標(biāo)的小分子TPD策略是非常需要的。大多數(shù)TM蛋白在合成過程中通常在內(nèi)質(zhì)網(wǎng)(ER)中折疊。然后它們被打包進(jìn)囊泡用于運(yùn)輸?shù)礁郀柣w,隨后再到質(zhì)膜,在此過程中它們在孤立狀態(tài)下大多無法被降解酶和降解機(jī)制接觸。因此,它們通常對當(dāng)前劫持細(xì)胞內(nèi)降解機(jī)制(如泛素-蛋白酶體系統(tǒng)(UPS)或自噬)的降解劑具有抗性。與此同時,由于跨膜(TM)蛋白通常在內(nèi)質(zhì)網(wǎng)(ER)中正確折疊,它們可以被ER相關(guān)降解(ERAD)所接觸。
二、核心優(yōu)勢
本研究建立“一種劫持ERAD的TPD策略“,ERAD是一條關(guān)鍵的降解通路,能夠通過多種不同途徑降解TM蛋白、分泌蛋白或錯誤折疊的胞質(zhì)蛋白。ERAD由內(nèi)質(zhì)網(wǎng)膜相關(guān)的E3連接酶(ER-E3)通過對目標(biāo)蛋白的多泛素化(poly-Ub)啟動。在多泛素化之后,底物被p97/VCP(含瓜氨酸蛋白)ATP酶轉(zhuǎn)運(yùn)到胞質(zhì)區(qū),并在提取過程中由p97/VCP結(jié)合的去泛素化酶(DUBs)去泛素化,然后底物重新被泛素化并靶向蛋白酶體降解。在TPD領(lǐng)域中,ERAD在很大程度上被忽視,并且此前沒有利用ERAD劫持的TPD方法。團(tuán)隊(duì)假設(shè),與ER-E3和目標(biāo)蛋白同時相互作用的化學(xué)嵌合體可能通過ERAD觸發(fā)選擇性降解,這在TPD中尚未被利用。基于這一假設(shè)以及意外發(fā)現(xiàn)的可與主要ER-E3 SYVN1相互作用的化學(xué)配體,建立了一種劫持ERAD的TPD策略,稱為ERAD-介導(dǎo)的嵌合體(ERADECs)。
三、實(shí)驗(yàn)方法與主要結(jié)果
1. 去索尼德被鑒定為SYVN1結(jié)合化合物
研究團(tuán)隊(duì)最近確定地塞尼德(desonide)是一種針對亨廷頓病(Huntington’s disease)致病突變型HTT蛋白(mHTT)的小分子降解劑。地塞尼德誘導(dǎo)mHTT多泛素化(poly-Ub)以增強(qiáng)其降解,因此我們使用小干擾RNA(siRNA)敲低測試了可能直接與mHTT相互作用的多泛素化相關(guān)酶的潛在參與(圖S1A和S1B)。這些酶的選擇基于HDinHD數(shù)據(jù)庫,并通過文獻(xiàn)確認(rèn)其在mHTT降解中可能的參與,這一作用通過地塞尼德誘導(dǎo)降低HEK293T細(xì)胞中外源表達(dá)的mHTT exon1 Q72片段來測量(圖S1A)。敲低SYVN1完全抵消了地塞尼德處理對mHTT水平的下降,提示SYVN1的參與(圖S1B),SYVN1是酵母Hrd1的哺乳動物同源物,也是ERAD中發(fā)揮主要作用的內(nèi)質(zhì)網(wǎng)E3。我們進(jìn)一步通過測試mHTT的多泛素化證實(shí)了這一點(diǎn),地塞尼德處理增強(qiáng)了多泛素化,而敲低SYVN1后這種效應(yīng)幾乎被阻斷(圖1A)。我們觀察到地塞尼德誘導(dǎo)的高分子量血凝素(HA)條帶增加,這與通過過表達(dá)泛素導(dǎo)致的mHTT多泛素化增加相對應(yīng)(圖S1C),從而確認(rèn)地塞尼德誘導(dǎo)mHTT多泛素化。為了測試其潛在機(jī)制,我們進(jìn)行了共免疫沉淀(coIP),觀察到地塞尼德處理增強(qiáng)了mHTT與SYVN1的相互作用(圖1B)。K6R突變(Q72K6R)對地塞尼德具有抗性,并且是已知的地塞尼德結(jié)合蛋白——糖皮質(zhì)激素。
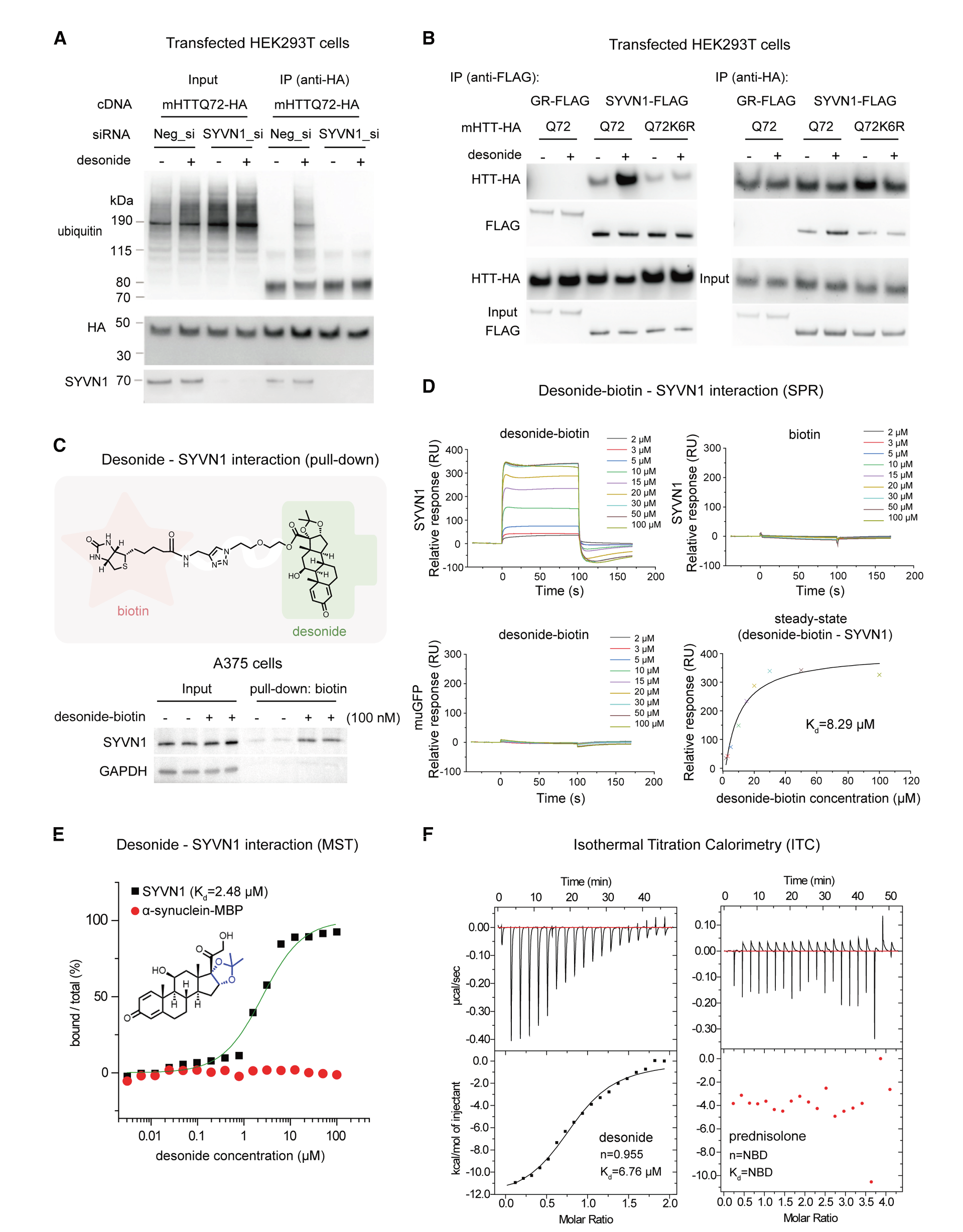 圖1:地索奈德直接與SYVN1相互作用
圖1:地索奈德直接與SYVN1相互作用
l (A) 使用HEK293T細(xì)胞進(jìn)行代表性免疫沉淀-西方印跡實(shí)驗(yàn),這些細(xì)胞轉(zhuǎn)染了所示的cDNA質(zhì)粒(24小時)和siRNA(48小時),然后用3 μM地索尼德(+)或含100 nM環(huán)氧霉素聯(lián)合處理的DMSO(-)對照處理24小時。
l (B) 使用HEK293T細(xì)胞進(jìn)行代表性免疫沉淀-西方印跡實(shí)驗(yàn),這些細(xì)胞轉(zhuǎn)染了GR-FLAG、SYVN1-FLAG和mHTT-HA cDNA質(zhì)粒(36小時),然后僅用3 μM地索尼德(+)或DMSO(-)對照處理2小時,以避免隨后降解。
l (C) 代表性下拉實(shí)驗(yàn),使用地塞米松-生物素(+)或生物素對照(-)與 A375 細(xì)胞孵育,通過西方印跡確認(rèn)其與 SYVN1 的相互作用。
l (D) 使用重組純化蛋白的代表性表面等離子體共振(SPR)檢測結(jié)果顯示,地塞米松-生物素而非生物素可直接與 SYVN1 相互作用。muGFP 蛋白被用作對照蛋白。
l (E) 類似于 (D),但使用 MST 測定法測試 desonide-SYVN1 相互作用。α-突觸核蛋白-MBP 蛋白被用作對照蛋白。
l (F) 類似于 (E),但使用 ITC 測定法。在本圖及以下圖的所有 Western 印跡中,未裁剪的凝膠圖像顯示在 Data S1 中。
2. 基于地塞米松的ERADECs能夠降低PD-L1蛋白水平
研究團(tuán)隊(duì)考慮將地塞米松連接到已知的TM蛋白靶點(diǎn)的配體/抑制劑上,以驗(yàn)證ERADEC的概念。通過比較地塞米松和其他保留或消除了SYVN1結(jié)合的GR激動劑的結(jié)構(gòu)(圖1E、1F、S1E和S1F),并考慮到將生物素連接到地塞米松的C-20位置并未破壞SYVN1結(jié)合(圖1C),C-21羥基可能不是SYVN1結(jié)合所必需的,并可用于連接鏈接物以合成潛在的ERADEC。 因此,我們通過將地塞米松與PD-L1配體BMS-202連接(圖2A),生成了靶向程序性死亡配體1(PD-L1)的ERADEC,并測試了它們對PD-L1水平的影響(圖2B和2C)。值得注意的是,10種不同的靶向PD-L1的ERADEC(P-ERADEC P1–P4和P8–P13)在MDA-MB-231和A375細(xì)胞中以pM–nM濃度范圍顯著降低了PD-L1水平(圖2B和2C;數(shù)據(jù)S2A和S2B)。然而,一些僅含柔性聚乙二醇(PEG)鏈接物的P-ERADEC(P5–P7)未能降低PD-L1(圖2C;數(shù)據(jù)S2B)。大多數(shù)有效的含酯鏈接物的P-ERADEC表現(xiàn)出亞nM的DC50和>90%的Dmax,而含酰胺鏈接物的P-ERADEC P12和P13對細(xì)胞內(nèi)水解更具抵抗力,其效力和效能類似(圖2B和2C)。我們進(jìn)一步通過流式細(xì)胞術(shù)分析完整A375細(xì)胞確認(rèn)了質(zhì)膜PD-L1水平的下降(圖2D)。P2誘導(dǎo)的PD-L1下降相對較慢(超過12小時)(圖2E),這可能是因?yàn)镋RADEC主要直接降解靶蛋白的內(nèi)質(zhì)網(wǎng)池而非跨膜池。
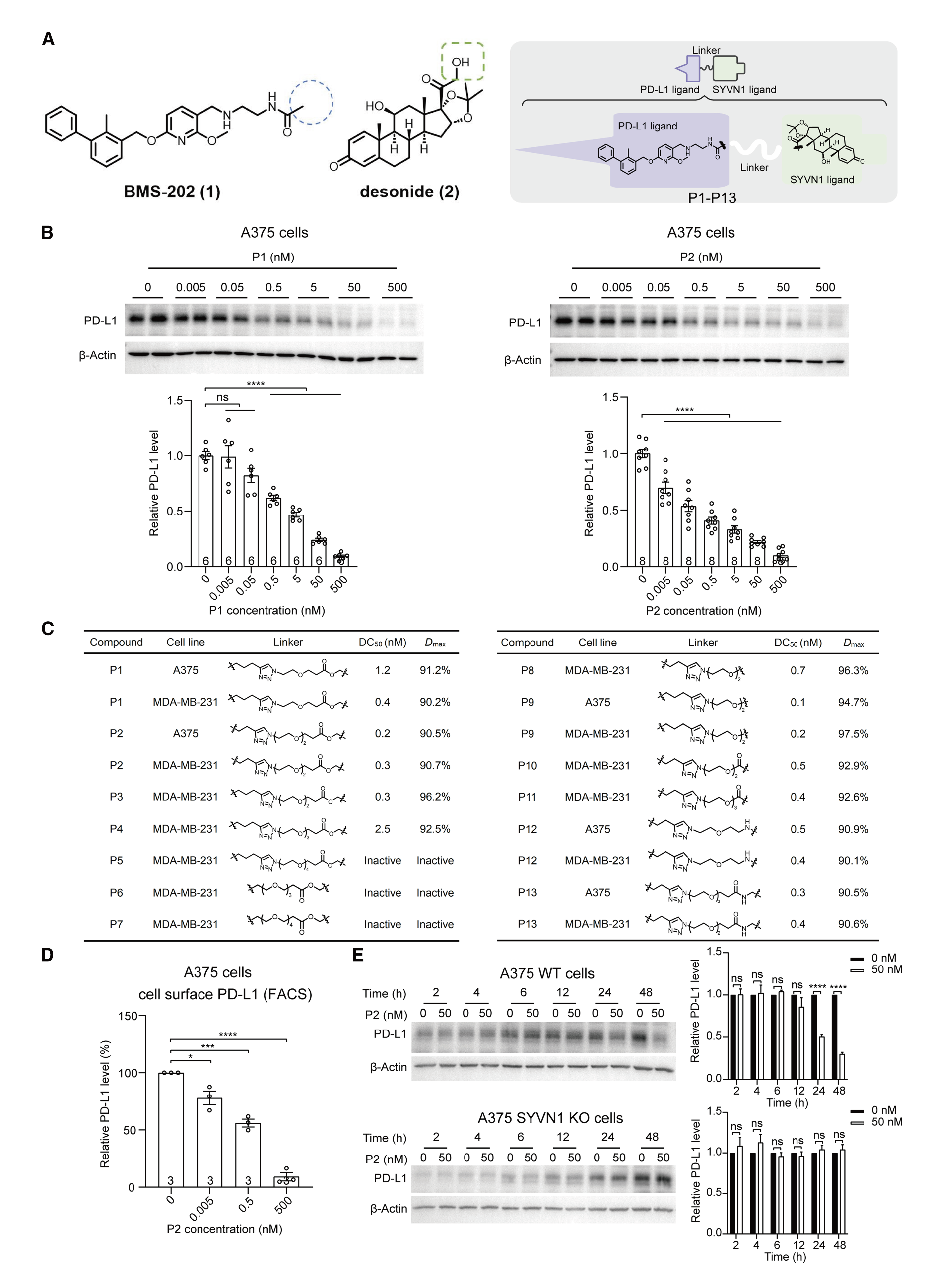
圖2. 基于地塞米松的ERADECs降低A375細(xì)胞中的PD-L1蛋白水平
l (A) P-ERADECs 的化合物設(shè)計圖和二維結(jié)構(gòu)。
l (B) 使用 A375 細(xì)胞在分別用指定濃度的 P1 或 P2 處理 48 小時后的代表性西方印跡及定量結(jié)果。
l (C) P-ERADECs 的 PD-L1 DC50(半最大降解濃度)和 Dmax(最大降解)的表格
l (D) 用流式細(xì)胞術(shù)分析 A375 細(xì)胞在用指定濃度 P2 處理 48 小時后的質(zhì)膜 PD-L1 蛋白水平。
l (E) 使用 A375 野生型(WT)細(xì)胞和 A375 SYVN1 敲除(KO)細(xì)胞,在有或沒有 50 nM P2 處理不同時間(分別為 2、4、6、12、24 和 48 小時)下的代表性西方印跡及定量分析。所有柱狀圖表示平均值 ± SEM。ns,p > 0.05;*p < 0.05,**p < 0.01,***p < 0.001,****p < 0.0001
3. ERADECs 通過 SYVN1 和 ERAD 降低 PD-L1 蛋白水平
關(guān)于ERADECs特異性的一個擔(dān)憂是,我們當(dāng)前的彈頭,它可以作用于SYVN1,同時也是一個GR激動劑。GR不太可能介導(dǎo)降解效應(yīng),因?yàn)槭褂昧硪环NGR激動劑潑尼松龍的化合物未能引起靶標(biāo)降解。
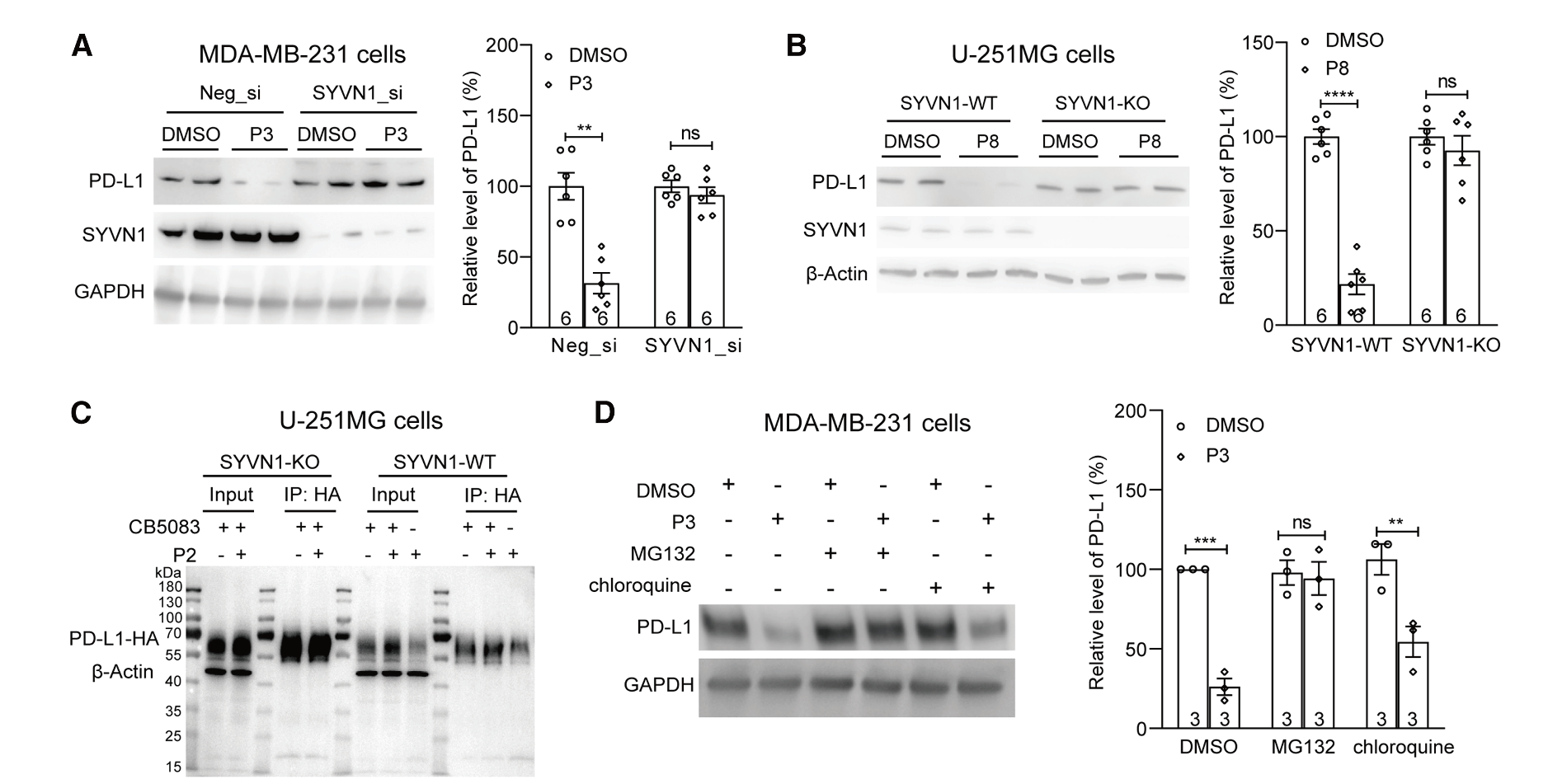
圖3. ERADECs 通過 SYVN1 和 ERAD 降低 PD-L1 蛋白水平
l (A) 在 MDA-MB-231 細(xì)胞中轉(zhuǎn)染所示 siRNA 48 小時后,再用 500 nM P3 或 DMSO 對照處理 24 小時,對 PD-L1 水平進(jìn)行代表性免疫印跡及定量分析。
l (B) 類似于 (A),但使用 U-251MG 細(xì)胞,有或沒有 SYVN1 基因敲除,處理 500 nM P8。
l (C) 使用轉(zhuǎn)染表達(dá) PD-L1-HA 和泛素質(zhì)粒的 U-251MG 細(xì)胞進(jìn)行代表性免疫共沉淀-免疫印跡及定量分析,以檢測 P2 誘導(dǎo)的 PD-L1 多聚泛素化。A375 細(xì)胞用 50 nM P2 處理 6 小時以誘導(dǎo)多聚泛素化,并用 500 nM CB5083 處理以防止多聚泛素化 PD-L1 的降解。
l (D) MDA-MB-231 細(xì)胞用所示化合物處理 48 小時后進(jìn)行代表性免疫印跡及定量分析。P3,500 nM;MG132,1 μM;氯喹 (CQ),20 μM。
4. ERADECs 在涉及 Tyr227 的 TM 囊口中與 SYVN1 相互作用,并誘導(dǎo)三元復(fù)合物的形成
鑒于KDM5B促進(jìn)糖酵解,我們首先試圖將這一代謝性狀與下游信號傳導(dǎo)聯(lián)系起來。TCGA-PRAD數(shù)據(jù)集的GSEA顯示,高KDM5B表達(dá)組中“通過切合體進(jìn)行替代mRNA剪接”通路富集(ES = 0.6876,NP = 0.0000)。這促使我們假設(shè)KDM5B驅(qū)動的乳酸積累可能影響AR切割,從而產(chǎn)生抗性相關(guān)變異體AR-V7。支持這一觀點(diǎn)的是,在我們的小鼠CDX模型中,KDM5B敲低細(xì)胞的腫瘤組織乳酸水平較低。當(dāng)腫瘤組織接受乳酸處理時,AR-V7 mRNA水平隨時間和劑量變化增加,確立乳酸與AR-V7表達(dá)之間的直接聯(lián)系。
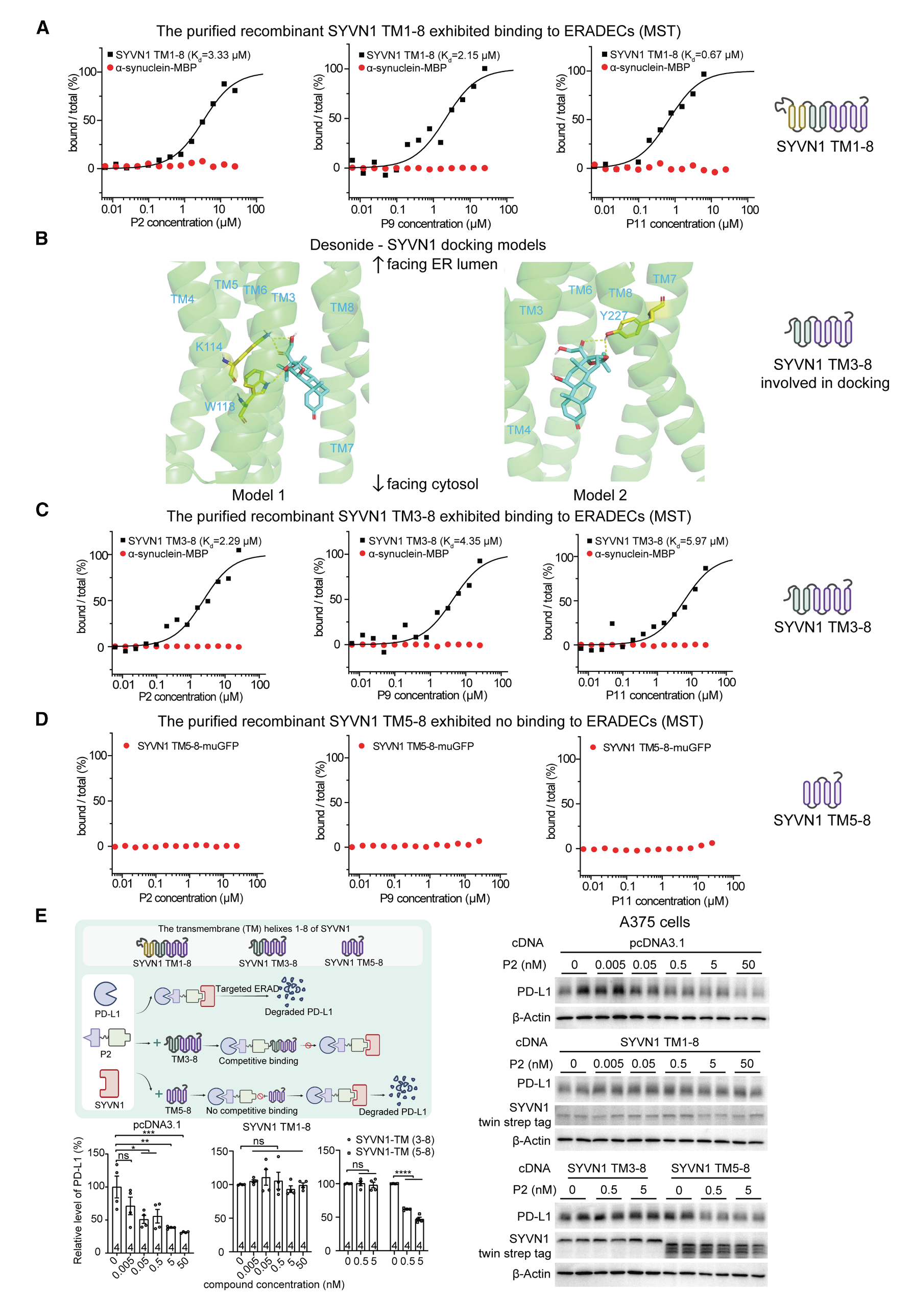
圖4. P-ERADECs 可能結(jié)合在 SYVN1 的 TM 域中的 TM3–8 口袋處
l (A) 代表性 MST 實(shí)驗(yàn)結(jié)果顯示,純化的重組 SYVN1 TM1–8 域?qū)λ镜?P-ERADECs 表現(xiàn)出結(jié)合。
l (B) Desonide(碳原子顯示為青色)與 SYVN1(碳原子顯示為綠色)的前兩個分子對接模型。圖中顯示了 TM 結(jié)構(gòu)、氫鍵長度(埃)、以及參與的殘基(碳原子顯示為黃色)。
l (C 和 D) 類似于 (A),但使用所示的 SYVN1 TM 片段。
l (E) 使用過表達(dá)的 SYVN1 TM 片段進(jìn)行競爭實(shí)驗(yàn)。對轉(zhuǎn)染了所示質(zhì)粒并在之后用 P2 處理 48 小時的 A375 細(xì)胞進(jìn)行的 Western 印跡及定量分析證實(shí)了競爭現(xiàn)象。柱狀圖表示均值 ± SEM。ns, p > 0.05;*p < 0.05,**p < 0.01,***p < 0.001,****p < 0.0001。另見圖 S4–S7
5. PD-L1 ERADECs 的特異性
我們進(jìn)一步基于模型1和模型2,通過LigPlot分析了可能與地索尼德相互作用的SYVN1氨基酸(圖5A)。我們在一個構(gòu)建體中(SYVN1-5mut)或在各自的單獨(dú)構(gòu)建體中進(jìn)行預(yù)測參與地索尼德與SYVN1結(jié)合的關(guān)鍵氨基酸突變(E87A、W118F、Y227F、L250S和Q254A)(圖5A),并在SYVN1敲除的U-251MG細(xì)胞中表達(dá)這些突變體或野生型(WT)全長SYVN1,以測試它們是否能夠恢復(fù)P-ERADEC的作用。與模型1預(yù)測的結(jié)合位點(diǎn)不一致,但與模型2預(yù)測一致,將全長SYVN1表達(dá)在SYVN1 KO U-251MG細(xì)胞中恢復(fù)了P-ERADEC P2處理下PD-L1的下降作用,而表達(dá)Y227F突變體或5突變SYVN1形式則未能實(shí)現(xiàn)這一點(diǎn)(圖5B、5C和S4E),將降解作用與化合物-SYVN1相互作用位點(diǎn)聯(lián)系起來,進(jìn)一步確認(rèn)了SYVN1的參與。結(jié)合位點(diǎn)通過直接生物物理實(shí)驗(yàn)檢測二元結(jié)合(通過MST和ITC)得到了進(jìn)一步確認(rèn)(圖5D和5E)。
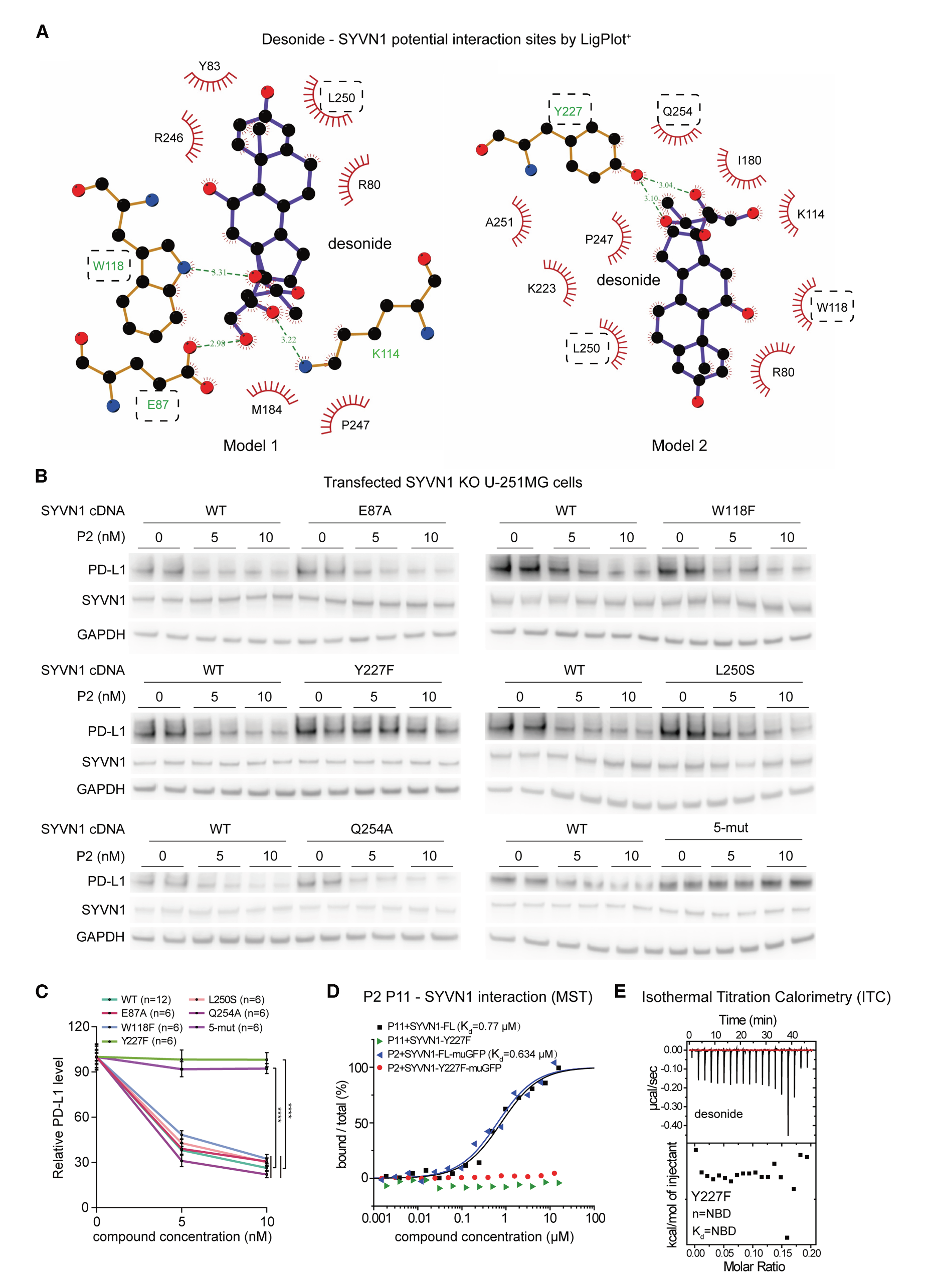 圖5. P-ERADECs可能與SYVN1的Y227相互作用以誘導(dǎo)靶向降解
圖5. P-ERADECs可能與SYVN1的Y227相互作用以誘導(dǎo)靶向降解
l 蛋白質(zhì)穩(wěn)定性分析。用WT或K179R突變hnRNPA1重構(gòu)的hnRNPA1-KO EnzR細(xì)胞,使用蛋白質(zhì)合成抑制劑環(huán)己酰亞胺(CHX)(40微分)處理,可加乳酸或無乳酸(20微分)。西方印跡(A)和hnRNPA1半衰期(B)定量顯示乳酸穩(wěn)定WT,但不穩(wěn)定K179R hnRNPA1。
l 體內(nèi)泛素化檢測。Flag-hnRNPA1的泛素化在EnzR細(xì)胞中低于親本細(xì)胞(C)。乳酸處理(20uM)減少,而氧酸鈉(20uM)增加,hnRNPA1泛素化(D)。
l (A) 前兩名對接模型的配體-受體相互作用的計算機(jī)預(yù)測。綠色標(biāo)記的殘基參與氫鍵,其他殘基參與疏水相互作用。突變實(shí)驗(yàn)中的突變氨基酸以黑圈標(biāo)出。
l (B和C) 使用SYVN1敲除的U-251MG細(xì)胞,將其轉(zhuǎn)染SYVN1 cDNA(有或沒有所示點(diǎn)突變的WT)24小時后,并用P2處理24小時的代表性免疫印跡(B)及其定量(C)。柱狀圖表示平均值 ± SEM。****p < 0.0001。
l (D) 使用重組純化蛋白的代表性MST實(shí)驗(yàn)結(jié)果顯示,SYVN1而非Y227F突變體表現(xiàn)出與P-ERADEC (P2或P11)的結(jié)合。
l (E) 類似于(D),但使用ITC檢測地塞米松的結(jié)合。NBD,未檢測到結(jié)合。另見圖S5–S7。
四、總結(jié)
該研究建立了一種新型TPD策略,稱為ERADECs,它劫持了ERAD,這是一個尚未在其他TPD中利用的細(xì)胞內(nèi)降解途徑。多種P-ERADECs表現(xiàn)出亞納摩爾級的DC50和超過90%的D max,明顯優(yōu)于傳統(tǒng)基于細(xì)胞質(zhì)E3的PD-L1靶向PROTACs,這些傳統(tǒng)方法通常表現(xiàn)為大于1 μM的DC50和約60%的D max。這可能是因?yàn)镻D-L1在ER中折疊,因此對細(xì)胞質(zhì)E3連接酶的可及性有限。膜PD-L1的自然半衰期約為3小時,表明膜中PD-L1部分降解迅速,降低了降解劑提升其降解的空間。總野生型PD-L1的半衰期約為17–18小時,稍長于P-ERADECs發(fā)揮作用所需的時間。ERADECs的體內(nèi)療效令人期待,表明具有良好的治療潛力。考慮到用于靶向ERADECs的SYVN1配體(地塞米松)親和力僅約為μM量級,ERADECs的療效仍有很大的進(jìn)一步提升空間。
五、關(guān)于中喬新舟
本研究中使用了中喬新舟的A-375人惡性黑色素瘤細(xì)胞專用培養(yǎng)基(貨號:ZM0042),NCI-H1975人肺腺癌細(xì)胞專用培養(yǎng)基(貨號:ZM0395),MDA-MB-231人乳腺癌細(xì)胞(貨號:ZQ0118),NCI-H1975人肺腺癌細(xì)胞(貨號:ZQ0395),A375人惡性黑色素瘤細(xì)胞(貨號:ZQ0042),印證了高端科研對高品質(zhì)細(xì)胞以及專用試劑產(chǎn)品的要求。
中喬新舟提供品種豐富的細(xì)胞培養(yǎng)基產(chǎn)品,主要分為基礎(chǔ)培養(yǎng)基,細(xì)胞系完全培養(yǎng)基,動物原代細(xì)胞完全培養(yǎng)基,人原代細(xì)胞完全培養(yǎng)基,永生化細(xì)胞完全培養(yǎng)基等。該系列產(chǎn)品均由公司技術(shù)研發(fā)團(tuán)隊(duì)歷經(jīng)數(shù)年精心設(shè)計優(yōu)化,可保持細(xì)胞良好的生長狀態(tài)。所有產(chǎn)品均有通過嚴(yán)格的質(zhì)控體系,經(jīng)過微生物檢測、PH值檢測、細(xì)跑生長驗(yàn)證實(shí)驗(yàn)等確保了培養(yǎng)基質(zhì)量的穩(wěn)定性。
如果您對我們的產(chǎn)品感興趣,歡迎聯(lián)系我們了解更多產(chǎn)品詳情。

