磁珠富集的前分析「陷阱」:血細胞、離心與抗凝劑對血漿蛋白組學的多重干擾

英文標題:Pre-Analytical Drivers of Bias in Bead-Enriched Plasma Proteomics
中文標題:血漿蛋白組學中磁珠富集前分析階段偏差的影響因素
研究背景
血液作為臨床研究中重要的樣本類型,在生物標志物研究領域(如早期疾病診斷和預后指導應用等)中具有重要的研究價值。近年來,商業化的Somascan和Olink技術與基于肽段檢測的質譜技術等檢測方法已經應用于大隊列血漿蛋白質組研究中。
遇到的主要困境包括:
-
血液樣本的復雜性:各種蛋白的含量動態范圍跨越了12個數量級;
-
低豐度蛋白的檢出存在偏差或漏檢;
-
大隊列檢測儀器系統的穩定性;
-
前處理方法不一,數據標準化與批次校正并不能解決所有偏差;
-
血漿樣本通常在常規臨床實踐中以不同的處理條件收集,在病例對照研究中,樣本收集或處理的系統差異可能導致錯誤的生物標志物候選物。
文章表明,約一半已發表的血漿蛋白質組學研究可能受到此類樣本相關質量問題的影響。
本研究旨在全面評估五種不同的血漿蛋白質組學工作流程在分析前各種因素方面的表現。
具體目標包括:
-
系統評估每個工作流程檢測低豐度蛋白質的能力;
-
表征它們對常見樣本污染物(如血小板、紅細胞和外周血單核細胞)的敏感性;
-
研究標準臨床離心方案和采血試管對血漿蛋白質組分析的影響,揭示樣本制備參數與蛋白質組組成之間的關系;
-
探討污染樣本是否可以通過額外的處理步驟“挽救”;
-
為基于磁珠的工作流程的潛力和局限性提供見解,并為前瞻性研究設計和存檔樣本的回顧性質量評估提供實用指導。
研究方法
實驗設計:比較5種不同的血漿蛋白質組學工作流程,所有流程均在安捷倫Bravo液體處理平臺上實現自動化,以確保96個樣本的可重復性和高通量并行處理。在液相色譜-質譜(LC-MS)方面,采用了將Evosep色譜系統與Orbitrap Astral耦合的先進工作流程。
具體工作流程如下:
-
純血漿工作流程:作為基線方法,采用簡單的蛋白質變性后進行酶消化,優化了速度和簡便性;
-
基于高氯酸沉淀中和的方法(PCA-N):通過蛋白質的溶解度進行分離,對某些污染物具有抗性,用于在不使用磁珠的情況下實現更深入的蛋白質組覆蓋;
-
三種基于磁珠的富集方法:使用具有代表性表面化學性質的磁性或非磁性磁珠。
加標實驗:使用各種血細胞類型(如血小板、紅細胞和外周血單核細胞)以及整個酵母蛋白質組進行精心設計的加標實驗,以系統評估每個工作流程檢測低豐度蛋白質的能力,并表征它們對常見樣本污染物的敏感性。此外,還研究了標準臨床離心方案和采血試管對血漿蛋白質組分析的影響,以揭示樣本制備參數與蛋白質組組成之間的關鍵關系。同時,探討是否可以通過額外的處理步驟來改善污染樣本的分析結果。
研究結果
1、不同工作流程對低豐度蛋白質的檢測能力
研究建立了一個多維度、系統化的實驗框架,旨在評估5種血漿蛋白質組學處理流程在不同前處理變量下的性能。5種流程包括:①簡便的直接血漿法(neat workflow),未經任何蛋白富集方法;②抗污染能力較強的PCA-N流程,經過高氯酸沉淀并中和;③兩種基于磁性磁珠的富集方法(強陰離子交換磁珠SAX與硅膠涂層磁珠Sera Sil 700);④一種基于非磁性磁珠的富集方法(non-magnetic beads)。這些流程代表了不同的檢測深度、速度與污染敏感性之間的權衡。
本部分結果明確指出,不同流程通過各自的蛋白富集與選擇性去除機制,重塑了血漿蛋白豐度的等級結構,有效壓縮了極端的動態范圍,其中磁珠法表現出更強的低豐度蛋白檢出能力(但易受到血小板和PBMC污染的系統偏差影響),而PCA-N表現較溫和但更穩定(圖1)。
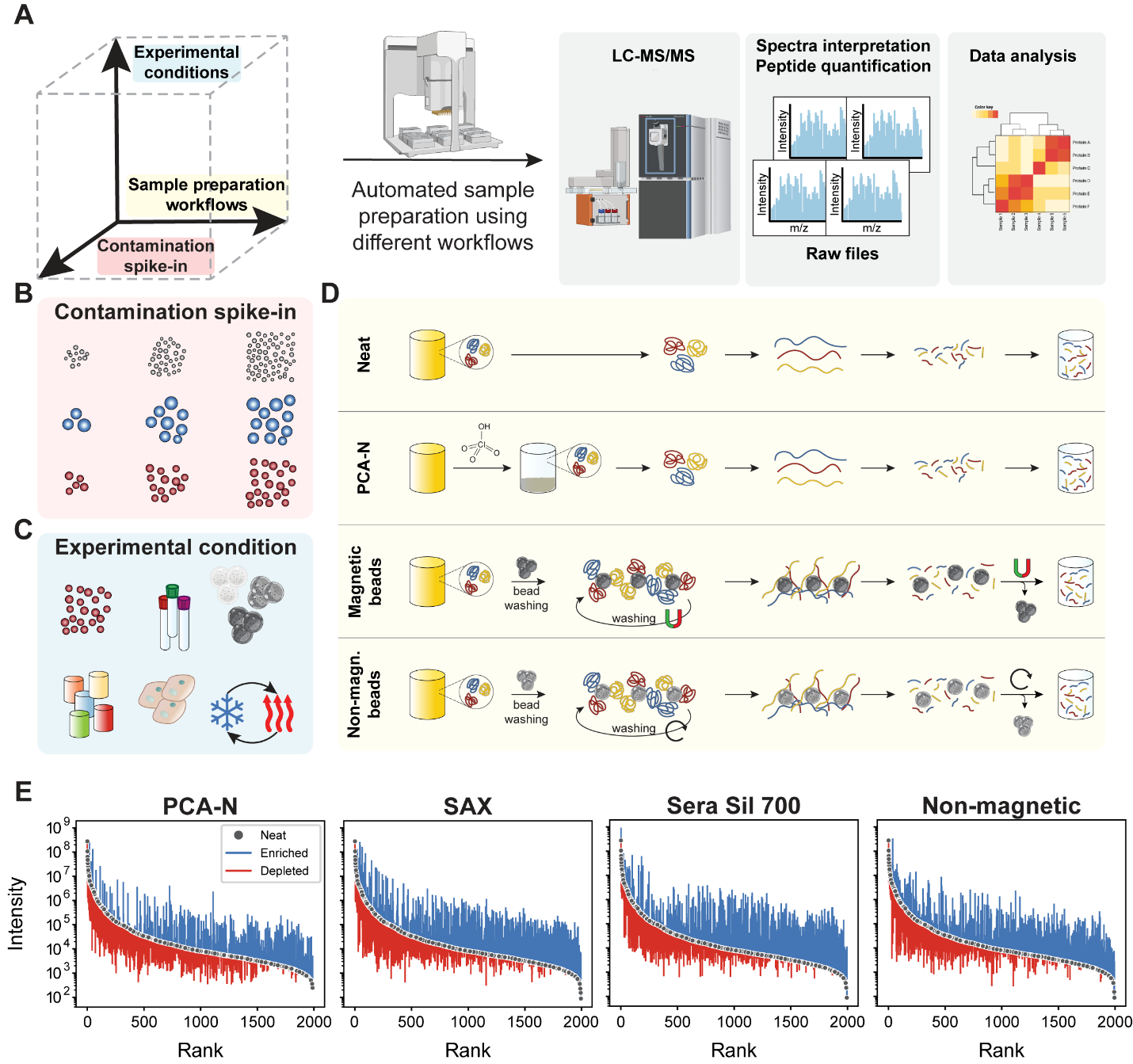
圖1. 用于比較血漿蛋白質組學工作流程的系統實驗框架
2、細胞污染分析
研究通過向純凈血漿中添加不同數量的紅細胞、血小板和PBMC,系統評估了5種蛋白質組學流程對細胞污染的敏感性。結果表明,磁珠法極易受到污染影響,即使低水平的PBMC(140 cells/μL)也能顯著增加蛋白鑒定數,某些條件下總檢出蛋白數高達8000–10000種。而PCA-N流程對紅細胞污染高度耐受,在不同污染濃度下保持穩定的蛋白數(約800–900種)。neat流程對紅細胞污染敏感,對血小板污染抗性較強。為定量評估污染影響,研究建立了血小板、紅細胞和PBMC的高特異性蛋白標志物panel,并據此計算“污染指數”(contamination index)和“細胞富集分數”(cellular enrichment score)。結果顯示,非磁性磁珠法的污染指數最高,磁珠法次之,而PCA-N和neat流程對污染反應較弱。總體而言,磁珠法在檢測靈敏度與污染易感性之間存在明顯權衡,需特別重視樣本質量控制(圖2)。
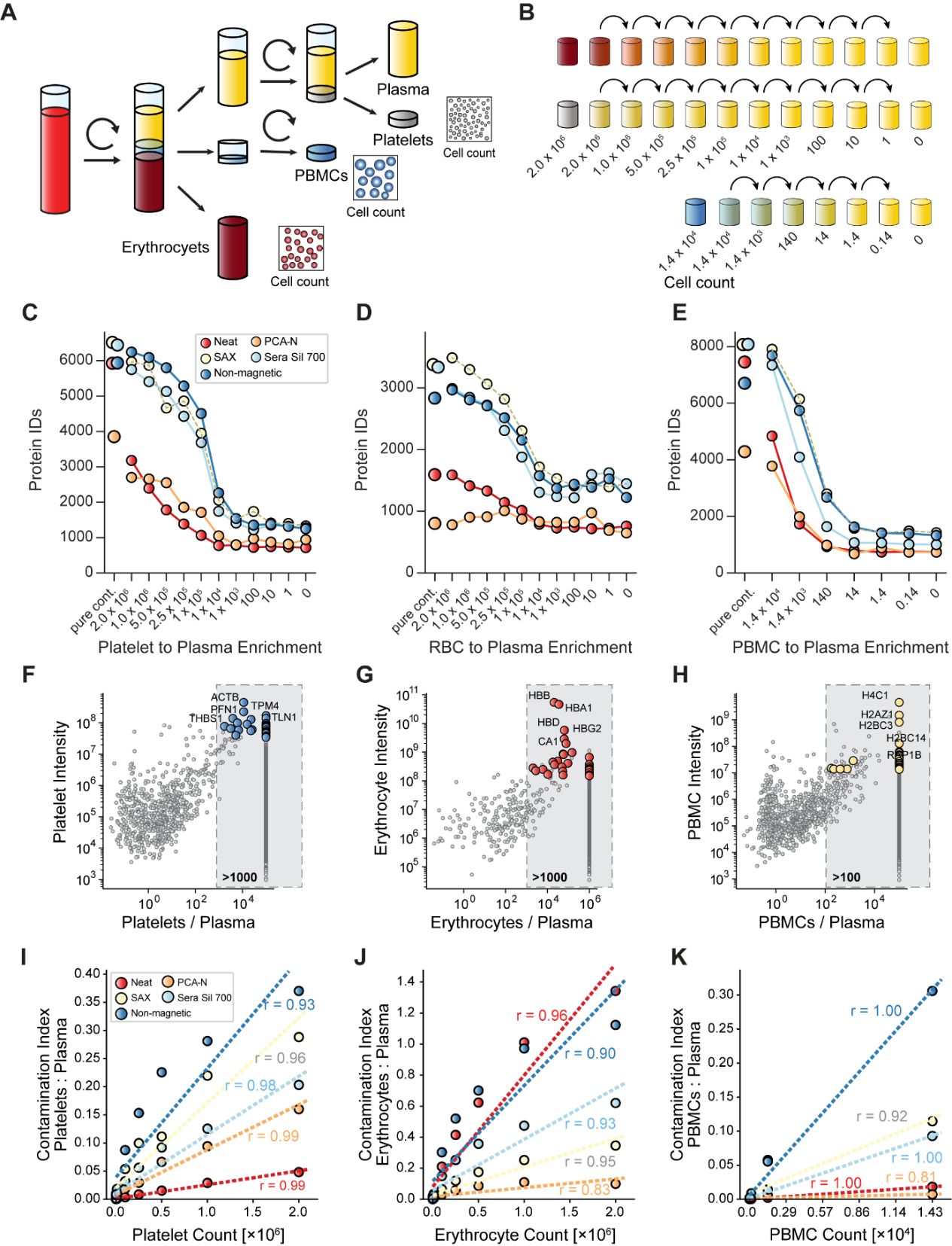
圖2. 細胞污染對血漿蛋白質組學工作流程影響的系統分析
3、酵母蛋白外源添加實驗:低豐度蛋白檢測能力評估
為評估各流程對低豐度蛋白的檢測能力,研究人員向血漿中加入了不同比例的酵母蛋白(圖3)。結果顯示,三種磁珠法(SAX、Sera Sil 700和non-magnetic beads)在1:100稀釋條件下可鑒定2,286種酵母蛋白,顯著優于PCA-N(471種)和 neat流程(317種),其中non-magnetic beads表現最優。
進一步分析代表性蛋白(如TDH3、RNQ1、FAB1)表明,磁珠法能在更低濃度下保持良好檢測,將濃度檢測下限提升至neat流程的100倍(如磁珠法可檢測0.01%酵母濃度,neat流程為1%)。不過,PCA-N雖穩定但變異較大,neat流程則對低豐度蛋白檢測能力有限。
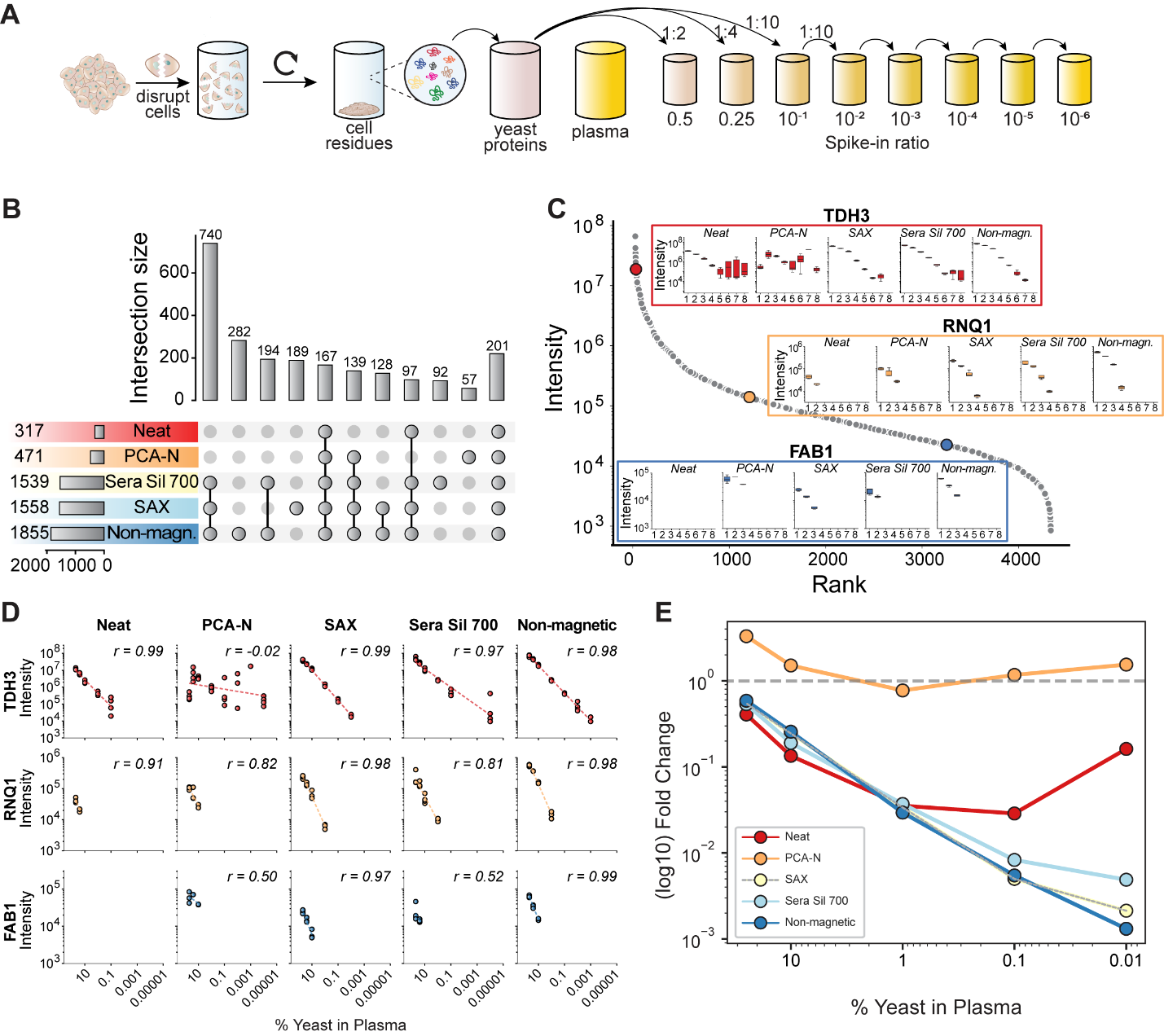
圖3. 酵母蛋白加標在血漿蛋白質組學工作流程中的分析
4、血小板活化與磁珠敏感性機制探討
為揭示磁珠法對血小板污染高度敏感的機制,研究比較了8種不同表面化學的磁/非磁珠與7種緩沖條件的組合,形成56種實驗條件(圖4)。結果顯示:非磁珠在HEPES緩沖液中鑒定蛋白最多,但也表現出最高的血小板富集水平,可能源于其需額外離心步驟帶來血小板共沉淀。在檢測血小板活化方面,部分條件(如CaCl2、低pH的TFA緩沖液)誘導血小板釋放特異蛋白(如PF4V1、PPBP),提示樣本制備本身可激活血小板。而非磁珠在PBSC緩沖中則表現為高血小板蛋白信號而非活化釋放,說明部分富集源于物理保留而非生物過程。這些發現強調了樣本處理方式對血小板相關偏差的影響。
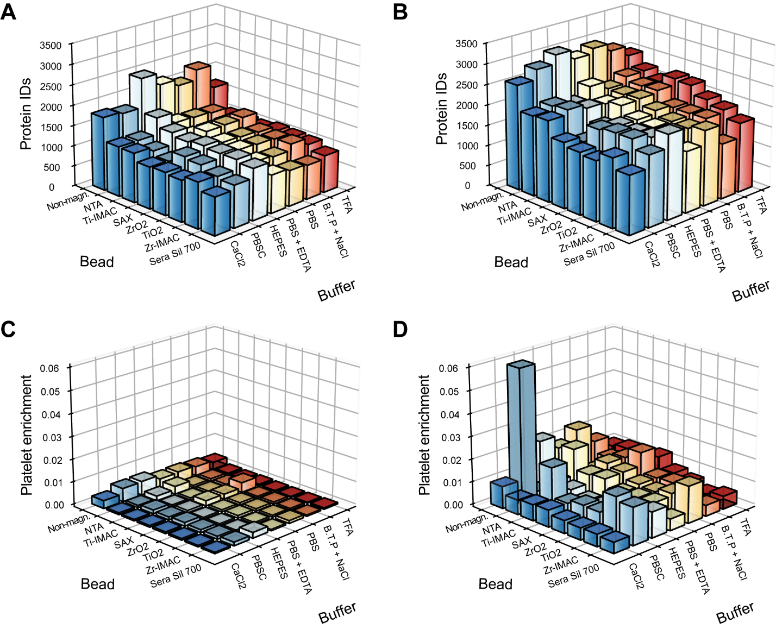
圖4. 純血漿和血小板污染血漿中珠子與緩沖液組合的分析
5、血小板污染樣本的“補救”策略評估
考慮到實際臨床樣本常含血小板污染,研究測試了凍融循環與離心處理是否能補救,實驗表明(圖5),磁性磁珠法污染最重,蛋白鑒定數由1400提升至2700,即使離心后仍僅下降15–20%;而非磁性磁珠法污染更嚴重但可緩解更多(降至約2000)。neat流程穩定性較高,PCA-N流程鑒定數增幅35%但變化小于磁珠法。主成分分析表明,血小板污染是蛋白組變化的主要驅動因素,凍融循環影響極小。離心處理可以較穩定地降低血小板標志物強度。這些結果為處理存儲樣本提供參考。
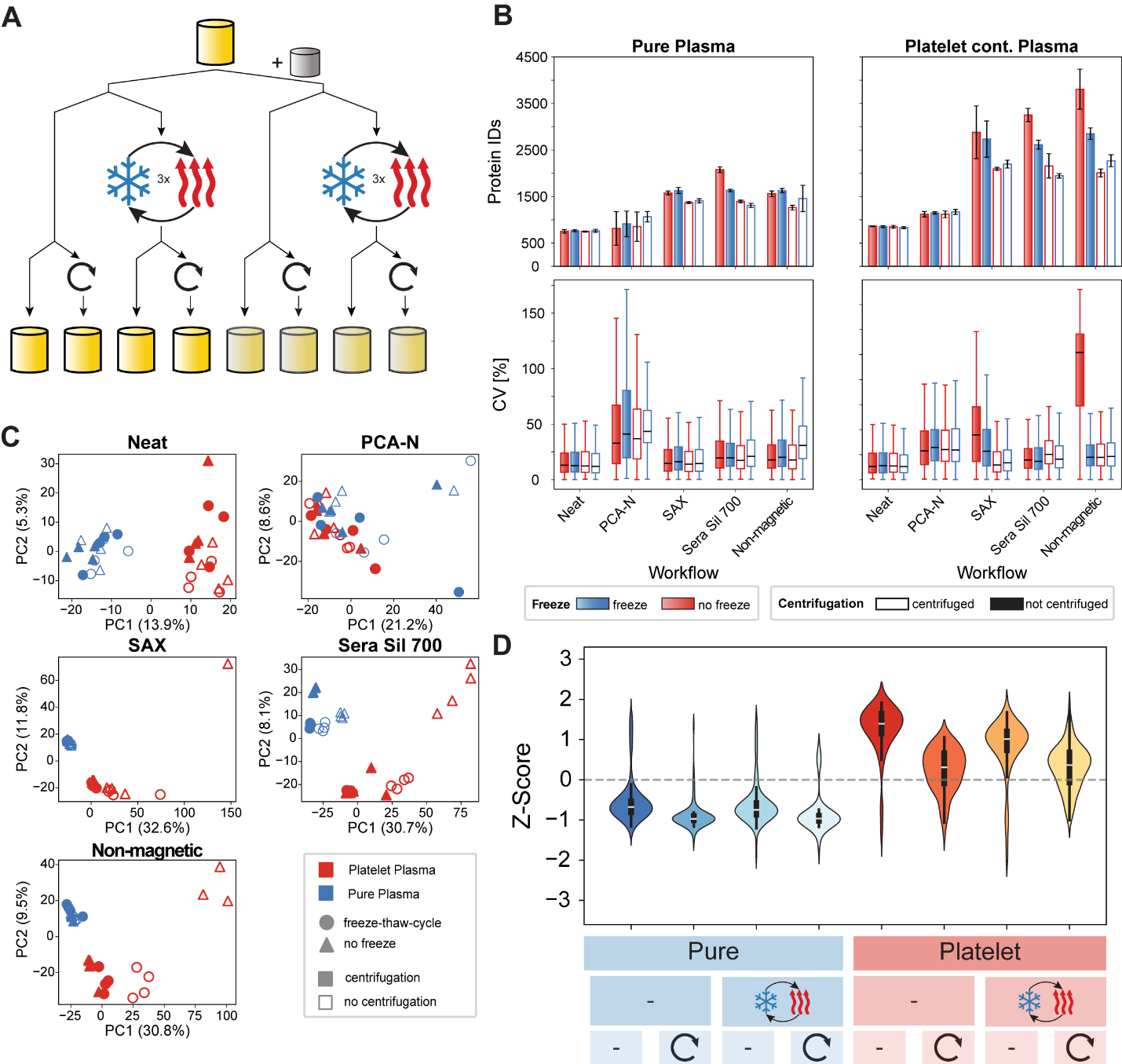
圖5. 血漿處理策略評估以應對血小板污染
6、推薦的血漿樣本制備條件
在血漿蛋白組學研究中,前分析階段的樣本處理條件(如離心設置和試管類型)對污染水平和蛋白質組譜影響顯著。研究顯示,低轉速離心時,凝膠試管因凝膠屏障未充分激活,血小板、紅細胞等污染顯著高于標準試管,且基于磁珠的富集方法鑒定的蛋白質數量遠高于常規法和PCA-N法。提高離心力和時間可有效降低污染。主成分分析表明,離心是影響蛋白質組譜的主要因素,磁珠工作流程按離心力明顯聚類,而PCA-N對處理差異敏感性低。
抗凝劑類型對磁珠工作流程影響顯著:EDTA血漿中磁珠法鑒定的蛋白質數最高,但血小板和紅細胞污染也最嚴重,而Li-肝素和血清樣本污染更少。因此,研究建議標準化抗凝劑類型,避免混合使用不同基質樣本,且高轉速離心可作為血漿蛋白組學,尤其是磁珠富集法的優選樣本處理條件,以減少污染偏差。
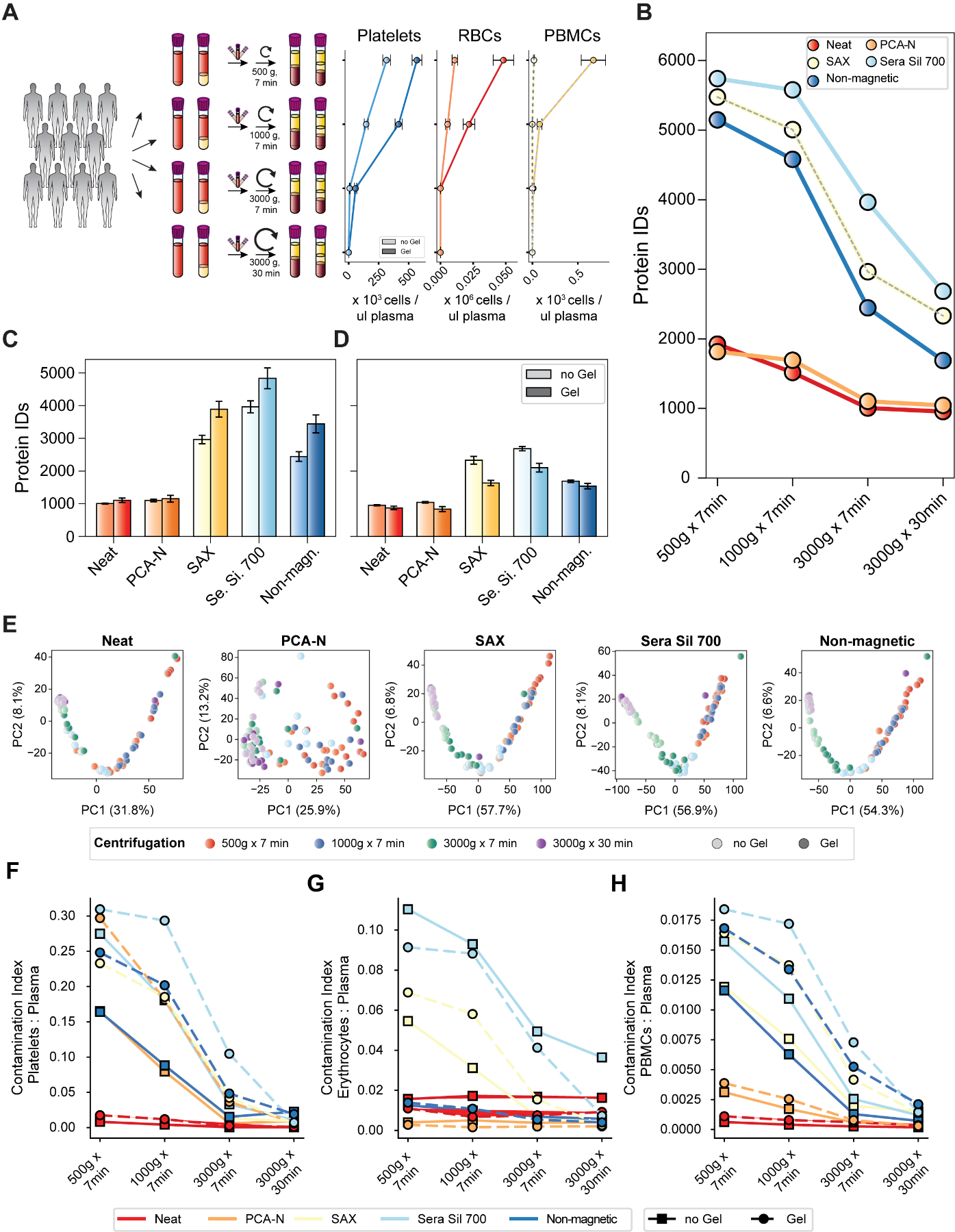
圖6. 離心條件對血漿蛋白質組分析的影響
研究結論
本研究結果為在可變樣本質量下評估工作流程性能提供了定量框架,并為臨床蛋白質組學研究中的生物標志物發現和質量控制提供了指導。
具體結論如下:
-
基于磁珠的富集方法雖然能提高低豐度蛋白質的檢測能力,但對血小板、PBMC等血細胞污染敏感,使用時需謹慎控制樣本質量;
-
高氯酸沉淀中和(PCA-N)方法對紅細胞污染具有高度抗性,對血小板衍生的污染具有一定耐受性,可作為一種可靠的替代方法;
-
優化樣本處理(如離心條件、抗凝劑選擇等)可以部分減輕分析前偏差的影響;
-
研究鑒定出的大量蛋白質組為進一步的生物標志物研究提供了豐富的資源。
END
Saitama 撰文
SY 校稿
