Cell Metab.|復(fù)旦大學(xué)儲(chǔ)以微、駱?lè)品茍F(tuán)隊(duì):Foxp3改造CAR-T,從「能量危機(jī)」到「代謝續(xù)航」的實(shí)體瘤治療新路徑
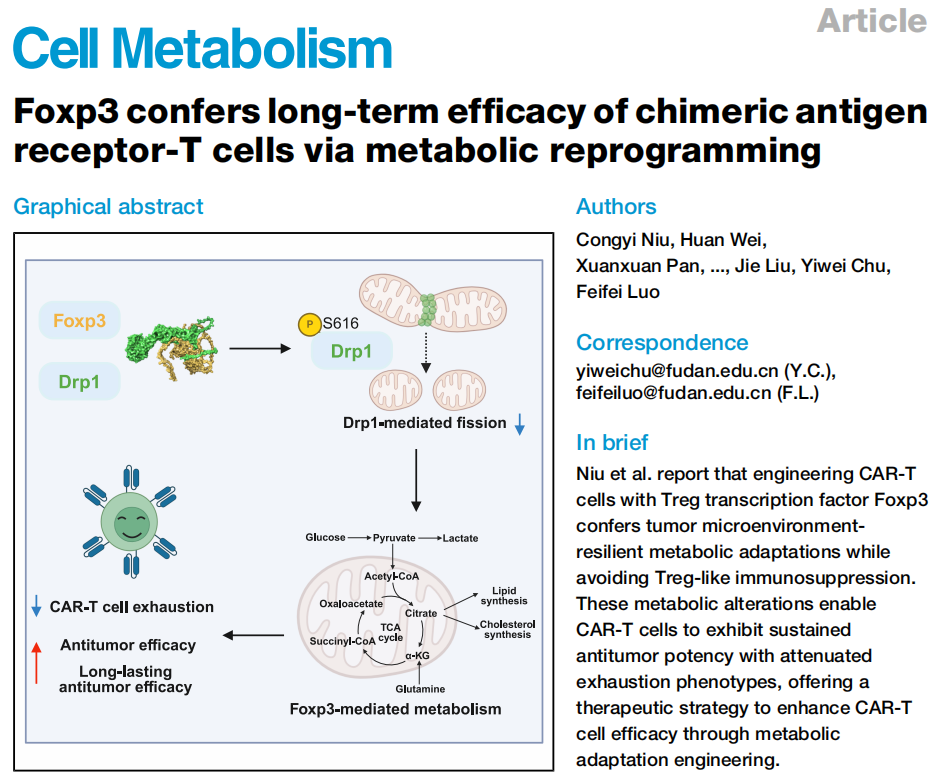
英文標(biāo)題:Foxp3 confers long-term efficacy of chimeric antigen receptor-T cells via metabolic reprogramming
中文標(biāo)題:Foxp3通過(guò)代謝重編程賦予嵌合抗原受體T細(xì)胞長(zhǎng)期療效
發(fā)表期刊:Cell Metabolism
影響因子:27.7
客戶單位:復(fù)旦大學(xué)生物醫(yī)學(xué)研究院/基礎(chǔ)醫(yī)學(xué)院、復(fù)旦大學(xué)附屬華山醫(yī)院
百趣提供服務(wù):經(jīng)典脂質(zhì)組
研究背景
嵌合抗原受體T細(xì)胞(Chimeric Antigen Receptor-T, CAR-T)免疫療法在血液癌癥治療中效果顯著,但用于實(shí)體瘤治療時(shí)面臨困境。腫瘤微環(huán)境(Tumor Microenvironment, TME)的低氧和營(yíng)養(yǎng)匱乏致使CAR-T細(xì)胞耗竭,限制了治療效果。調(diào)節(jié)性T細(xì)胞(Regulatory T Cells, Tregs)可在TME中生存和發(fā)揮作用,其代謝模式獨(dú)特,F(xiàn)oxp3作為Tregs的關(guān)鍵轉(zhuǎn)錄因子,對(duì)維持Tregs代謝和功能意義重大。因此,探究將Tregs代謝優(yōu)勢(shì)引入CAR-T細(xì)胞,借助調(diào)控其代謝來(lái)克服TME障礙、防止細(xì)胞耗竭,有望提升CAR-T細(xì)胞在實(shí)體瘤治療中的療效。
研究結(jié)果
1、CAR-TFoxp3細(xì)胞獲得了與CAR-TConv細(xì)胞不同的代謝特征
研究者為探究Foxp3過(guò)表達(dá)對(duì)CAR-T細(xì)胞代謝的影響,選用具有更強(qiáng)擴(kuò)增能力和持久性的第三代CAR。通過(guò)激活健康供體的人T淋巴細(xì)胞,分別用GPC3-CAR感染得到常規(guī)的 GPC3-CAR-T(CAR-TConv)細(xì)胞,用GPC3-CAR和Foxp3共同感染培育出GPC3-CAR-TFoxp3(CAR-TFoxp3)細(xì)胞(圖1A)。
在檢測(cè)細(xì)胞代謝參數(shù)時(shí)發(fā)現(xiàn),GPC3蛋白刺激后,CAR-TFoxp3細(xì)胞的細(xì)胞外酸化率(Extracellular Acidification Rate, ECAR)和耗氧率(Oxygen Consumption Rate, OCR)低于CAR-TConv細(xì)胞(圖1B)。利用LC-MS評(píng)估[U-C13]葡萄糖和[U-C13]谷氨酰胺代謝通量,結(jié)果顯示,CAR-TFoxp3細(xì)胞從[U-C13]葡萄糖產(chǎn)生的相關(guān)代謝產(chǎn)物低于CAR-TConv細(xì)胞,且谷氨酰胺進(jìn)入三羧酸(Tricarboxylic Acid, TCA)循環(huán)的量減少,相關(guān)代謝產(chǎn)物水平也更低(圖1C-F)。添加丙酮酸也無(wú)法恢復(fù)CAR-TFoxp3細(xì)胞降低的ECAR和OCR。同時(shí),CAR-TFoxp3細(xì)胞內(nèi)ATP水平更低,NAD/NADH比值更高,表明其糖酵解和氧化磷酸化(Oxidative Phosphorylation, OXPHOS)適度下調(diào)(圖1G)。
進(jìn)一步利用非靶LC-MS篩選,發(fā)現(xiàn)CAR-TFoxp3細(xì)胞中與脂質(zhì)和氨基酸代謝相關(guān)的代謝物表達(dá)有差異,涉及甘油磷脂代謝等多條途徑。脂質(zhì)組學(xué)及BODIPY染色證實(shí),CAR-TFoxp3細(xì)胞甘油三酯水平和細(xì)胞內(nèi)脂滴含量增加(圖1H-I)。用二氯乙酸鈉(Sodium Dichloroacetate, DCA)處理后,CAR-TFoxp3細(xì)胞脂滴含量降低,暗示Foxp3介導(dǎo)的OXPHOS減少與脂質(zhì)代謝上調(diào)有關(guān)(圖1I)。同時(shí),CAR-TFoxp3細(xì)胞線粒體膜電位和質(zhì)量降低,線粒體功能改變(圖1J) 。綜上,CAR-TFoxp3細(xì)胞的代謝特征與調(diào)節(jié)性T細(xì)胞(Tregs)相似,與CAR-TConv細(xì)胞不同。
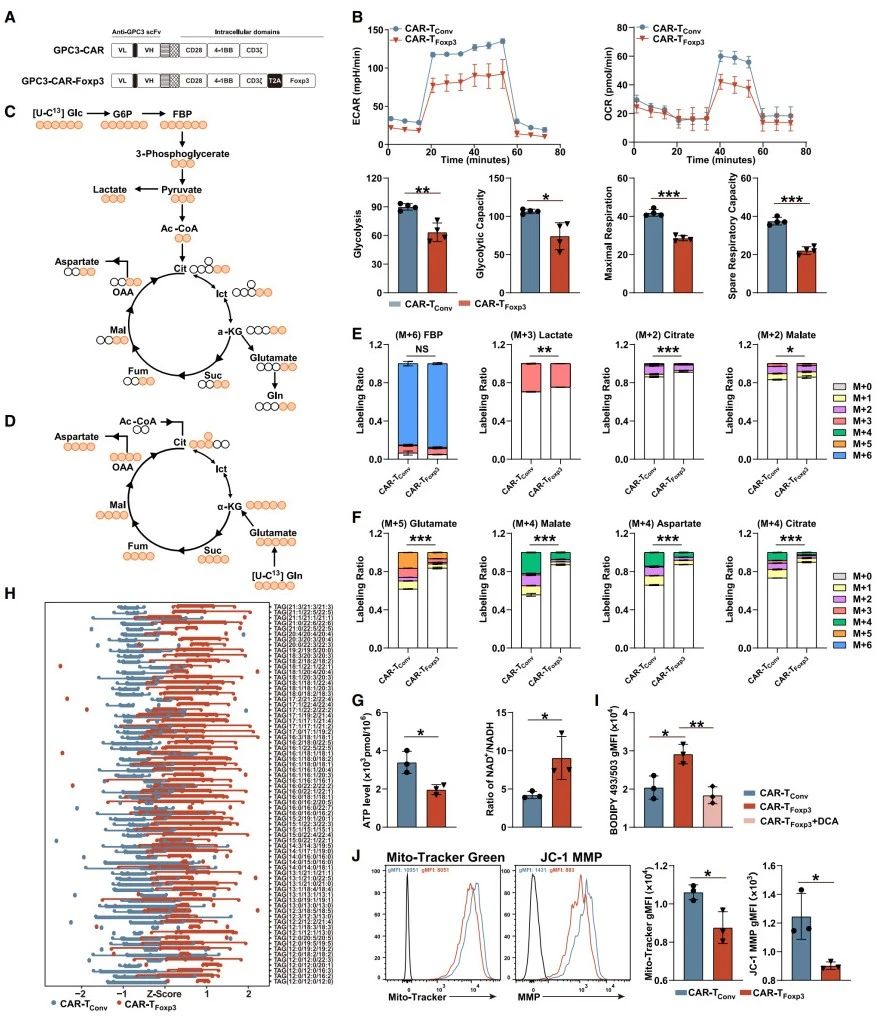
圖1.CAR-TFoxp3細(xì)胞獲得了與CAR-TConv細(xì)胞不同的代謝特征
2、CAR-TFoxp3細(xì)胞的代謝特征由Foxp3與Drp1的結(jié)合所決定
研究者探究CAR-TFoxp3細(xì)胞代謝模式與Foxp3和線粒體動(dòng)力學(xué)相關(guān)蛋白的關(guān)系,發(fā)現(xiàn)其代謝重編程由Foxp3與Drp1的結(jié)合介導(dǎo)。
探究Foxp3與線粒體動(dòng)力學(xué)相關(guān)蛋白的相互作用:鑒于CAR-TFoxp3細(xì)胞線粒體膜電位(Mitochondrial Membrane Potential, MMP)和質(zhì)量改變,研究人員探究Foxp3對(duì)Opa1、Drp1、Mfn1和Mfn2等線粒體動(dòng)力學(xué)相關(guān)蛋白的作用,以明確其代謝模式的成因。雙分子熒光互補(bǔ)(Bimolecular Fluorescence Complementation, BiFC)實(shí)驗(yàn)顯示,在HEK293T細(xì)胞中Foxp3僅與Drp1存在相互作用(圖2A),谷胱甘肽S-轉(zhuǎn)移酶下拉(Glutathione S-transferase Pull-down Assay, GST pull-down Assay)實(shí)驗(yàn)加以驗(yàn)證(圖2B)。構(gòu)建融合蛋白觀察到Drp1 定位于細(xì)胞質(zhì),F(xiàn)oxp3在細(xì)胞質(zhì)和細(xì)胞核均有分布(圖2C),二者在細(xì)胞質(zhì)共定位,此現(xiàn)象經(jīng)HEK293T細(xì)胞免疫熒光實(shí)驗(yàn)(圖2D)以及以Tregs為對(duì)照的CAR-T細(xì)胞實(shí)驗(yàn)(圖2E)證實(shí)。
研究Foxp3對(duì)Drp1磷酸化及線粒體的影響:已知Drp1絲氨酸616位點(diǎn)磷酸化促線粒體裂變,637位點(diǎn)磷酸化助融合。研究發(fā)現(xiàn),F(xiàn)oxp3不影響Drp1表達(dá)及絲氨酸637位點(diǎn)磷酸化,卻顯著降低絲氨酸616位點(diǎn)磷酸化水平(圖2F-M)。利用AlphaFold軟件預(yù)測(cè)結(jié)構(gòu)和對(duì)接結(jié)果表明,絲氨酸616位點(diǎn)磷酸化影響Foxp3與Drp1結(jié)合穩(wěn)定性。顯微鏡觀察顯示,CAR-TFoxp3細(xì)胞線粒體聚集伸長(zhǎng)且數(shù)量少于CAR-TConv細(xì)胞(圖2G-I)。此外,F(xiàn)oxp3對(duì)Drp1上游激酶CDK1和ERK1/2無(wú)明顯抑制作用(圖2M)。綜合這些結(jié)果可知,F(xiàn)oxp3與Drp1結(jié)合可能影響Drp1磷酸化和線粒體裂變,進(jìn)而重編程CAR-T細(xì)胞代謝。
確定Foxp3與Drp1結(jié)合位點(diǎn)及對(duì)代謝的影響:為確定Foxp3與Drp1結(jié)合位點(diǎn)及其對(duì)代謝的影響,研究人員利用薛定諤軟件進(jìn)行對(duì)接研究,篩選出5個(gè)結(jié)合穩(wěn)定性最高的構(gòu)象。通過(guò)構(gòu)建多種Foxp3序列部分缺失質(zhì)粒,BiFC實(shí)驗(yàn)發(fā)現(xiàn)缺失340-390位氨基酸片段會(huì)破壞二者相互作用。構(gòu)建缺失該片段的CAR-TFoxp3(340-390)細(xì)胞后,觀察到其融合線粒體消失、線粒體數(shù)量恢復(fù)、脂滴含量降低,線粒體質(zhì)量、MMP、ECAR和OCR增加(圖2G-L),且Drp1絲氨酸616位點(diǎn)磷酸化增強(qiáng)(圖2M)。研究還預(yù)測(cè)Foxp3的340-390片段與Drp1的600-620片段結(jié)合,構(gòu)建缺失600-620片段的Drp1變體后,其BiFC平均熒光強(qiáng)度顯著降低,表明該片段參與二者相互作用,解釋了Drp1絲氨酸616位點(diǎn)磷酸化下調(diào)的原因(詳情可查閱補(bǔ)充材料)。
綜上,CAR-TFoxp3細(xì)胞代謝重編程由Foxp3與Drp1結(jié)合介導(dǎo)。
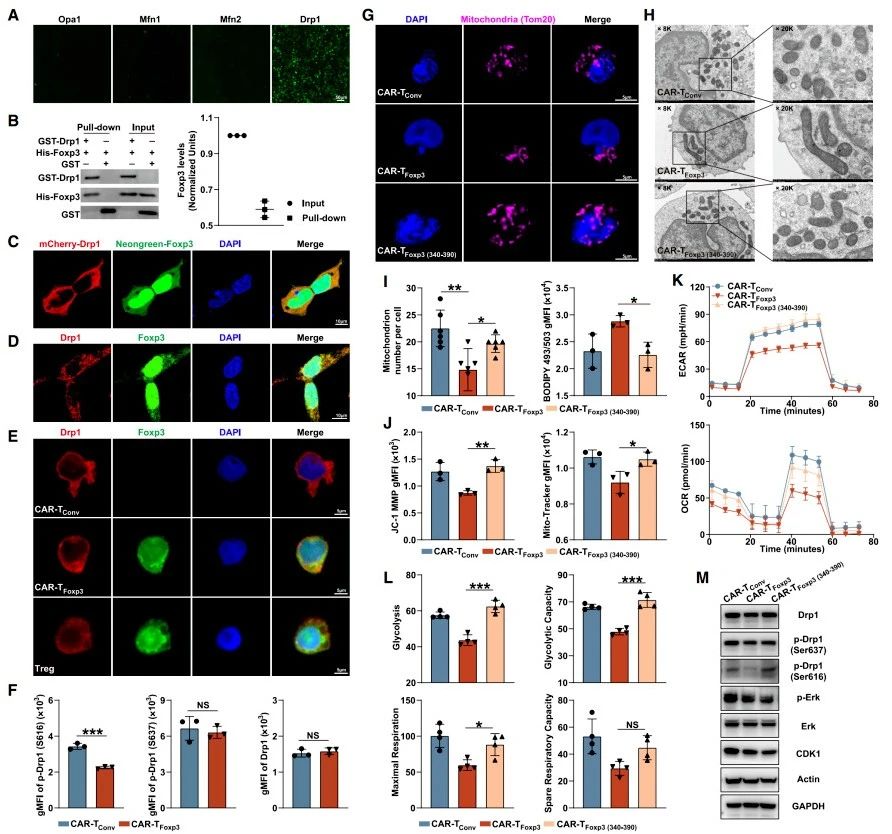
圖2.CAR-TFoxp3細(xì)胞的代謝特征由Foxp3與Drp1的結(jié)合決定
3、CAR-TFoxp3細(xì)胞不會(huì)獲得Tregs的染色質(zhì)可及性和抑制功能
染色質(zhì)可及性分析:研究人員利用ATAC-seq技術(shù)分析Tregs、CAR-TConv和CAR-TFoxp3細(xì)胞全基因組染色質(zhì)可及性,發(fā)現(xiàn)ATAC-seq峰主要集中于啟動(dòng)子、內(nèi)含子和遠(yuǎn)端基因間區(qū)域,降維分析可清晰區(qū)分三類細(xì)胞(圖3A)。轉(zhuǎn)錄起始位點(diǎn)(TSS)周圍平均ATAC-seq信號(hào)顯示,Tregs讀數(shù)濃度低于其余兩組,而CAR-TConv與CAR-TFoxp3細(xì)胞信號(hào)相近(圖3B)。深入分析發(fā)現(xiàn),Tregs中顯著升高的峰高度富集于TRPS1、RUNX2等轉(zhuǎn)錄因子識(shí)別基序,這些基序與Tregs的抑制功能相關(guān)。然而,在CAR-TFoxp3細(xì)胞中,這些基序并不富集,表明二者染色質(zhì)格局存在差異(圖3C-E)。
細(xì)胞因子與標(biāo)志物檢測(cè):檢測(cè)T細(xì)胞相關(guān)標(biāo)志物和細(xì)胞因子發(fā)現(xiàn),與Tregs相比,CAR-TFoxp3細(xì)胞分泌的IL-10、TGF-β水平較低,CTLA-4抑制性受體表達(dá)也降低,且與CAR-TConv細(xì)胞情況相近(圖3F)。GPC3抗原刺激后,CAR-TFoxp3、CAR-TConv和Tregs細(xì)胞中CD39和CD73表達(dá)無(wú)顯著差異(圖3F)。
抑制功能驗(yàn)證:通過(guò)共培養(yǎng)實(shí)驗(yàn)驗(yàn)證CAR-TFoxp3細(xì)胞對(duì)TConv細(xì)胞增殖的抑制作用,結(jié)果顯示CAR-TFoxp3組中TConv細(xì)胞增殖明顯強(qiáng)于Tregs組,與CAR-TConv組相近,表明CAR-TFoxp3細(xì)胞無(wú)抑制作用。
差異峰與代謝物分析:研究發(fā)現(xiàn),在CAR-TFoxp3細(xì)胞上調(diào)、CAR-TConv細(xì)胞下調(diào)的峰中,僅有少量能在Tregs中共同富集(圖3G-H)。通路富集分析表明這些峰集中于細(xì)胞代謝過(guò)程(圖3I)。質(zhì)譜檢測(cè)發(fā)現(xiàn),CAR-TFoxp3細(xì)胞中乳酸、富馬酸和NADH水平顯著低于CAR-TConv細(xì)胞,或可解釋CAR-TFoxp3細(xì)胞染色質(zhì)可及性與代謝相關(guān)的變化。
綜上,CAR-TFoxp3細(xì)胞在染色質(zhì)格局和抑制功能上與Tregs存在根本差異,不會(huì)轉(zhuǎn)化為Tregs。
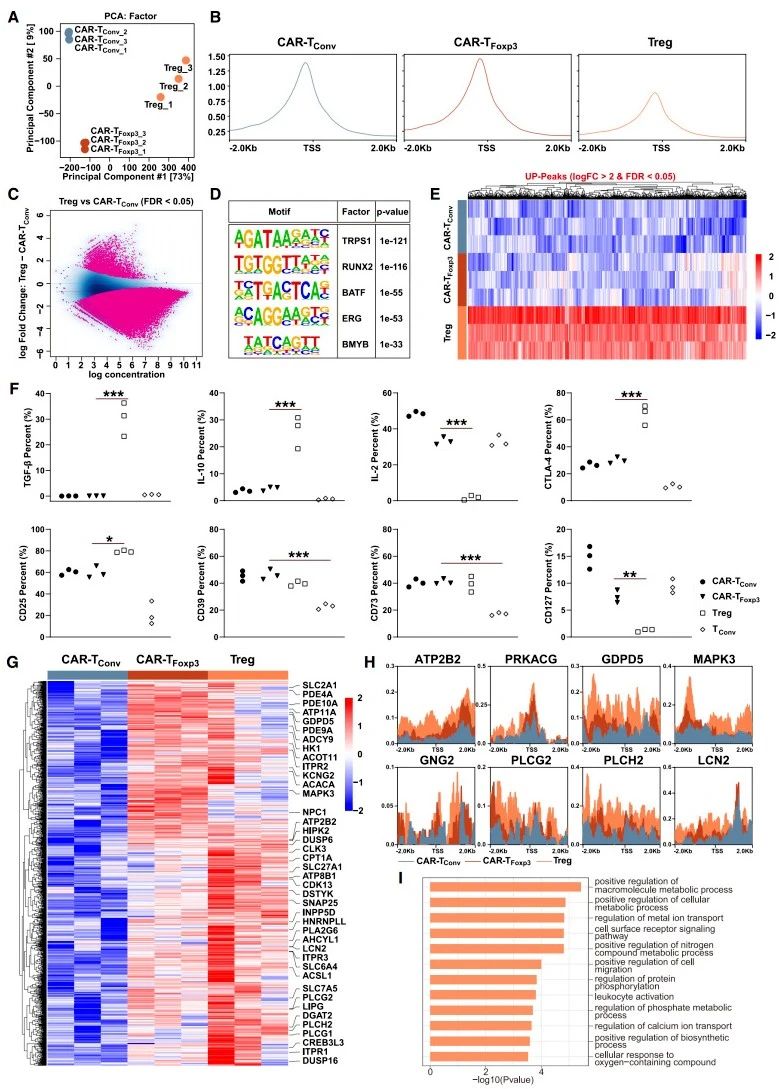
圖3.CAR-TFoxp3 細(xì)胞未獲得Tregs的染色質(zhì)可及性和抑制功能
4、Foxp3介導(dǎo)的代謝下調(diào)了CAR-TFoxp3細(xì)胞中與耗竭相關(guān)的抑制性分子的表達(dá)
接下來(lái),研究者探究了Foxp3介導(dǎo)的代謝對(duì)CAR-TFoxp3細(xì)胞活化和功能的影響。
細(xì)胞表型與功能檢測(cè):將CAR-TFoxp3和CAR-TConv細(xì)胞與GPC3+Huh7腫瘤細(xì)胞孵育72小時(shí)后,CAR-TFoxp3細(xì)胞的CD27、CD28等活化及表型標(biāo)志物和BCL-6轉(zhuǎn)錄因子水平更高,CD95、EOMES等水平更低(圖4A-B)。細(xì)胞毒性評(píng)估表明,CAR-TFoxp3細(xì)胞與CAR-TConv細(xì)胞殺傷能力相似(圖4C) ,但前者釋放的顆粒酶B、IFN-γ等細(xì)胞因子更少(圖4D)。
耗竭標(biāo)志物分析:GPC3抗原刺激72小時(shí)后,CAR-TFoxp3細(xì)胞中PD-1、LAG-3等耗竭標(biāo)志物表達(dá)及三重/雙重陽(yáng)性比例均低于CAR-TConv細(xì)胞(圖4E-F);經(jīng)三輪抗原刺激后,第12天時(shí)CAR-TFoxp3細(xì)胞耗竭分子減少、干細(xì)胞標(biāo)志物CD62L增加,而CAR-TFoxp3(340–390)細(xì)胞未維持該優(yōu)勢(shì)(圖4G)。
機(jī)制探究:用P110處理增加Drp1絲氨酸616位點(diǎn)磷酸化后,CAR-TFoxp3細(xì)胞耗竭標(biāo)志物顯著上升,CAR-TConv細(xì)胞無(wú)變化(圖4H);DCA處理或抑制脂肪酸β氧化,僅使CAR-TFoxp3細(xì)胞耗竭標(biāo)志物表達(dá)增加(圖4I)。表明Foxp3與Drp1的相互作用、p-Drp1受損及Foxp3介導(dǎo)的代謝模式,共同作用下調(diào)CAR-TFoxp3細(xì)胞耗竭標(biāo)志物。
綜上,F(xiàn)oxp3介導(dǎo)的代謝不影響CAR-TFoxp3細(xì)胞毒性,但可下調(diào)其與耗竭相關(guān)的抑制性分子表達(dá),對(duì)細(xì)胞功能調(diào)控具有重要意義。
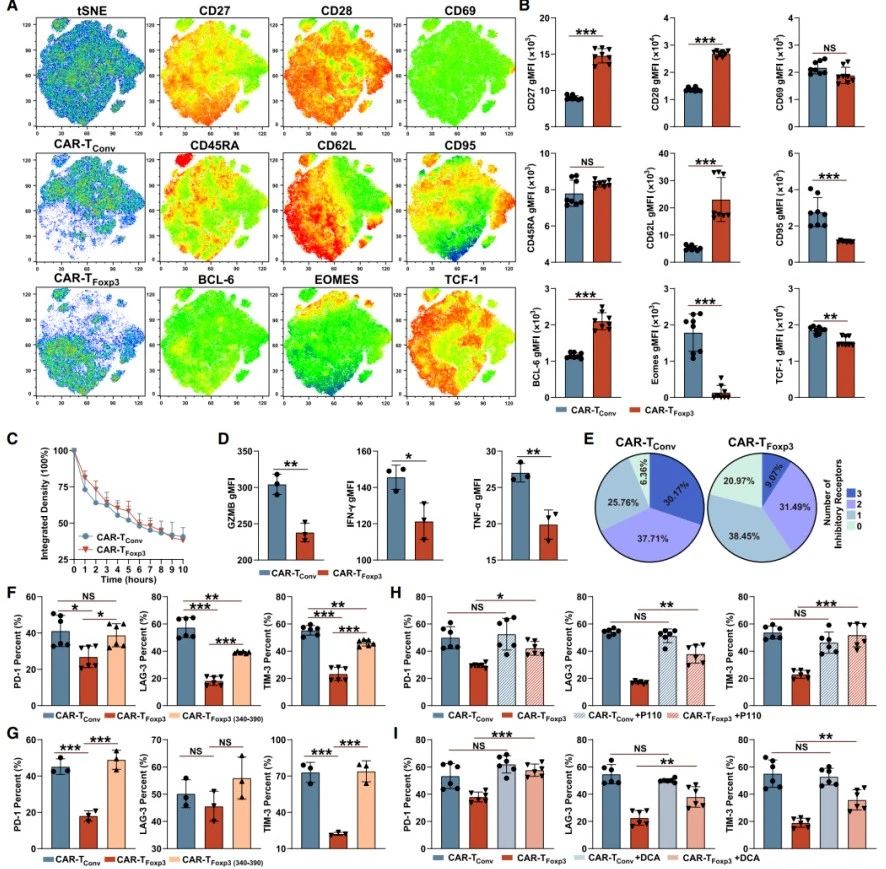
圖4. Foxp3介導(dǎo)的代謝下調(diào)了CAR-TFoxp3細(xì)胞中與耗竭相關(guān)的抑制分子的表達(dá)
5、CAR-TFoxp3細(xì)胞在體內(nèi)表現(xiàn)出強(qiáng)大的抗腫瘤活性,且耗竭標(biāo)志物水平降低
通過(guò)小鼠皮下異種移植瘤模型及后續(xù)分子檢測(cè),證實(shí)CAR-TFoxp3細(xì)胞在體內(nèi)抗腫瘤能力更強(qiáng)且耗竭程度更低。
體內(nèi)抗腫瘤效果驗(yàn)證:構(gòu)建小鼠皮下腫瘤模型,在腫瘤體積約100mm3時(shí)(圖5A),注射不同T細(xì)胞。結(jié)果顯示,CAR-TFoxp3細(xì)胞治療組腫瘤生長(zhǎng)最慢(圖5B-C),腫瘤重量更輕(圖5D),表明其具有更強(qiáng)的體內(nèi)抗腫瘤活性 。
細(xì)胞表型與功能分析:第20天對(duì)腫瘤組織進(jìn)行流式細(xì)胞術(shù)分析發(fā)現(xiàn),與CAR-TConv細(xì)胞相比,CAR-TFoxp3細(xì)胞CD28表達(dá)顯著增加,PD-1、LAG-3、TIM-3等耗竭標(biāo)志物明顯降低(圖5E-G),三重或雙重陽(yáng)性率也大幅下降(圖5F);共聚焦免疫熒光分析顯示,CAR-TFoxp3細(xì)胞中PD-1與CD3積分密度比值更低(圖5H-I),進(jìn)一步說(shuō)明其耗竭程度低。
轉(zhuǎn)錄組水平探究:對(duì)腫瘤浸潤(rùn)的CAR-T細(xì)胞進(jìn)行RNA-seq,主成分分析明確區(qū)分CAR-TFoxp3與CAR-TConv細(xì)胞;CAR-TFoxp3細(xì)胞中Foxp3持續(xù)高表達(dá),TIM-3等耗竭相關(guān)基因顯著下調(diào)(圖5J),基因集富集分析證實(shí)其耗竭狀態(tài)更低(圖5K)。此外,轉(zhuǎn)錄組分析表明CAR-TFoxp3細(xì)胞與Tregs存在根本差異,但部分上調(diào)基因在細(xì)胞代謝通路富集,提示二者代謝特征有相似之處(圖5L);同時(shí),CAR-TFoxp3細(xì)胞中線粒體相關(guān)通路顯著富集,且Foxp3靶基因在兩類細(xì)胞中的表達(dá)有差異。
綜上,CAR-TFoxp3細(xì)胞在體內(nèi)展現(xiàn)出優(yōu)于CAR-TConv細(xì)胞的抗腫瘤能力,且耗竭相關(guān)抑制性分子表達(dá)更低,在腫瘤免疫治療中具有潛在優(yōu)勢(shì)。
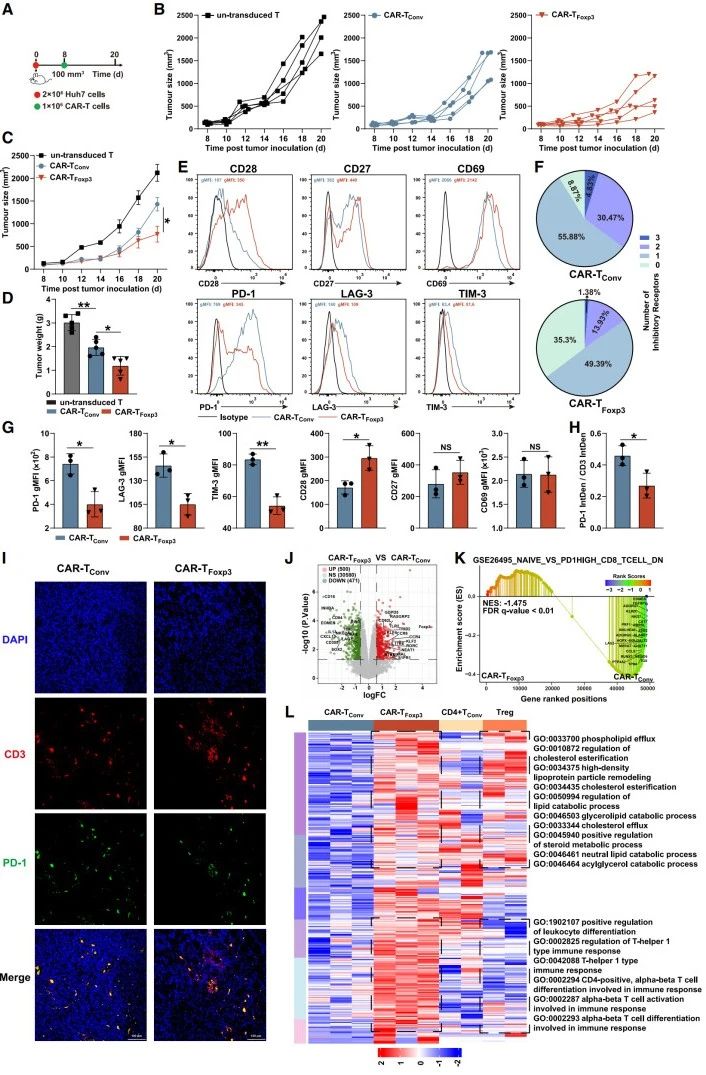
圖5.CAR-TFoxp3細(xì)胞在體內(nèi)展現(xiàn)出強(qiáng)大的抗腫瘤活性,且耗竭標(biāo)記物減少
6、Foxp3在體內(nèi)使CAR-TFoxp3細(xì)胞維持持久的抗腫瘤效果以及較低水平的耗竭標(biāo)志物
腫瘤再攻擊模型實(shí)驗(yàn):當(dāng)腫瘤體積達(dá)50mm3時(shí)(圖6A),預(yù)先給予CAR-T細(xì)胞,CAR-TFoxp3組腫瘤清除速度略快于CAR-TConv組(圖6B)。腫瘤清除后,兩組外周血CAR-T細(xì)胞計(jì)數(shù)無(wú)差異(圖6C),但CAR-TFoxp3組初始/干細(xì)胞記憶T細(xì)胞比例更高,終末效應(yīng)記憶T細(xì)胞比例更低(圖6D-E)。第29天再次用腫瘤細(xì)胞攻擊,CAR-TFoxp3組腫瘤生長(zhǎng)最慢(圖6F)。
驗(yàn)證Foxp3關(guān)鍵作用:將CAR-TFoxp3(340–390)、CAR-TFoxp3和CAR-TConv細(xì)胞注射到荷瘤小鼠(圖6G),初期腫瘤均快速清除(圖6H)。再次攻擊后,CAR-TFoxp3(340–390)組腫瘤生長(zhǎng)速度與CAR-TConv組相似且快于CAR-TFoxp3組(圖6I),其TIM-3和LAG-3比例與CAR-TConv組相當(dāng)且高于CAR-TFoxp3組。
綜上,CAR-TFoxp3細(xì)胞增強(qiáng)的抗腫瘤效果及較低的耗竭相關(guān)抑制分子水平依賴于Foxp3的第340-390位殘基,證實(shí)了Foxp3在CAR-T細(xì)胞抗腫瘤活性中的關(guān)鍵作用。
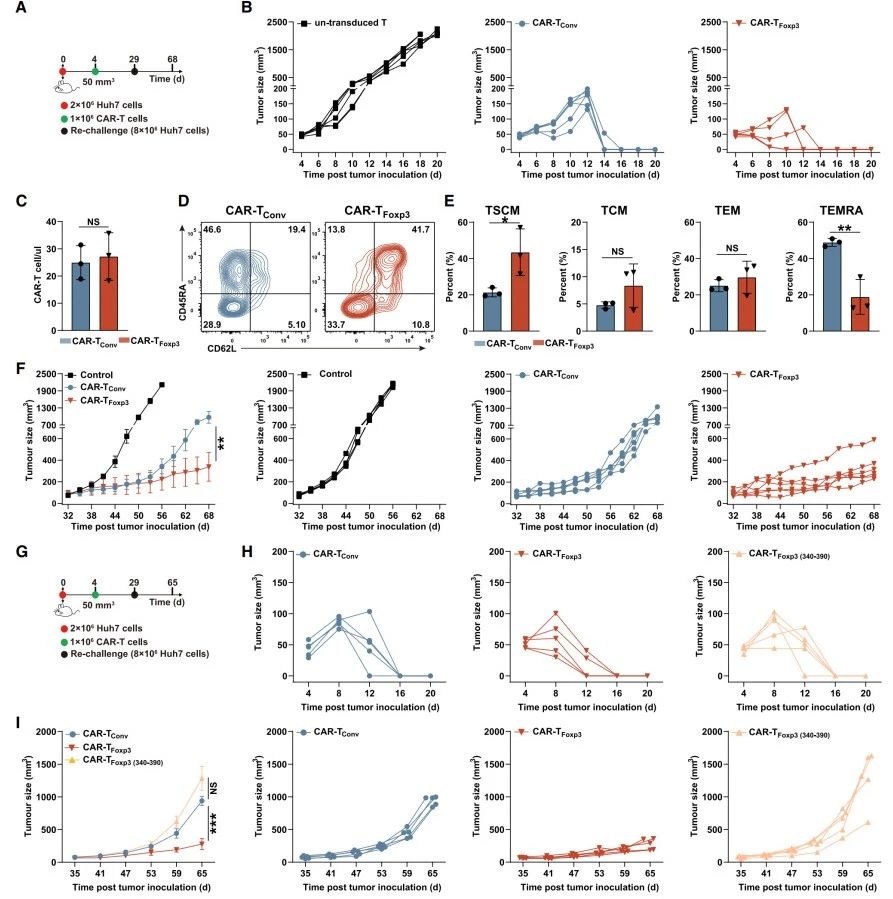
圖6.Foxp3介導(dǎo)CAR-TFoxp3細(xì)胞在體內(nèi)的持久抗腫瘤效應(yīng)與低耗竭特性
7、人源化NSG模型下CAR-TFoxp3細(xì)胞的雙重特性——強(qiáng)抗癌、無(wú)免疫抑制
模型構(gòu)建與細(xì)胞檢測(cè):使用CD34造血干細(xì)胞構(gòu)建人源化NSG小鼠,在外周血和脾臟中檢測(cè)到多種人類免疫細(xì)胞,外周血中人類免疫細(xì)胞(hCD45+)占總免疫細(xì)胞比例超60%,脾臟中人類免疫細(xì)胞占活細(xì)胞比例可達(dá)80%。
抗腫瘤效果:建立皮下異種移植瘤模型并給予不同CAR-T細(xì)胞治療(圖7A),CAR-TFoxp3細(xì)胞顯著抑制腫瘤生長(zhǎng),五只小鼠中有兩只完全緩解,其余三只腫瘤大小也明顯減小(圖7B-C)。
細(xì)胞及因子分析:第25天分析顯示,與CAR-TConv組相比,CAR-TFoxp3細(xì)胞耗竭相關(guān)抑制分子(PD-1和LAG-3)水平更低,腫瘤浸潤(rùn)的CD4+T細(xì)胞更多(圖7D-F);兩組腫瘤浸潤(rùn)的人類免疫細(xì)胞組成相似(圖7F),小鼠脾臟重量和重要器官無(wú)顯著差異(圖7E)。多重細(xì)胞因子檢測(cè)表明,CAR-TFoxp3組中TNF-α和IL-10分泌量更低,細(xì)胞因子水平更穩(wěn)定,IL-1β、IL-4等多種細(xì)胞因子平均水平低于CAR-TConv組,提示細(xì)胞因子風(fēng)暴減輕,而對(duì)CAR-T細(xì)胞活化增殖關(guān)鍵的IL-2濃度兩組無(wú)顯著差異(圖7G)。
綜上,CAR-TFoxp3細(xì)胞在人源化NSG模型中展現(xiàn)出增強(qiáng)的抗腫瘤活性,同時(shí)維持安全性,未誘導(dǎo)免疫抑制。
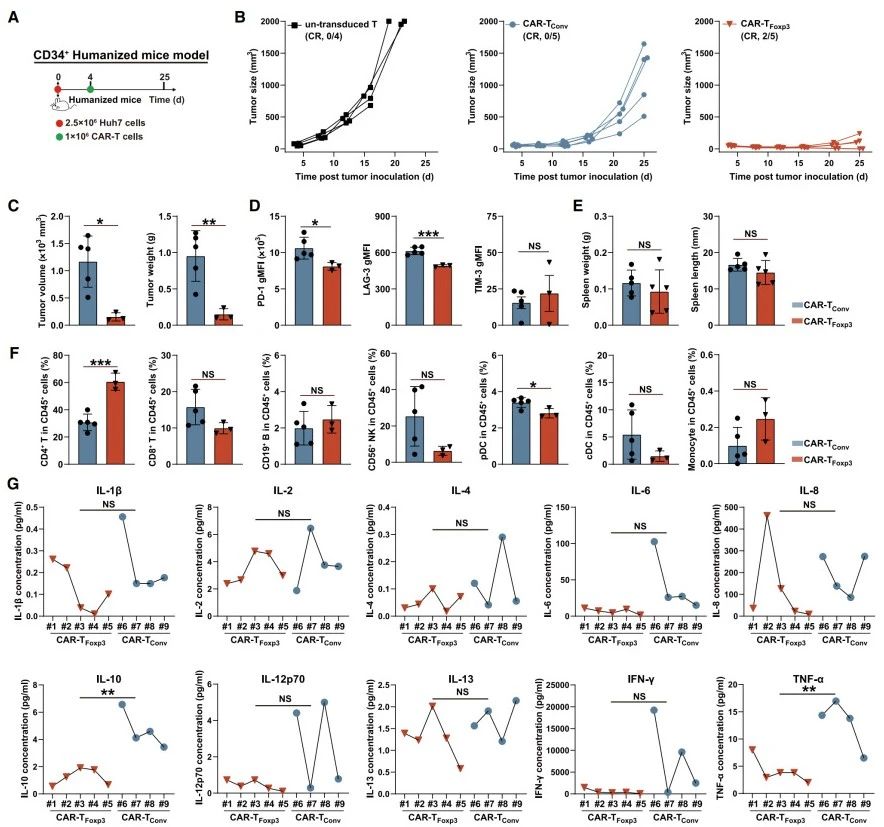
圖7.人源化NSG模型中CAR-TFoxp3細(xì)胞的強(qiáng)效抗腫瘤活性與非免疫抑制特性
研究結(jié)論
本研究圍繞CAR-TFoxp3細(xì)胞的抗腫瘤作用展開(kāi)深入探究。通過(guò)構(gòu)建小鼠皮下異種移植瘤模型、腫瘤再攻擊模型以及人源化NSG小鼠模型,從多維度驗(yàn)證了CAR-TFoxp3細(xì)胞的特性。在小鼠皮下異種移植瘤模型中,CAR-TFoxp3細(xì)胞腫瘤抑制效果顯著,細(xì)胞耗竭程度低,且在轉(zhuǎn)錄組水平展現(xiàn)出獨(dú)特的基因表達(dá)模式。腫瘤再攻擊模型證實(shí)其抗腫瘤作用的持久性,且該效果依賴于Foxp3的第340-390位殘基。在人源化NSG模型中,CAR-TFoxp3細(xì)胞不僅能有效抑制腫瘤生長(zhǎng),實(shí)現(xiàn)部分小鼠腫瘤完全緩解,還能維持較低的耗竭標(biāo)志物水平,減輕細(xì)胞因子風(fēng)暴 ,且不誘導(dǎo)免疫抑制,同時(shí)對(duì)其他免疫細(xì)胞組成及小鼠重要器官無(wú)不良影響。這些結(jié)果表明,CAR-TFoxp3細(xì)胞在體內(nèi)具有優(yōu)異的抗腫瘤活性和良好的安全性,為腫瘤免疫治療提供了新的潛在策略和理論依據(jù)。
END
Peng 撰文
Tang 校稿
