Adv. Sci.|南醫大倪春輝團隊破局肺纖維化:鎖定脂肪酸氧化與糖酵解 “失衡點”,挖掘關鍵治療靶點

英文標題:Fatty Acid Oxidation-Glycolysis Metabolic Transition Affects ECM Homeostasis in Silica-Induced Pulmonary Fibrosis
中文標題:脂肪酸氧化-糖酵解代謝轉換影響二氧化硅誘導的肺纖維化中細胞外基質穩態
發表期刊:Advanced Science
影響因子:14.3
客戶單位:南京醫科大學
百趣提供服務:新一代代謝組學NGM 2
1研究背景
肺纖維化是慢性致命性疾病,長期接觸二氧化硅粉塵可引發硅肺,是常見且嚴重的職業病,給個人和社會帶來沉重負擔。纖維化以成肌纖維細胞異常增殖和細胞外基質(Exracellular Matrix, ECM)過度產生為特征。代謝重編程在肺纖維化中起重要作用,糖酵解和脂肪酸氧化(Fatty Acid Oxidation, FAO)代謝紊亂可能影響ECM的平衡,但具體機制不明。本研究旨在探究其機制,并評估針對調控相關代謝途徑和缺氧誘導因子-1α(HIF-1α)的治療潛力。
2研究結果
1、小鼠肺纖維化的發生伴隨著細胞代謝的重構
為分析二氧化硅刺激后的細胞代謝狀態,構建經氣管內單次滴注二氧化硅懸液的小鼠模型,于暴露后7天、14天、28天收集肺組織。H&E染色結果(圖1A)顯示,隨硅肺進展,肺部炎癥和纖維化程度逐漸加重。羥脯氨酸測定表明,肺組織膠原水平隨二氧化硅暴露時間延長顯著升高(圖1B)。在硅肺進展過程中,細胞外基質成分(如纖維連接蛋白、膠原蛋白 I、彈性蛋白)的蛋白質水平通過Western blot檢測呈時間依賴性增加(圖1C)。為進一步明確膠原沉積形式,對肺組織病理切片進行Masson染色、天狼星紅染色及偏振光成像,結果顯示纖維化肺組織中膠原纖維大量沉積,結構紊亂且以不溶性膠原為主(圖1D)。
為深入探究代謝重構機制,進一步開展轉錄組和代謝組分析。代謝組學分析(圖1E)顯示,肺纖維化小鼠肺組織中糖酵解中間產物(如3-磷酸甘油酸、葡萄糖-6-磷酸、磷酸烯醇丙酮酸)含量顯著增加,而FAO相關代謝物(如3-羥基丁酸、L-肉堿、硬脂酰肉堿)水平降低,提示糖酵解增強、FAO 減弱的代謝表型。Western blot檢測(圖1F)進一步證實,糖酵解關鍵蛋白(HIF-1α、己糖激酶2(HK2)、葡萄糖轉運蛋白3(GLUT3)、磷酸果糖激酶2(PFK2))表達上調,而FAO調控蛋白(肉堿棕櫚酰轉移酶1a(CPT1a)、過氧化物酶體增殖物激活受體γ(PPAR-γ)、PPAR-α水平顯著下降,與轉錄組和代謝組結果一致。
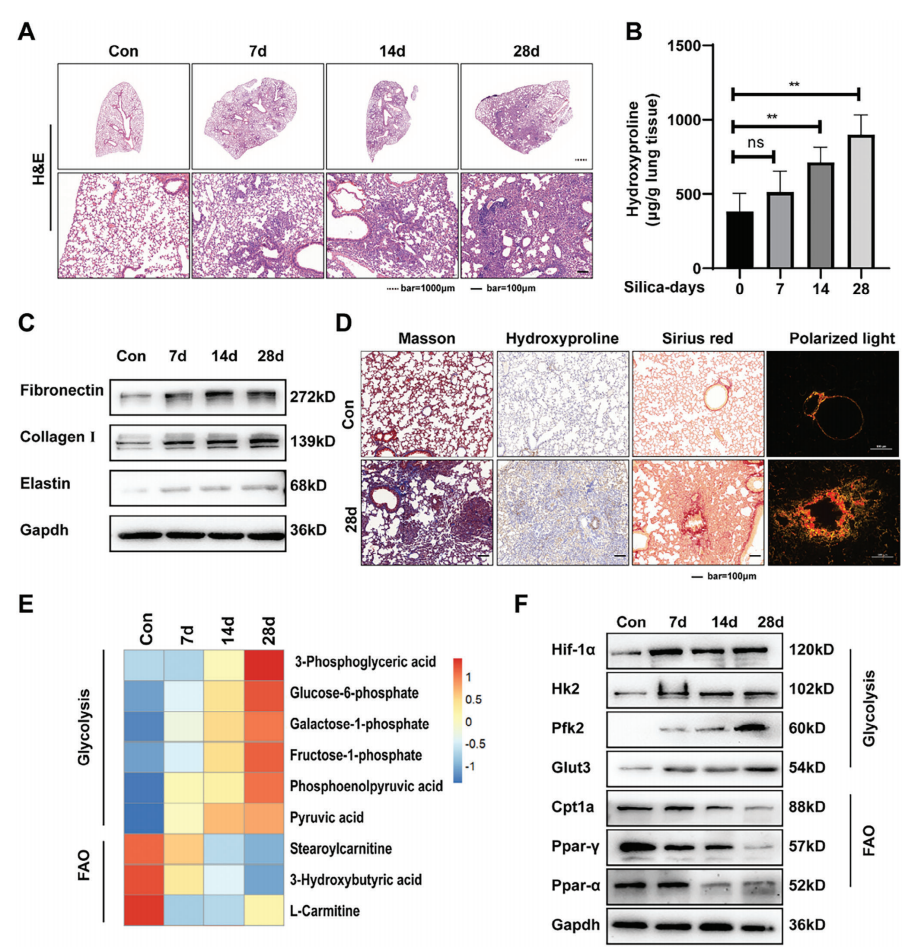
圖1 小鼠肺纖維化的發展伴隨著細胞代謝的重組
2、活化的成纖維細胞通過糖酵解和FAO的代謝擾動實現ECM的沉積
為探究成纖維細胞活化與代謝轉變的關聯,通過轉化生長因子-β1(TGF-β1)誘導建立MRC-5成纖維細胞活化模型。結果顯示,隨TGF-β1濃度增加,α-平滑肌肌動蛋白(α-SMA)和I型膠原mRNA水平顯著升高(圖2A)。Western blot和免疫熒光分析表明,活化細胞中纖維連接蛋白、膠原蛋白I、彈性蛋白等ECM 蛋白表達顯著增加(圖2B-C)。線粒體熒光探針(Mito-Tracker)標記顯示,TGF-β1處理后線粒體信號強度顯著減弱,提示線粒體功能受損(圖2D)。同時,能量穩態核心調控因子AMP激活蛋白激酶(AMPK)的磷酸化水平(p-AMPK)顯著下降(圖2E),進一步表明代謝狀態異常。
qRT-PCR和Western blot顯示,活化成纖維細胞中糖酵解關鍵基因(HIF-1α、HK2、PFK2)及蛋白表達上調,而FAO相關基因(CPT1a、PPAR-γ)及蛋白水平下調,與硅肺小鼠肺組織中的代謝表型一致。細胞代謝功能檢測(ECAR和OCR)證實,活化細胞糖酵解能力增強,FAO水平降低(圖2H-I)。綜上,肺纖維化發展與成纖維細胞中FAO下調、糖酵解上調的代謝擾動密切相關。
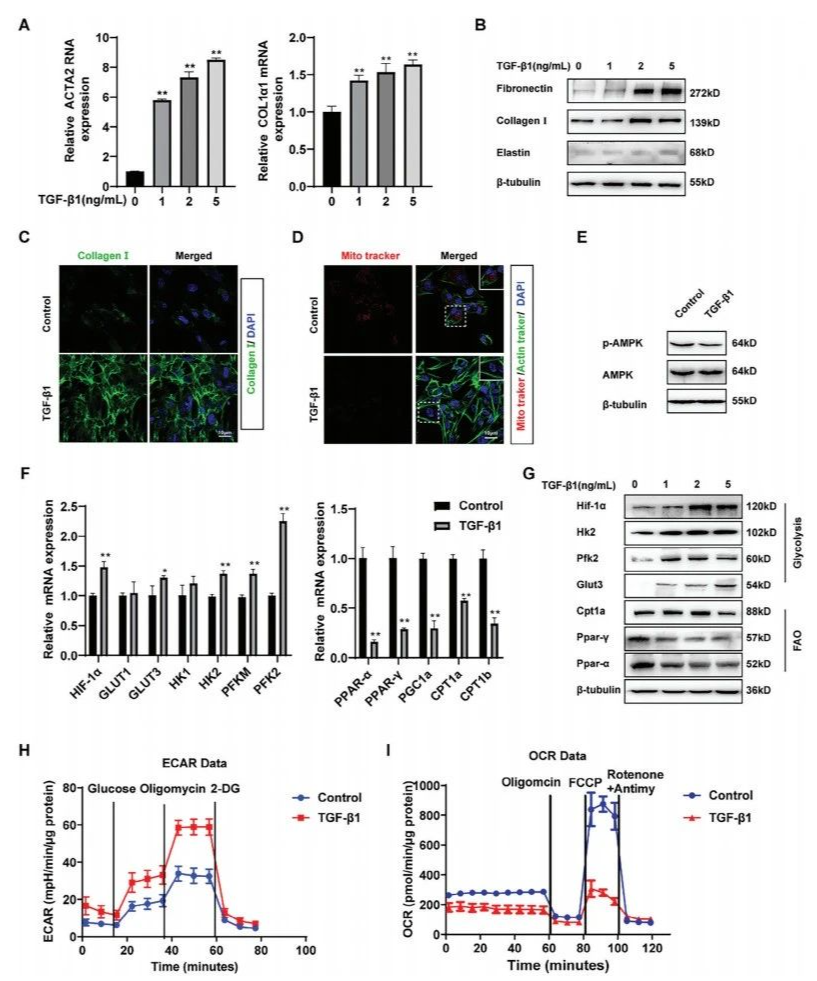
圖2 活化成纖維細胞的ECM沉積是通過糖酵解和FAO的代謝擾動完成的
3、抑制糖酵解或增強FAO會影響活化成纖維細胞中的ECM沉積
為探究代謝干預對ECM沉積的影響,使用糖酵解抑制劑3PO或FAO激活劑吡格列酮處理TGF-β1活化的成纖維細胞。結果顯示,兩種干預均能顯著減少ECM蛋白(纖維連接蛋白、膠原I、彈性蛋白)的表達(圖3A)。免疫熒光染色表明,3PO處理導致細胞外膠原I熒光信號減弱,而吡格列酮處理則使細胞內膠原I信號降低(圖3B),提示兩者通過不同機制影響膠原分布。進一步分析顯示,抑制糖酵解可減少不溶性ECM,同時增加培養基中可溶性膠原含量(圖3C-D),伴隨賴氨酸氧化酶(LOX)活性降低和甘氨酸合成減少(圖3E-F);而增強FAO對ECM溶解度無顯著影響,但可促進溶酶體與膠原的共定位(圖3G),并增強外源性DQ-膠原的內吞降解(圖3H)。綜上,抑制糖酵解通過削弱ECM合成與修飾發揮作用,增強FAO則通過促進細胞內降解途徑抑制ECM沉積,兩者均能有效抑制纖維化相關ECM積累。

圖3 抑制糖酵解或增強FAO影響活化成纖維細胞中ECM沉積
4、抑制糖酵解和增強脂肪酸氧化在體內的干預和治療效果
為驗證代謝干預的體內療效,構建二氧化硅誘導的肺纖維化小鼠模型,分別在暴露后立即(干預組)或纖維化形成后(治療組)給予糖酵解抑制劑3PO或FAO激活劑吡格列酮。干預結果(圖4A-B)顯示,暴露后立即給藥可顯著減輕肺泡結構破壞和肺纖維化程度,Masson染色和天狼星紅染色顯示Ⅰ型膠原、纖維連接蛋白等ECM沉積顯著減少。然而,3PO干預組肺組織仍存在羥脯氨酸陽性染色(圖4B),提示殘留膠原降解不完全;吡格列酮干預組則通過CHP染色顯示細胞內膠原降解信號增強(圖4D),表明其促進ECM內吞降解的作用。
治療效果(圖5A-B)顯示,對已形成的纖維化(造模28天后給藥),吡格列酮僅部分緩解膠原沉積,而3PO可減輕肺損傷但仍有膠原碎片殘留。Western blot證實,兩種干預均能下調纖維連接蛋白、膠原I、彈性蛋白的表達(圖5C)。CHP染色(圖5D)進一步顯示,3PO治療組肺組織中CHP熒光強度較低,提示變性膠原減少;而吡格列酮組CHP信號較強且集中于細胞核周圍,表明其促進膠原內吞降解的作用。然而,羥脯氨酸染色與CHP結果不完全一致,可能因前者檢測完整膠原,后者特異性結合變性膠原,提示兩種藥物對ECM的作用路徑不同:3PO主要抑制膠原合成,吡格列酮則通過增強FAO促進膠原的細胞內降解。

圖4 抑制糖酵解或增強FAO可以阻止體內纖維化的進展
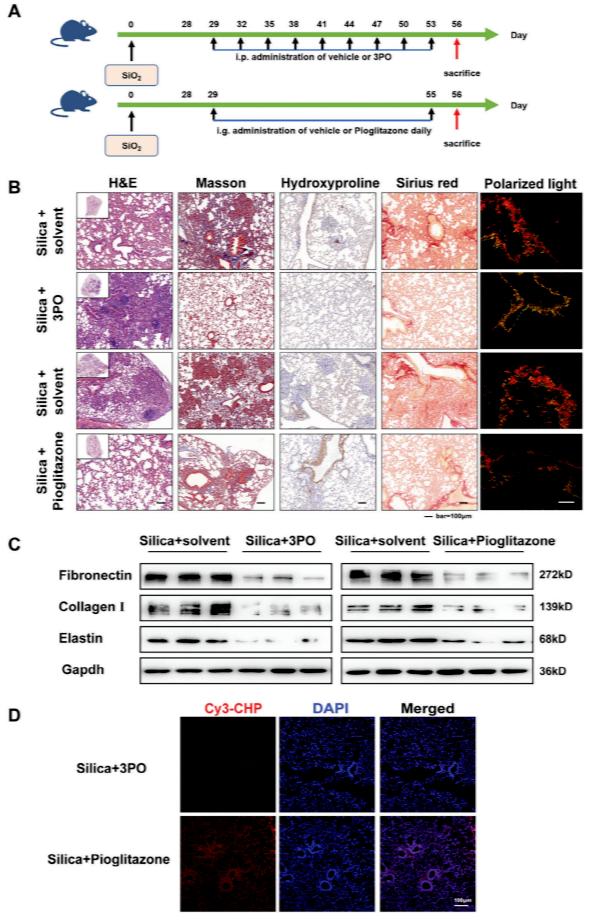
圖5 3PO或吡格列酮給藥可在體內緩解已建立的肺纖維化
5、HIF-1α調節成纖維細胞中脂肪酸氧化-糖酵解的轉化
為解析單一代謝干預的復雜效應,研究發現:3PO抑制糖酵解可顯著增加耗氧率(Oxygen Consumption Rates, OCR),提示FAO代償性激活;而吡格列酮增強FAO僅輕度減少細胞外酸化率(Extracellular Acidification Rates, ECAR),糖酵解未顯著受抑。這表明,單獨干預糖酵解或FAO會引發難以預測的代謝補償,因此篩選調控雙代謝途徑的核心因子尤為重要。
轉錄組分析顯示,HIF-1α在纖維化肺組織中顯著上調。進一步實驗(圖6B-C)顯示,在TGF-β1誘導的成纖維細胞活化模型中,HIF-1α mRNA和蛋白水平均呈時間依賴性升高:刺激24小時后,HIF-1α mRNA表達增加2.3倍(圖6B),蛋白水平在48小時達到峰值(圖6C),且其降解被環己酰亞胺(CHX)抑制,提示TGF-β1通過延長蛋白半衰期增強HIF-1α穩定性。免疫組化證實,特發性肺纖維化(IPF)和硅肺患者的纖維化區域中,HIF-1α表達上調,而FAO關鍵轉錄因子PPAR-γ表達下調,且兩者在小鼠硅肺模型中呈現一致趨勢(圖6A)。
機制研究表明,TGF-β1通過抑制HIF-1α泛素化,在常氧條件下穩定其蛋白水平。進一步功能實驗顯示,敲低HIF-1α可逆轉TGF-β1誘導的糖酵解增強(ECAR降低)和FAO減弱(OCR恢復),并恢復線粒體數量及AMPK活性(圖6D-H),證實HIF-1α是調控FAO-糖酵解代謝切換的核心分子。
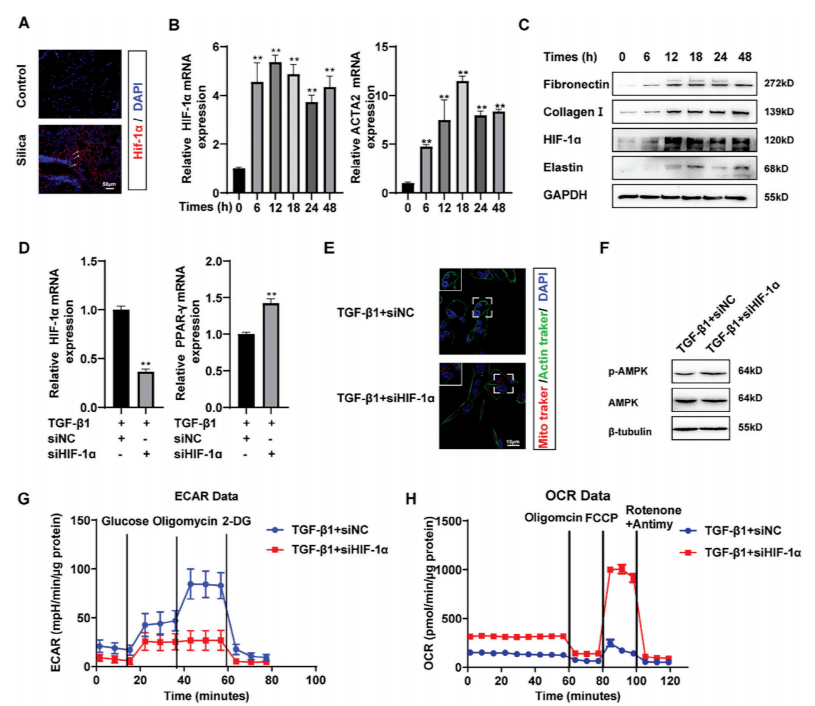
圖6 HIF-1α調控成纖維細胞FAO糖酵解的轉化
6、HIF-1α抑制通過調節糖酵解-FAO代謝紊亂減少ECM沉積
為探究抑制HIF-1α能否通過調控糖酵解-FAO代謝失衡增強ECM清除,在MRC-5細胞中敲低HIF-1α,結果顯示ECM相關蛋白(如纖維連接蛋白、膠原I)表達顯著降低(圖7A)。免疫熒光證實,胞內及胞外膠原I熒光強度均顯著減弱(圖7C),表明HIF-1α抑制可有效減少體外TGF-β1誘導的ECM沉積。
機制研究發現,敲低HIF-1α后,膠原編碼基因(如 COL1A1)轉錄水平未顯著改變(圖7B),但ECM修飾酶(LOX、LOXL2、P4AH1、PLOD1、PLOD2)的mRNA 水平顯著下調(圖7D),伴隨LOX酶活性降低和可溶性膠原增加(圖7F)。此外,成纖維細胞對DQ-膠原的內吞效率及溶酶體共定位顯著增強(圖7G-I),提示ECM交聯減少且降解途徑激活。
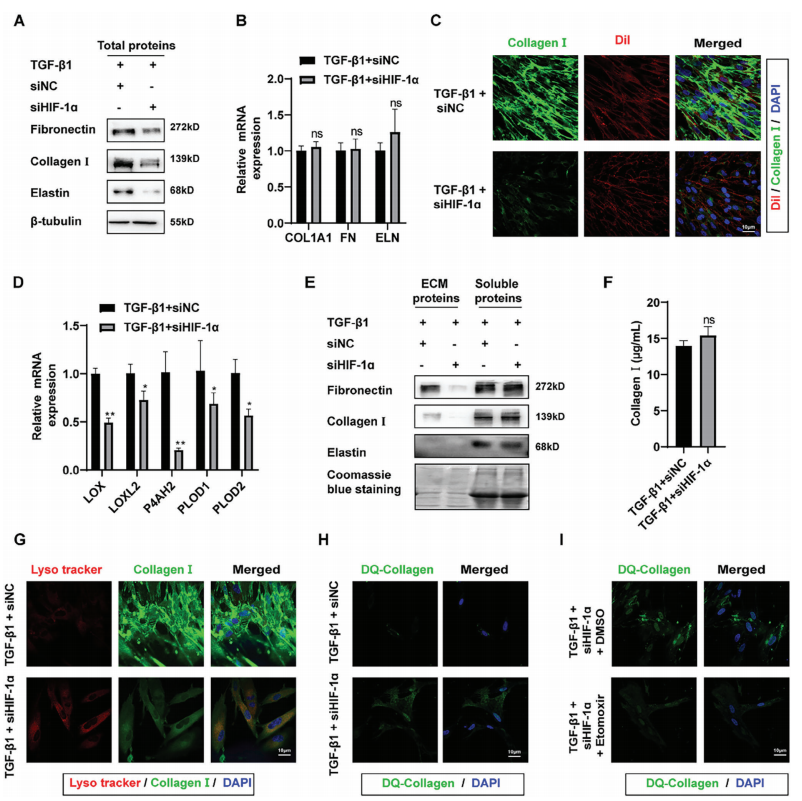
圖7 HIF-1α抑制通過調節糖酵解-FAO代謝紊亂減少ECM沉積
7、抑制HIF-1α調節的脂肪酸氧化-糖酵解代謝擾動在體內減輕肺纖維化
為驗證HIF-1α抑制的體內治療效果,在二氧化硅粉塵滴注后的第二天或已形成纖維化的小鼠(造模28天后),分別用兩種代謝調節劑(3PO聯合吡格列酮)或一種HIF-1α抑制劑(LW6)處理小鼠,以評估干預或治療效果(圖8A和圖9A)。
對小鼠肺組織進行的H&E染色顯示,LW6組和3PO聯合吡格列酮組小鼠的肺部纖維化程度有所減輕。此外,Masson染色和羥脯氨酸免疫組化結果表明,小鼠肺組織中的膠原沉積相對減少。同時,天狼星紅染色顯示膠原沉積減少,偏振光顯微鏡觀察發現,LW6組和3PO聯合吡格列酮組中復雜且緊密堆積的膠原減少(圖8B和圖9B)。Western blot結果顯示,LW6組和3PO聯合吡格列酮組中纖連蛋白、I型膠原和彈性蛋白的表達下調(圖8C和圖9C)。與此一致的是,研究者發現纖維化病變的嚴重程度和位置有了明顯改善(圖8D和圖9D)。這些結果表明,在體內抑制HIF-1α調控的代謝轉變能夠有效減少暴露于二氧化硅粉塵的小鼠肺部ECM的過度沉積。
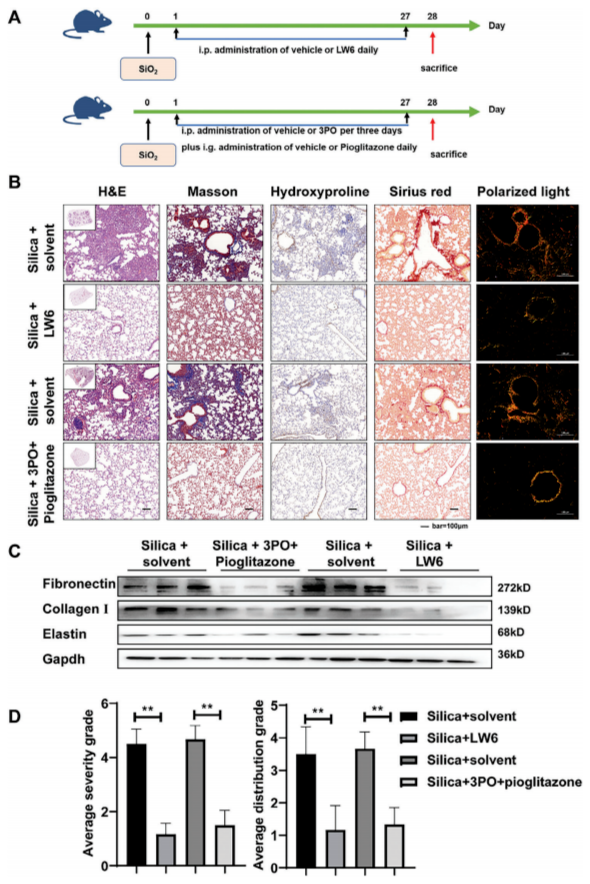
圖8 抑制HIF-1β或FAO-糖酵解代謝擾動可阻止體內纖維化的進展
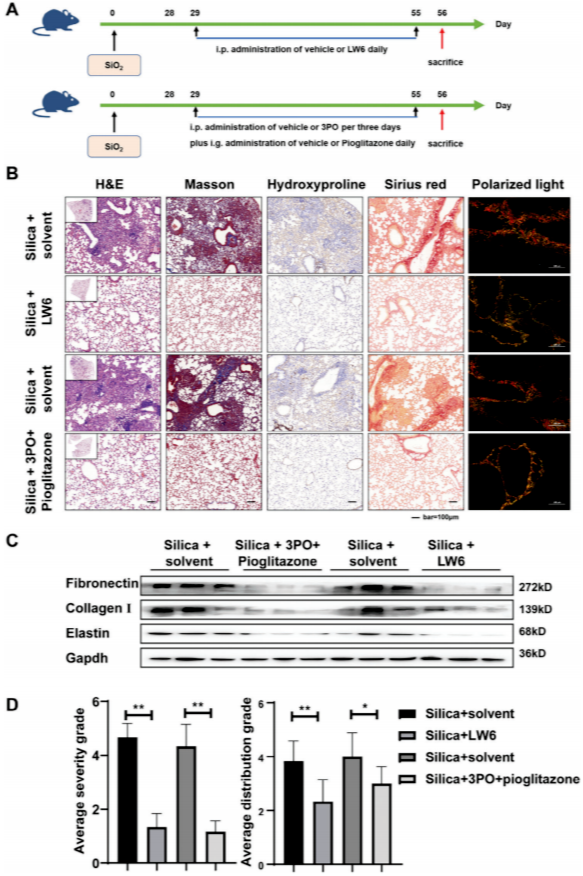
圖9 抑制HIF-1α或改善FAO-糖酵解代謝擾動促進體內已建立的纖維化消退
3
研究結論
本研究發現,在二氧化硅誘導的肺纖維化中,糖酵解增強和FAO減少,促使細胞外基質合成與降解失衡,推動疾病發展。HIF-1α在調節FAO-糖酵解代謝轉換、影響ECM重塑方面至關重要。因此,代謝療法或靶向HIF-1α有望成為清除纖維化ECM、改善肺功能的有效策略。
END
楊炎 撰文
Peng 校稿
