J Ethnopharmacol.|福中醫(yī)研究團(tuán)隊(duì)新發(fā)現(xiàn)!清解扶正顆粒精準(zhǔn)操控巨噬細(xì)胞,讓結(jié)直腸癌“剎車”!

英文標(biāo)題:Mechanism of Qingjie Fuzheng Granules in inhibiting colitis associated colorectal cancer by regulating TLR4 and IL-4R mediated macrophage polarization
發(fā)表期刊:Journal of Ethnopharmacology
影響因子:5.4
合作單位:福建中醫(yī)藥大學(xué)
百趣提供服務(wù):DIA中藥入血組、中藥NGM 2
研究背景
清解扶正顆粒(QFG)是一種中藥復(fù)方,已被用作結(jié)腸炎相關(guān)結(jié)直腸癌(CAC)的輔助治療,但其作用機(jī)制尚不明確。福建中醫(yī)藥大學(xué)研究團(tuán)隊(duì)在Journal of Ethnopharmacology(IF=5.4)上發(fā)表了題為“Mechanism of Qingjie Fuzheng Granules in inhibiting colitis associated colorectal cancer by regulating TLR4 and IL-4R mediated macrophage polarization”的研究文章,旨在探究QFG抗CAC的潛在機(jī)制是否與巨噬細(xì)胞極化相關(guān),通過動(dòng)物及細(xì)胞模型,最終證實(shí)了,QFG中的多種單體成分可分別結(jié)合MD2或IL-4R,通過誘導(dǎo)巨噬細(xì)胞極化從而抑制CAC的發(fā)生發(fā)展。
技術(shù)路線
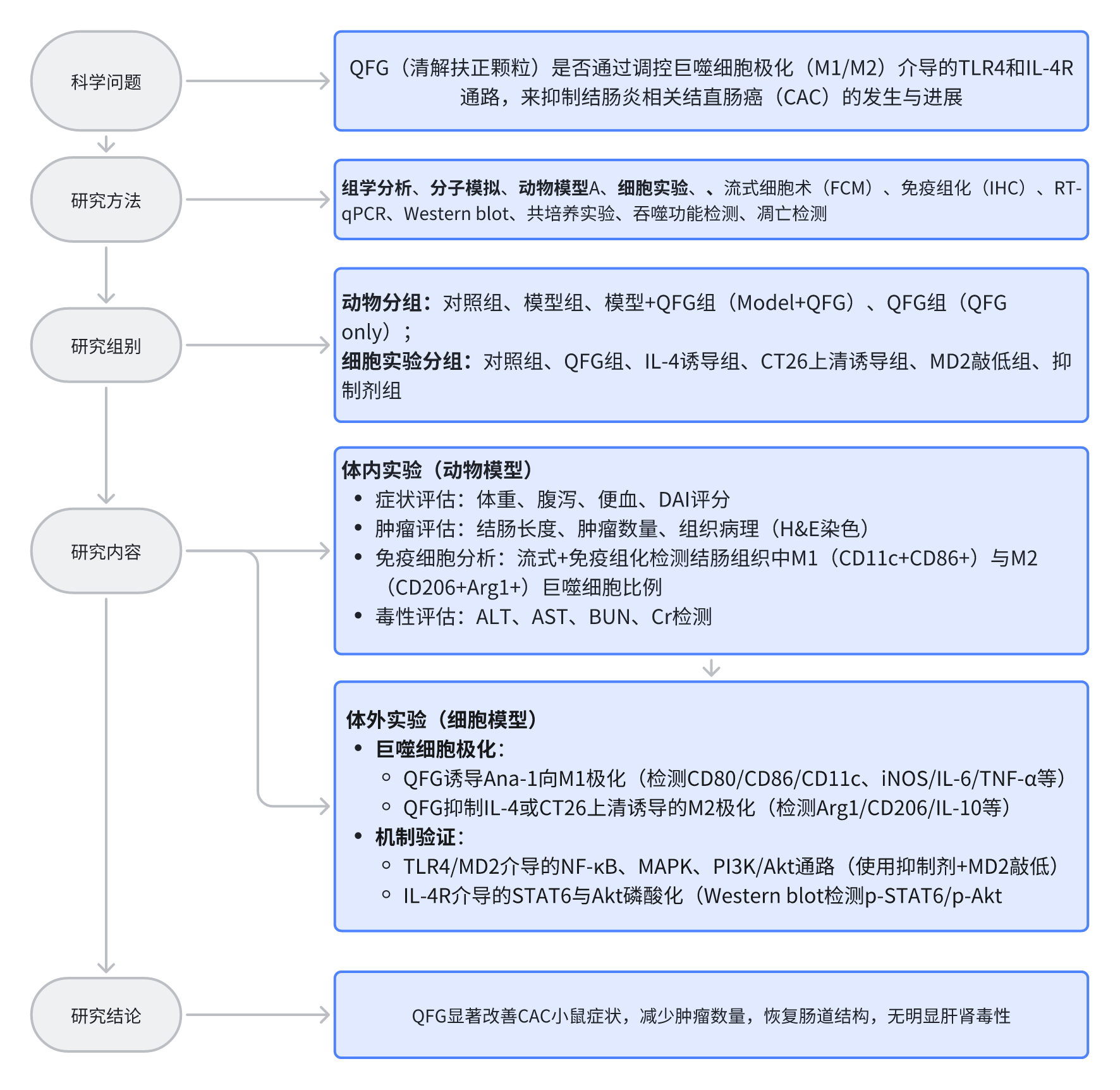
研究結(jié)果
1.QFG的活性成分與TLR4/MD2受體復(fù)合物或IL-4受體表現(xiàn)出強(qiáng)結(jié)合親和力
為探究QFG抑制CAC發(fā)生的機(jī)制是否與巨噬細(xì)胞極化相關(guān),研究人員先利用非靶向代謝組學(xué)對(duì)QFG粉末的成分進(jìn)行了鑒定(圖1A-B),其鑒定出的化合物與Biotree TCM和BT-HERB數(shù)據(jù)庫中的1506個(gè)條目匹配。
有研究表明,TLR4/MD2受體復(fù)合物和IL-4R介導(dǎo)的通路在調(diào)節(jié)M1型和M2型巨噬細(xì)胞中至關(guān)重要,因此研究人員利用分子對(duì)接分析,對(duì)探究QFG與其的關(guān)系,結(jié)果共鑒定出10種活性成分與TLR4/MD2受體復(fù)合物以及IL-4R之間均具有強(qiáng)結(jié)合親和力,表明QFG具有調(diào)節(jié)巨噬細(xì)胞極化的潛力(圖1C)。
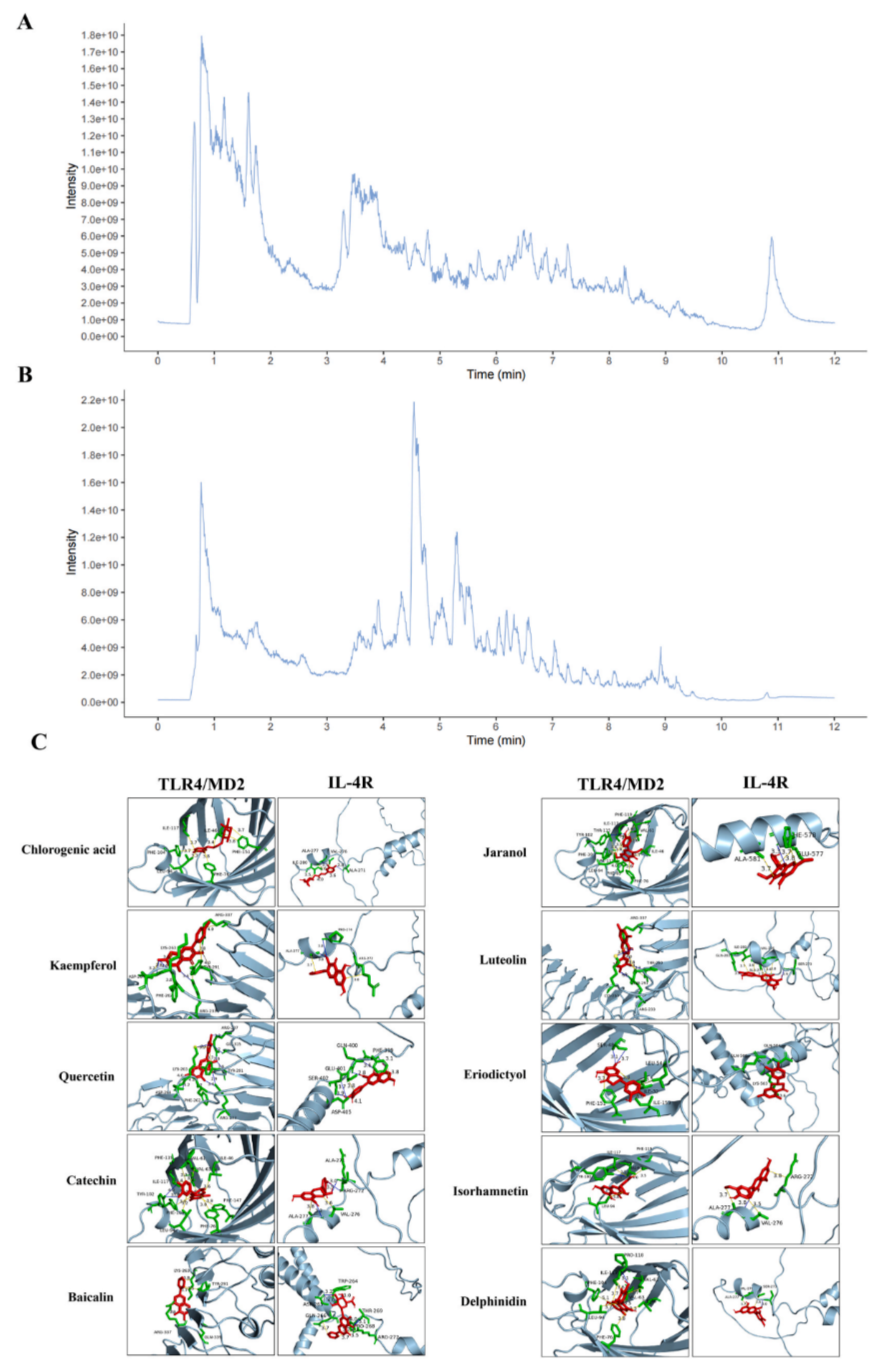
圖1. QFG中化合物的LC-MS/MS分析和巨噬細(xì)胞極化相關(guān)潛在成分的分子對(duì)接分析
2.QFG改善CAC小鼠的癥狀并抑制腫瘤發(fā)展
為了更加清楚QFG的作用機(jī)制,研究人員構(gòu)建了CAC小鼠模型,6只/組,共設(shè)計(jì)了4個(gè)實(shí)驗(yàn)分組,分別是Control組、Model+QFG組、Model組、QFG組(圖2A)。喂養(yǎng)期間進(jìn)行了體重記錄、糞便隱血評(píng)分、腹瀉指數(shù)評(píng)分;2個(gè)月后,分別記錄了每只鼠的結(jié)腸長度、結(jié)腸表面腫瘤數(shù)量、肝臟、胸腺和脾臟的重量(圖2B-C),并對(duì)結(jié)腸組織進(jìn)行HE染色,同時(shí)采集血樣用做其他分析。
結(jié)果顯示,與對(duì)照組相比,模型組小鼠的結(jié)腸長度顯著縮短、腫瘤數(shù)量增多、脾指數(shù)顯著升高、體重下降、腹瀉和便血等情況均被QFG改善,且并未造成肝腎功能損傷(圖2D-E);此外,QFG對(duì)結(jié)腸的生理結(jié)構(gòu)也有一定改善(圖2F)。這些數(shù)據(jù)表明,QFG可以抑制CAC小鼠的腫瘤發(fā)展。
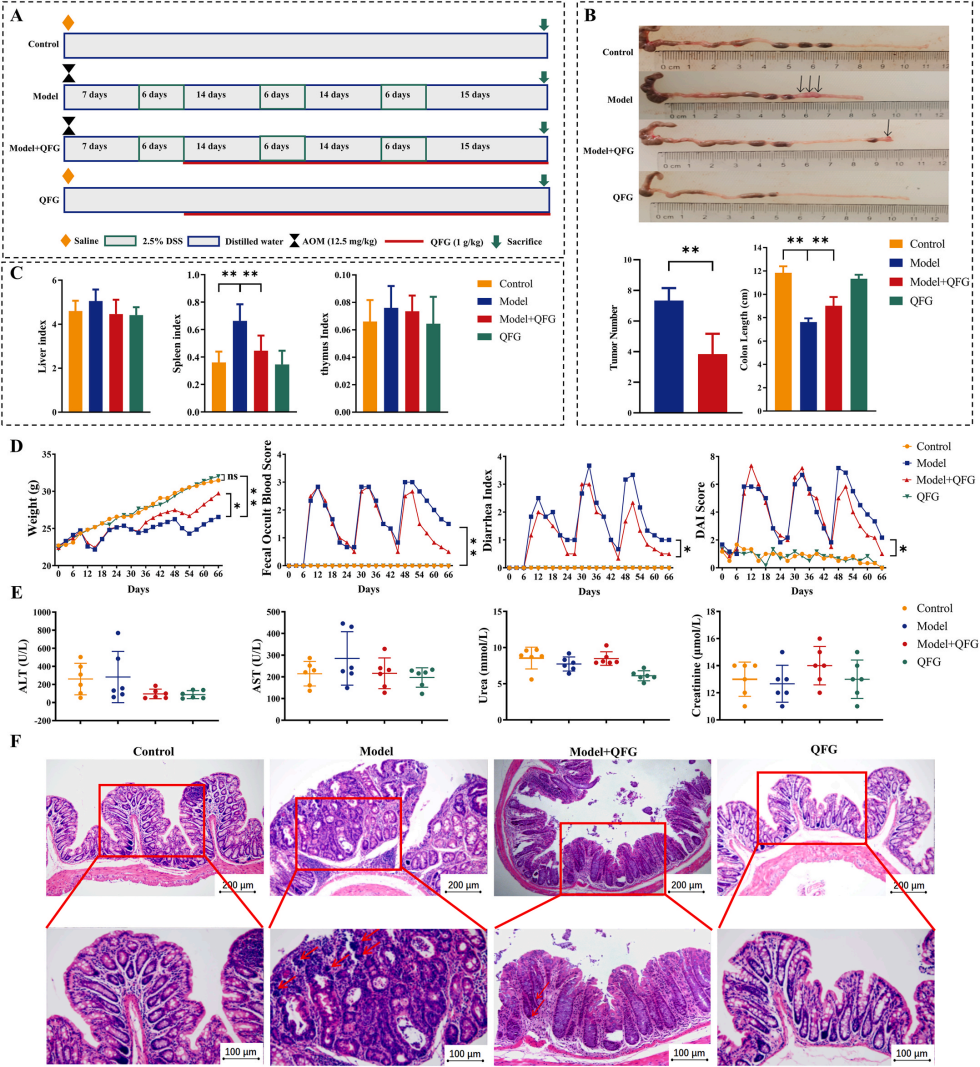
圖2. QFG對(duì)CAC小鼠整體健康狀況和腫瘤形成的影響
3.QFG調(diào)節(jié)CAC小鼠腸道組織的巨噬細(xì)胞極化
流式和免疫組化實(shí)驗(yàn)顯示,M2樣標(biāo)志物CD206呈現(xiàn)顯著下降,而M1樣標(biāo)志物CD11c則顯著增加,表明QFG可以增加M1樣巨噬細(xì)胞的存在并減少M(fèi)2樣巨噬細(xì)胞的數(shù)量(圖3A);此外,相較對(duì)照組,模型組中F4/80、CD68及離子鈣結(jié)合適配分子(IBA1)的表達(dá)水平較對(duì)照組顯著升高,表明QFG能有效減輕由AOM/DSS誘導(dǎo)的小鼠CAC結(jié)腸黏膜炎癥(圖3B-D)。
與此同時(shí),在AOM/DSS誘導(dǎo)的CAC模型中,與對(duì)照組相比,巨噬細(xì)胞M2標(biāo)志物、巨噬細(xì)胞M1標(biāo)志物的表達(dá)量顯著升高,但QFG處理后,CD206和精氨酸酶1的表達(dá)量顯著降低(圖3E-F),同時(shí)CD11c和CD86的表達(dá)量明顯增加(圖3G-H),這些結(jié)果表明,相較于模型組,QFG可促進(jìn)M1樣巨噬細(xì)胞的募集,同時(shí)抑制M2樣巨噬細(xì)胞的浸潤。這些結(jié)果與流式細(xì)胞術(shù)獲得的數(shù)據(jù)一致。
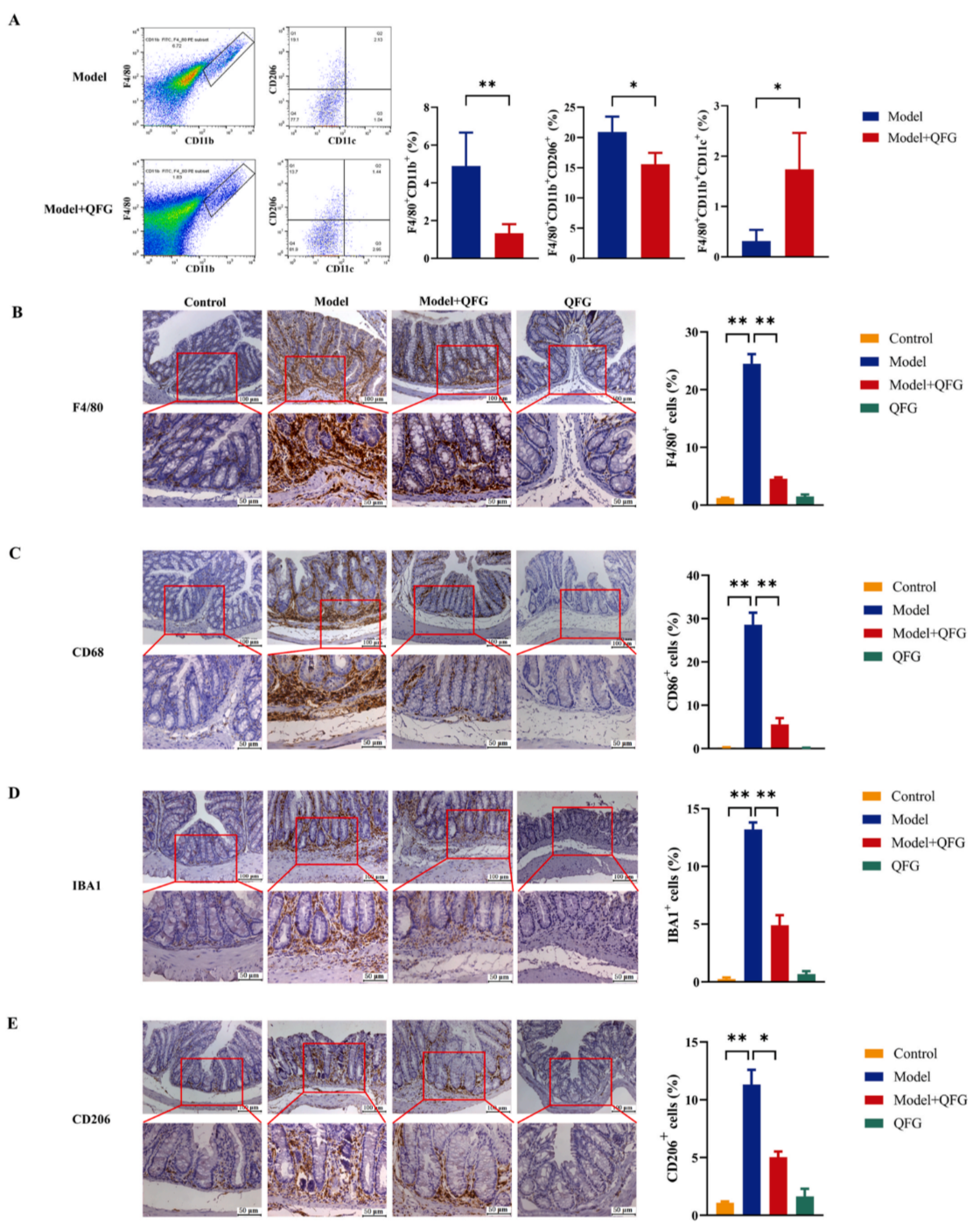
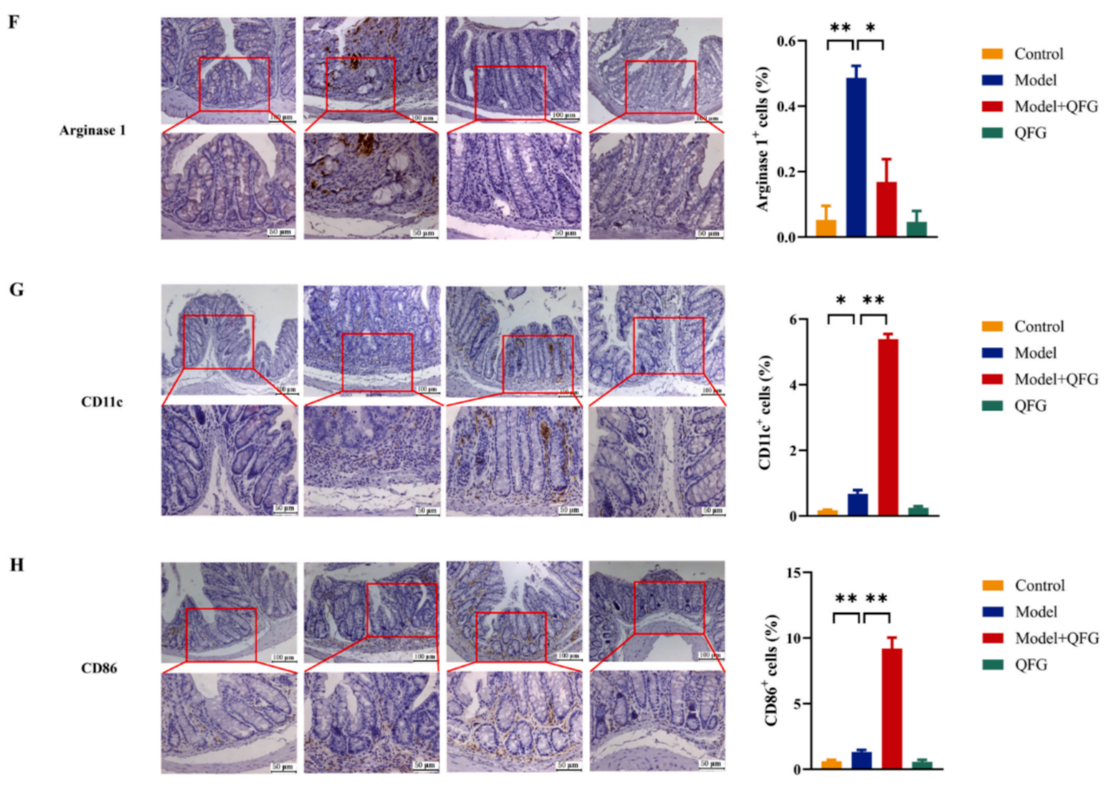
圖3. QFG對(duì)CAC小鼠腸道巨噬細(xì)胞極化的影響
4.QFG在體外促進(jìn)Ana-1巨噬細(xì)胞向M1型表型極化
為驗(yàn)證QFG對(duì)M1樣表型的促進(jìn)作用,研究人員在體外實(shí)驗(yàn)中檢測(cè)了QFG對(duì)Ana-1細(xì)胞中CD80、CD86、CD11c、IL-1β、IL-6、TNF-α、MCP-1和iNOS水平的影響。流式實(shí)驗(yàn)顯示,QFG處理后CD80、CD86和CD11c的熒光強(qiáng)度呈現(xiàn)顯著劑量依賴性增強(qiáng)(圖4A)。RT-qPCR分析表明,IL-1β、IL-6、TNF-α、MCP-1和iNOS的mRNA表達(dá)量也呈QFG劑量依賴性上升(圖4B)。此外,TNF-α、MCP-1和IL-6的蛋白表達(dá)量也出現(xiàn)類似增長(圖4C)。這些結(jié)果有力證明了QFG能夠促進(jìn)Ana-1巨噬細(xì)胞向M1樣表型轉(zhuǎn)化。進(jìn)一步實(shí)驗(yàn)顯示,經(jīng)QFG處理后TRITC-葡聚糖的熒光強(qiáng)度呈現(xiàn)劑量依賴性增強(qiáng),表明QFG能顯著提升Ana-1細(xì)胞的吞噬活性(圖4D)。此外,CT26細(xì)胞共培養(yǎng)實(shí)驗(yàn)表明,與單獨(dú)使用CT26細(xì)胞的對(duì)照組相比,Ana-1+CT26聯(lián)合治療組的細(xì)胞凋亡率顯著升高(圖4E)。這些結(jié)果進(jìn)一步證實(shí),QFG不僅能誘導(dǎo)Ana-1巨噬細(xì)胞向M1樣表型轉(zhuǎn)變,還能增強(qiáng)其吞噬和細(xì)胞毒性功能。
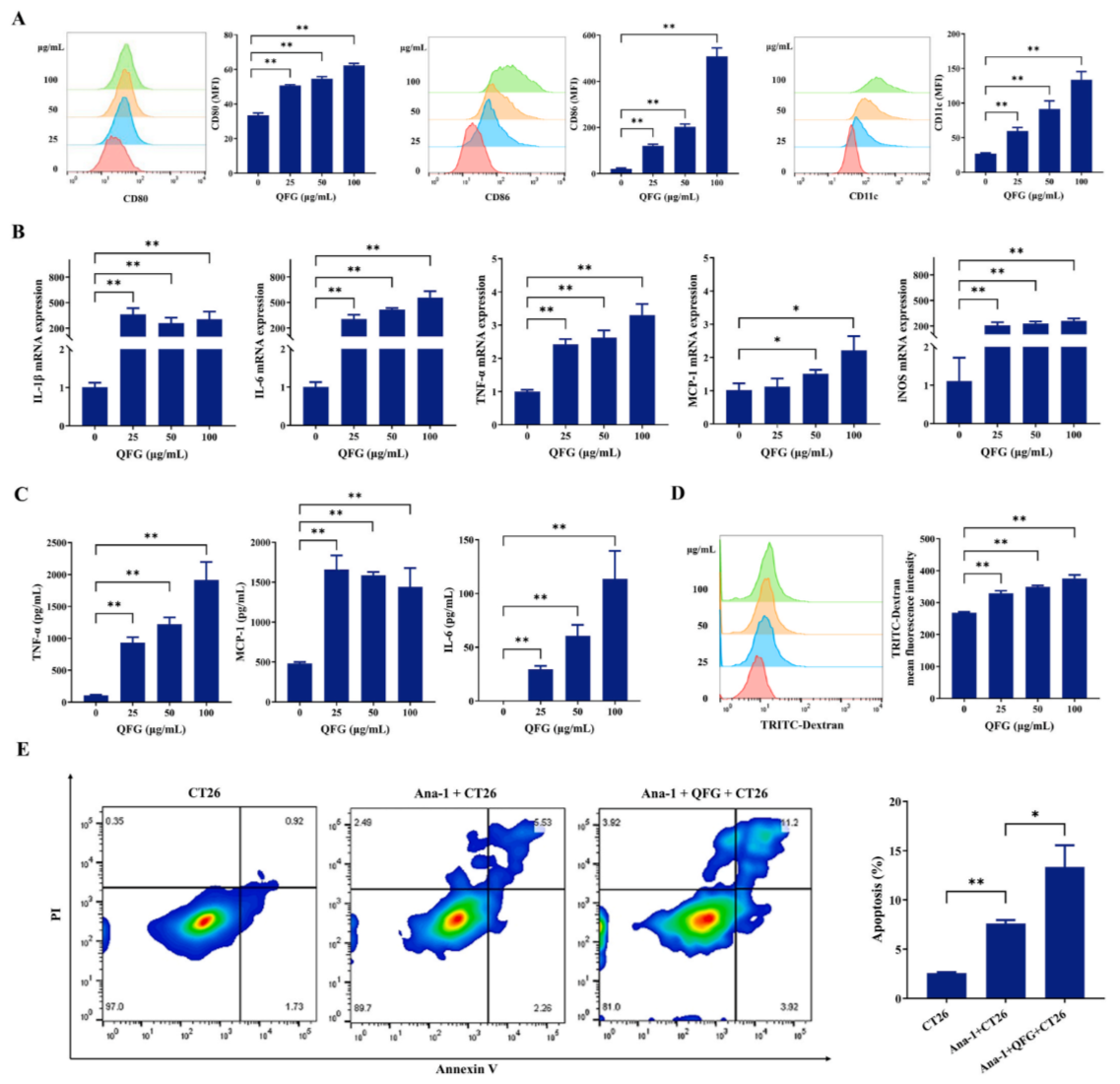
圖4. QFG促進(jìn)Ana-1巨噬細(xì)胞在體外向M1樣表型轉(zhuǎn)變
5.當(dāng)受到IL-4或CT26細(xì)胞培養(yǎng)上清刺激時(shí),QFG在體外可抑制Ana-1巨噬細(xì)胞向M2型表型極化
研究人員進(jìn)一步探究QFG處理是否能誘導(dǎo)Ana-1巨噬細(xì)胞向M2樣巨噬細(xì)胞轉(zhuǎn)化。RT-qPCR結(jié)果顯示QFG處理抑制了Ym1和CD206 mRNA的表達(dá),同時(shí)促進(jìn)了精氨酸酶1和IL-10 mRNA的表達(dá)(圖5A)。此外,研究人員利用兩種體外模型:IL-4誘導(dǎo)的M2樣巨噬細(xì)胞和CT26細(xì)胞培養(yǎng)上清液誘導(dǎo)的M2樣巨噬細(xì)胞,進(jìn)一步探究QFG處理抑制M2樣巨噬細(xì)胞形成的潛力。結(jié)果發(fā)現(xiàn),IL-4成功誘導(dǎo)了M2樣巨噬細(xì)胞(圖5B)。此外,兩種模型在QFG處理后,精氨酸酶1和CD206 mRNA表達(dá)量均顯著受到抑制(圖5C)。這些結(jié)果表明,QFG能顯著影響暴露于IL-4或CT26細(xì)胞培養(yǎng)上清液誘導(dǎo)的M2樣巨噬細(xì)胞。
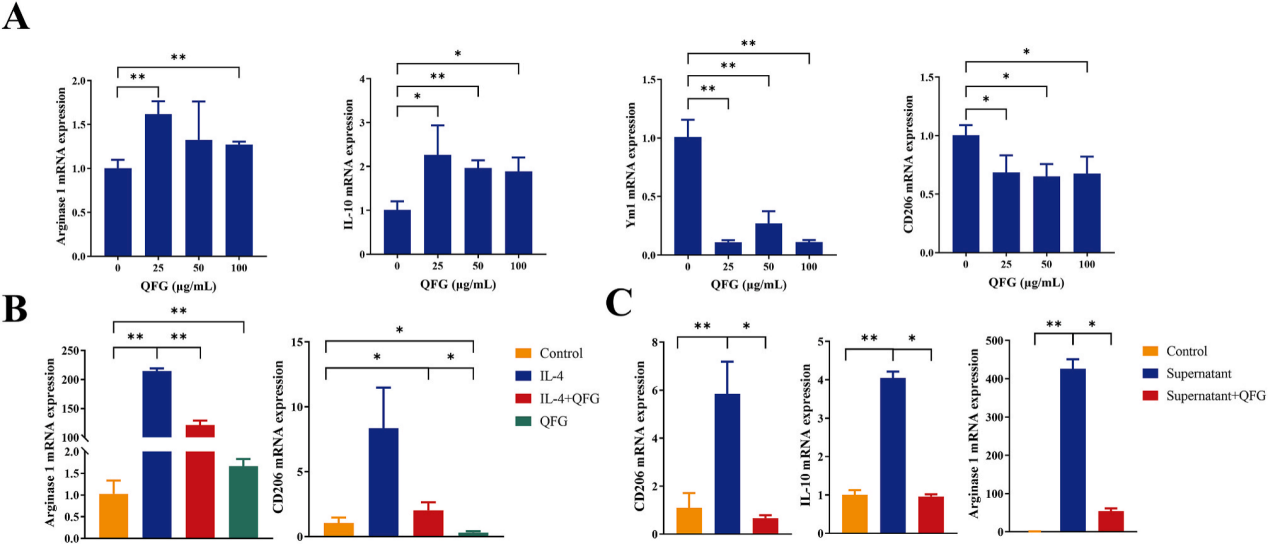
圖5. QFG抑制IL-4或CT26細(xì)胞培養(yǎng)上清誘導(dǎo)的Ana-1巨噬細(xì)胞向M2樣表型分化
6.TLR4通路參與QFG誘導(dǎo)的M1型巨噬細(xì)胞極化
研究發(fā)現(xiàn),TLR4和IL-4R分別參與調(diào)節(jié)M1型和M2型極化,為了探究QFG對(duì)巨噬細(xì)胞的極化作用是否與他們相關(guān),研究人員用6種不同的TLR4及其下游通路物質(zhì)拮抗劑對(duì)Ana-1細(xì)胞進(jìn)行處理后,用QFG干預(yù)。結(jié)果顯示,除KG501外,其他5種拮抗劑均不同程度地減弱了QFG誘導(dǎo)的IL-6、TNF-α、iNOS或IL-1β mRNA的上調(diào)(圖6A-F)。表明QFG誘導(dǎo)巨噬細(xì)胞向M1型極化與TLR4和IL-4R及其相關(guān)的通路相關(guān)。
為深入探究MD2與QFG誘導(dǎo)巨噬細(xì)胞極化之間的關(guān)系,研究人員構(gòu)建了Sh-MD2(MD2敲除)慢病毒轉(zhuǎn)染Ana-1細(xì)胞,并用QFG進(jìn)行干預(yù)。結(jié)果顯示,與NC組相比,Sh-MD2組的MD2 mRNA和蛋白表達(dá)量顯著降低(圖7A-B),表明成功構(gòu)建了MD2敲低的Ana-1細(xì)胞系。此外,相較于NC組,Sh-MD2組的IL-6、IL-1β和iNOS mRNA水平下降(圖7C),而在MD2敲低的Ana-1細(xì)胞中,使用QFG處理并未導(dǎo)致IL-6、IL-1β、iNOS和TNF-α的mRNA水平顯著升高,說明QFG促進(jìn)巨噬細(xì)胞向M1樣表型轉(zhuǎn)化的作用與MD2密切相關(guān)。
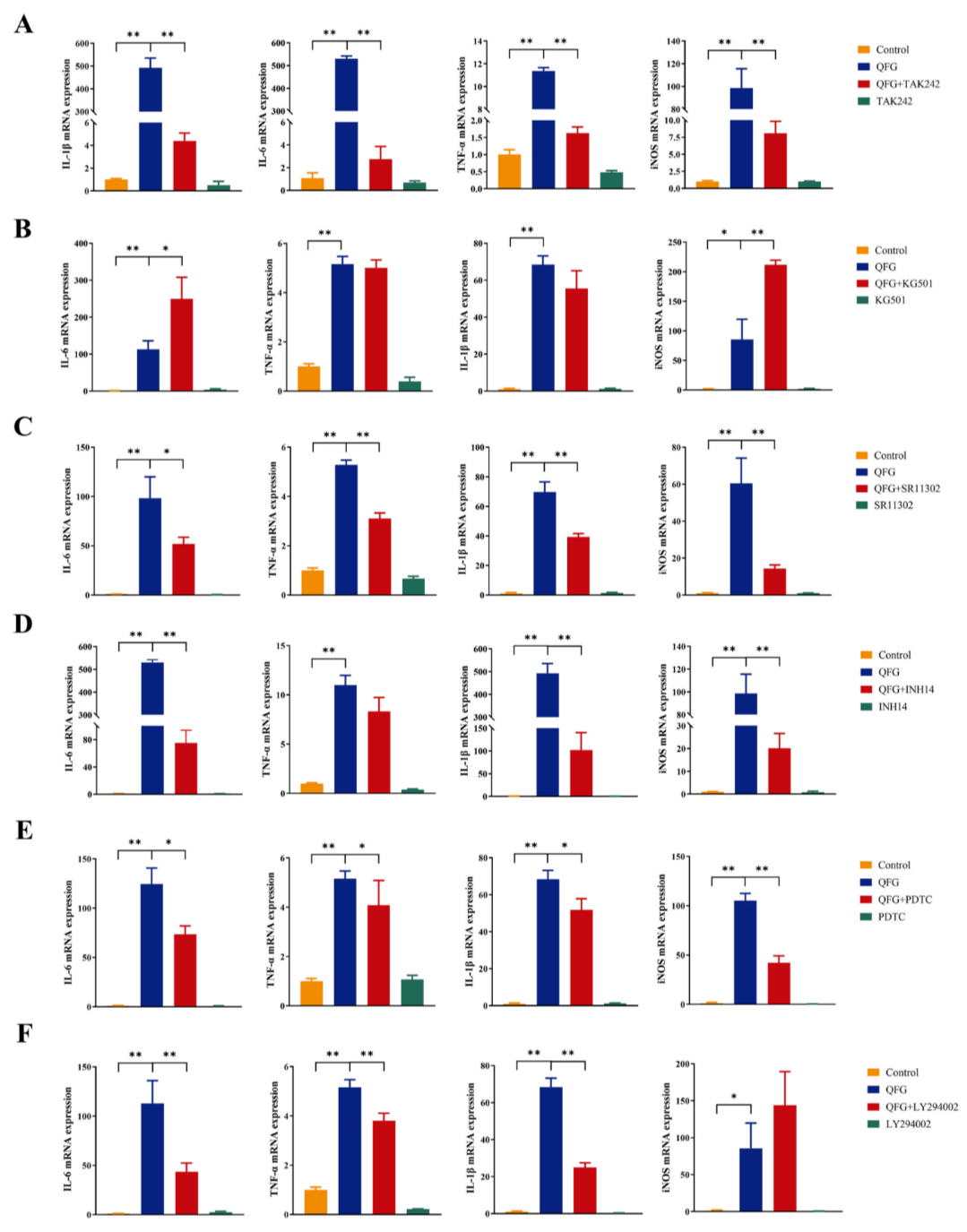
圖6. QFG通過TLR4通路促進(jìn)Ana-1巨噬細(xì)胞向M1樣表型轉(zhuǎn)變的機(jī)制
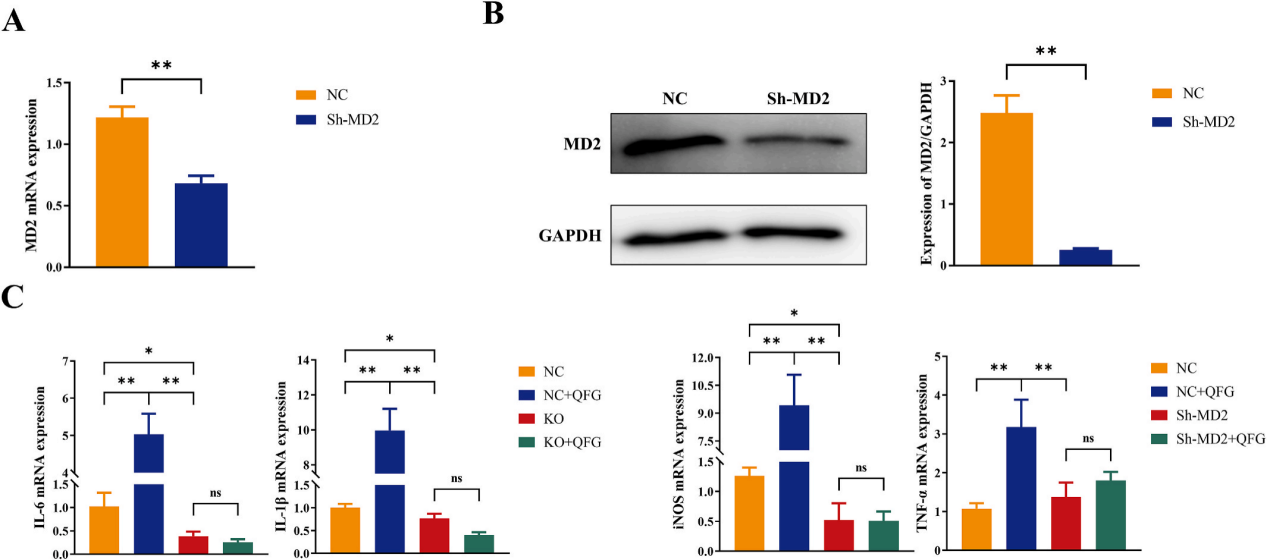
圖7. QFG對(duì)MD2敲低Ana-1細(xì)胞巨噬細(xì)胞極化的影響
7.IL-4R通路參與QFG誘導(dǎo)的M2型巨噬細(xì)胞極化
此外,研究人員進(jìn)一步探究了QFG抑制IL-4誘導(dǎo)的M2樣巨噬細(xì)胞是否與IL-4受體(IL-4R)及其下游STAT6和PI3K/Akt信號(hào)通路相關(guān)。通過Western blot檢測(cè)STAT6、p-STAT6、Akt及p-Akt蛋白水平。結(jié)果顯示,與對(duì)照組相比,IL-4誘導(dǎo)的p-STAT6和p-Akt水平顯著升高),而經(jīng)QFG干預(yù)后兩者均顯著降低(圖8A)。這些結(jié)果表明,QFG可能通過拮抗IL-4受體介導(dǎo)的STAT6和PI3K/Akt信號(hào)通路,抑制Ana-1細(xì)胞向M2樣極化的進(jìn)程。
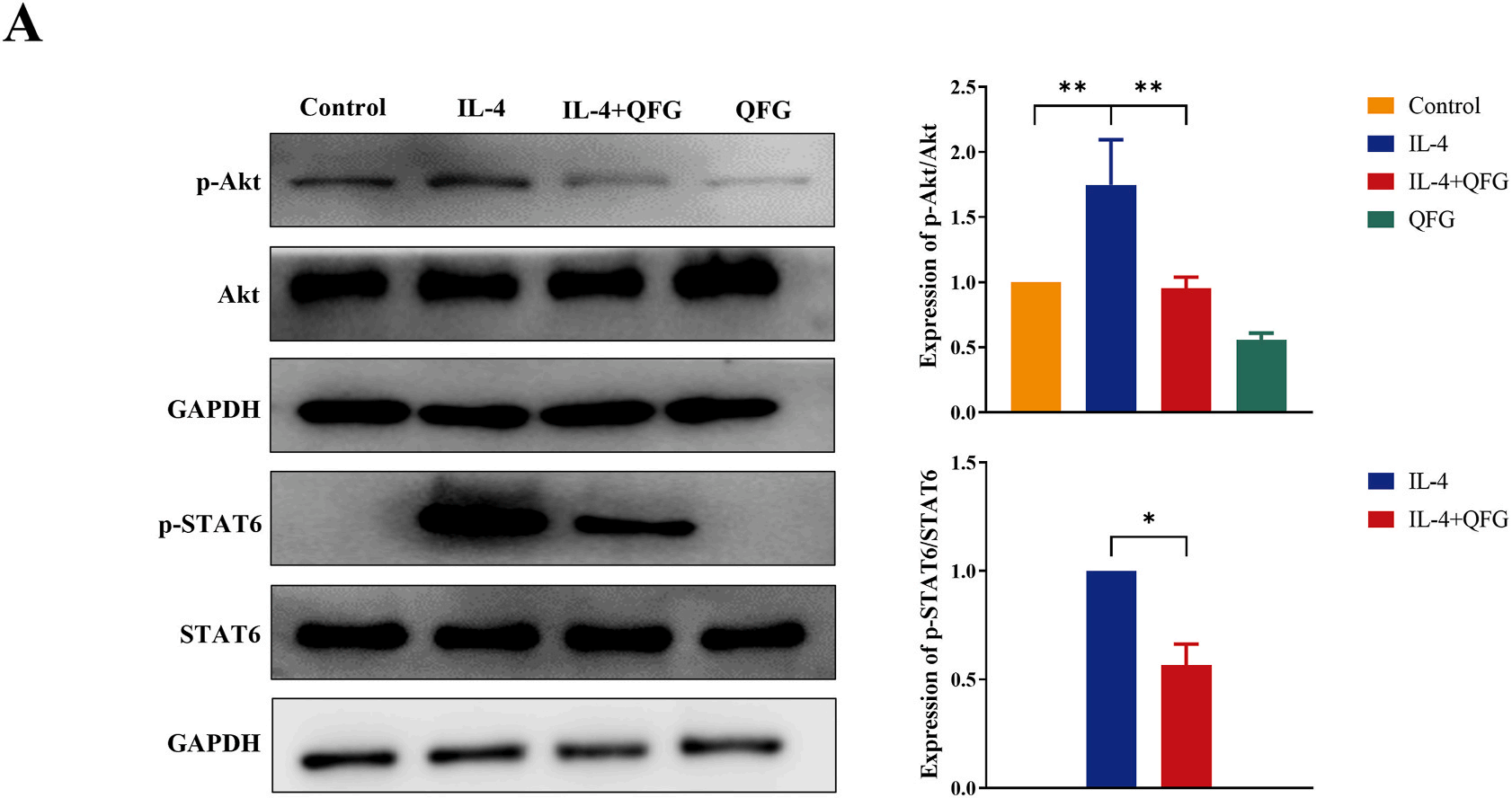
圖8. QFG拮抗IL-4介導(dǎo)的STAT6和Akt磷酸化
研究結(jié)論
本研究中,研究人員驗(yàn)證了清解扶正顆粒(QFG)中的單體成分能夠與MD2或IL-4R結(jié)合,通過TLR4介導(dǎo)的NF-κB、MAPK和PI3K/Akt通路激活巨噬細(xì)胞向M1型表型極化,或通過抑制IL-4R介導(dǎo)的JAKs通路抑制巨噬細(xì)胞向M2型表型極化,最終會(huì)抑制結(jié)直腸癌的發(fā)生和發(fā)展,為QFG在CAC治療中的潛在應(yīng)用提供了有價(jià)值的見解。
然而,研究也發(fā)現(xiàn)過多的巨噬細(xì)胞向M1型表型轉(zhuǎn)化可能會(huì)對(duì)腸道組織造成炎癥損傷,最終加劇CAC的嚴(yán)重程度。因此,精確調(diào)控QFG的給藥劑量對(duì)于防止巨噬細(xì)胞過度激活為M1型表型至關(guān)重要。
DIA中藥入血組,百趣生物創(chuàng)新性地運(yùn)用DIA數(shù)據(jù)采集模式采集血清中的中藥藥物成分,從數(shù)據(jù)采集上避免入血/入組織藥物信息的遺漏,盡可能全面采集進(jìn)入血液和組織的中藥藥物成分。并通過檢索百趣生物自建中藥標(biāo)準(zhǔn)品數(shù)據(jù)庫和中藥專屬數(shù)據(jù)庫,對(duì)血液樣本或組織樣本中的藥效成分進(jìn)行準(zhǔn)確鑒定,同時(shí)結(jié)合藥物成分在體內(nèi)的代謝變化,并通過深入的分析內(nèi)容呈現(xiàn)中藥治療疾病的作用機(jī)制。
中藥NGM 2,是在新一代代謝組學(xué)基礎(chǔ)上發(fā)展而來,沿襲了其精準(zhǔn)的特點(diǎn),主要解決中藥相關(guān)研究群體核心需求:準(zhǔn)確鑒定藥用成分。
若您對(duì)“DIA中藥入血組/中藥NGM 2”等服務(wù)感興趣,百趣生物可提供專業(yè)技術(shù)服務(wù),歡迎后臺(tái)私信咨詢!
END
快樂小包子 撰文
SY 校稿
