近日,武漢大學(xué)人民醫(yī)院發(fā)表最新研究成果“IGF I receptor inhibition amplifies the effects of cancer drugs by autophagy and immune- dependent mechanisms”,實(shí)驗(yàn)證實(shí)采用IGF-I R抑制劑,聯(lián)合化療藥物奧沙利鉑、以及免疫檢查點(diǎn)PD-1抑制劑,不僅能夠顯著抑制那些不會(huì)引起免疫系統(tǒng)反應(yīng)的“冷腫瘤”的生長(zhǎng),并成功誘導(dǎo)機(jī)體對(duì)同種腫瘤的免疫記憶功能,在部分案例中甚至可以完全治愈腫瘤。該研究表明IGF-I R抑制劑或可為腫瘤免疫治療提供新的方案。
結(jié)構(gòu)和功能
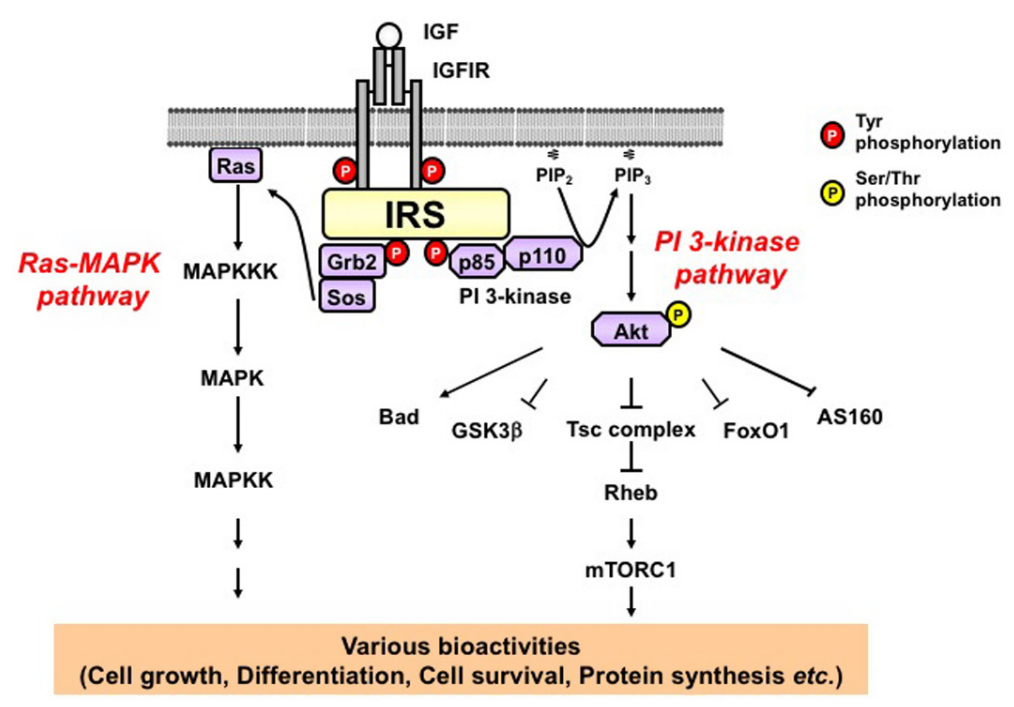
IGF-I R結(jié)合IGF激活胞內(nèi)信號(hào)轉(zhuǎn)導(dǎo)機(jī)制
IGF-I R(Insulin-like Growth Factor I Receptor)是胰島素樣生長(zhǎng)因子1的受體,屬于受體酪氨酸激酶(receptor tyrosine kinases, RTKs),是胰島素受體亞家族成員之一。IGF-I R前體為一條單鏈多肽,經(jīng)剪切加工去除30個(gè)氨基酸的信號(hào)肽序列后,肽鏈被糖基化,并斷裂成一條具有706個(gè)氨基酸的胞外α亞單位和626個(gè)氨基酸構(gòu)成的穿膜β亞單位。α和β亞單位通過(guò)二硫健形成一個(gè)αβ半受體,它與另一個(gè)αβ半受體構(gòu)成一個(gè)完整受體(α2β2)。IGF-l R是一類跨膜受體,胞外的α亞單位決定與配體結(jié)合的特異性,穿膜的β亞單位則穿越細(xì)胞膜,傳導(dǎo)配基誘導(dǎo)的信號(hào)。IGF-l R可以被胰島素樣生長(zhǎng)因子(IGF-I或IGF-II)激活,引起自身酪氨酸激酶結(jié)構(gòu)域的磷酸化并起始胞內(nèi)信號(hào)傳導(dǎo),調(diào)控細(xì)胞的生長(zhǎng)和分化。
IGF-I R表達(dá)于多種類型的細(xì)胞表面,表達(dá)過(guò)度時(shí)細(xì)胞則可以向惡性表型轉(zhuǎn)化。1988年首次提出該分子在前列腺癌患者的血液中高表達(dá),近年的研究發(fā)現(xiàn)該靶點(diǎn)在惡性神經(jīng)系統(tǒng)腫瘤、惡性黑色素瘤、乳腺癌,結(jié)腸癌,頭頸鱗癌,非小細(xì)胞肺癌,卵巢癌,肝癌以及宮頸癌等多種惡性腫瘤組織中呈高表達(dá)狀態(tài),其酪氨酸激酶活性也有所增強(qiáng)。除了促進(jìn)腫瘤細(xì)胞的形成與增殖,IGF-I R還與惡性腫瘤的發(fā)生、發(fā)展及浸潤(rùn)和轉(zhuǎn)移有密切的聯(lián)系。通過(guò)調(diào)節(jié)腫瘤細(xì)胞表面的IGF-l R的表達(dá),使腫瘤細(xì)胞的增殖受到抑制,促進(jìn)腫瘤細(xì)胞凋亡,使得IGF-l R成為一個(gè)極具吸引力的腫瘤靶向治療的靶點(diǎn)。
在IGF-I R的發(fā)現(xiàn)早期,就有研究表明IGF-I R的單克隆抗體可以抑制小鼠體內(nèi)的腫瘤細(xì)胞生長(zhǎng),同時(shí)也發(fā)現(xiàn)其與生長(zhǎng)激素的調(diào)節(jié)密切相關(guān)。目前針對(duì)IGF-I R的主要藥物包括小分子藥物和生物藥物兩大類,小分子藥物以抑制劑和激活劑為主要作用機(jī)理,生物藥物以重組細(xì)胞因子以及抗體類藥物為主。也正因?yàn)镮GF-IR參與多個(gè)生理功能,藥物開發(fā)涉及腫瘤、內(nèi)分泌以及皮膚病等多種領(lǐng)域的多種適應(yīng)癥。
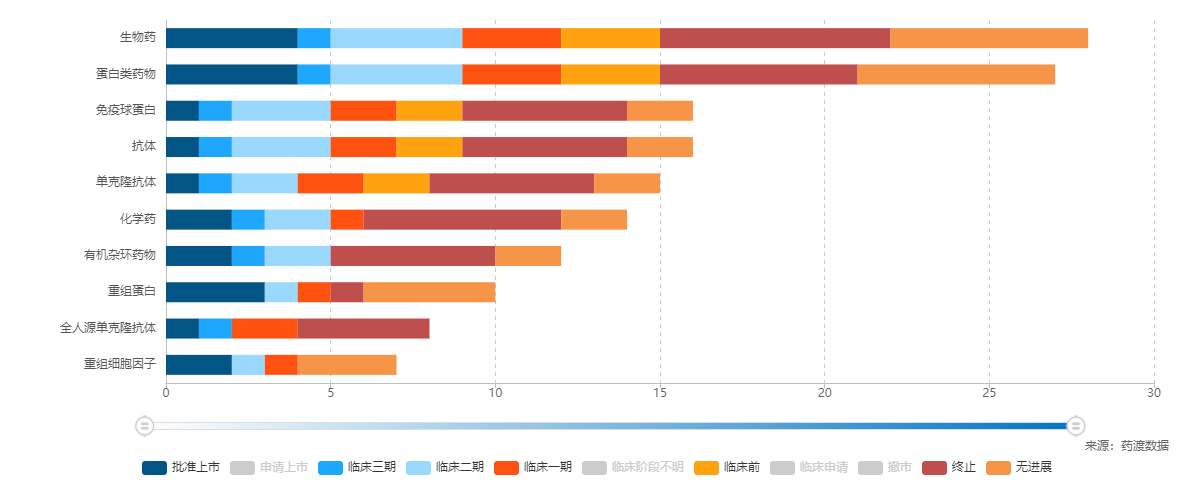
靶向IGF-I R藥物類型
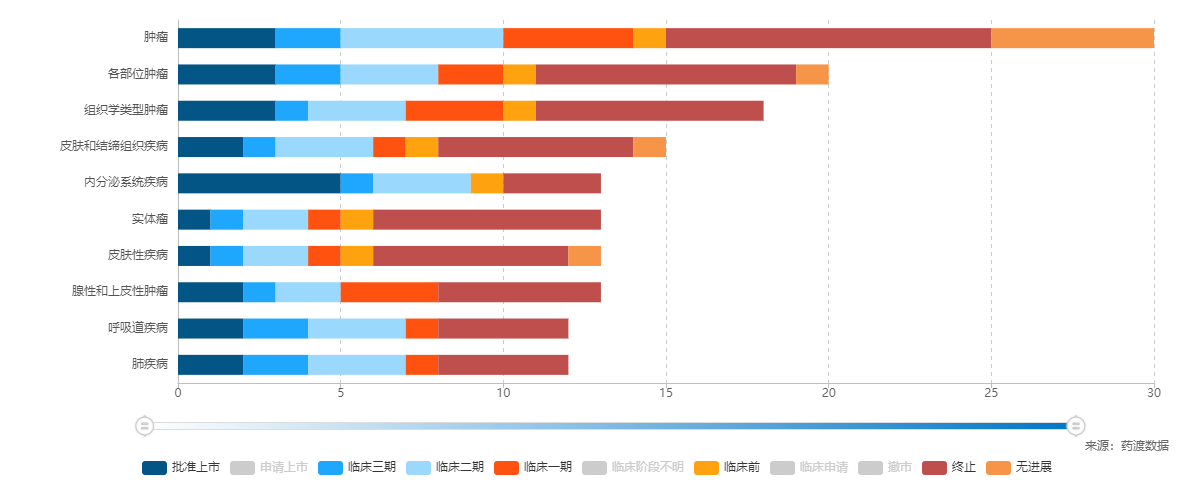
靶向IGF-I R藥物治療領(lǐng)域及適應(yīng)癥
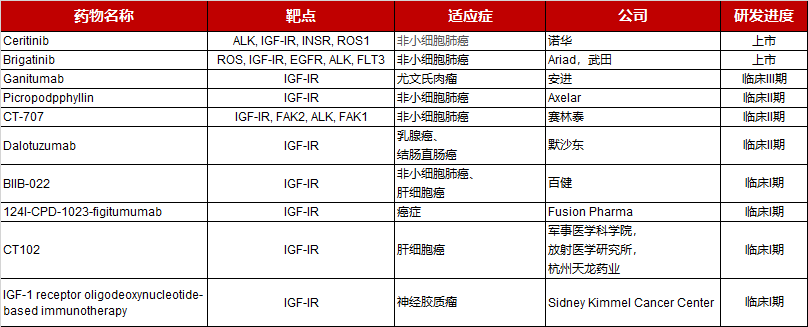
2020年1月美國(guó)FDA批準(zhǔn)的Tepezza作為第一款也是唯一一款治療甲狀腺眼病的藥物,也是目前唯一獲批的靶向IGF-I R抗體類藥物。目前靶向IGF-IR的抗體類藥物大多處于臨床階段,其中臨床階段較高的是安進(jìn)的Ganitumab,已經(jīng)進(jìn)入臨床三期,該藥物在多種實(shí)體瘤中顯示出療效。國(guó)內(nèi)藥企對(duì)靶向IGF-I R的抗體類藥物鮮有布局。
靶向IGF-I R腫瘤領(lǐng)域藥物一覽表(藥渡數(shù)據(jù))
此次武漢大學(xué)人民醫(yī)院提出的聯(lián)合用藥策略,證實(shí)IGF-I R抑制劑在抑制癌細(xì)胞擴(kuò)增的同時(shí)可以有效的激活細(xì)胞免疫,聯(lián)合用藥策略或許會(huì)成為IGF-I R靶向單抗藥物的治療新方向。IGF-I R促進(jìn)腫瘤細(xì)胞的形成與增殖,還與諸多惡性腫瘤的發(fā)生、發(fā)展及浸潤(rùn)和轉(zhuǎn)移有密切關(guān)聯(lián),以IGF-I R為靶點(diǎn)的抗腫瘤免疫治療很有前景,值得關(guān)注。
ACROBiosystems可提供IGF-I、IGF-II和不同種屬、不同標(biāo)簽的IGF-IR,助力靶向IGF-1 R藥物研發(fā)。
產(chǎn)品列表
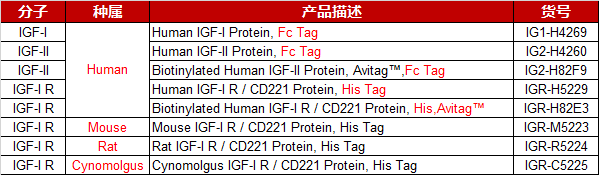
點(diǎn)擊圖片內(nèi)容可查看產(chǎn)品詳情
驗(yàn)證數(shù)據(jù)
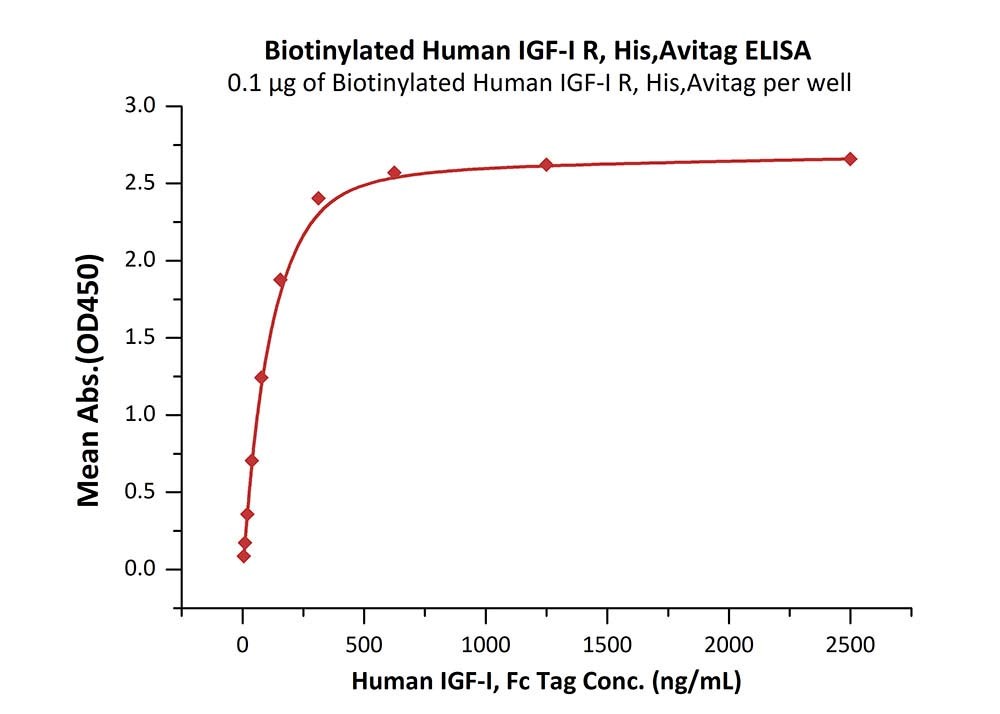
經(jīng)ELISA測(cè)定,Human IGF-I, Fc Tag (Cat. No.IG1-H4269) 可以與Biotinylated Human IGF-IR, His, Avitag(Cat. No. IGR-H82E3) 特異性結(jié)合,線性區(qū)間為5-156 ng/mL。
點(diǎn)擊申請(qǐng)protocol
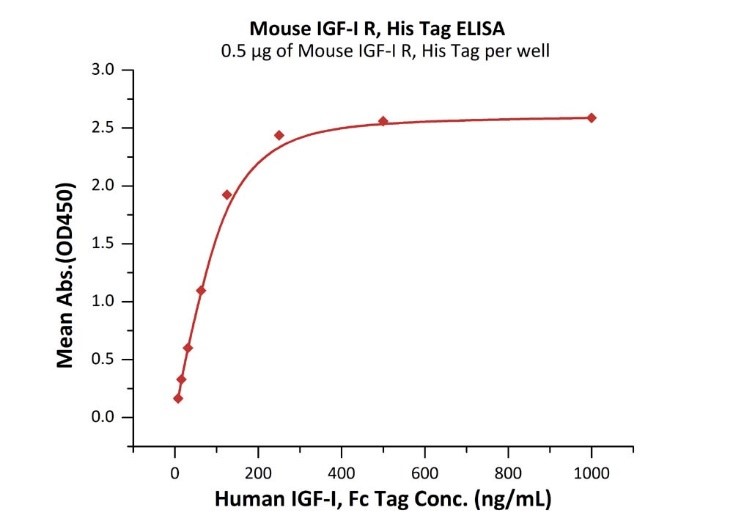
經(jīng)ELISA測(cè)定,Human IGF-I, Fc Tag (Cat. No.IG1-H4269) 可以與Mouse IGF-I R, His Tag (Cat. No. IGR-M5223) 特異性結(jié)合,線性區(qū)間為7.8-125ng/mL。

(請(qǐng)備注:公司+姓名)
快點(diǎn)擊識(shí)別上方二維碼,加入抗體藥資源分享群吧~
參考文獻(xiàn)
[1] F Hakuno ,S-I Takahashi. 40 YEARS OF IGFI: IGFI receptor signaling pathways[J]. Journal of Molecular Endocrinology, 2018, 61(1):69-86.
[2] J Tsui, Qi S, Perrino S, et al. Identification of a Resistance Mechanism to IGF-IR Targeting in Human Triple Negative MDA-MB-231 Breast Cancer Cells[J]. Biomolecules, 2021, 11(4):527.
[3] Li J, Choi E, Yu H, et al. Structural basis of the activation of type 1 insulin-like growth factor receptor[J]. Nature Communications, 2019, 10(1).

您可通過(guò)以下方式聯(lián)系到ACROBiosystems:
郵件:inquiry@acrobiosystems.com
電話:15117918562
(備注:姓名+公司)
