ELISA背景介紹
酶聯(lián)免疫吸附實(shí)驗(yàn)(Enzyme-Linked Immunosorbent Assay, ELISA)是一種基于抗體-抗原-抗體特異性結(jié)合形成三明治復(fù)合物的高靈敏度、高特異性的免疫檢測(cè)技術(shù)。鑒于其發(fā)展歷史較久,技術(shù)積累成熟,且操作簡(jiǎn)便、成本較低、可高通量檢測(cè),廣泛應(yīng)用于醫(yī)學(xué)(醫(yī)療器械和精密儀器)、生物學(xué)、藥學(xué)、農(nóng)業(yè)、食品安全等領(lǐng)域。根據(jù)使用應(yīng)用的需要,可以分為直接法,間接法,夾心法和競(jìng)爭(zhēng)法等。
根據(jù)ELISA的特點(diǎn),其常見(jiàn)應(yīng)用有:病毒/細(xì)菌/寄生蟲(chóng)的定性檢測(cè),蛋白抗原定量,抗體效價(jià)和信號(hào)通路的定性和定量研究;藥物研發(fā)與質(zhì)量控制相關(guān)的血液和組織液中的藥物定量,生物制品的效價(jià)測(cè)定等。
ELISA的顯著特點(diǎn)有:通過(guò)標(biāo)準(zhǔn)曲線,精確定量抗原分子濃度;定性篩查樣本中目標(biāo)抗原的存在與否;高通量檢測(cè)大量樣本;檢測(cè)限度達(dá)到ng/mL,pg/mL的高靈敏度分析;以及抗原抗體特異性反應(yīng)的親和能力。
其中,標(biāo)準(zhǔn)曲線是定量的最終依據(jù),其主要體現(xiàn)的方面有:1.標(biāo)曲是定量分析的核心依據(jù),通過(guò)已知濃度標(biāo)準(zhǔn)品和對(duì)應(yīng)的檢測(cè)出信號(hào),擬合成數(shù)學(xué)模型,來(lái)反算樣本濃度;2.通過(guò)最低檢測(cè)限和最低定量限,線性范圍和重復(fù)性,來(lái)驗(yàn)證實(shí)驗(yàn)的可靠;3.根據(jù)斜率和截距判斷獨(dú)立實(shí)驗(yàn)的正常與否;數(shù)據(jù)可比性和標(biāo)準(zhǔn)化,來(lái)校正數(shù)據(jù)和減少批間差異。
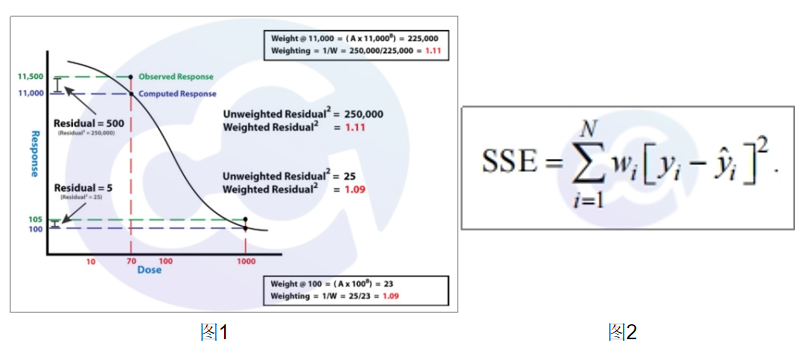
在ELISA檢測(cè)中,Sum of Squares Error (SSE,誤差平方和) 是數(shù)據(jù)分析的重要統(tǒng)計(jì)量,主要用于評(píng)估標(biāo)準(zhǔn)曲線擬合的準(zhǔn)確性以及實(shí)驗(yàn)數(shù)據(jù)的離散程度。表示實(shí)際觀測(cè)值(實(shí)驗(yàn)數(shù)據(jù)點(diǎn))與擬合曲線(如標(biāo)準(zhǔn)曲線)預(yù)測(cè)值之間的偏差平方和。可以評(píng)估標(biāo)準(zhǔn)曲線的擬合優(yōu)度,SSE越小,說(shuō)明實(shí)際數(shù)據(jù)點(diǎn)與擬合曲線的偏差越小,曲線擬合效果越好,反之,提示此次實(shí)驗(yàn)?zāi)P筒磺‘?dāng);另外,在同一批次ELISA板中,不同標(biāo)準(zhǔn)曲線的SSE應(yīng)接近,并結(jié)合R²等統(tǒng)計(jì)項(xiàng)目,來(lái)判斷實(shí)驗(yàn)條件的重復(fù)性、可靠性和穩(wěn)定性。見(jiàn)圖1,圖2。
ELISA Blank作用
Blank孔不僅直接影響SSE的計(jì)算(校正OD=實(shí)測(cè)OD-Blank OD,Blank孔OD值不穩(wěn)定或異常,會(huì)導(dǎo)致校正后的數(shù)據(jù)偏差增大,從而增加SSE,降低擬合精度。);Blank孔的較大差異,會(huì)體現(xiàn)實(shí)驗(yàn)的系統(tǒng)誤差;高Blank信號(hào)導(dǎo)致低濃度標(biāo)準(zhǔn)點(diǎn)的計(jì)量為負(fù)數(shù),扭曲標(biāo)準(zhǔn)曲線,增大SSE。
另外,在《酶聯(lián)免疫吸附法檢測(cè)試劑注冊(cè)技術(shù)審查指導(dǎo)原則》,《定量檢測(cè)試劑分析性能評(píng)估指導(dǎo)原則》,EP17-A2和《Immunoassay Devices Guidance for Industry》中,均提到定量檢測(cè)中的Blank孔,明確要求ELISA實(shí)驗(yàn)需設(shè)置空白孔,并規(guī)定其信號(hào)應(yīng)顯著低于最低校準(zhǔn)品信號(hào)(通常要求Blank OD≤最低校準(zhǔn)品OD的50%);或者要求空白孔用于確定檢測(cè)限(LOD),其OD值需滿足:均值+2SD≤低濃度校準(zhǔn)品OD值;TMB顯色時(shí)450nm波長(zhǎng)下OD值一般≤0.1;強(qiáng)調(diào)空白孔的重復(fù)性(CV值應(yīng)≤20%)等。
實(shí)際應(yīng)用
因?yàn)槊庖邔?shí)驗(yàn)的所有形式測(cè)量,都需要標(biāo)準(zhǔn)化。所以對(duì)Blank孔的控制是ELISA水平重要的具體體現(xiàn)之一。
賽唐生物歷時(shí)10年,在開(kāi)發(fā)E.coli/CHO/293/SC Yeast/HS Yeast/PP Yeast HCP ELISA過(guò)程中,長(zhǎng)期堅(jiān)持打磨基礎(chǔ)技術(shù),對(duì)Blank本底進(jìn)行了顯著的控制,下降比例達(dá)10倍。并統(tǒng)計(jì)上百次實(shí)驗(yàn)數(shù)據(jù),發(fā)現(xiàn)Blank從0.1,降低到0.05水平,再到0.01水平(見(jiàn)圖3-圖9)。
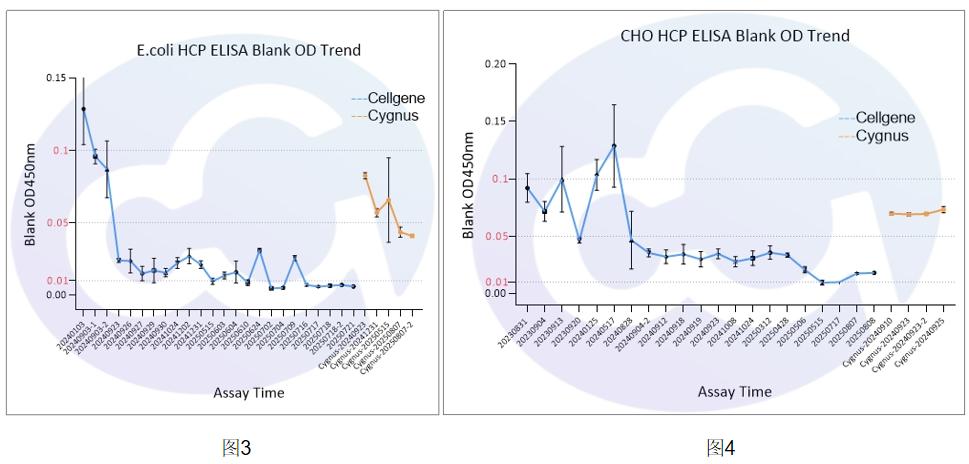
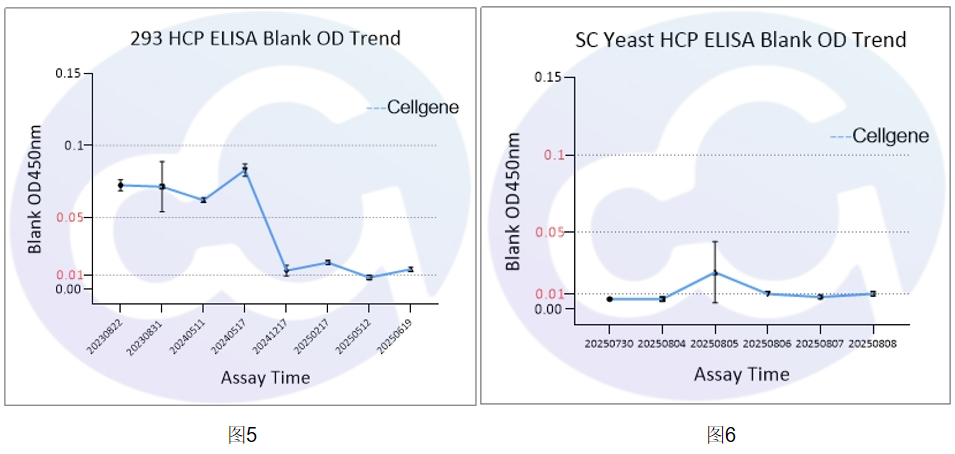
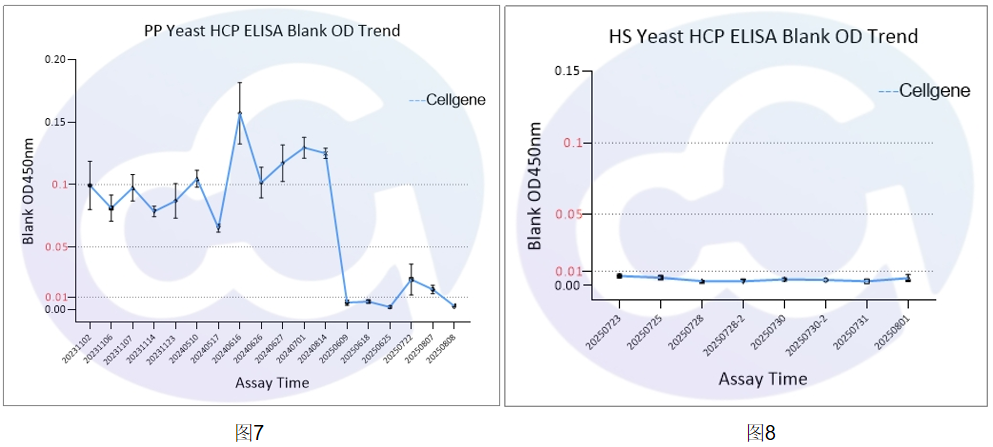
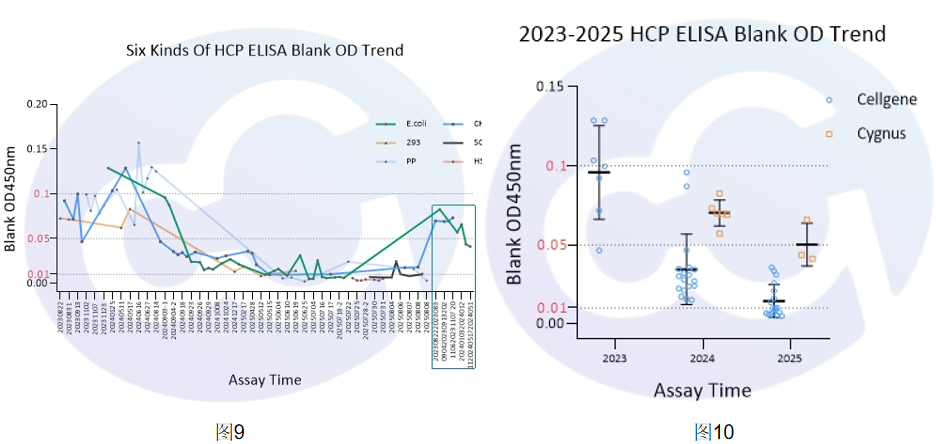
與Cygnus相比,本底降低2-10倍,見(jiàn)表1,圖10。為后續(xù)藥物ELISA定量檢測(cè),提供了扎實(shí)的體系支持。
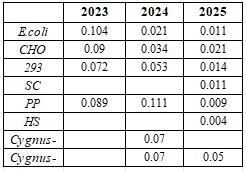
表1
參考標(biāo)準(zhǔn)
《酶聯(lián)免疫吸附法檢測(cè)試劑注冊(cè)技術(shù)審查指導(dǎo)原則》
《定量檢測(cè)試劑分析性能評(píng)估指導(dǎo)原則》
《EP17-A2: Evaluation of Detection Capability for Clinical Laboratory Measurement Procedures; Approved Guideline—Second Edition》
《Immunoassay Devices Guidance for Industry》
