快速出方案,高性價比,短周期交付
胰腺癌的治療一直面臨嚴峻挑戰,其不良預后與腫瘤對常規治療方法(包括免疫檢查點抑制劑)的耐受密切相關。這種抵抗主要源于兩方面:一是腫瘤周圍形成致密的物理屏障,限制藥物進入;二是腫瘤微環境呈現免疫抑制狀態,缺乏有效的免疫細胞浸潤。
近年來,溶瘤病毒和放射性免疫療法分別顯示出獨特的治療潛力。溶瘤病毒能夠特異性地在腫瘤細胞內復制并破壞腫瘤,同時可通過攜帶的免疫調節因子改善腫瘤周圍的免疫環境。而放射性免疫療法則能借助放射性核素將輻射精準聚焦于腫瘤,從而誘導具有免疫刺激作用的腫瘤細胞死亡。
2026年4月9日,韓國漢陽大學在Journal for Immunotherapy of Cancer(IF=10.6)發表Oncolytic adenovirus in combination with PD-L1-targeted radioimmunotherapy exerts synergistic antitumor effect against pancreatic cancer的研究論文,發現了一種經過工程化改造、可表達特定免疫因子的溶瘤腺病毒,能夠有效降解腫瘤基質,并促進腫瘤細胞表面PD-L1的表達。在此基礎上,聯合使用靶向PD-L1的放射性免疫治療藥物,可顯著提升藥物在腫瘤區域的蓄積,并產生協同抗腫瘤免疫應答,從而在胰腺癌模型中取得顯著的治療增強效果。

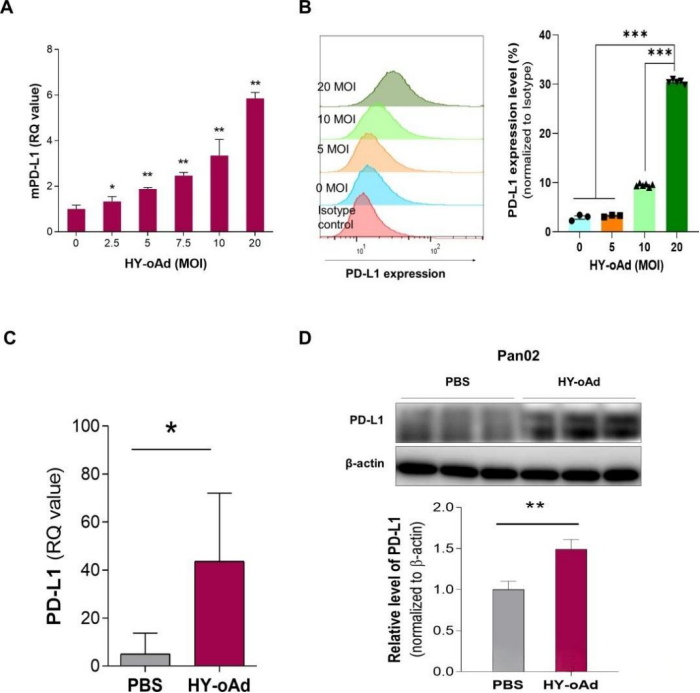
HY-oAd在體內外上調腫瘤細胞PD-L1表達
在體外培養的小鼠胰腺癌細胞中,隨著該病毒使用濃度的提高,細胞內的PD-L1基因轉錄水平和細胞膜上的對應蛋白量均呈現梯度上升。在動物模型中也驗證了這一效果,向腫瘤局部注射該病毒后,瘤組織內的PD-L1表達量明顯增加。這些發現表明,該病毒療法能主動塑造一個PD-L1高表達的腫瘤微環境,從而為后續精準靶向PD-L1的聯合治療策略創造了有利條件。
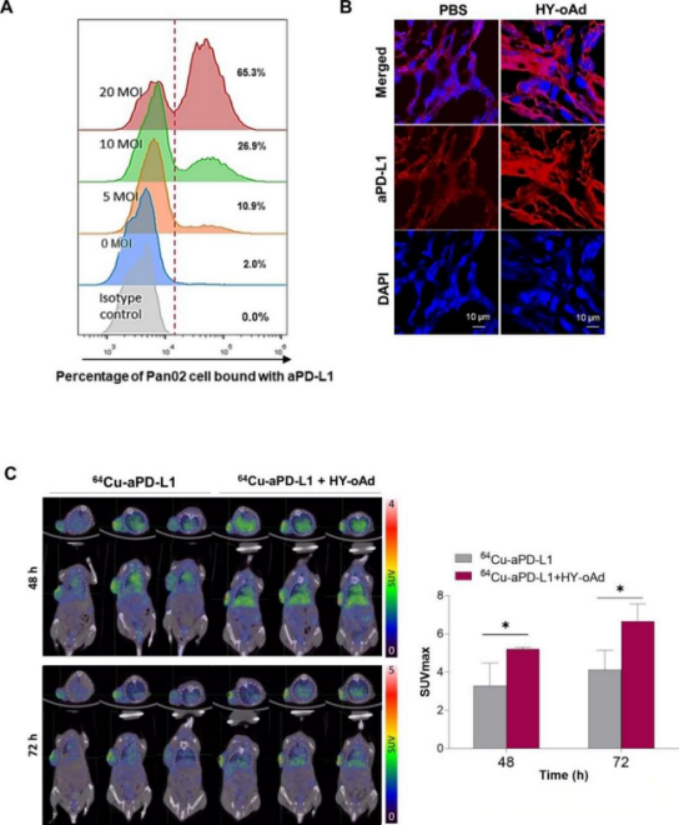
HY-oAd增強PD-L1抗體在腫瘤內的結合與蓄積
實驗數據進一步表明,經工程化溶瘤腺病毒處理的腫瘤細胞,對PD-L1抗體的親和力與結合量明顯提升。在活體成像研究中,通過放射性標記的PD-L1抗體進行追蹤,發現在病毒預處理后,抗體在腫瘤部位的聚集與滯留顯著增強,并且該處理未加重對肝臟的安全性影響。
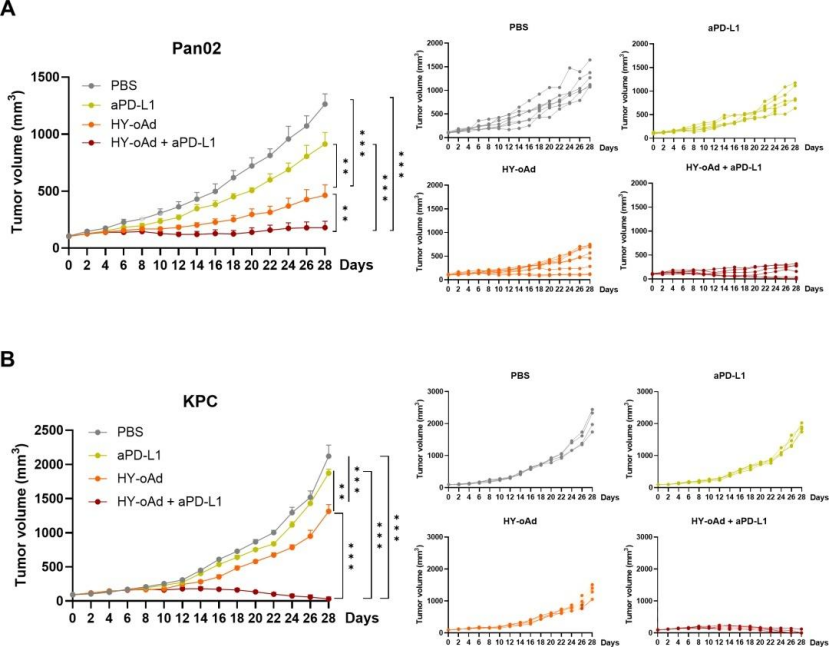
HY-oAd聯合aPD-L1在皮下瘤模型中展現協同療效
在小鼠實驗中,研究人員通過建立兩種不同的胰腺癌皮下移植模型(Pan02與KPC模型)來評估聯合治療的效果。結果顯示,與單獨使用溶瘤腺病毒或PD-L1抗體相比,兩者聯合應用能夠更有效地抑制腫瘤的生長,表現出明顯的協同抗腫瘤作用。
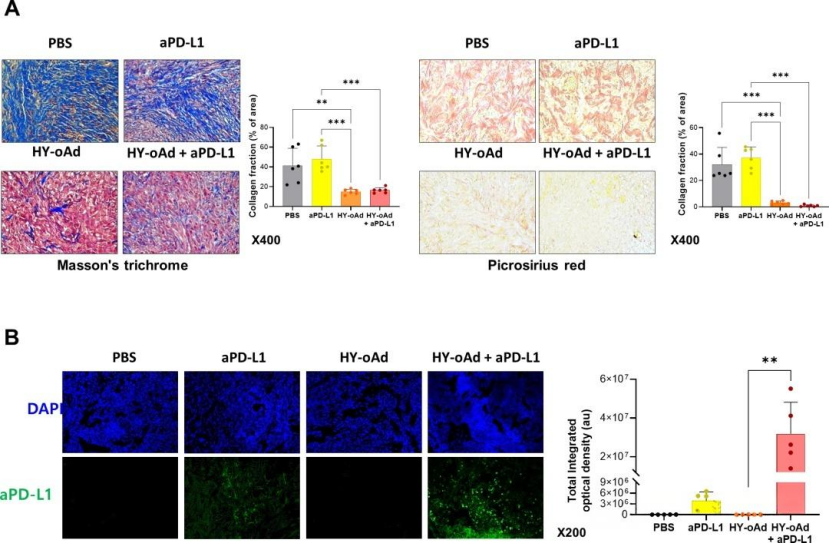
HY-oAd降解腫瘤細胞外基質,促進抗體滲透
通過對腫瘤組織進行病理學染色分析發現,經改造的溶瘤腺病毒(因其攜帶松弛素基因)能夠顯著重塑腫瘤的細胞外基質,有效減少致密的膠原成分。進一步的免疫熒光分析證實,在這種基質結構變得相對疏松的腫瘤組織中,PD-L1抗體的滲透深度和分布范圍均得到了顯著改善。
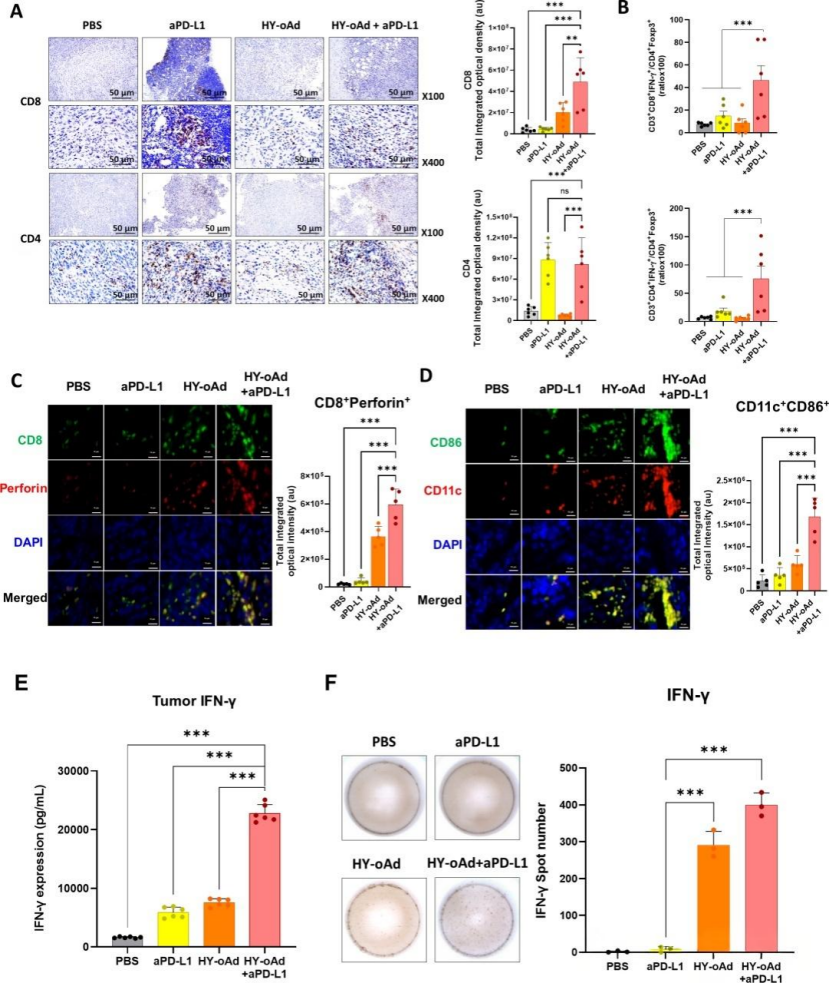
聯合療法重塑腫瘤免疫微環境,激活T細胞應答
通過對腫瘤組織的免疫染色和流式細胞術分析發現,在接受聯合治療的小鼠腫瘤中,細胞毒性CD8+ T淋巴細胞和輔助性CD4+ T淋巴細胞的浸潤數量均明顯增多。同時,CD8+ T細胞的活化標志穿孔素及其效應因子干擾素-γ的表達水平也顯著提升。此外,樹突狀細胞的浸潤與活化狀態得到增強,巨噬細胞也更多地向具有促炎功能的M1型分化。
這些結果共同揭示了該聯合策略在免疫層面的協同作用機制:改造后的溶瘤腺病毒通過表達IL-12和GM-CSF,能夠將免疫抑制的“冷”腫瘤轉變為免疫活躍的“熱”腫瘤,有效募集和激活免疫細胞;而PD-L1抗體則通過阻斷免疫抑制信號,使被激活的T細胞功能得以充分發揮,從而實現抗腫瘤免疫效應的最大化。
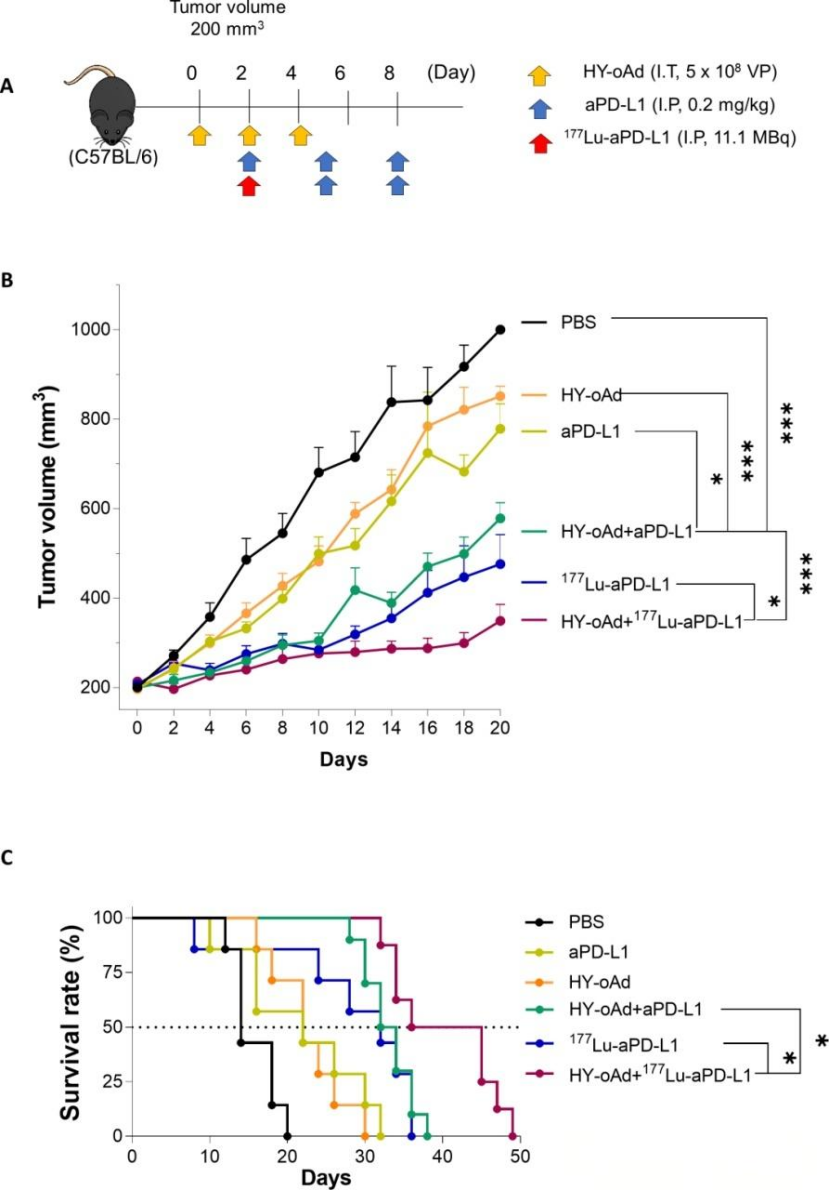
HY-oAd聯合PD-L1靶向放射性免疫治療(177Lu-aPD-L1)在皮下及原位模型中實現卓越療效與完全緩解
在皮下荷瘤模型中,即使使用較低劑量的改造溶瘤腺病毒,其與放射性核素標記的PD-L1靶向療法聯用,依然展現出最強的腫瘤生長抑制效果,并顯著延長了小鼠生存期,療效明顯優于使用非放射性標記抗體的聯合方案。在更貼近真實病理狀況的胰腺原位癌模型中,單獨使用放射性靶向療法或溶瘤病毒與非標記抗體的聯合方案,僅能延緩疾病進展,所有小鼠最終均死亡。然而,溶瘤腺病毒與放射性靶向療法聯合治療組的所有小鼠均存活至實驗觀察期結束(第43天),其中部分小鼠經后期解剖及病理學檢查確認,其體內腫瘤已完全清除。進一步的分布研究證實,經全身給藥的溶瘤病毒能夠在腫瘤組織中進行特異性復制。
本研究針對胰腺導管腺癌(PDAC)治療中兩大關鍵瓶頸——致密的纖維化物理屏障與免疫抑制性的“冷”腫瘤微環境,提出了一種創新的協同治療新策略。該策略的核心是一種經基因工程改造的溶瘤腺病毒,其可共表達IL-12、GM-CSF及松弛素。研究發現,該病毒能雙重重塑腫瘤微環境:不僅可誘導腫瘤細胞表面PD-L1表達上調,還能有效降解致密的細胞外基質,從而顯著提升靶向PD-L1的放射性免疫治療藥物在腫瘤組織的富集與滲透。在臨床前研究中,該溶瘤病毒與放射性核素¹??Lu標記的PD-L1抗體聯用,產生了顯著的協同抗腫瘤效應。尤其在模擬人體疾病特征的原位胰腺癌模型中,聯合治療實現了優異的腫瘤抑制效果,部分動物甚至達到完全緩解,為這一協同策略的臨床轉化提供了有力的實證依據。
要實現上述突破性療效,關鍵在于獲得經過精準工程化改造的溶瘤病毒。為此,「DIFF CRO」提供專業的溶瘤病毒構建與藥效評價一站式服務。
「DIFF CRO」溶瘤病毒構建與藥效評價服務
「DIFF CRO」憑借其特色的重組病毒載體平臺,提供從病毒載體構建、改造、擴增純化到臨床前藥效學評價的一站式、高效率CRO服務。公司通過對病毒株基因組進行精準改造,以提升溶瘤病毒的抗腫瘤活性,并憑借優化的流程實現快速的方案輸出和顯著縮短研發周期。
服務內容:
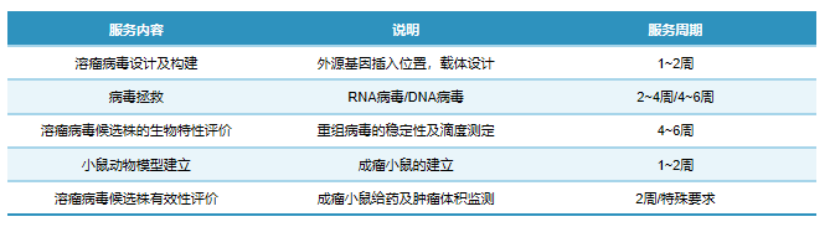
溶瘤病毒載體類“閉環式”持續開發能力
「DIFF CRO」依托全球領先的反向遺傳操作技術平臺,建立了獨特的‘閉環式’持續開發能力。平臺采用模塊化的DCVL(設計-構建-驗證-學習)循環,不僅能持續迭代優化病毒載體,更確保了服務流程的高度標準化和高效性,從而為客戶帶來高性價比的研發體驗。
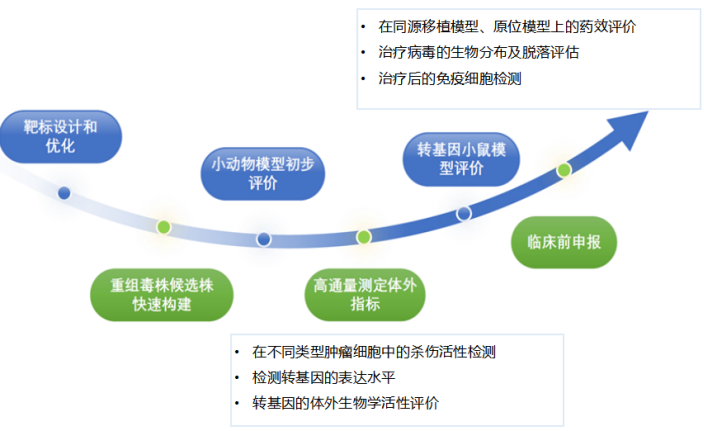
服務案例1:以VSV載體為例
水皰性口炎病毒(VSV)天然具有嗜神經性。「DIFF CRO」通過替換VSV的G蛋白,有效去除其神經毒性,顯著提升安全性。同時,在基因組中插入特定細胞因子,使病毒在感染腫瘤細胞后能局部釋放免疫因子,強力激活抗腫瘤免疫,實現“溶瘤”與“免疫”雙重增效。
DIFF VSV載體優勢:

體外藥效驗證:展現廣譜殺傷潛力
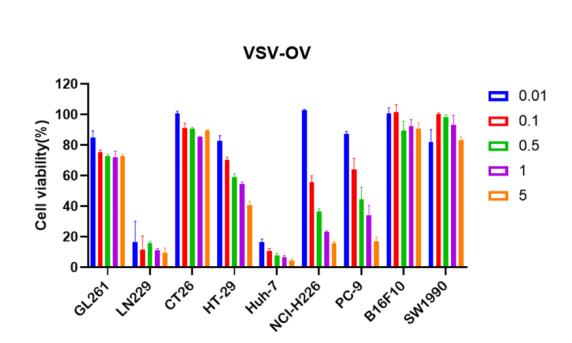
圖1.VSV-OV在體外藥效實驗中對多種腫瘤細胞具有抑制活性
「DIFF CRO」研發團隊構建的VSV-OV在體外藥效試驗中對膠質瘤、結直腸癌、肝癌、肺癌等多種腫瘤細胞系均顯示出強大的直接殺傷活性。
體內藥效確證:在不同動物模型中獲得卓越腫瘤抑制效果
利用CT26小鼠移植瘤模型,VSV OV給藥治療后,大部分小鼠達到完全緩解(CR),8周后re-challenge實驗(在同一部位用同樣數量的腫瘤細胞系進行荷瘤),暫未觀察到CR小鼠再次長瘤(對照組小鼠荷瘤時年齡與VSV-OV給藥組小鼠相匹配,為20周齡), 體現出持久免疫保護效果。
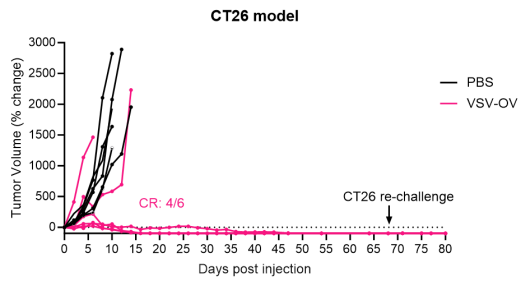
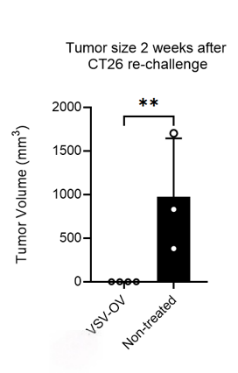
圖2.VSV-OV在CT26小鼠移植瘤模型中具有抑制活性以及持續的免疫保護效果
服務案例2:以NDV載體為例
除對VSV載體進行改造外,「DIFF CRO」也可對NDV,HSV-1等載體進行改造,以NDV載體為例構建溶瘤病毒株候體內藥效評價:
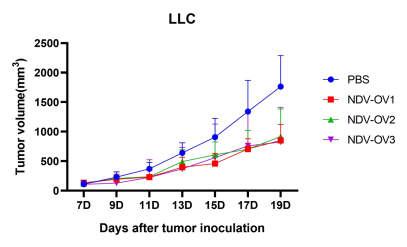
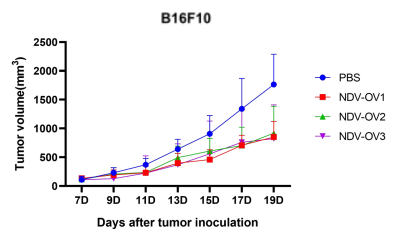
圖3. 以NDV為載體的改造溶瘤病毒候選株(NDV-OV1,NDV-OV2,NDV-OV3)給藥后,成瘤小鼠腫瘤生長相較于空白對照組被顯著抑制。A:LLC成瘤小鼠;B:B16F10成瘤小鼠。
公司擁有符合P2生物安全標準的專用動物實驗室,致力于為創新藥企提供省時省力的一站式解決方案,顯著縮短研發周期,為IND申報提供堅實、可靠的數據支持。選擇「DIFF CRO」的一站式溶瘤病毒開發平臺,即是選擇一條更高效、更經濟的研發路徑。我們憑借快、省、全的服務優勢,為您提供從開發到IND申報的可靠數據支持,共同加速突破!
參考文獻:
Yoon AR, Kim S, Yi J, et al. Oncolytic adenovirus in combination with PD-L1-targeted radioimmunotherapy exerts synergistic antitumor effect against pancreatic cancer. J Immunother Cancer. 2026 Apr 9;14(4):e014508.
