

你是否經(jīng)歷過這樣的至暗時刻? 顯微鏡下,背景著色比目標抗原還深,非特異性染色如滿天星斗;又或者,心心念念的目標抗原似乎“憑空消失”了,只留下一片蒼白的背景。明明使用了相同的抗體、遵循了相同的實驗步驟,得到的結果卻天差地別。如果你也曾有過這樣的困擾,那么問題或許既不在抗體,也不在于實驗操作,而是出在最初、也最容易被忽視的一步:樣本制備。
Vectorlabs 作為免疫組化、免疫熒光試劑領域的領導者,在本文中系統(tǒng)梳理了一套具備高重復性的IHC樣本制備完整流程。
免疫組化(IHC)樣本制備流程包括:樣本固定、切片、脫蠟復水、抗原修復以及免疫組化筆(PAP)的應用。
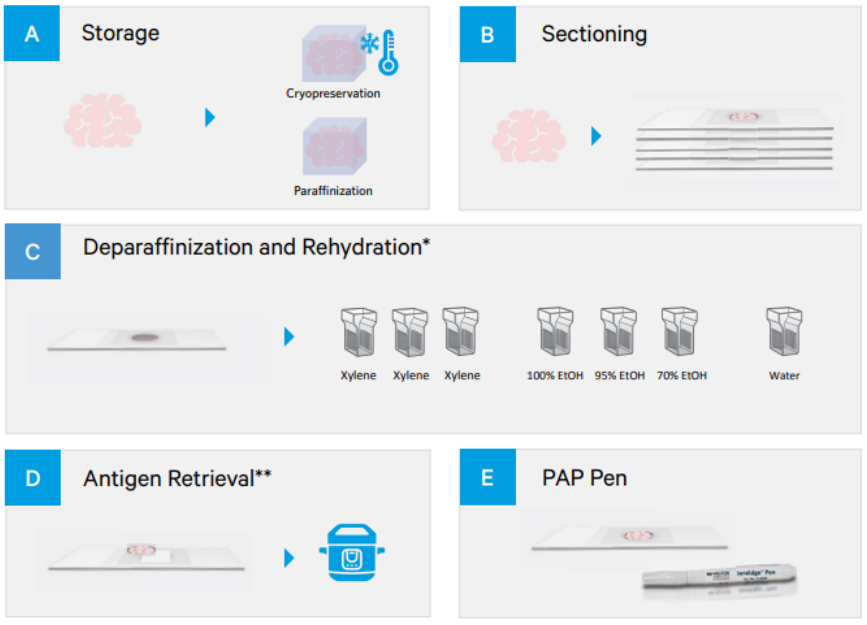
圖1:樣本制備流程。
A. 組織保存:石蠟包埋(FFPE)和冷凍保存;
B. 根據(jù)最終應用,組織塊切成不同厚度的切片;
C. 在二甲苯、梯度酒精中進行脫蠟和水化;
D. 熱誘導抗原修復;
E. PAP筆在組織切片周圍畫圈施加疏水屏障,將試劑限制在特定范圍內。
*脫蠟和水化僅適用于FFPE組織切片;
**對于解剖后速凍的組織,可能不需要熱誘導 抗原修復;無論后續(xù)選擇石蠟包埋還是冷凍保存,經(jīng)過福爾馬林固定的標本進行抗原修復都能改善染色。
組織樣本的長期保存主要分為2類:石蠟包埋和冷凍保存
石蠟包埋:?.醛類固定; ?.梯度酒精脫水; ?.二甲苯透明; ?.石蠟浸透。
經(jīng)由福爾馬林固定( 防止組織自溶和腐敗;保存組織形態(tài));接著,固定的組織經(jīng)過一系列從低濃度到高濃度的梯度酒精處理;然后,與有機溶劑(如二甲苯)孵育去除酒精;最后一步,使用溫熱的石蠟浸透組織,然后冷卻硬化,形成福爾馬林固定、石蠟包埋的蠟塊(FFPE)。
冷凍保存:將生物樣本在-20℃或-80℃下冷凍,是保存組織用于IHC應用的另一種選擇。常規(guī)冷凍流程:新鮮組織在液氮、異戊烷或干冰中速凍,用OCT包埋,再用冷凍切片機切片。組織固定通常在切片后進行,固定劑可選擇丙酮、甲醇、乙醇和甲醛等。
|
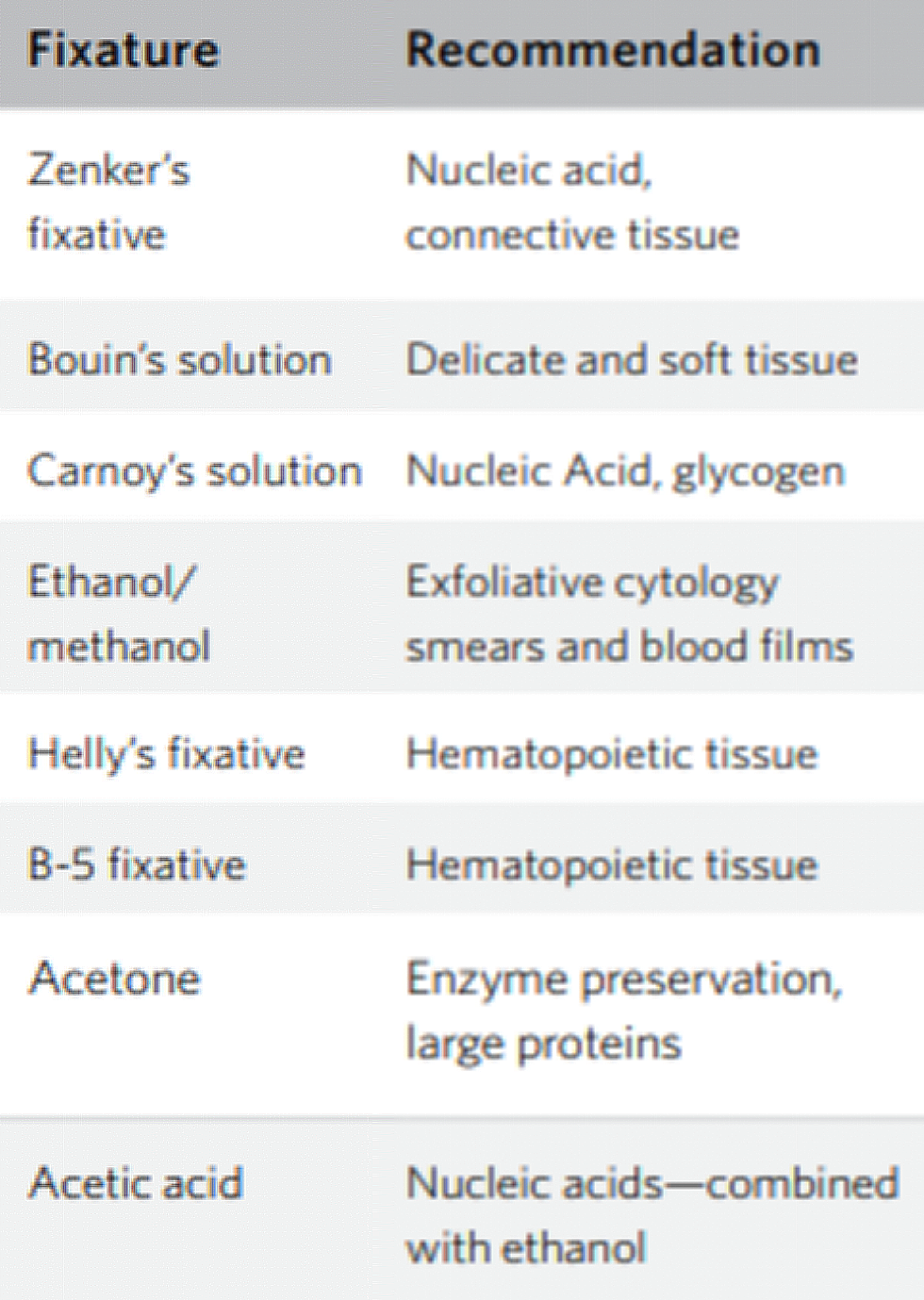
固定劑選擇tips(左圖) |
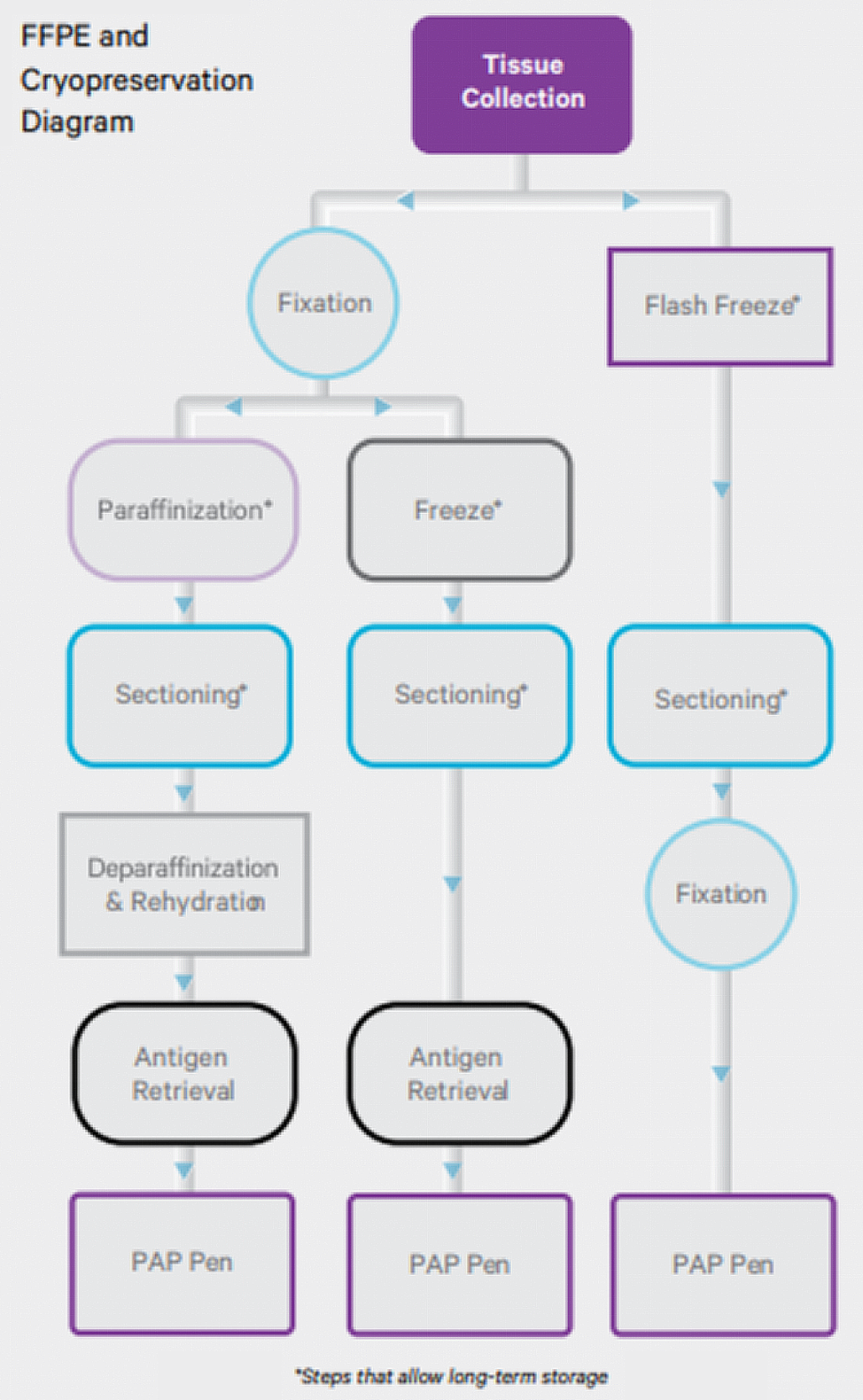
石蠟包埋和冷凍保存流程圖(右圖) |
 |
 |
石蠟包埋和冷凍保存對比
|
石蠟包埋組織(FFPE) |
新鮮冷凍組織 |
福爾馬林固定冷凍組織 |
|
|
固定時機 |
包埋前 |
切片后 |
冷凍前 |
|
固定液 |
甲醛 |
丙酮、甲醇、乙醇等 |
甲醛 |
|
包埋/防凍保護 |
石蠟 |
OCT |
冷凍前用防凍劑浸透 |
|
保存 |
FFPE塊:室溫下數(shù)年 |
冷凍OCT塊(未固定):-80°C下約1年 |
若以漂浮切片形式保存,則浸于防凍劑 |
|
抗原性 |
可能被固定誘導的交聯(lián)掩蓋 |
保留抗原性,通常不需要抗原修復 |
可能被固定誘導的交聯(lián)掩蓋 |
|
切片厚度 |
可薄至1um |
6-10um |
6-20um |
|
形態(tài)學 |
保存完好 |
冰晶形成可能影響組織形態(tài) |
保存完好 |
Tips:
快速冷凍樣本是保持組織和細胞形態(tài)的關鍵。如果冷凍速度過慢,會導致大冰晶的形成,從而破壞形態(tài)結構。下面是兩種快速冷凍樣本的方法:
?. 在一個盛有液氮的小型杜瓦瓶中,放入一個裝有異戊烷的金屬容器。用鋁箔紙包裹組織,然后將其浸入冰冷的異戊烷中。
?. 將干冰粉碎并放入一個小型聚苯乙烯泡沫盒(泡沫箱)中。將組織放入盒中,并用粉碎后的干冰將其覆蓋。
組織經(jīng)冷凍或石蠟包埋后,需分別使用冰凍切片機或石蠟切片機進行切片。切片的常規(guī)厚度需根據(jù)最終實驗目的而定。FFPE蠟塊和冷凍組織都適用于制備薄切片和厚切片;但在需要超薄切片(<6μm)的應用中,F(xiàn)FPE蠟塊的切片效果通常優(yōu)于冷凍組織。研究人員可針對不同實驗目的嘗試多種切片厚度,以確定最佳條件。
薄切片:需要高顯微鏡分辨率,且視野內僅需觀察少量細胞時,薄切片是首選;
厚切片(>6μm):研究腦組織3D形態(tài)或神經(jīng)軸突通路時,可選擇>6μm的厚切片;
超厚切片(20–40μm):適合細胞體視學定量分析和漂浮切片實驗;
注:較厚的切片可能需要在后續(xù)流程中進行更長時間的孵育;厚冷凍切片可在封閉步驟中加入去污劑以提高組織通透性。
切片完成后,載玻片需要在室溫下自然晾干約24小時,或者在50-60℃的烘箱中烘干1小時,在烘箱中烘干時必須密切留意,因為在高溫下長時間烤片可能會降低免疫原性。有些組織還可以放在50℃恒溫烤片機上加熱30-60分鐘,這樣可以避免樣本從載玻片上脫落。使用化學粘附試劑(如VECTABOND® Reagent, Tissue Section Adhesion,貨號SP-1800),有助于組織在原位雜交、高溫抗原修復等嚴苛條件下仍牢固附著在載玻片上。
FFPE樣本切片后需進行脫蠟和水化。這個過程的順序(圖2)與石蠟浸透時的脫水步驟完全相反:
?. 二甲苯脫蠟
?. 梯度酒精復水
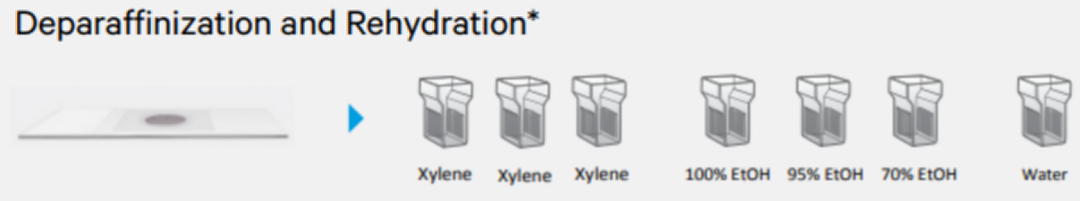
圖2. 脫蠟、復水步驟簡易圖
脫蠟不徹底會導致同一樣本中同一 抗原染色出現(xiàn)不均勻或呈斑片狀,使用新鮮配制的試劑是避免這一問題的措施之一。另外,載玻片在每種溶液中浸泡的時間必須適當,且切片越厚所需時間越長;例如,4-5μm的切片完全脫蠟,至少需要2次二甲苯浸泡,每次5分鐘;更厚的切片可延長時間或增加次數(shù)。
福爾馬林固定會使組織蛋白質的氨基酸之間形成交聯(lián)。雖然這一過程對于硬化組織和維持形態(tài)至關重要,但該過程也會掩蓋抗原表位、降低抗原性,導致染色弱或無染色。抗原修復步驟可幫助恢復被掩蓋的表位,從而獲得最佳的染色效果。
熱誘導抗原修復(HIER):即在特定緩沖液中加熱組織以破壞交聯(lián)(圖3),相比于酶解法具有明顯的優(yōu)勢。可選擇的加熱設備有微波爐、高壓鍋、水浴鍋或高壓滅菌器,高壓鍋和高壓滅菌器可以在不發(fā)生劇烈沸騰的情況下將樣本加熱至100℃以上,微波爐也具備這個優(yōu)勢,且專業(yè)的實驗室型號可以控制溫度,但需要密切監(jiān)控,并隨時補充蒸發(fā)掉的緩沖液。水浴鍋也能控制溫度,并允許在較低溫度下進行熱誘導抗原修復,這可能非常適合某些特定的應用。無論選擇哪種設備,都需要確定理想的溫度(如果設備允許)和孵育時間。一般的建議是:從低溫開始,根據(jù)需要逐漸升高,并在組織出現(xiàn)損傷跡象之前停止。
溫度對抗原修復效果的影響比緩沖液的選擇更為顯著,緩沖液的pH值同樣重要,檸檬酸鹽和Tris體系溶液是最常用的選擇。選擇修復緩沖液時,可以優(yōu)先參考抗體說明書,無說明書時需自行測試決定。
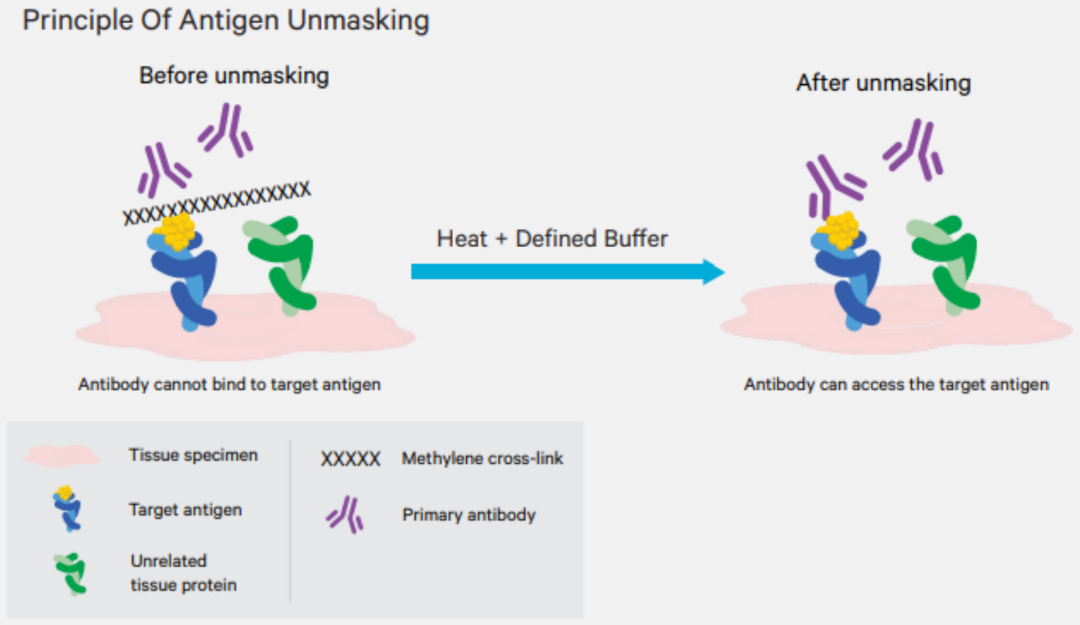
圖3. 熱誘導抗原修復原理圖
樣本制備的最后一步:使用PAP筆在切片周圍畫疏水屏障圈,能將試劑限制在特定區(qū)域內,避免同張載玻片上多種試劑混合。與傳統(tǒng)PAP筆相比,ImmEdge® PAP筆(貨號H-4000)具備以下特點:
?. 適用于含或不含去污劑(Tween 20、Triton X-100等)的緩沖液,屏障穩(wěn)定
?. 淺藍色疏水圈,清晰可見,兼容酶法與熒光檢測系統(tǒng)
?. 可溶于各類常用透明劑(如二甲苯等),方便清理
?. 環(huán)保:不含《蒙特利爾議定書》及歐盟理事會認定的破壞臭氧層的物質
規(guī)范的樣本制作,不僅是染色成功的基石,更是確保鏡檢過程順暢無憂的關鍵。每一步選擇都必須貼合實驗需求,任何環(huán)節(jié)操作不當都可能影響結果。唯有前瞻性的全盤考量、科學的決策以及全程使用優(yōu)質試劑,方能確保實驗圓滿成功。
|
產(chǎn)品名稱 |
貨號 |
此外,Vector還提供其他一系列IHC/IF的相關產(chǎn)品和資料,更多詳情請咨詢Vectorlabs中國獨家代理商—欣博盛生物
全國服務熱線: 4006-800-892 郵箱: market@neobioscience.com
深圳: 0755-26755892 北京: 010-88594029
上海: 021-34613729 廣州: 020-87615159 香港: 852-69410778
欣博盛代理網(wǎng)站: www.nbs-bio.com
欣博盛品牌網(wǎng)站: www.neobioscience.net
