肝內(nèi)膽管癌(ICC)是第二大常見(jiàn)的原發(fā)性肝癌,具有高度惡性且預(yù)后極差,5年生存率低于10%。目前,手術(shù)切除術(shù)是主要治療手段,但對(duì)于無(wú)法切除或晚期疾病的患者,現(xiàn)有療法效果有限。ICC中脂質(zhì)合成受抑,但氨基酸和核苷酸代謝異常活躍,提示其可能依賴(lài)該通路維持惡性增殖。SIRT6(Sirtuin(沉默信息調(diào)節(jié)因子)家族成員)作為NAD?依賴(lài)的去乙酰化酶,既往在多種癌癥中被視為抑癌基因,可通過(guò)調(diào)控糖脂代謝抑制腫瘤,但在ICC中作用未知。
2025年10月,華中科技大學(xué)同濟(jì)醫(yī)學(xué)院研究團(tuán)隊(duì)在Gut上在線(xiàn)發(fā)表了題為“SIRT6 promotes intrahepatic cholangiocarcinoma development by reprogramming glutamine metabolism via enhanced GLUL”的研究文章,通過(guò)多組學(xué)+多模型策略,發(fā)現(xiàn)SIRT6在肝內(nèi)膽管癌中作為癌基因,通過(guò)增強(qiáng)GLUL的轉(zhuǎn)錄激活與蛋白穩(wěn)定性調(diào)控谷氨酰胺代謝重編程,靶向SIRT6-GLUL軸可抑制ICC進(jìn)展并提升化療敏感性,為ICC治療提供新策略。(麥特繪譜提供有機(jī)酸+代謝流(15N-NH4CL)技術(shù)檢測(cè)服務(wù))
研究設(shè)計(jì)
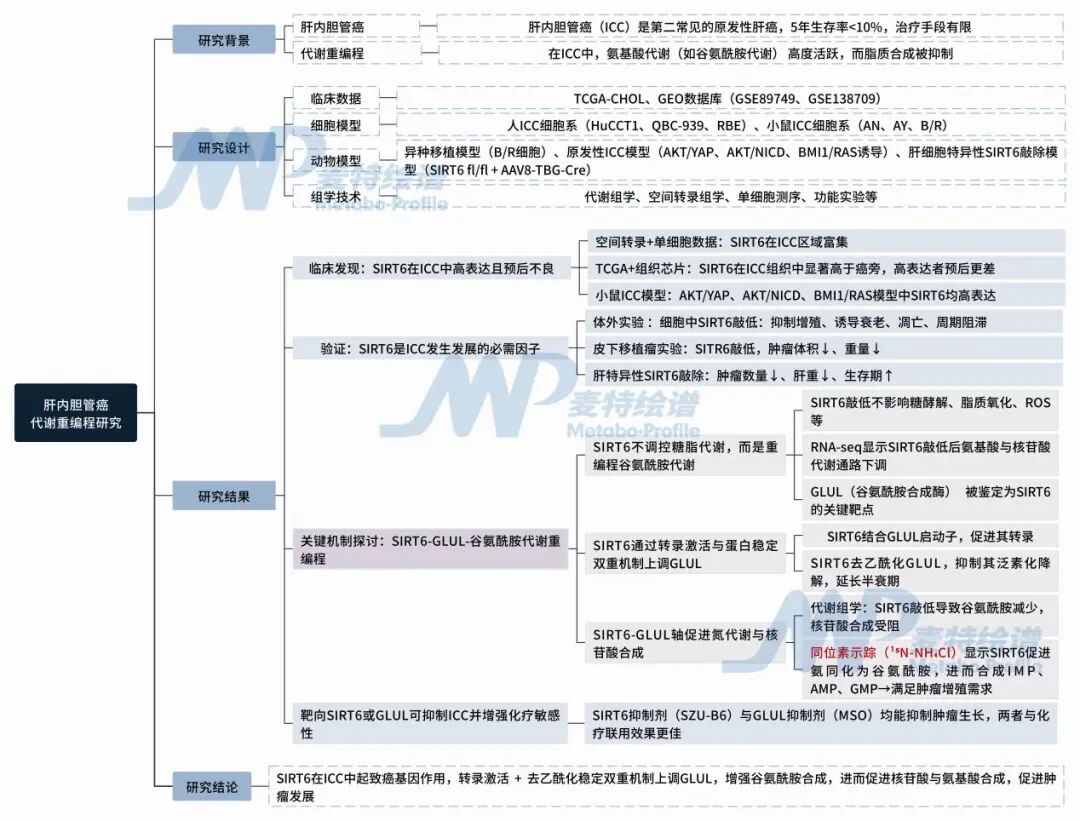
圖1. 技術(shù)思路
研究結(jié)果
1. SIRT6在ICC中高表達(dá),與預(yù)后不良有關(guān)
通過(guò)空間轉(zhuǎn)錄數(shù)據(jù)(GSE89749)和單細(xì)胞測(cè)序數(shù)據(jù)(GSE138709),發(fā)現(xiàn)SIRT6高表達(dá)細(xì)胞簇與ICC區(qū)域富集相關(guān),在TCGA-CHOL和GSE107943數(shù)據(jù)庫(kù)中也驗(yàn)證了人類(lèi)ICC腫瘤組織中SIRT6 mRNA水平顯著升高。此外,SIRT6在臨床ICC組織中顯著高于癌旁且高表達(dá)者預(yù)后更差,在AKT/YAP等小鼠ICC模型中也證實(shí)SIRT6高表達(dá)。
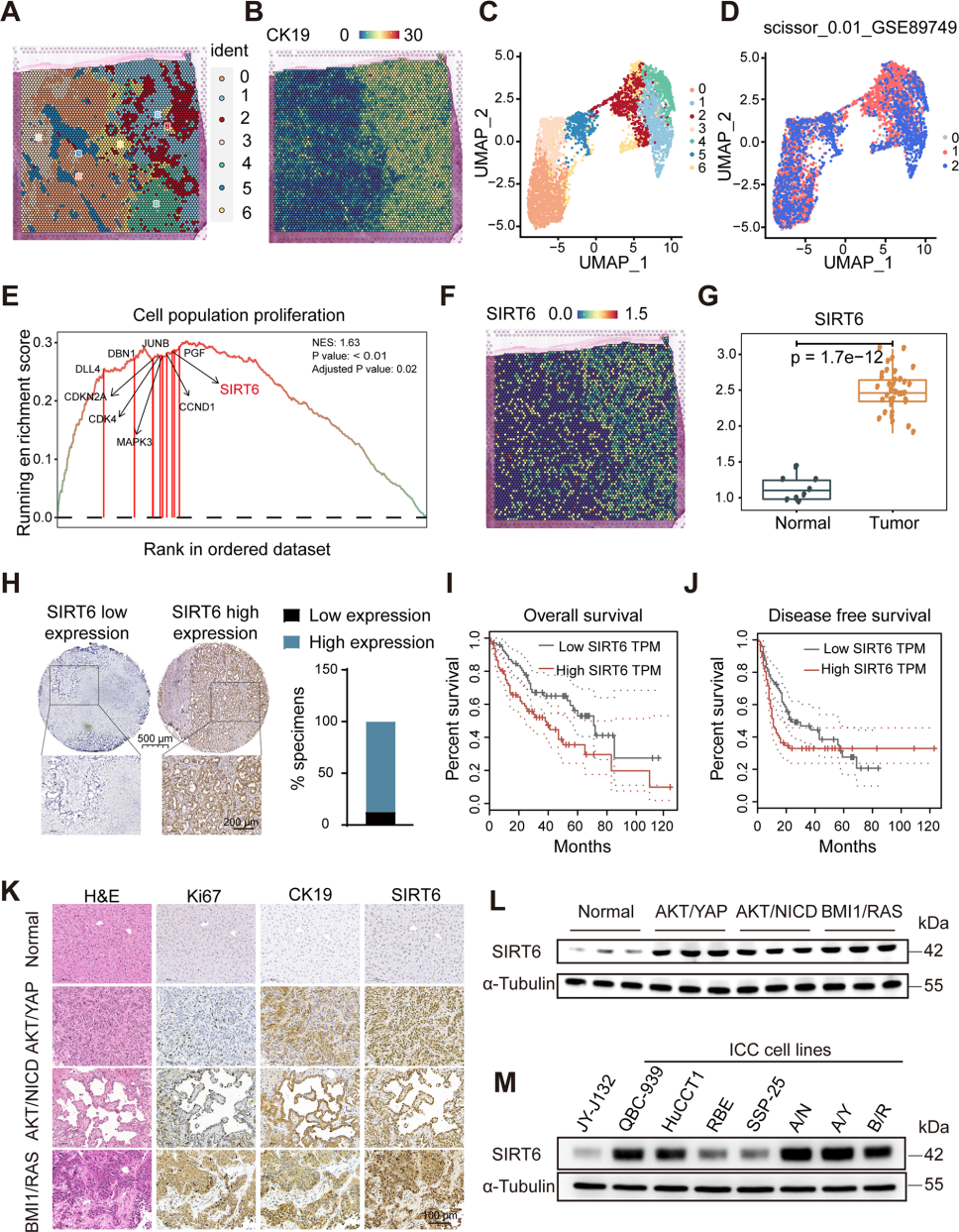
圖2. 肝組織中SIRT6表達(dá)上調(diào)與肝細(xì)胞癌患者預(yù)后不良相關(guān)
2. SIRT6促進(jìn)ICC細(xì)胞增殖與腫瘤形成
進(jìn)一步探究SIRT6的功能,在人和小鼠的ICC細(xì)胞中敲低SIRT6發(fā)現(xiàn)其抑制細(xì)胞活力并誘導(dǎo)細(xì)胞衰老及凋亡;過(guò)表達(dá)則促進(jìn)RBE細(xì)胞(人肝內(nèi)膽管癌細(xì)胞系)存活增殖;在B/R小鼠ICC細(xì)胞構(gòu)建的皮下移植瘤模型中,SIRT6敲低顯著減小腫瘤體積和重量,延長(zhǎng)AKT/YAP誘導(dǎo)的ICC小鼠生存期;在肝特異性敲除SIRT6小鼠中,同樣延遲了AKT/YAP誘導(dǎo)的ICC形成。
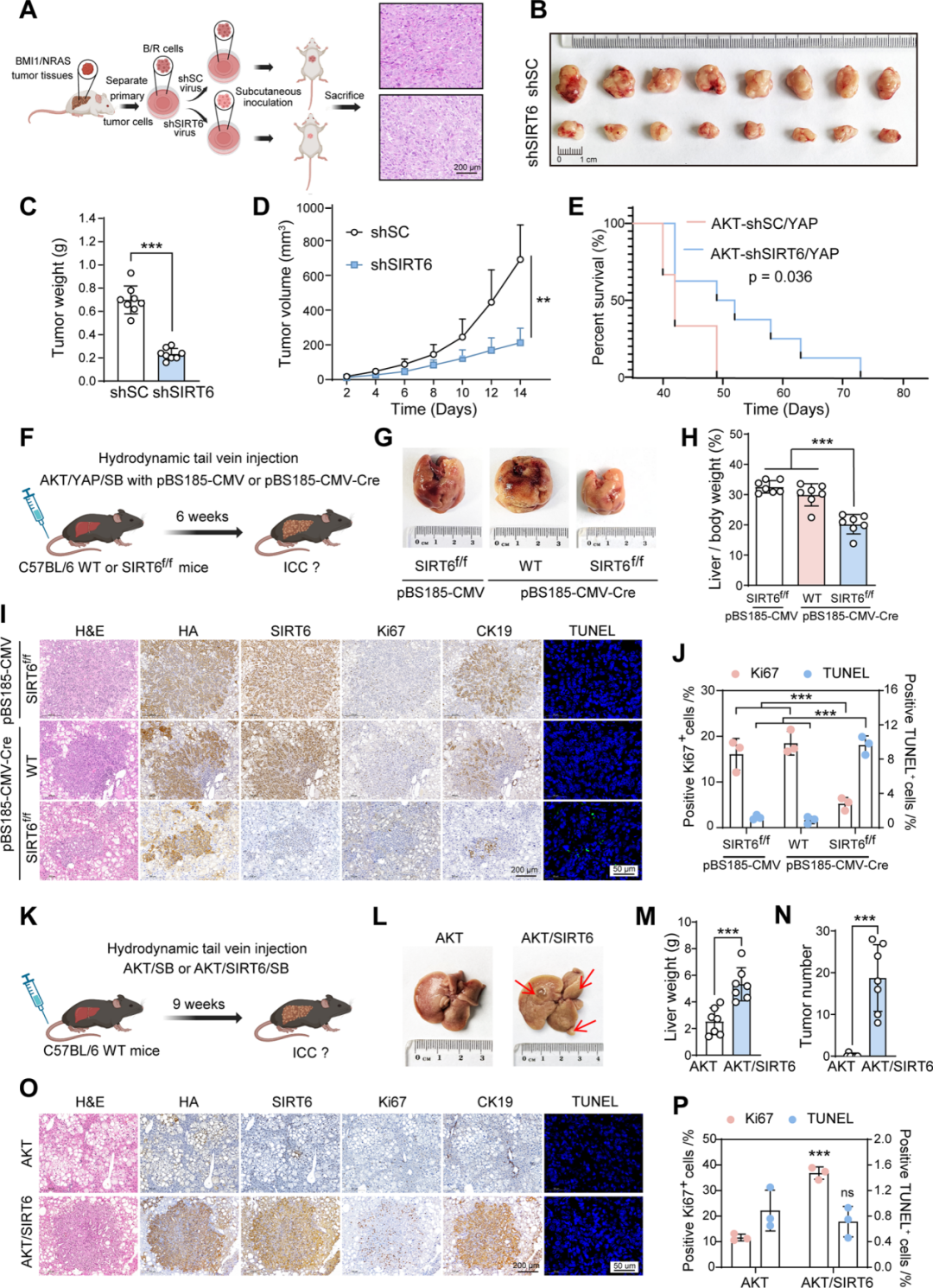
圖3. SIRT6是ICC發(fā)生發(fā)展的關(guān)鍵驅(qū)動(dòng)因子
3. SIRT6不調(diào)控糖脂代謝,而是通過(guò)GLUL調(diào)控谷氨酰胺代謝
● SIRT6不調(diào)節(jié)ICC的糖脂代謝及氧化還原動(dòng)態(tài)平衡
既往研究表明,SIRT6在不同類(lèi)型的癌癥中調(diào)節(jié)葡萄糖和脂肪代謝。進(jìn)一步在ICC細(xì)胞和組織中進(jìn)行了探索,發(fā)現(xiàn)SIRT6敲低不影響ICC細(xì)胞的脂質(zhì)β-氧化速率 (OCR)和糖酵解速率 (ECAR) 。在氧化應(yīng)激調(diào)節(jié)中,SIRT6基因敲除對(duì)ICC細(xì)胞中的還原型谷胱甘肽(GSH)、氧化谷胱甘肽(GSSG)或活性氧物種(ROS)水平幾乎沒(méi)有影響。
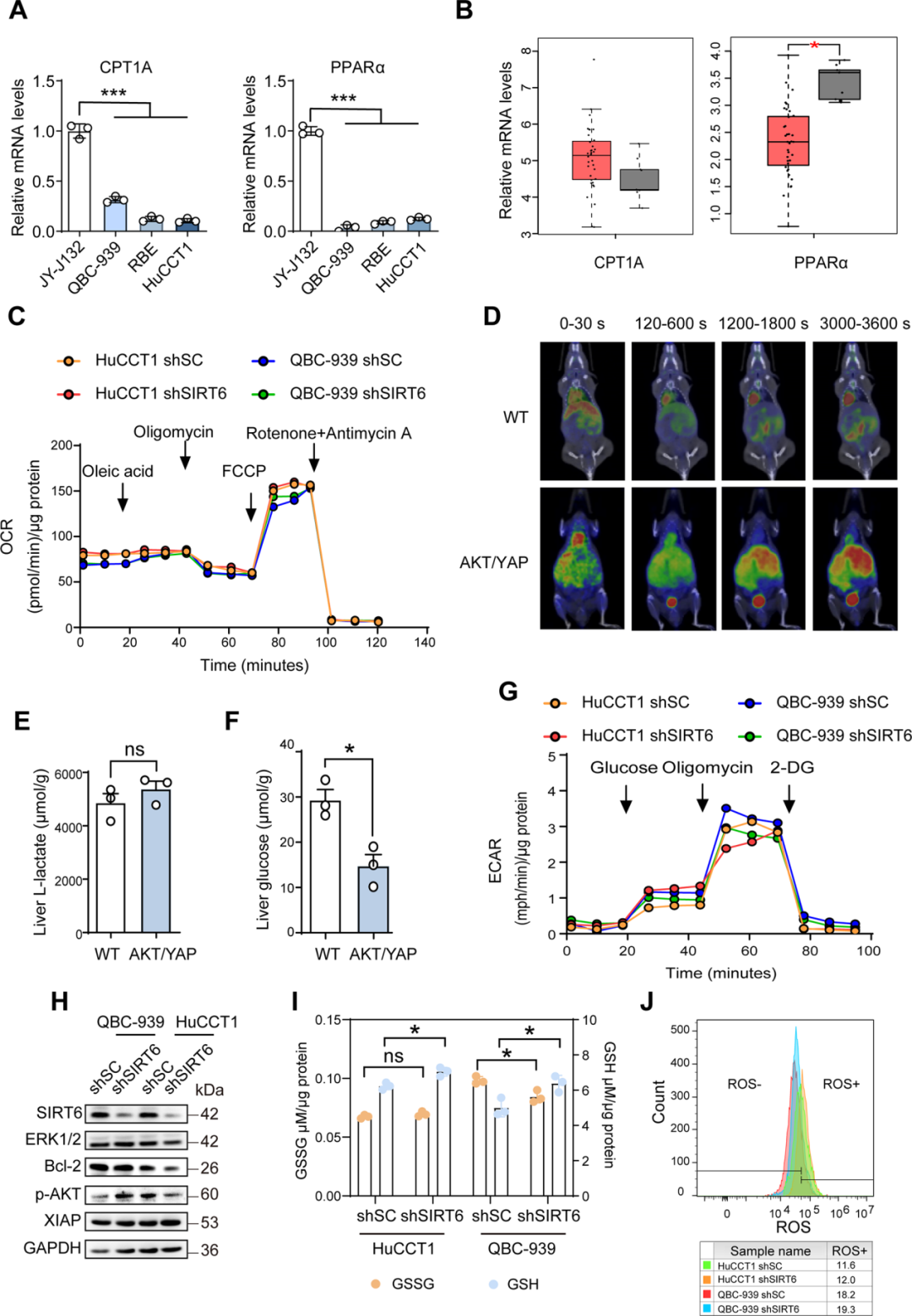
圖4. 驗(yàn)證SIRT6在促進(jìn)ICC細(xì)胞生長(zhǎng)中的潛在功能
●SIRT6增強(qiáng)ICC谷氨酰胺代謝
RNA測(cè)序結(jié)果表明,在SIRT6基因敲除后,ICC細(xì)胞的氨基酸生物合成和嘌呤代謝途徑下調(diào),且谷氨酰胺水平降低,添加谷氨酰胺可增強(qiáng)OXPHOS,而SIRT6敲低則減弱此效應(yīng),表明SIRT6影響了谷氨酰胺供養(yǎng)的TCA循環(huán)。通過(guò)靶向代謝組學(xué)對(duì)TCA通路循環(huán)通量進(jìn)行測(cè)定,證實(shí)在SIRT6沉默后,TCA通路明顯被抑制。
●SIRT6通過(guò)GLUL調(diào)控谷氨酰胺代謝
RNA測(cè)序結(jié)果發(fā)現(xiàn)在排名前20位的基因中,GLUL是與谷氨酰胺代謝相關(guān)的排名最高的基因。此外,qRT-PCR和Western blot證實(shí)SIRT6調(diào)節(jié)ICC細(xì)胞和AKT/YAP ICC組織中GLUL的mRNA和蛋白水平以及催化活性。免疫染色顯示39對(duì)ICC患者的FFPE標(biāo)本中SIRT6和GLUL蛋白水平呈正相關(guān),證實(shí)GLUL是SIRT6調(diào)控谷氨酰胺代謝的關(guān)鍵靶點(diǎn)。
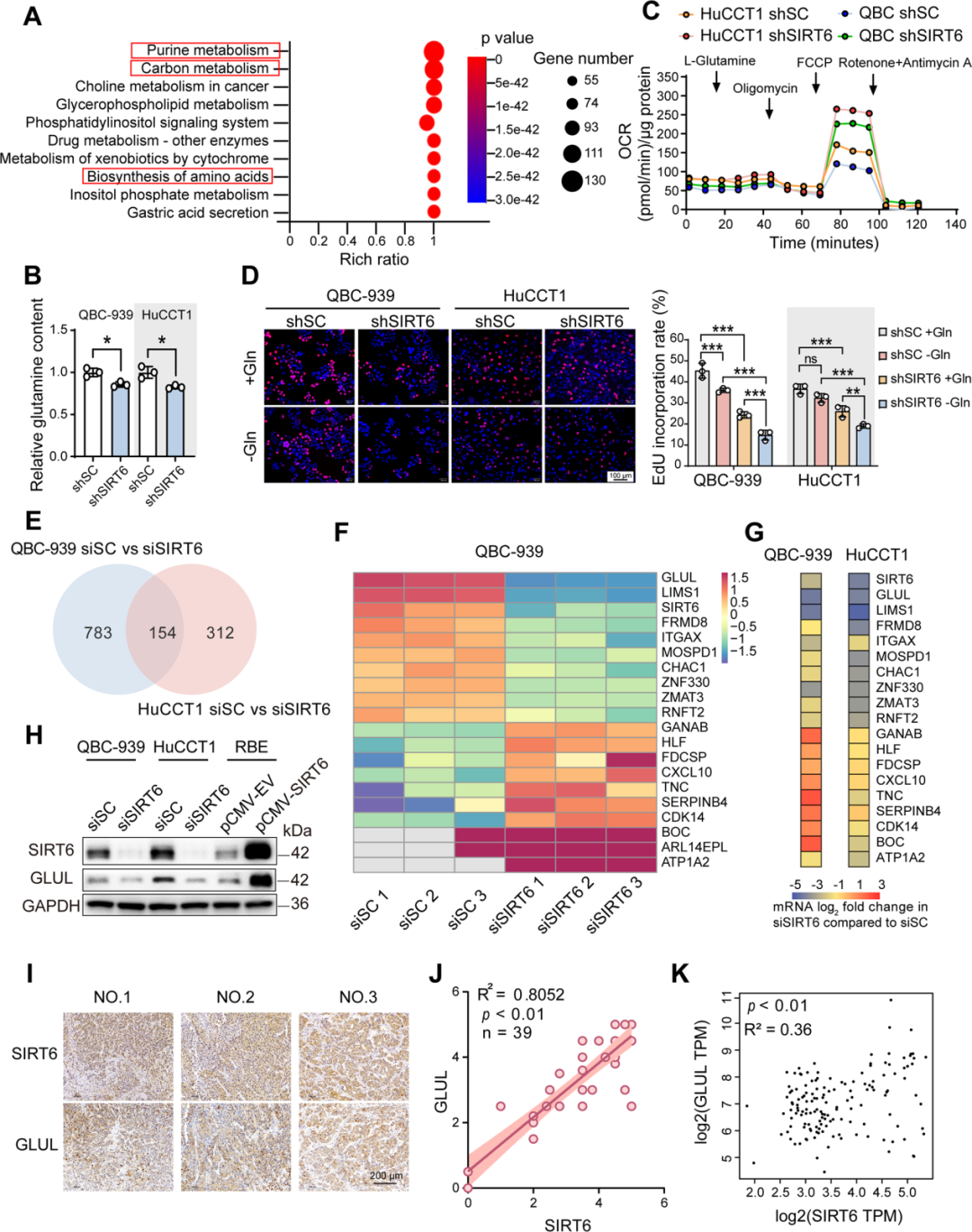
圖5. SIRT6對(duì)ICC中谷氨酰胺代謝的調(diào)節(jié)
4. SIRT6通過(guò)轉(zhuǎn)錄激活與蛋白穩(wěn)定雙重機(jī)制上調(diào)GLUL
進(jìn)一步探究SIRT6是否作為轉(zhuǎn)錄因子直接促進(jìn)GLUL表達(dá),發(fā)現(xiàn)過(guò)表達(dá)SIRT6的293T和RBE細(xì)胞中,GLUL的mRNA水平顯著上調(diào)。熒光素酶報(bào)告基因和染色質(zhì)免疫沉淀實(shí)驗(yàn)表明,SIRT6能結(jié)合GLUL啟動(dòng)子,促進(jìn)其轉(zhuǎn)錄。
基于GLUL乙酰化會(huì)促進(jìn)其泛素化和蛋白酶體降解,研究了SIRT6能否通過(guò)去乙酰化穩(wěn)定GLUL蛋白。敲低SIRT6縮短了QBC-939和HuCCT1細(xì)胞中GLUL的半衰期,表明其降解加速;過(guò)表達(dá)SIRT6可降低GLUL乙酰化,而催化失活突變體則增加乙酰化,表明SIRT6直接去乙酰化GLUL。
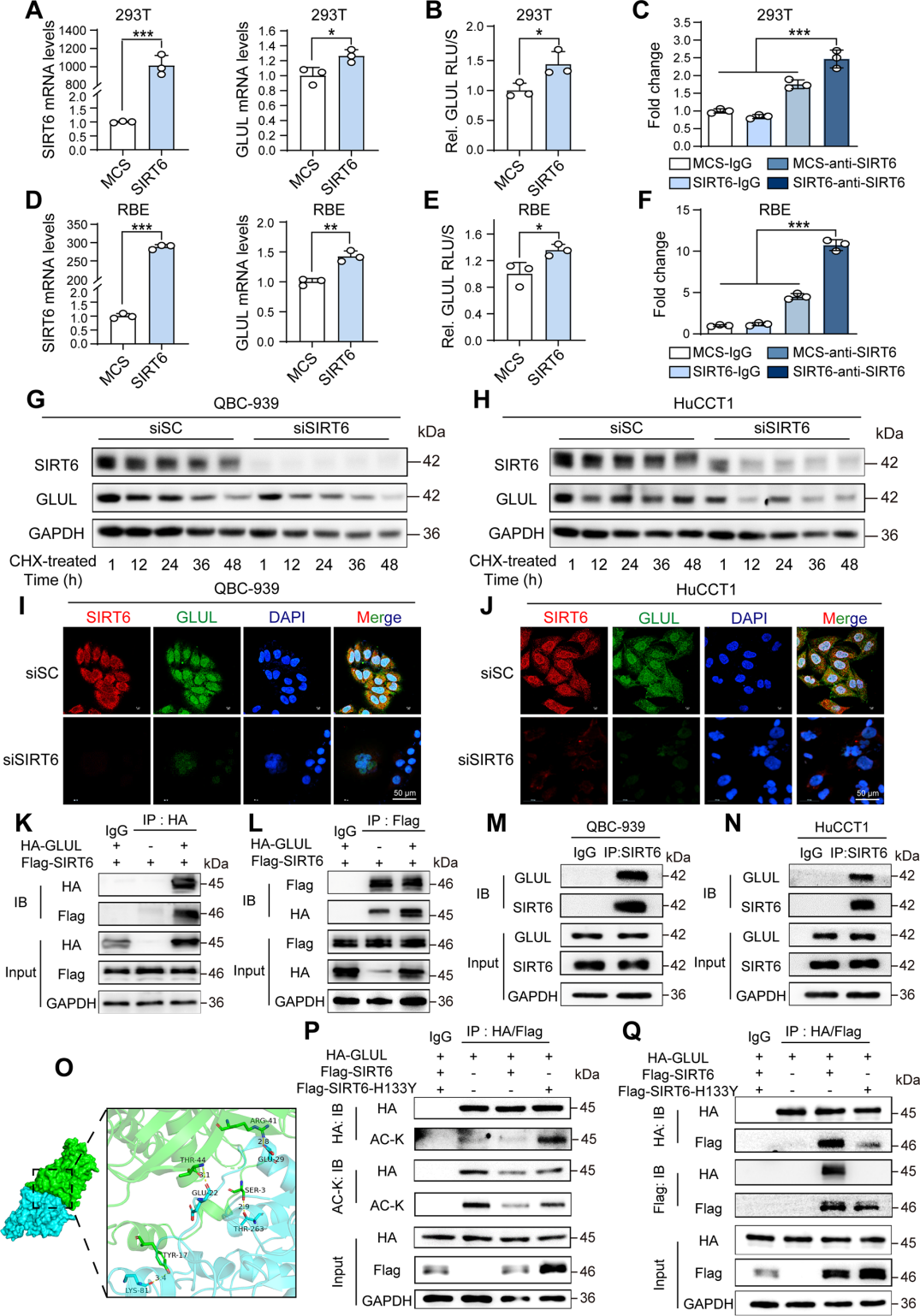
圖6. SIRT6增強(qiáng)GLUL轉(zhuǎn)錄并防止其降解
5. SIRT6-GLUL軸促進(jìn)氮代謝與核苷酸合成
通過(guò)代謝組學(xué)進(jìn)一步分析了SIRT6激活對(duì)ICC細(xì)胞代謝的影響,發(fā)現(xiàn)SIRT6敲低導(dǎo)致多種代謝物變化,尤其富集于核苷酸、氨基酸及其衍生物。進(jìn)一步通過(guò)15N-NH4Cl同位素示蹤代謝流技術(shù)發(fā)現(xiàn)SIRT6沉默減少了新合成IMP, AMP, GMP核苷酸的比例,15N標(biāo)記的谷氨酰胺含量減少,谷氨酸含量增加,GLUL過(guò)表達(dá)可恢復(fù)此效應(yīng)。在GSE89749數(shù)據(jù)集中,ICC患者的SIRT6表達(dá)水平和核苷酸含量之間存在顯著的正相關(guān)。上述結(jié)果表明,SIRT6通過(guò)GLUL促進(jìn)谷氨酰胺利用,進(jìn)而支持核苷酸和氨基酸生物合成,滿(mǎn)足腫瘤快速增殖合成的生物需求。
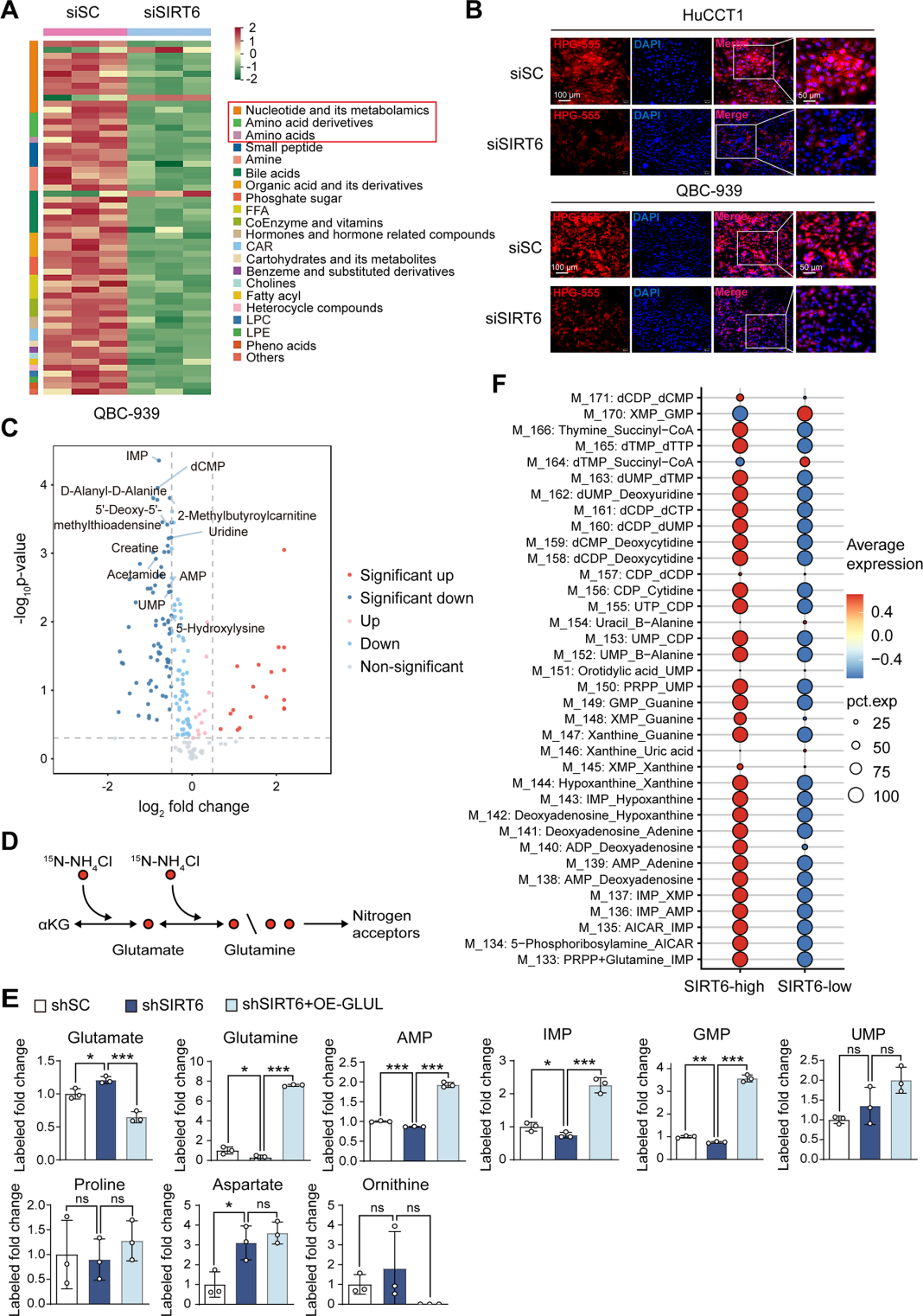
圖7.SIRT6沉默抑制ICC細(xì)胞的核苷酸和氨基酸代謝
6. 靶向SIRT6或GLUL可抑制ICC并增強(qiáng)化療敏感性
在AKT/YAP ICC小鼠模型中,SIRT6抑制劑(SZU-B6)和GLUL抑制劑(MSO)均能顯著抑制腫瘤生長(zhǎng) (圖5Q-S)。兩者均能協(xié)同增強(qiáng)吉西他濱/順鉑化療效果 (圖5Q-S)。而抗PD-1單一治療沒(méi)有顯示出抗腫瘤活性,且抑制劑不增強(qiáng)其療效。
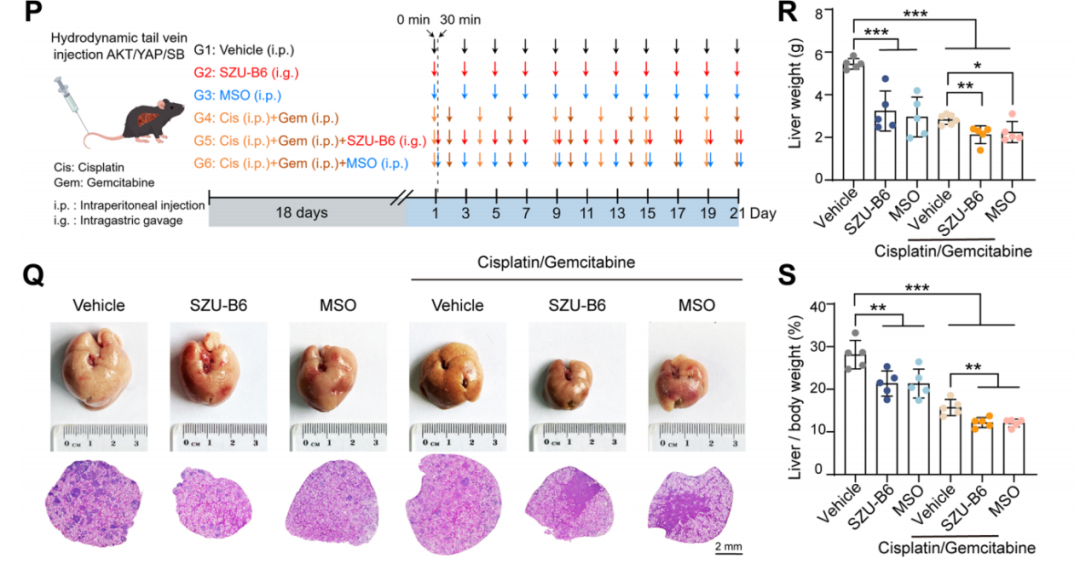
圖8. 靶向SIRT6或GLUL可抑制ICC并增強(qiáng)化療敏感性
研究結(jié)論
在不同癌癥類(lèi)型中,SIRT6可表現(xiàn)為腫瘤抑制因子或腫瘤促進(jìn)因子。本研究揭示了SIRT6在ICC中作為促癌基因的新功能,明確SIRT6通過(guò)轉(zhuǎn)錄激活和翻譯后穩(wěn)定 GLUL,調(diào)控谷氨酰胺代謝重編程,為ICC細(xì)胞增殖提供代謝支持的核心機(jī)制。證實(shí)SIRT6-GLUL軸是ICC治療的潛在靶點(diǎn),抑制劑單獨(dú)使用或與化療聯(lián)合均可有效抑制ICC進(jìn)展,為臨床治療提供新方向。
參考文獻(xiàn)
SIRT6 promotes intrahepatic cholangiocarcinoma development by reprogramming glutamine metabolism via enhanced GLUL. Gut. 2025
繪譜幫你測(cè)
本研究中通過(guò)代謝組學(xué)發(fā)現(xiàn)SIRT6對(duì)ICC細(xì)胞的氨基酸生物合成及嘌呤代謝通路具有關(guān)鍵調(diào)控作用,結(jié)合麥特繪譜提供的15N-NH4Cl同位素示蹤技術(shù)進(jìn)一步證實(shí),SIRT6通過(guò)增強(qiáng)GLUL介導(dǎo)的谷氨酰胺合成,推動(dòng)氨的氮同化過(guò)程并為核苷酸生物合成提供前體,最終驅(qū)動(dòng)ICC的發(fā)生發(fā)展。麥特繪譜開(kāi)創(chuàng)性地搭建了醫(yī)學(xué)領(lǐng)域高端代謝組學(xué)技術(shù)平臺(tái),覆蓋了非靶向-全定量-代謝流等全方位的高端醫(yī)學(xué)代謝組解決方案,同時(shí)全面布局微生物組學(xué)、轉(zhuǎn)錄組學(xué)和蛋白質(zhì)組學(xué)等多組學(xué)技術(shù)服務(wù),已成為全球多組學(xué)研究者的優(yōu)選合作伙伴。麥特繪譜已為數(shù)百家三甲醫(yī)院、科研院所和企業(yè)提供多組學(xué)一站式整體解決方案,協(xié)助客戶(hù)與合作伙伴發(fā)表SCI文章600+篇,累計(jì)影響因子6000+,平均IF>10,涵蓋Cell, Science, Nature, Cancer Cell, Signal Trans-duction and Targeted Therapy, Nature Biotechnology, Cell Metabolism等權(quán)威期刊。
