導(dǎo)讀聚焦
本期繪譜導(dǎo)讀聚焦于8篇近期發(fā)表的腸道微生物-宿主代謝互作的頂刊論文:
①解鎖膽汁酸互作的健康網(wǎng)絡(luò):腸道微生物與膽汁酸存在雙向調(diào)控網(wǎng)絡(luò),結(jié)合BXD遺傳參考群體的研究,解析基因背景與飲食如何共同塑造微生物 - 膽汁酸互作,揭示次級膽汁酸在西方飲食相關(guān)結(jié)直腸癌中的關(guān)鍵作用。
②從炎癥到癌變的 “隱秘免疫炎癥推手”:重點(diǎn)解析特定腸道菌株(如P. excrementihominis)通過致病性NETosis激活炎癥、驅(qū)動結(jié)直腸癌的機(jī)制,同時梳理菌群氨基酸代謝產(chǎn)物調(diào)控CD8?T細(xì)胞功能、影響腫瘤免疫的前沿發(fā)現(xiàn)。
③吲哚類代謝“雙生花”:吲哚-3-丙酸&吲哚-3-乙酸可分別從重塑骨髓造血和抑制結(jié)直腸癌細(xì)胞增殖、腫瘤生長及肝轉(zhuǎn)移。
④腸道菌群的整體功能出新:腸道微生物組預(yù)測糖尿病前期個體對膳食纖維干預(yù)的響應(yīng),口服微生物群療法攻克復(fù)發(fā)性艱難梭菌感染。
導(dǎo)讀目錄
-
Nature Communication | BXD遺傳參考群體中腸道微生物組-膽汁酸互作的遺傳與飲食決定因素
-
Nature Medicine | VOS口服微生物群療法破解復(fù)發(fā)性艱難梭菌感染長效復(fù)發(fā)
-
Gut | P. excrementihominis通過致病性NETosis激活加劇實驗性結(jié)腸炎及結(jié)腸炎相關(guān)結(jié)直腸癌
-
Gut | 腸道細(xì)菌產(chǎn)生的次級膽汁酸促進(jìn)西方飲食相關(guān)的結(jié)直腸癌發(fā)生
-
Nature Comunications | 化療誘導(dǎo)的腸道菌群失調(diào)與吲哚-3-丙酸重塑骨髓造血,促進(jìn)抗轉(zhuǎn)移狀態(tài)
-
Nature Comunications | 腸道微生物組預(yù)測糖尿病前期個體對膳食纖維干預(yù)的個性化反應(yīng)
-
Cell Host & Microbe | 腸道微生物氨基酸代謝通過調(diào)控CD8?T細(xì)胞功能影響癌癥進(jìn)展及抗腫瘤免疫力
-
Advanced Science | 結(jié)直腸癌細(xì)胞的武器:RNF32與SPP1+巨噬細(xì)胞結(jié)合以促進(jìn)肝臟轉(zhuǎn)移,以吲哚-3-乙酸為靶點(diǎn)
資源領(lǐng)取
本期導(dǎo)讀文獻(xiàn)原文,請在公眾號后臺回復(fù)“2026年1月繪譜導(dǎo)讀”,即可獲取資源鏈接。
#1
Nature Communication | BXD遺傳參考群體中腸道微生物組-膽汁酸互作的遺傳與飲食決定因素

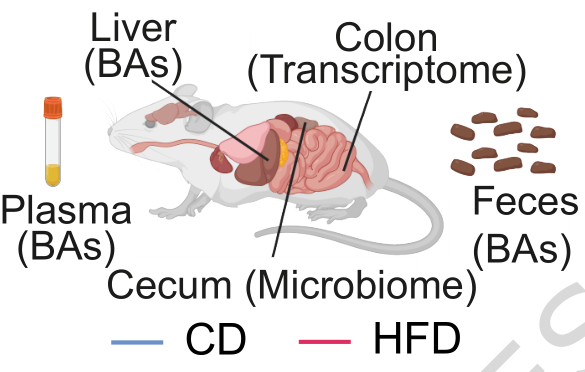
腸道微生物群在整體生理調(diào)節(jié)中起著關(guān)鍵作用,并通過多種微生物衍生的代謝物(如次級膽汁酸)與宿主相互作用。然而,腸道微生物群與膽汁酸之間的相互作用機(jī)制(gMxB)仍不清楚。本研究系統(tǒng)分析了喂食普通飼料或高脂肪飼料的雄性BXD小鼠的盲腸微生物群、膽汁酸水平以及結(jié)腸轉(zhuǎn)錄組,發(fā)現(xiàn)遺傳和飲食因素共同改變微生物群組成并影響gMxB。通過系統(tǒng)遺傳學(xué)方法,進(jìn)一步鑒定出4個與gMxB相關(guān)的飲食依賴性共定位遺傳位點(diǎn)。通過整合人類MiBioGen數(shù)據(jù)庫,篩選出PTGR1與PTPRD作為調(diào)控上述互作的潛在宿主基因,為深入理解腸道微生物與宿主的分子交流機(jī)制提供了新的見解。
1、通過微生物組分析發(fā)現(xiàn),高脂飲食顯著降低了菌群的α多樣性,并鑒定出15個差異豐度菌屬,其中Lactococcus豐度明顯升高、Turicibacter明顯降低,且Firmicutes/Bacteroidota比值呈品系特異性變化。
2、通過靶向膽汁酸檢測以及關(guān)聯(lián)分析發(fā)現(xiàn),普通飼料條件下,香農(nóng)指數(shù)(菌群多樣性)與糞便、肝臟和血漿中的次級膽汁酸/初級膽汁酸(secondary BA/primary BA)比值呈正相關(guān)。而在高脂飲食喂養(yǎng)后這些相關(guān)性便消失了,高脂飲食破壞了微生物群與膽汁酸代謝的相互作用。
3、通過轉(zhuǎn)錄組分析發(fā)現(xiàn),高脂飲食誘導(dǎo)炎癥相關(guān)基因(Saa1、Saa3)上調(diào),抑癌基因(Cyp2c55)及腸道保護(hù)基因(Ces2a)下調(diào)。進(jìn)一步通過稀疏典型相關(guān)分析發(fā)現(xiàn),高脂飲食特異性地誘導(dǎo)了腸道菌群與宿主炎癥、免疫相關(guān)基因通路(如干擾素反應(yīng)、白細(xì)胞介素信號)的關(guān)聯(lián)。
4、進(jìn)一步鑒定出4個與菌群-膽汁酸互作相關(guān)的共定位遺傳位點(diǎn):gMxB1調(diào)控正常飲食下Turicibacter sanguinis的豐度與血漿/肝臟中的膽酸、鵝去氧膽酸水平。gMxB2調(diào)控正常飲食下 T. sanguinis 的豐度與肝臟膽酸水平。gMxB3調(diào)控高脂飲食下Bacteroides uniformis的豐度與糞便中的α-MCA、TLCA、UDCA水平。gMxB4調(diào)控高脂飲食下Bacteroides屬的豐度與糞便中的7-酮基-LCA和DCA水平。
參考文獻(xiàn):Li X, Perino A, Sulc J, et al. Genetic and dietary determinants of gut microbiome-bile acid interactions in the BXD genetic reference population. Nature Communications. 2025
#2
Nature Medicine | VOS口服微生物群療法破解復(fù)發(fā)性艱難梭菌感染長效復(fù)發(fā)

艱難梭菌感染所引發(fā)的嚴(yán)重腹瀉是由細(xì)菌毒素的產(chǎn)生導(dǎo)致的,盡管使用抗生素是當(dāng)前的標(biāo)準(zhǔn)治療手段,仍有20%-30%的患者會出現(xiàn)反復(fù)感染,僅依靠抗生素治療復(fù)發(fā)型艱難梭菌感染(rCDI)復(fù)發(fā)率高,還存在住院和死亡風(fēng)險。該研究通過對VOS(原 SER-109)的三項臨床試驗數(shù)據(jù)進(jìn)行分析,發(fā)現(xiàn)VOS顯著改變了患者腸道微生物組成,顯著增加了厚壁菌門物種,并降低了艱難梭菌及機(jī)會致病菌豐度,同時調(diào)節(jié)膽汁酸和脂肪酸代謝產(chǎn)物,為rCDI的臨床治療提供了新的理論依據(jù)和治療策略。
1、通過臨床試驗分析發(fā)現(xiàn),在III期高劑量試驗中,VOS治療組8周復(fù)發(fā)率僅12%,顯著低于安慰劑組(40%)。
2、通過微生物組分析發(fā)現(xiàn),III期高劑量VOS的植入率顯著高于安慰劑組,VOS組厚壁菌門豐度顯著升高,變形菌門豐度顯著降低,且艱難梭菌及條件致病菌的豐度也顯著低于安慰劑組。
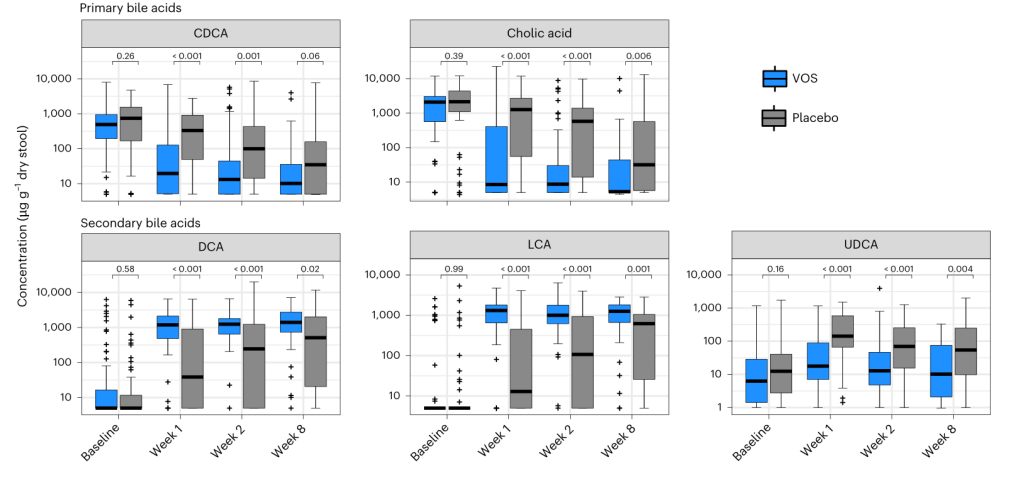
3、通過靶向膽汁酸檢測發(fā)現(xiàn),VOS 治療后,初級膽汁酸(膽酸、鵝去氧膽酸)濃度顯著降低,次級膽汁酸(脫氧膽酸、石膽酸)濃度顯著升高。進(jìn)一步通過脂肪酸檢測發(fā)現(xiàn),VOS顯著提高了短鏈及中鏈脂肪酸(如丁酸、戊酸和己酸)的水平。
4、體外實驗進(jìn)一步證實丁酸、戊酸和己酸能抑制艱難梭菌生長,且抑制效果隨碳鏈長度增加而增強(qiáng)。
參考文獻(xiàn):Bryant JA, Vuli? M, Walsh EA, et al. The impact of an oral purified microbiome therapeutic on the gastrointestinal microbiome. Nature Medicine. 2026
#3
Gut | P. excrementihominis通過致病性NETosis激活加劇實驗性結(jié)腸炎及結(jié)腸炎相關(guān)結(jié)直腸癌

腸道菌群失調(diào)是潰瘍性結(jié)腸炎(UC)及結(jié)腸炎相關(guān)結(jié)直腸癌(CAC)發(fā)生發(fā)展的重要驅(qū)動因素,然而關(guān)鍵致病菌及其具體作用機(jī)制尚未完全闡明。本研究發(fā)現(xiàn),一種在UC患者中顯著富集的β-變形菌綱細(xì)菌——Parasutterella excrementihominis(P. excrementihominis)可通過其代謝產(chǎn)物琥珀酸(Suc)和6-羥基己酸(6-HHA)激活中性粒細(xì)胞胞外誘捕網(wǎng)(NETs)的形成,從而加劇結(jié)腸慢性炎癥并促進(jìn)腫瘤發(fā)生。該研究揭示了細(xì)菌代謝產(chǎn)物在炎癥相關(guān)結(jié)直腸癌中的作用機(jī)制。
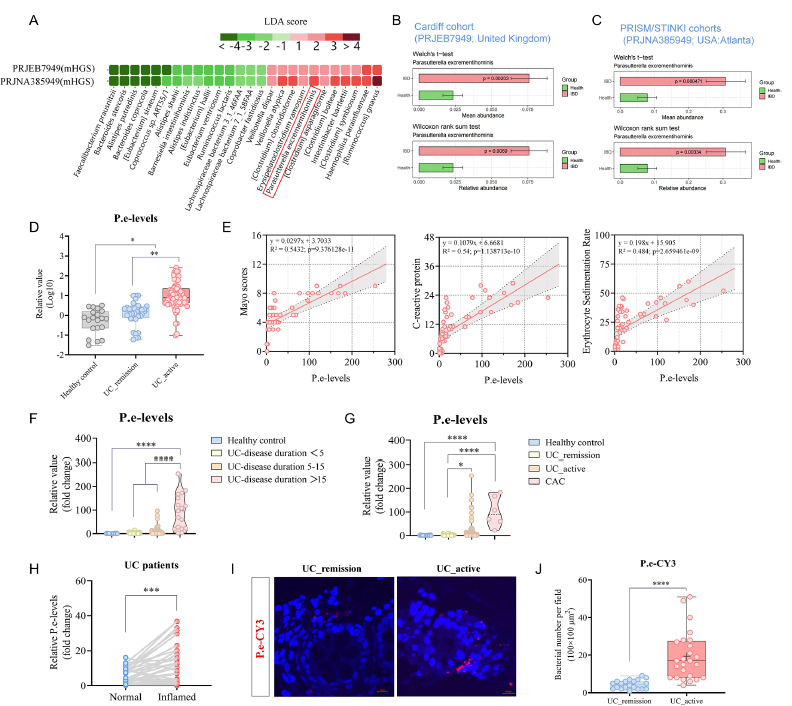
1、首先,通過對GMrepo數(shù)據(jù)庫的分析以及115例UC患者糞便樣本的qPCR檢測,發(fā)現(xiàn)P. excrementihominis在活動期UC患者中的豐度顯著升高,且其水平與Mayo評分呈正相關(guān)。在DSS誘導(dǎo)的小鼠結(jié)腸炎模型中進(jìn)一步驗證,僅活菌及其培養(yǎng)上清能夠加重結(jié)腸炎癥并促進(jìn)中性粒細(xì)胞浸潤;利用Ly6G中和抗體耗竭中性粒細(xì)胞或采用PADI4基因敲除小鼠進(jìn)行實驗,表明該菌主要通過激活NETosis途徑加劇腸道炎癥。
2、其次,通過多組學(xué)技術(shù)闡明P. excrementihominis的代謝調(diào)控機(jī)制。對無菌小鼠進(jìn)行單菌定植后,利用RNA測序和非靶向代謝組學(xué)分析發(fā)現(xiàn),該菌顯著增強(qiáng)宿主的碳水化合物代謝能力,導(dǎo)致其特異性代謝產(chǎn)物琥珀酸(Suc)和6-羥基己酸(6-HHA)在糞便、血清及細(xì)菌上清中顯著積累。體外實驗證實,這兩種代謝物能夠選擇性激活經(jīng)LPS預(yù)刺激的中性粒細(xì)胞,上調(diào)NETs相關(guān)基因表達(dá),并通過分子對接驗證其與GPR84/SUCNR1受體的結(jié)合,進(jìn)而促進(jìn)NLRP3炎癥小體活化及GSDMD切割,最終驅(qū)動NETs形成。
3、進(jìn)一步地,在AOM/DSS誘導(dǎo)的CAC模型中,灌胃P. excrementihominis或直接補(bǔ)充Suc與6-HHA均顯著增加結(jié)腸腫瘤負(fù)荷并上調(diào)NETs標(biāo)志物表達(dá);而在中性粒細(xì)胞特異性GSDMD缺失小鼠中,上述促腫瘤效應(yīng)明顯減弱,證實GSDMD依賴性NETosis在代謝物驅(qū)動的腫瘤進(jìn)展中發(fā)揮關(guān)鍵作用。
4、最后,通過衰老模型與飲食干預(yù)實驗,揭示了環(huán)境因素對P. excrementihominis定植及其致病性的調(diào)控作用。通過對老年與年輕小鼠進(jìn)行16S rRNA測序分析,發(fā)現(xiàn)老年小鼠腸道中P. excrementihominis豐度顯著升高;進(jìn)一步的糞菌移植實驗證實,老年供體菌群可加速年輕受體小鼠的CAC發(fā)展。飲食干預(yù)實驗發(fā)現(xiàn),高碳水化合物飲食促進(jìn)P. excrementihominis的定植與擴(kuò)張,而生酮飲食則能有效抑制其生長,為通過膳食策略靶向該致病菌提供了實驗依據(jù)。
參考文獻(xiàn):Tan H, Huang L, Wang J, et al.Parasutterella excrementihominis exacerbates experimental colitis and colitis-associated colorectal cancer via pathogenic NETosis activation. Gut. 2025
#4
Gut | 腸道細(xì)菌產(chǎn)生的次級膽汁酸促進(jìn)西方飲食相關(guān)的結(jié)直腸癌發(fā)生

腸道微生物群在西方飲食相關(guān)的結(jié)直腸癌(CRC)發(fā)生發(fā)展中具有重要作用,但特定菌群及其代謝產(chǎn)物在其中的因果機(jī)制仍不明確。本研究通過多物種模型和干預(yù)實驗證實,腸道細(xì)菌經(jīng)7α-脫羥基化(7αDH)產(chǎn)生的次級膽汁酸尤其是脫氧膽(DCA)是西方飲食促進(jìn)CRC的關(guān)鍵介質(zhì),揭示了從飲食、微生物代謝到腫瘤發(fā)生的因果鏈條,為基于菌群干預(yù)的CRC預(yù)防提供了新思路。
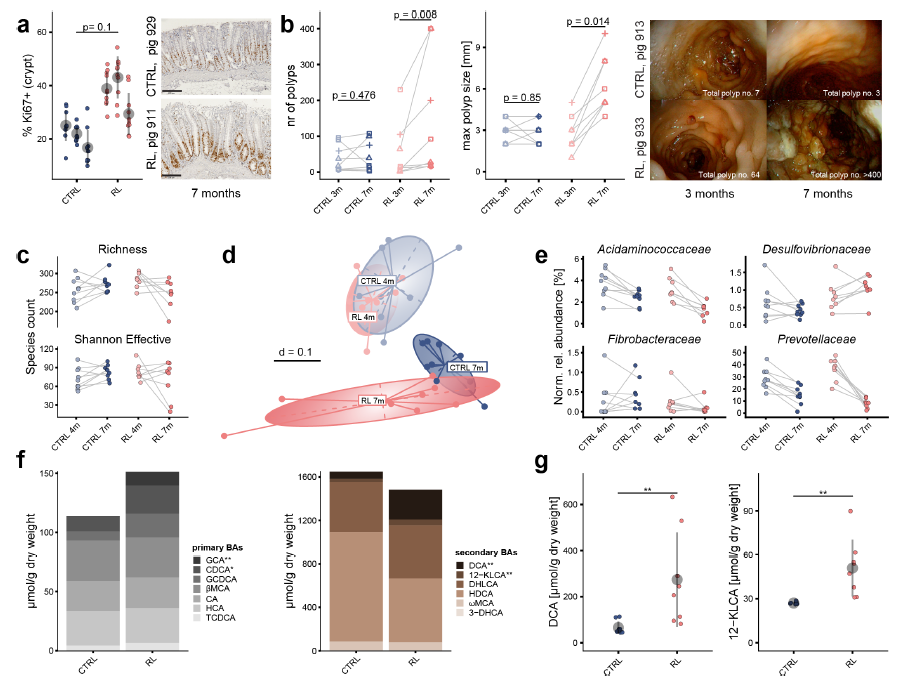
1、首先,對攜帶APC基因突變的轉(zhuǎn)基因豬模型進(jìn)行為期3個月的飲食干預(yù)。結(jié)果顯示,高紅肉與豬油飲食顯著增加結(jié)腸息肉數(shù)量和大小,伴隨上皮細(xì)胞增殖加劇,糞便中DCA等次級膽汁酸水平也明顯升高。在此基礎(chǔ)上,使用膽汁酸螯合劑考來替蘭(COL)處理發(fā)現(xiàn),COL能有效抑制飲食誘導(dǎo)的上皮細(xì)胞增殖,減少進(jìn)展性息肉比例,并促進(jìn)膽汁酸隨糞便排出,說明通過阻斷膽汁酸吸收可緩解西方飲食的促瘤作用,初步確立了膽汁酸在CRC進(jìn)展中的功能角色。
2、進(jìn)一步通過分析多個人群隊列的宏基因組數(shù)據(jù),鑒定出與CRC密切相關(guān)的特定7αDH+細(xì)菌。宏基因組操作分類單元(mOTU)分析表明,Clostridium scindens和C. hylomona的bai基因簇在CRC患者糞便中富集。隨后在定植簡化菌群(BACOMI)的無菌小鼠模型中證實,引入C. scindens可誘導(dǎo)DCA生成,激活結(jié)腸上皮中與增殖、分化相關(guān)的信號通路,并顯著增加Ki67+細(xì)胞數(shù)量,說明特定菌株可通過產(chǎn)生DCA直接驅(qū)動上皮增殖。
3、為在體內(nèi)驗證7αDH+菌對腫瘤形成的直接影響,在化學(xué)誘導(dǎo)和遺傳誘導(dǎo)的小鼠CRC模型中進(jìn)行實驗。結(jié)果顯示,定植C. scindens或E. muris的小鼠結(jié)腸中DCA水平升高,腫瘤數(shù)量(尤其小型腫瘤)顯著增加。而使用7αDH活性缺失的F. contorta突變菌株則無法誘導(dǎo)DCA產(chǎn)生或增加腫瘤負(fù)荷,表明細(xì)菌的7αDH活性是結(jié)腸腫瘤發(fā)生的關(guān)鍵驅(qū)動因素。
4、最后,利用人結(jié)腸類器官模型在體外驗證DCA的直接促增殖作用。類器官暴露于野生型F. contorta(含DCA)的培養(yǎng)上清后,Ki67+細(xì)胞比例顯著上升,而突變菌株上清無此效應(yīng),說明細(xì)菌來源的DCA可直接促進(jìn)人結(jié)腸上皮細(xì)胞增殖,為其促瘤機(jī)制提供了直接證據(jù)。
參考文獻(xiàn):Osswald A, Wortmann E, Wylensek D, et al. Secondary bile acid production by gut bacteria promotes Western diet-associated colorectal cancer. Gut. 2025
#5
Nature Comunications | 化療誘導(dǎo)的腸道菌群失調(diào)與吲哚-3-丙酸重塑骨髓造血,促進(jìn)抗轉(zhuǎn)移狀態(tài)

結(jié)直腸癌術(shù)后化療雖有獲益,但30-50%患者仍出現(xiàn)肝轉(zhuǎn)移。臨床數(shù)據(jù)顯示,圍手術(shù)期抗生素使用會縮短無病生存期,暗示腸道菌群可能左右化療的遠(yuǎn)期效果,但化療所致腸黏膜炎如何經(jīng)菌群調(diào)控轉(zhuǎn)移,其機(jī)制尚不清楚。基于此本研究聚焦FOLFOX方案(氟尿嘧啶+奧沙利鉑),提出"化療記憶"假說:腸黏膜損傷通過長期改變菌群代謝,系統(tǒng)性重塑免疫微環(huán)境以抑制轉(zhuǎn)移。團(tuán)隊利用小鼠模型、多組學(xué)及臨床樣本,旨在闡明菌群-代謝-免疫軸在化療防轉(zhuǎn)移中的作用,為臨床合理用藥和開發(fā)新型佐劑提供理論支撐。
1、16S rRNA擴(kuò)增子測序+PICRUSt2:FO化療后Firmicutes門及Clostridia綱擴(kuò)張,色氨酸代謝通路顯著富集;門靜脈血IPA(吲哚丙酸)升高>10倍且持續(xù)10天以上,抗生素清除菌群后IPA升高消失,證實IPA來源于化療誘導(dǎo)的菌群失調(diào)。
2、LC-MS代謝組:非靶向代謝組檢出95種上調(diào)代謝物中IPA最顯著;靶向定量顯示FO組IPA超對照組10倍;臨床隊列(n=14)中64%CRC患者化療后IPA升高,且與單核細(xì)胞計數(shù)顯著負(fù)相關(guān)(r=-0.59,P=0.002)。
3、流式細(xì)胞術(shù)+CyTOF成像:IPA使Ly6Chigh CCR2+免疫抑制性單核細(xì)胞減少40-50%,MHCII+髓系細(xì)胞增加;Th1(T-bet+IFN-γ+)效應(yīng)細(xì)胞比例上升,Treg顯著減少;CD8+T細(xì)胞與Th1空間共定位增強(qiáng),與Treg相互作用消失。
4、骨髓造血功能研究(CFU+RNA-seq+SCENIC)發(fā)現(xiàn):IPA直接抑制骨髓CFU形成,促使共同髓系祖細(xì)胞(CMP)向巨噬細(xì)胞分化而非Ly6Chigh單核細(xì)胞;激活Rbpj/Irf8/Mafb巨噬細(xì)胞分化網(wǎng)絡(luò),抑制未成熟髓系特征基因(Ms4a3等)。
5、功能驗證與臨床轉(zhuǎn)化:CD4+T細(xì)胞耗竭完全消除IPA的抗轉(zhuǎn)移效應(yīng);IPA聯(lián)合化療顯著降低腫瘤負(fù)荷(P<0.0001);高單核細(xì)胞(>0.8 G/L)預(yù)示CRC患者較差總生存期(P<0.0001),提示IPA可作為化療佐劑通過重編程髓系造血增強(qiáng)抗腫瘤免疫。
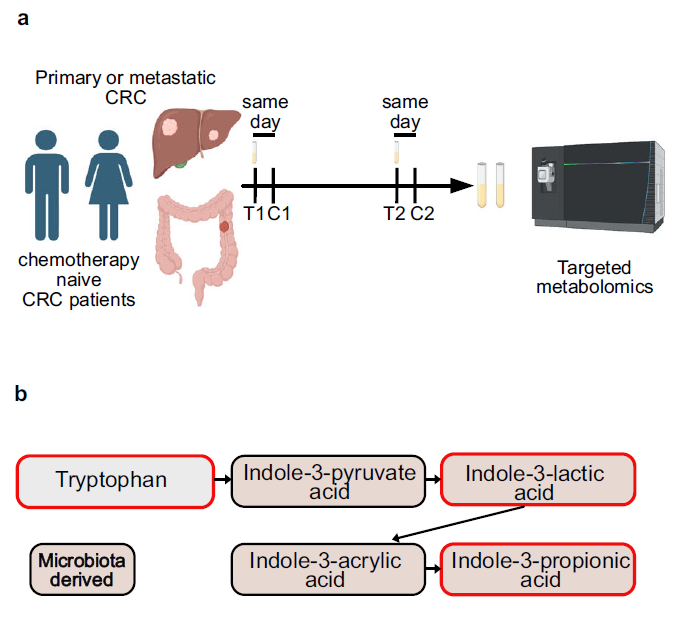
參考文獻(xiàn):Bersier, L., Lorenzo-Martin, L. F., Chiang, Y.-H., et al. Chemotherapy-driven intestinal dysbiosis and indole-3-propionic acid rewire myelopoiesis to promote a metastasis-refractory state. Nature Communications. 2025
#6
Nature Comunications | 腸道微生物組預(yù)測糖尿病前期個體對膳食纖維干預(yù)的個性化反應(yīng)

全球約7.2億糖尿病前期人群,65%將進(jìn)展為2型糖尿病,但現(xiàn)有空腹血糖、HbA1c等診斷標(biāo)準(zhǔn)無法反映胰島素抵抗與β細(xì)胞功能的異質(zhì)性,導(dǎo)致干預(yù)效果差異大。膳食纖維被證實可通過腸道菌群發(fā)酵產(chǎn)生短鏈脂肪酸,提升GLP-1、改善胰島素分泌,然而不同個體對高纖維飲食的血糖反應(yīng)不一,菌群特征可能是關(guān)鍵決定因素。既往研究樣本小、缺乏隨機(jī)對照證據(jù),難以建立臨床可用的菌群預(yù)測模型。為此,作者開展多中心隨機(jī)開放標(biāo)簽試驗,納入802例糖尿病前期受試者,先以年齡、BMI、HbA1c、HOMA2-IR與HOMA2-B等多維指標(biāo)重新聚類為4個代謝亞群,再隨機(jī)給予膳食纖維補(bǔ)充或常規(guī)教育干預(yù)6個月,旨在明確菌群基線特征是否決定纖維干預(yù)的血糖獲益,并構(gòu)建可推廣的個性化預(yù)測模型,為糖尿病精準(zhǔn)預(yù)防提供依據(jù)。
1、16S rRNA擴(kuò)增子測序:將802例樣本劃分為4個代謝亞群,Cluster-3/4的菌群結(jié)構(gòu)、α-多樣性及共豐度網(wǎng)絡(luò)與Cluster-1/2顯著不同;鑒定49個差異 ASV,獲益組(Cluster-3/4)干預(yù)后Guild-2(產(chǎn)丁酸/乙酸)/Guild-1(耐藥)比值升高,Parabacteroides distasonis等9個纖維響應(yīng)菌顯著富集。
2、PICRUSt2功能預(yù)測:發(fā)現(xiàn)Guild-2富集碳水化合物利用及SCFA生成基因;Guild-1富集藥物耐藥與細(xì)菌毒力基因,證實兩派菌群功能對立。
3、血清非靶向LC-MS代謝組:Cluster-3/4干預(yù)后49–61種代謝物顯著改變,芳香族及支鏈氨基酸代謝通路下調(diào),與菌群SCFA產(chǎn)生同步增強(qiáng)。
4、LightGBM機(jī)器學(xué)習(xí)+SHAP 解釋:以基線44個ASV建立預(yù)測模型,ROC-AUC達(dá)0.81;計算微生物-纖維評分(MFS),cut-off以17/25為截點(diǎn) 在訓(xùn)練集與兩個獨(dú)立驗證隊列均以99–100%準(zhǔn)確率區(qū)分高/低響應(yīng)者。
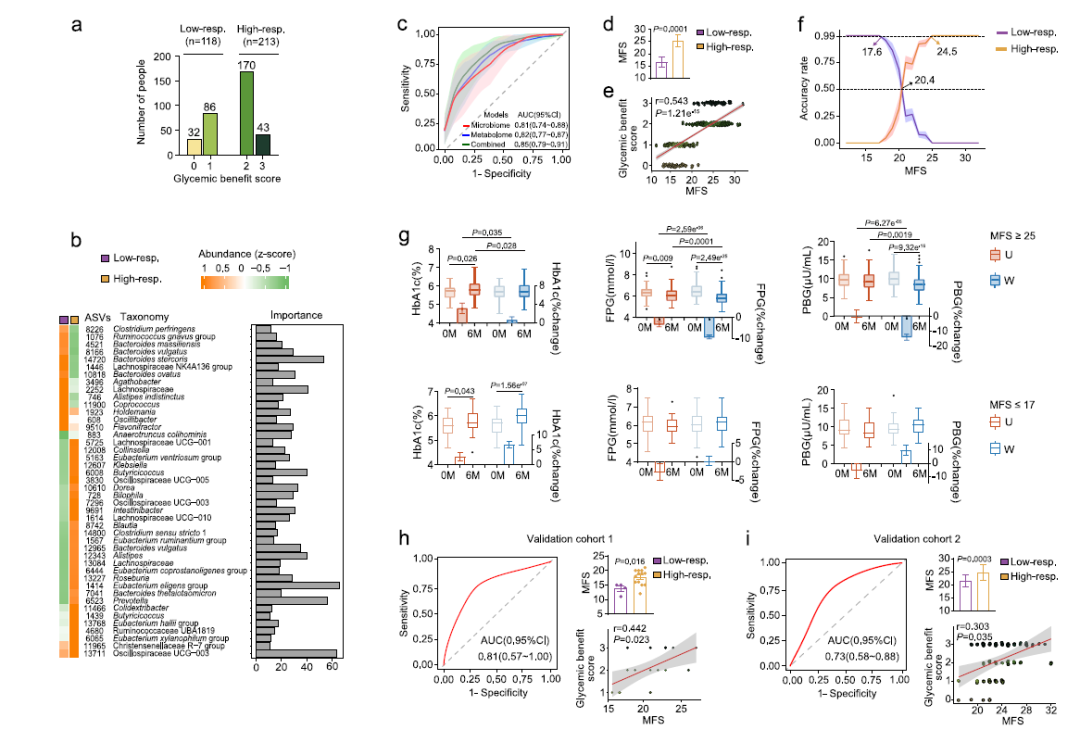
參考文獻(xiàn):Song, D., Feng, G., Ma, Y., et al. Gut microbiome predicts personalized responses to dietary fiber in prediabetes: A randomized, open-label trial. Nature Communications. 2025
#7
Cell Host & Microbe | 腸道微生物氨基酸代謝通過調(diào)控CD8?T細(xì)胞功能影響癌癥進(jìn)展及抗腫瘤免疫力

腸道菌群與癌癥進(jìn)展及免疫治療效果密切相關(guān),但具體機(jī)制尚不明確。結(jié)直腸癌患者的腸道微生物氨基酸代謝與健康人群存在顯著差異,腸道微生物對腸道氨基酸的消耗會影響宿主氨基酸穩(wěn)態(tài),進(jìn)而可能調(diào)控癌癥發(fā)生發(fā)展。本研究旨在探究腸道微生物中調(diào)控氨基酸水平的通路對結(jié)直腸癌進(jìn)展的影響,明確關(guān)鍵微生物基因、膳食氨基酸與抗腫瘤免疫之間的關(guān)聯(lián),為癌癥治療提供新的靶點(diǎn)。
1、動物模型構(gòu)建與飲食干預(yù):高氨基酸飲食在無菌(GF)小鼠中顯著促進(jìn)腫瘤生長,但在特定病原體(SPF)小鼠中該效應(yīng)被削弱。
2、人糞便微生物移植給抗生素處理小鼠:16S rRNA測序分析發(fā)現(xiàn),被移植氨基酸高消耗效率微生物的小鼠,血清和糞便氨基酸水平更低,腫瘤負(fù)擔(dān)顯著高于低消耗效率組。
3、bo-ansB基因的功能驗證與機(jī)制探究:擬桿菌屬的bo-ansB基因核心功能是編碼天冬酰胺酶,可消耗腸道及腫瘤微環(huán)境中的天冬酰胺(Asn),導(dǎo)致腫瘤浸潤C(jī)D8?T細(xì)胞的干細(xì)胞樣特性和效應(yīng)功能受損,腫瘤進(jìn)展加快。
4、結(jié)直腸癌模型與人類隊列分析:結(jié)果顯示,Δbo-ansB(敲除bo-ansB基因)定植的結(jié)腸癌小鼠腫瘤負(fù)擔(dān)減輕、CD8+T細(xì)胞功能增強(qiáng)。人類中ansB、argD等微生物氨基酸消耗基因豐度與結(jié)直腸癌進(jìn)展相關(guān),ansB豐度與糞便Asn水平呈負(fù)相關(guān)。
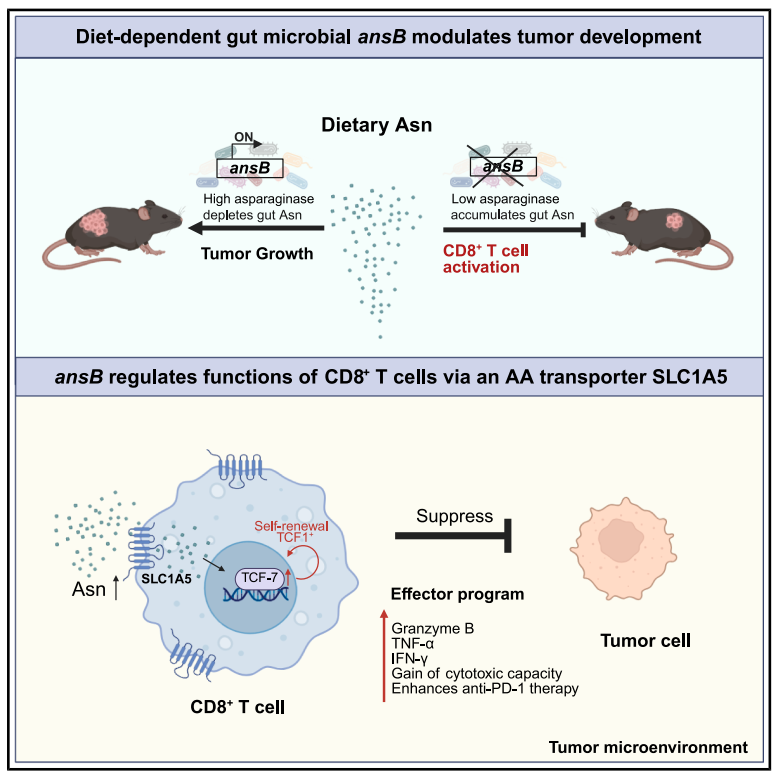
參考文獻(xiàn):Qiao S, et al. Microbiota utilization of intestinal amino acids modulates cancer progression and anticancer immunity. Cell Host Microbe. 2026
#8
Advanced Science | 結(jié)直腸癌細(xì)胞的武器:RNF32與SPP1+巨噬細(xì)胞結(jié)合以促進(jìn)肝臟轉(zhuǎn)移,以吲哚-3-乙酸為靶點(diǎn)

結(jié)直腸癌(CRC)是全球高發(fā)癌癥,肝轉(zhuǎn)移是其主要致死原因,50%-60%的患者會發(fā)生轉(zhuǎn)移,且近80%為不可切除肝轉(zhuǎn)移,預(yù)后極差。基因治療雖具潛力,但受靶點(diǎn)篩選等問題限制,臨床轉(zhuǎn)化受阻。RNF32作為RING指蛋白家族的E3泛素連接酶,已被發(fā)現(xiàn)與部分腫瘤進(jìn)展相關(guān),可能促進(jìn)結(jié)直腸癌增殖和巨噬細(xì)胞極化,但它在CRC肝轉(zhuǎn)移中的具體功能、分子機(jī)制及靶向藥物仍不明確。
1、基因篩選與驗證:結(jié)合多數(shù)據(jù)庫驗證,確定RNF32為結(jié)直腸癌肝轉(zhuǎn)移關(guān)鍵驅(qū)動基因,其高表達(dá)與患者不良預(yù)后相關(guān)。
2、體內(nèi)外功能驗證:RNF32可促進(jìn)結(jié)直腸癌細(xì)胞增殖、上皮-間質(zhì)轉(zhuǎn)化(EMT)及體內(nèi)腫瘤生長和肝轉(zhuǎn)移。
3、分子機(jī)制探究:采用RNA測序、蛋白相互作用實驗、泛素化實驗等,發(fā)現(xiàn)RNF32通過△2結(jié)構(gòu)域結(jié)合GSK3β的D3結(jié)構(gòu)域,催化其K60位點(diǎn)K48連接泛素化降解,激活Wnt/β-連環(huán)蛋白通路驅(qū)動EMT。
4、腫瘤微環(huán)境調(diào)控:經(jīng)質(zhì)譜流式、巨噬細(xì)胞耗竭、條件培養(yǎng)基共培養(yǎng)等實驗,揭示RNF32通過Wnt通路上調(diào)CCL2,激活巨噬細(xì)胞CCR2/FABP1/PPARG軸誘導(dǎo)SPP1表達(dá),SPP1+巨噬細(xì)胞與腫瘤細(xì)胞CD44結(jié)合增強(qiáng)干細(xì)胞特性,重塑免疫抑制微環(huán)境。
5、藥物篩選與驗證:通過虛擬篩選、分子對接及微量熱泳動(MST)驗證,發(fā)現(xiàn)吲哚-3-乙酸(IAA)為RNF32高親和力抑制劑;體內(nèi)外實驗證實IAA可抑制結(jié)直腸癌細(xì)胞增殖、腫瘤生長及肝轉(zhuǎn)移,逆轉(zhuǎn)免疫抑制,且生物安全性良好。
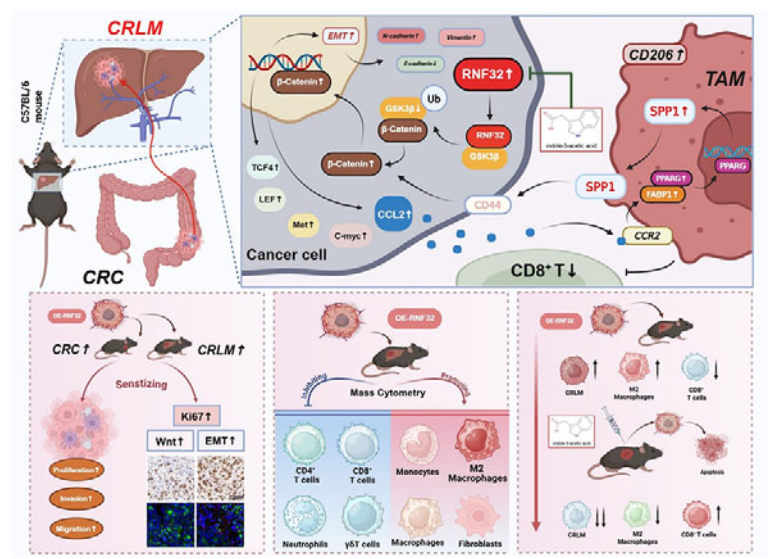
參考文獻(xiàn):Wang H, et al. Colorectal Cancer Cell's Weapon: RNF32 Engages SPP1+ Macrophages to Foster Liver Metastasis, Targeted by Indole-3-Acetic Acid. Adv Sci (Weinh). 2025
