2025年7月7日,美國國立衛(wèi)生研究院(NIH)在與美國食品藥品監(jiān)督管理局(FDA)聯(lián)合舉辦的研討會上宣布了一項歷史性決策:不再資助僅依賴動物試驗的新研究項目,所有新的NIH資助機會都應(yīng)納入新方法(NAMs)的考量。這一決策標志著跨越近一個世紀的動物試驗主導時代迎來終結(jié)。

NIH負責項目協(xié)調(diào)、規(guī)劃與戰(zhàn)略事務(wù)的副主任Nicole Kleinstreuer博士著重強調(diào),所謂的“新方法”(NAMs),指從計算機建模、人工智能,到器官芯片與類器官技術(shù)等前沿動物替代技術(shù)。未來,NIH的自主機會將會向相關(guān)領(lǐng)域著重偏移。
與此同時,NIH將不再專門尋求動物模型的提案。不過該政策并非完全禁止動物試驗,而是打破了“純動物試驗”的單一模式:即便研究仍以動物試驗為主體,只要包含少量新方法學的試驗內(nèi)容,即可滿足資助要求。這種靈活設(shè)計為科研體系的平穩(wěn)過渡預留了充足空間。
此前2022年,美國FDA已經(jīng)發(fā)布了現(xiàn)代化法案2.0,大力推動NAMs的普及。2024年10月7日,F(xiàn)DA再度發(fā)布相關(guān)報告著重強調(diào)了類器官和器官芯片作為新型動物替代模型的意義。今年4月10日,F(xiàn)DA再次宣布將“逐漸取消單克隆抗體及其他藥物的動物試驗要求”。4月29日,NIH啟動新倡議,成立研究創(chuàng)新、驗證與應(yīng)用辦公室,推動類器官、計算模型等非動物技術(shù)的開發(fā)與應(yīng)用。而本次NIH與FDA兩大權(quán)威機構(gòu)的聯(lián)動,更是進一步顯示出美國在推動研究范式轉(zhuǎn)型升級上的一致共識和堅定決心。

圖:4月10日,F(xiàn)DA宣布取消動物試驗要求
01 轉(zhuǎn)折點背后的多重推力
長期以來,動物模型面臨著培養(yǎng)周期長、成本昂貴、倫理限制以及低轉(zhuǎn)化率等問題。基因修飾的小鼠等動物模型需要6-9周齡(1-2個月),猴子則更長,需要1-2年,臨床試驗申請中的動物毒性試驗期限同樣長達1-6個月。此外,因缺乏符合實驗標準的模型,近年來實驗動物的造價一路走高,食蟹猴的單價已經(jīng)從2020.年的3萬元一路上漲至2025年的約12.2萬元/只(中檢院采購單價)。而動物保護組織如善待動物組織(PETA)長期呼吁的實驗倫理問題也引發(fā)了公眾的討論和促使科研機構(gòu)審視實驗必要性與合理性。
最令人震驚的數(shù)據(jù)來自FDA的統(tǒng)計。超過90%通過動物試驗的藥物最終因在人體中缺乏安全性或有效性而失敗。這一數(shù)字在腫瘤藥物研發(fā)領(lǐng)域尤為突出,大量動物有效的藥物在人體試驗中無效,延長了研發(fā)周期和患者等待時間。以神經(jīng)退行性疾病和腫瘤為例,十余年來多種藥物在鼠、猴等模型中效果顯著,但在早期或晚期臨床均以失敗告終。究其根本,動物模型與人類生物系統(tǒng)存在遺傳多樣性和藥物基因組差異,難以滿足精準醫(yī)學時代的研究需求。
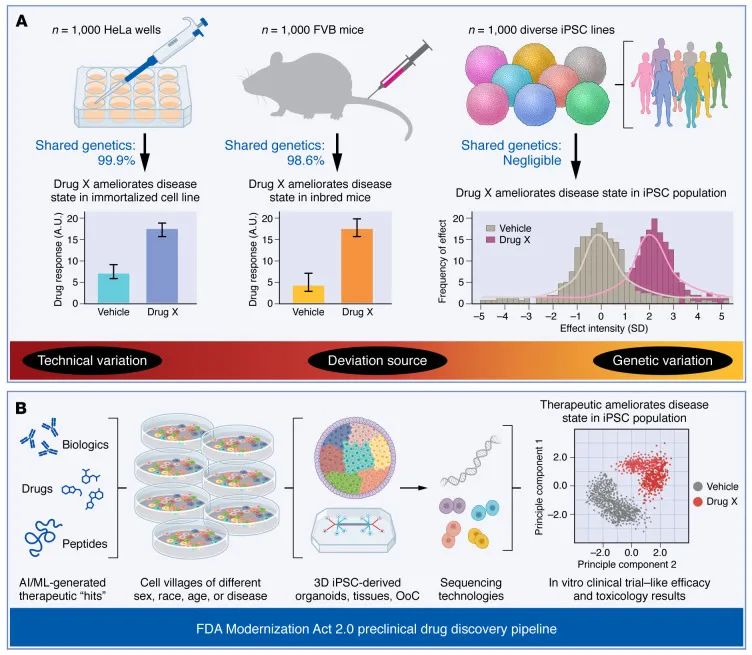
圖:動物模型缺乏基因多樣性且與人類間存在表型差異[3]
02 類器官何以成為新的支點?
在如此臨床失利、轉(zhuǎn)化困難的前提下,人源類器官和多細胞互作平臺已成為提高轉(zhuǎn)化成功率的關(guān)鍵路徑 。事實上,不止FDA,歐洲方面也早已建立了歐盟“地平線2020”計劃,將大量資源向類器官技術(shù)在組織工程、再生醫(yī)學和個性化醫(yī)療中的研究傾斜。
類器官技術(shù)通過干細胞三維自組裝方法再現(xiàn)組織微結(jié)構(gòu),并在一定程度上模擬“疾病—反應(yīng)—調(diào)控”鏈條。相對于動物模型,類器官技術(shù)體現(xiàn)出了顯著的成本優(yōu)勢。歐洲器官芯片協(xié)會測算顯示,在肝毒性研究中器官芯片的成本僅為動物實驗的10%。與此同時,類器官的高通量篩選能力使研究人員能夠同時測試數(shù)百種化合物,大幅提高研發(fā)效率。
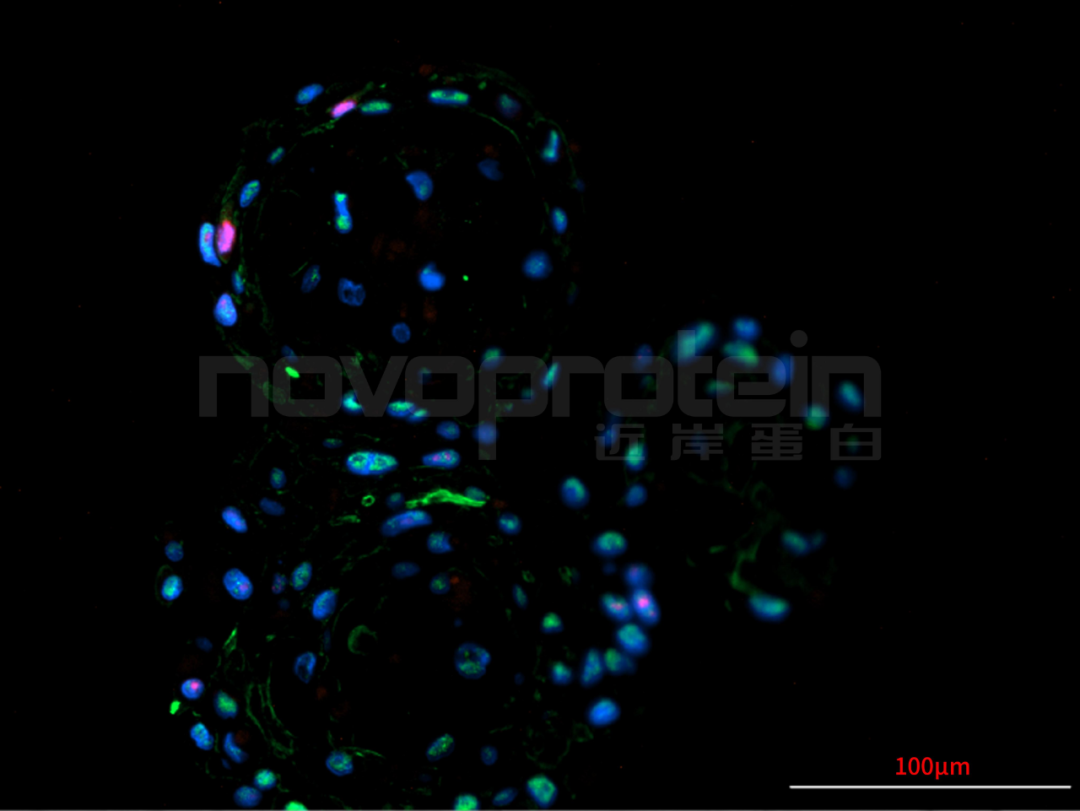
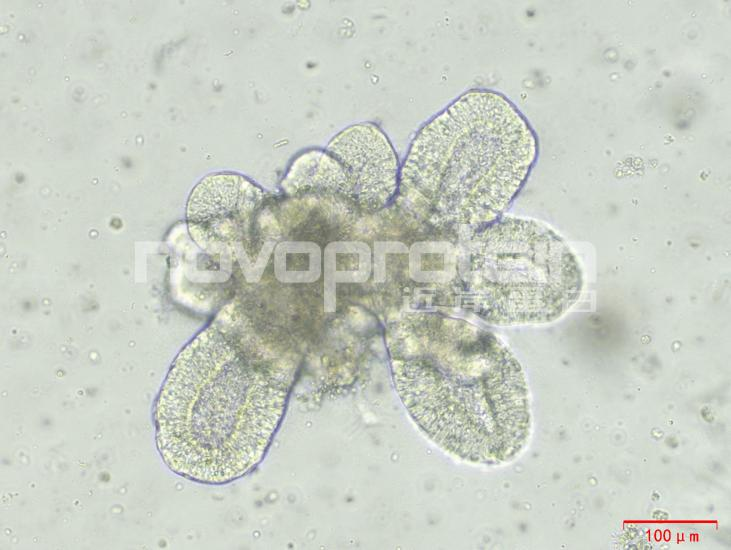
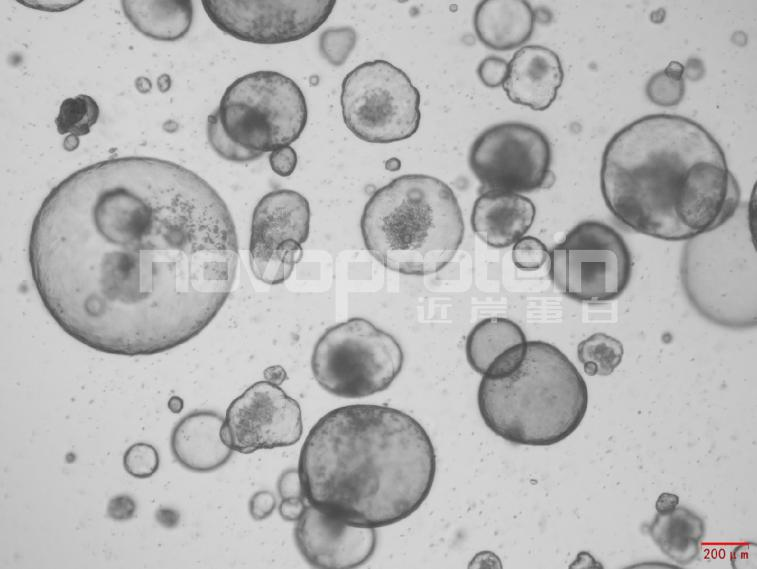
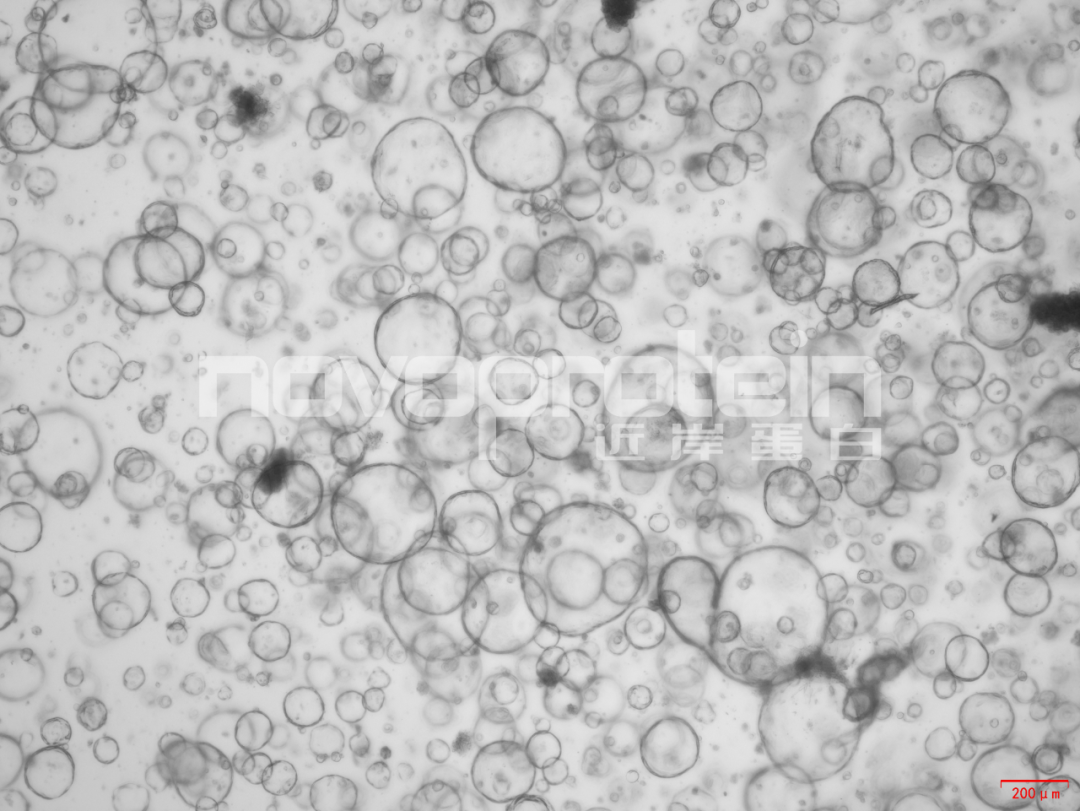
圖:經(jīng)近岸蛋白細胞因子驗證培養(yǎng)的類器官(乳腺癌類器官、ipsc來源的人小腸類器官、小鼠胃類器官及小鼠膽管類器官)
患者來源的類器官(PDO),尤其是腫瘤類器官是目前最具臨床應(yīng)用價值的方向。其保留了患者來源的異質(zhì)性,因此在預測化療藥物反應(yīng)方面展現(xiàn)出獨特優(yōu)勢。這一技術(shù)對晚期轉(zhuǎn)移、出現(xiàn)耐藥的患者具有極大的價值。
目前類器官的三大挑戰(zhàn):血管化缺失、神經(jīng)支配不足和免疫微環(huán)境模擬不完整也正在被迅速攻克。尤其在在5-6月,頂刊Science、Nature與Cell與接連刊發(fā)多篇論文,分別報道了僅需5天的功能性血管類器官培養(yǎng)方案、可兼容心臟及肝臟的類器官血管化普適方案、以及第一個血管化功能肺類器官培養(yǎng)方案等。從而將類器官的血管化向前推進了一大步,顯著拓寬了類器官的應(yīng)用范圍與臨床精確度。
根據(jù)Grand View Research,2024年全球類器官市場規(guī)模約為8.04億美元,預計到2030年將達到27.156 億美元,2025年至2030年的復合年增長率為22.8%,凸顯出行業(yè)作為戰(zhàn)略新興產(chǎn)業(yè)的持續(xù)增長潛力。同在2025年,ARK Invest基金年度報告《Big Ideas 2025》中也特別提到,類器官/器官芯片和人工智能的結(jié)合能夠助力創(chuàng)新藥物的高效研發(fā),幫助藥企度過“研發(fā)死亡谷”。
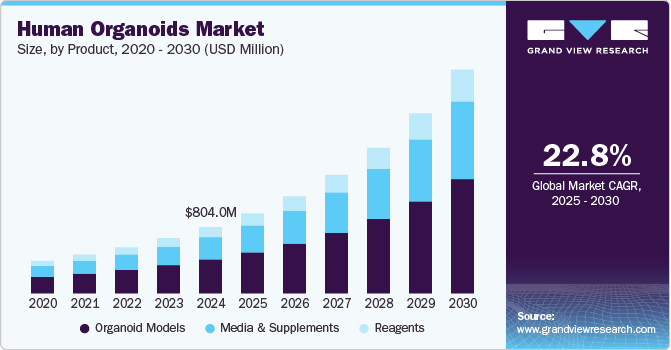
圖:類器官市場規(guī)模走勢
03 行業(yè)趨勢與現(xiàn)實效益
為了大力推動非動物研究方法NAMs,NIH在2025年設(shè)立了ORIVA(Office of Research Innovation, Validation, and Application,研究創(chuàng)新、驗證與應(yīng)用辦公室)。據(jù)悉,ORIVA的核心目標是擴大對類器官、器官芯片、計算建模及真實世界數(shù)據(jù)等非動物技術(shù)的資助與培訓,提升這些方法的轉(zhuǎn)化效率,并逐步替代動物實驗。其中,類器官和器官芯片同一定義為“微生理系統(tǒng)”。ORIVA將推動“類器官優(yōu)先 + 動物實驗精準化”的新模式,例如在抗癌藥物研發(fā)中,先使用類器官高通量篩選,再輔以精簡的動物驗證。
ORIVA的介入,使得研究項目評估不再一味參考“是否有動物桿實驗”,而轉(zhuǎn)向“是否具備人類生物學相關(guān)性、是否具備可重復性”。這意味著,類器官研究者不僅獲得政策紅利,還得到標準化評估與多機構(gòu)協(xié)同的機會 。
業(yè)內(nèi)觀察人士指出,美國每年約 48億美元資助落在動物研究上,此次重定方向?qū)⑶袑嵏淖兛蒲匈Y源分配結(jié)構(gòu),同時為以類器官為核心的新技術(shù)公司提供市場機遇。FAANG式的制藥創(chuàng)新團隊將逐步由“小鼠優(yōu)先”向“人相關(guān)優(yōu)先”轉(zhuǎn)型。
正如CN Bio 的 CTO Tomasz Kostrzewski 所言:“動物研究不應(yīng)再是默認選項”,新藥研發(fā)必須整合人源模型、計算模擬和真實健康數(shù)據(jù)。這意味著機構(gòu)與實驗室必須重構(gòu)培訓、人才投入與資金預算結(jié)構(gòu)。
本次NIH與FDA協(xié)同推動,加速類器官從實驗室到臨床的轉(zhuǎn)化。藥企(如輝瑞、默克)嘗試用類器官進行早期毒性篩選。未來探索將類器官數(shù)據(jù)納入新藥申報材料,縮短周期,降低成本。
近岸蛋白相關(guān)產(chǎn)品
近岸蛋白依靠專業(yè)的研發(fā)團隊,精心打造類器官驗證平臺,可提供一系列經(jīng)驗證、高活性、高穩(wěn)定性的類器官培養(yǎng)產(chǎn)品,助您高效快速開展類器官實驗!
NovoMatrix-經(jīng)類器官培養(yǎng)驗證的基質(zhì)膠
近岸蛋白提供經(jīng)類器官/干細胞培養(yǎng)驗證的系列NovoMatrix基質(zhì)膠,產(chǎn)品批次穩(wěn)定可控,讓您的類器官/干細胞培養(yǎng)更可控!
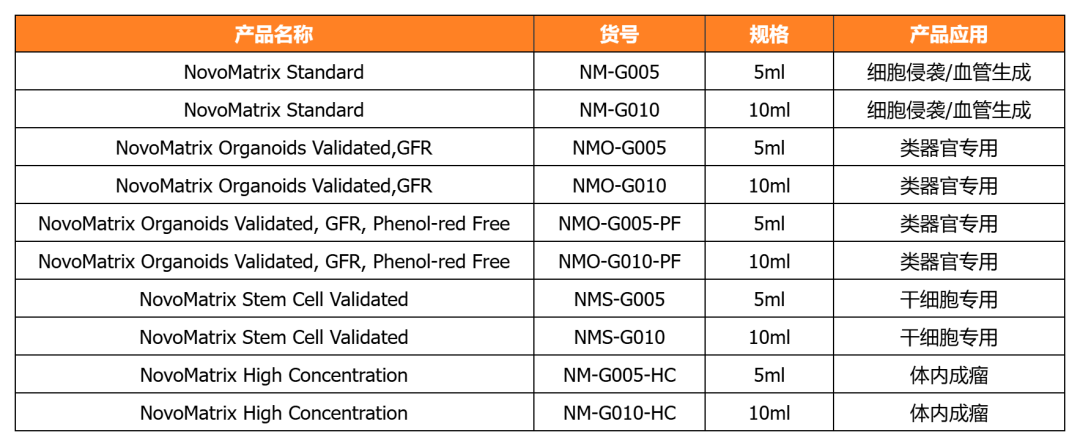
NovoMatrix支持多種類器官培養(yǎng)
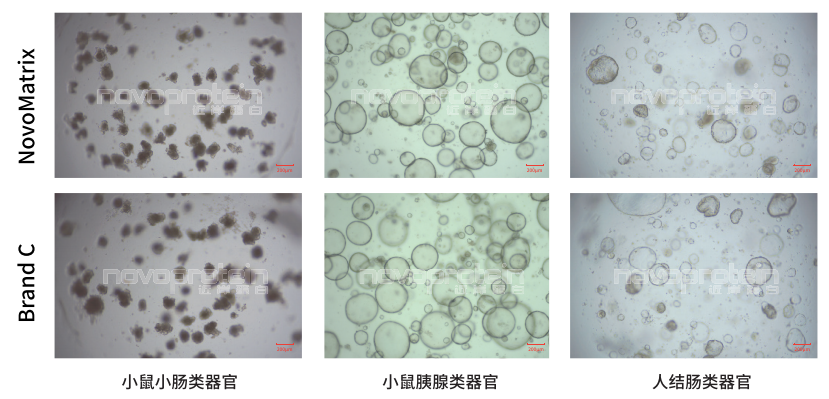
NovoMatrix Organoid Validated,GFR,Phenol Red-Free (Cat.No.:NMO-G005-PF) and a similar product of Brand C were used for culture of different oragnoid models
NovoMatrix支持類器官穩(wěn)定傳代

NovoMatrix Organoid Validated,GFR,Phenol Red-Free (Cat.No.:NMO-G005-PF) maintain stable passage of organoids comparable to a similar product of Brand C
經(jīng)類器官培養(yǎng)驗證的細胞因子
近岸蛋白自主研發(fā)生產(chǎn)并經(jīng)過類器官培養(yǎng)驗證的低內(nèi)毒素Activin A、BMP-4、EGF、FGF-7、FGF-10、FGFb、FGF8b、HGF、IGF1、Noggin、NRG1、R-Spondin 1/3和Wnt3a等細胞因子,已經(jīng)在人腫瘤類器官如垂體瘤類器官、腦膜瘤類器官、乳腺癌類器官,人正常類器官如ipsc來源的人小腸類器官,以及小鼠正常類器官如小腸類器官、結(jié)腸類器官、胃類器官以及膽管類器官等體外模型上進行了驗證。
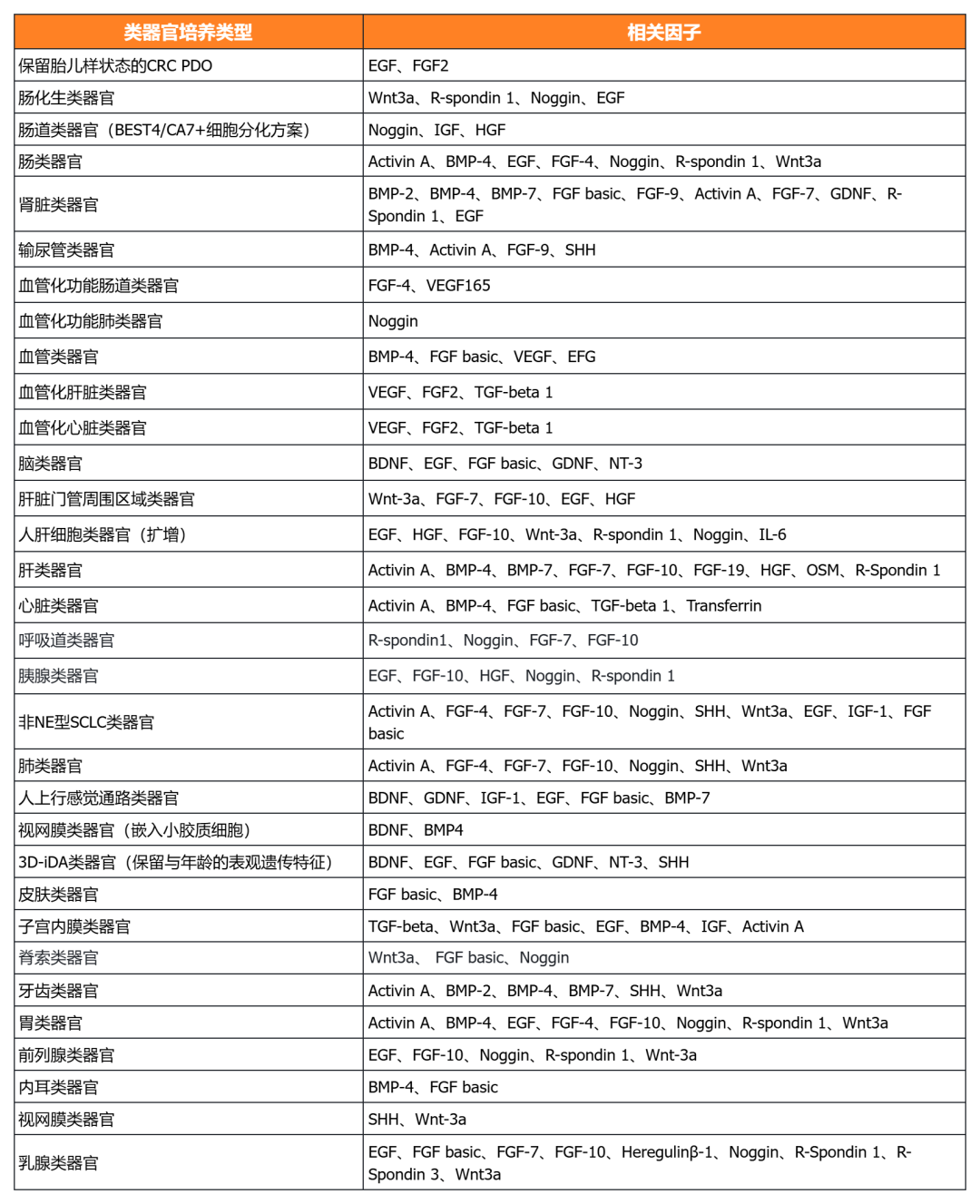
經(jīng)類器官培養(yǎng)驗證的完全培養(yǎng)基
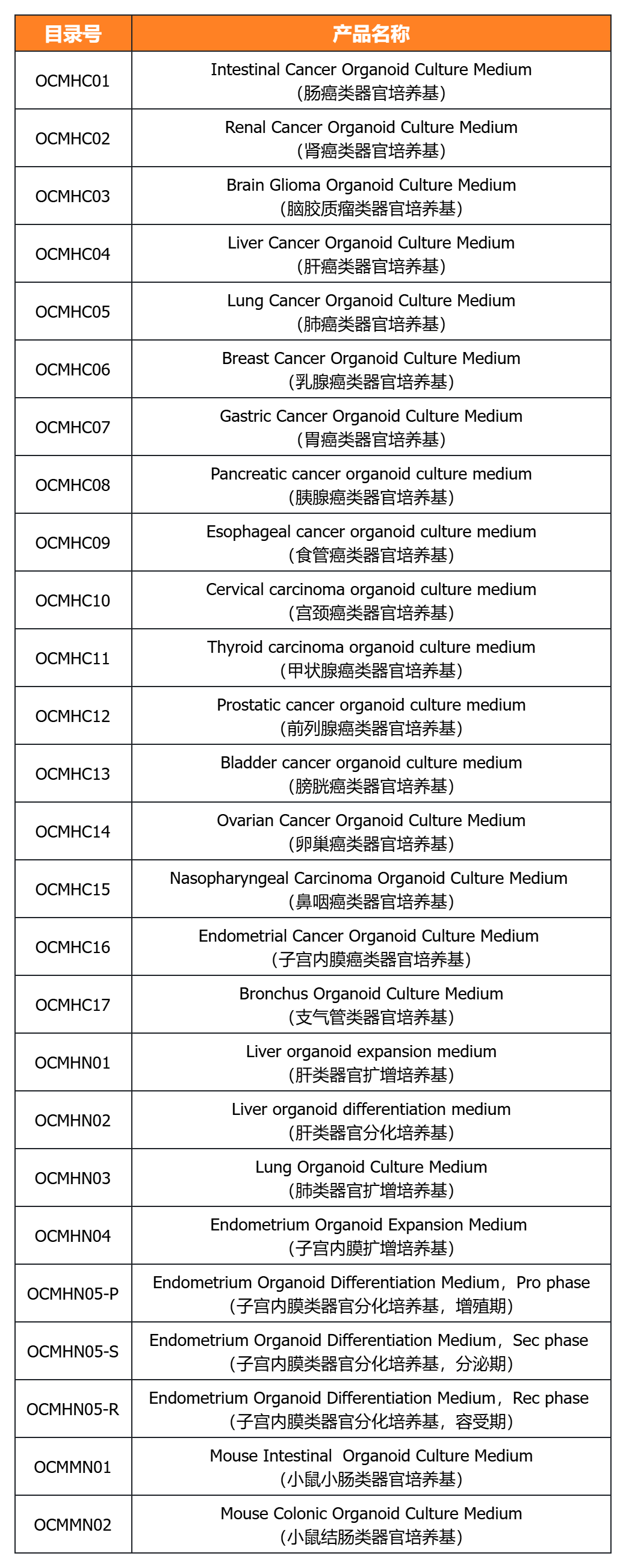
參考資料
Zushin, Peter-James H et al. “FDA Modernization Act 2.0: transitioning beyond animal models with human cells, organoids, and AI/ML-based approaches.” The Journal of clinical investigation vol. 133,21 e175824. 1 Nov. 2023, doi:10.1172/JCI175824
