在全世界男性中,前列腺癌(PCa)是最常見的惡性腫瘤,也是癌癥相關死亡的第二大原因。雖然大多數PCa患者可以通過局部治療治愈,但一些患者會隨著前列腺特異性抗原(prostate-specific antigen,PSA)值升高而進展,并發展為轉移性去勢抵抗性前列腺癌(mCRPC),迫切需要找到PCa的新生物標志物和靶點[1]。近年來,PSMA(前列腺特異性膜抗原)、STEAP1(六跨膜上皮抗原前列腺1)及KLK2(人激肽釋放酶相關肽酶2)三大腫瘤特異性靶點的發現與開發,為前列腺癌精準治療帶來革命性突破,成為腫瘤免疫治療藥物研發的焦點。
近岸蛋白提供高質量PSMA、STEAP1以及KLK2等前列腺癌系列靶點蛋白,多種屬、多標簽、經過ELISA/BLI等活性驗證,現貨供應。
PSMA:成熟且經典的靶點
前列腺特異性膜抗原(Prostate-specific membrane antigen,PSMA)于20世紀80年代初被發現,與前列腺組織密切相關,正常情況下主要在前列腺中表達。研究發現,前列腺癌的上皮分泌細胞中PSMA水平可升高至正常水平的1000倍,多項研究表明PSMA的高表達與高Gleason評分、高前列腺特異性抗原(PSA)血清水平、晚期疾病階段以及轉移性去勢抵抗性前列腺癌(mCRPC)具有相關性[2,3,4,5]。因此,被認為是前列腺癌重要的生物標志物和治療靶點。同時,PSMA在多種實體腫瘤中亦存在表達,可作為腫瘤抗血管生成治療的潛在靶點。PSMA作為前列腺癌領域研究是最深入、應用最廣泛的靶點。基于PSMA的靶向治療策略包括放射配體療法、抗體藥物偶聯物(ADC)、CAR-T細胞療法以及雙特異性T細胞重定向療法。
目前,靶向PSMA批準上市的單抗藥物僅一款由Eusa Pharma研發的Capromab pendetide。2024年強生以20億美元收購Ambrx,囊獲一款靶向前列腺特異性膜抗原(PSMA)的ADC藥物ARX517,該藥物獲FDA授予快速通道資格,現處于臨床一期階段。目前已有17種藥物處于臨床二期,21種藥物處于臨床一期,另有40種藥物處于臨床前階段,且目前國內尚無批準上市藥物。
表1. 靶向PSMA藥物全球研發進展(部分)
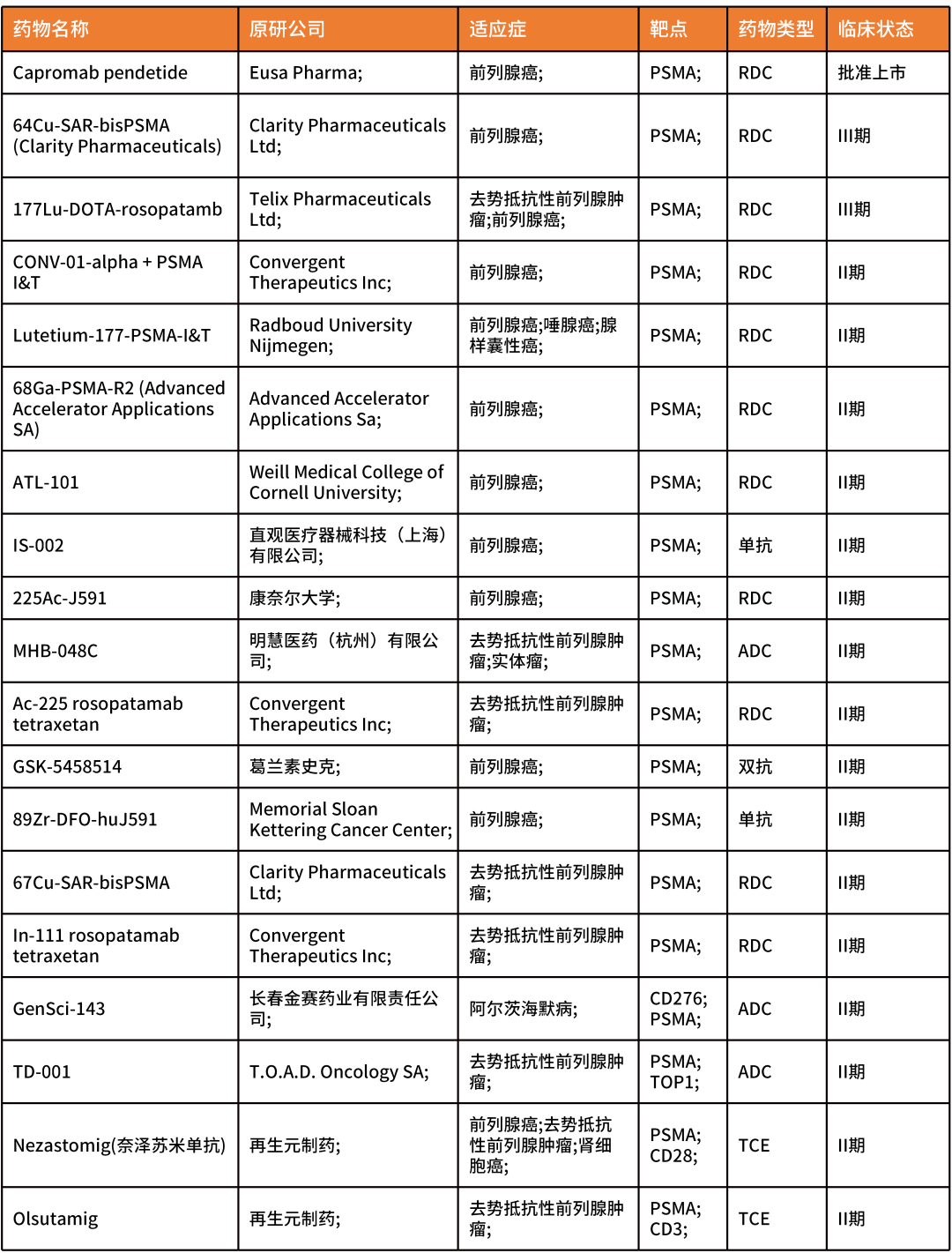
STEAP1:后起之秀的潛力靶點
STEAP1是一種細胞表面蛋白,屬于STEAP家族。該家族包括四個相關蛋白:STEAP1、STEAP2、STEAP3和STEAP4。所有成員都是具有六個跨膜結構域和胞質N末端的多次跨膜蛋白。STEAP1分子構型使其能夠形成同源三聚體或與其他STEAP蛋白形成異源三聚體復合物,從而增強其活性并可能影響細胞間通訊[6,7,8]。
在前列腺癌中,STEAP1顯著過表達(超過85%的病例中存在),以及其他惡性腫瘤,如膠質母細胞瘤、尤文肉瘤和胰腺癌[9]。這種過表達在轉移性去勢抵抗性前列腺癌(mCRPC)中尤為重要,高水平的STEAP1與高Gleason評分和較差的臨床結果等侵襲性疾病特征相關,表明其作為治療靶點的前景[10]。有研究顯示在mCRPC中,STEAP1的表達(87.7%)比前列腺特異性膜抗原(PSMA)(60.5%)更為廣泛[11]。除了在前列腺癌中的作用外,STEAP1還能通過增強細胞增殖、遷移和侵襲來促進腫瘤進展,并通過JAK2/STAT3等信號通路參與上皮-間質轉化和轉移等過程,并在多種癌癥類型中參與活性氧的調節[6]。STEAP1在超過85%的前列腺腫瘤中高表達,但在正常組織中幾乎不表達,已成為ADC、CAR-T細胞治療、雙特異性抗體等多種新型療法的理想靶點[8]。
AMG-509是安進開發的STEAP1/CD3雙特異性抗體,在轉移性去勢抵抗性前列腺癌(mCRPC)患者中展現出良好療效:PSA50達49%,ORR達41%,DCR達79%,腫瘤縮小明顯,安全性可控。隨著三期臨床啟動,AMG 509有望成為前列腺癌免疫治療的新突破口。目前,根據藥渡數據庫顯示國外至少已有10家公司圍繞STEAP1靶點開展不同階段的臨床研究,國內也有3家相關研發管線。
表2. 靶向STEAP1藥物全球研發進展
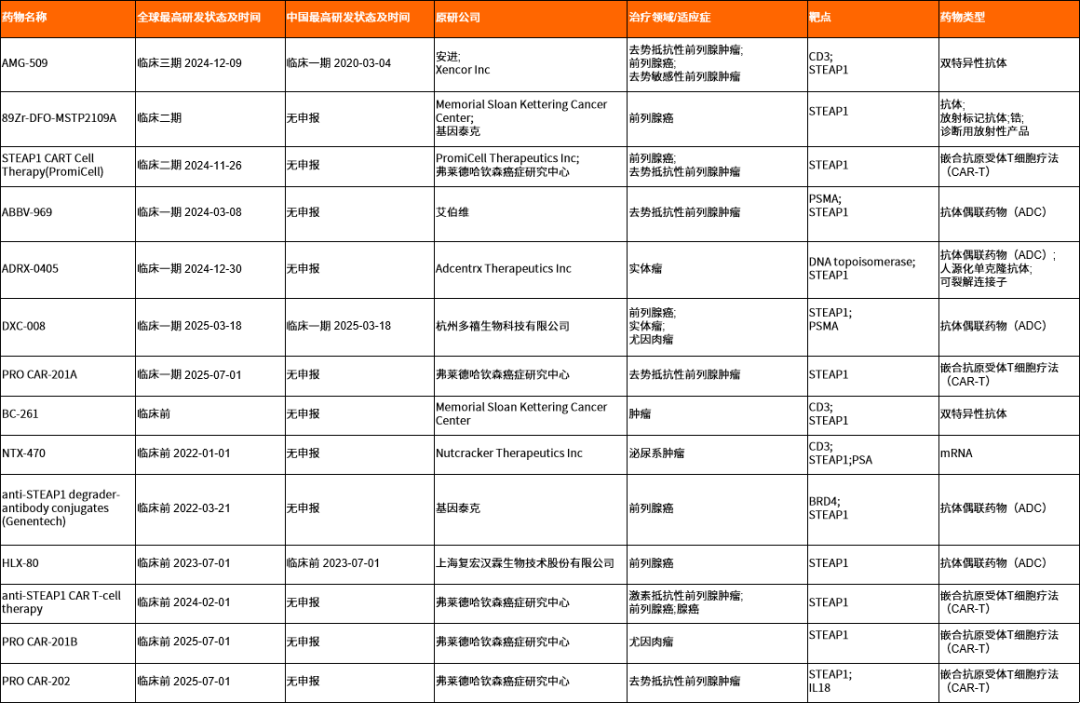
KLK2:高特異性的靶點
KLK2作為激肽釋放酶家族成員,與PSA同源,其最大優勢在于組織特異性。KLK2的表達主要集中在前列腺組織,其他正常組織表達水平極低。而PSMA與STEAP1的表達特異性較低,它們在多種非前列腺組織中表達更為廣泛。因此,KLK2具有較高的組織特異性。在不同前列腺癌階段,KLK2表達呈現一定的異質性,但整體保持高水平和均一性,尤其在LPC和mHSPC階段。與PSMA相比,KLK2在前列腺癌樣本中的表達更加廣泛和均一[12]。
強生開發的KLK2×CD3雙特異性抗體Pasritamig(PAS)是一種首創的(first-in-class)人激肽釋放酶2(KLK2)T細胞銜接器(TCE),同時結合前列腺癌細胞上的KLK2和T細胞上的CD3受體,激活T細胞并介導癌細胞裂解。2026年ASCO GU會議上,強生再次更新了聯合多西他賽(DOCE)治療轉移性去勢抵抗性前列腺癌(mCRPC)的1b期臨床研究結果。PAS+DOCE的安全性與DOCE已知安全性特征一致,耐受性良好,無CRS發生,未出現新的安全性信號。在既往經ARPI、Lu-177 PSMA RLT和/或化療治療的患者中顯示出深度且持久的PSA應答。
表3.靶向KLK2的藥物全球研發進展
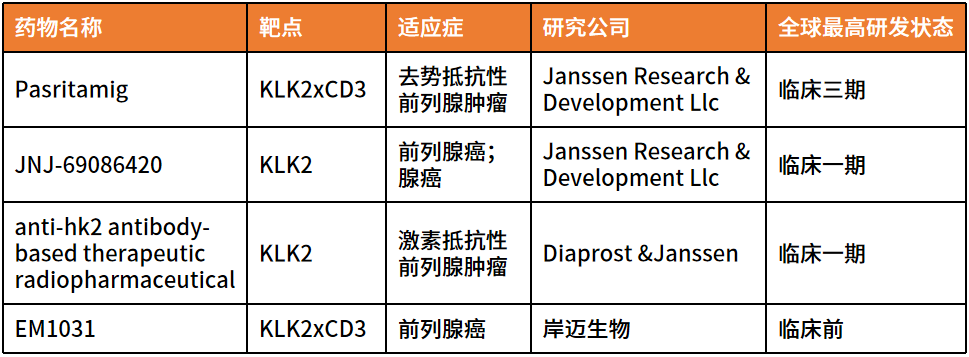
三大前列腺癌特異性靶點,腫瘤免疫治療未來可期
PSMA、STEAP1及KLK2三大靶點的崛起,為前列腺癌治療打開新的治療局面。從臨床價值來看,PSMA 成熟穩健,是當前精準治療的主力;STEAP1療效突出,有望成為后線治療的核心選擇;KLK2特異性極強,為安全治療提供新可能,三者形成互補協同,覆蓋不同階段、不同表達特征的患者需求。未來,隨著臨床研究的深入與技術的持續突破,PSMA、STEAP1及KLK2將繼續引領前列腺癌治療進入更精準、更高效的新時代,為全球前列腺癌患者帶來新的希望。
推薦產品
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
前列腺癌相關靶點[13]
|
B7-H3 |
CD36 |
CD46 |
CXCR4 |
HER3 |
|
DLL3 |
FAP |
HER3 |
KLK2 |
PSMA |
|
PSCA |
ROR1 |
STEAP1 |
TROP2 |
|
參考文獻
[1] Xu, M.; Evans, L.; Bizzaro, C.L.; Quaglia, F.; Verrillo, C.E.; Li, L.; Stieglmaier, J.; Schiewer, M.J.; Languino, L.R.; Kelly, W.K. STEAP1–4 (Six-Transmembrane Epithelial Antigen of the Prostate 1–4) and Their Clinical Implications for Prostate Cancer. Cancers 2022, 14, 4034.
[2] Lauri C, Chiurchioni L, Russo VM, Zannini L, Signore A. PSMA Expression in Solid Tumors beyond the Prostate Gland: Ready for Theranostic Applications?. J Clin Med. 2022;11(21):6590. Published 2022 Nov 7. doi:10.3390/jcm11216590
[3] Eiber M., Fendler W.P., Rowe S.P., Calais J., Hofman M.S., Maurer T., Schwarzenboeck S.M., Kratowchil C., Herrmann K., Giesel F.L. Prostate-specific membrane antigen ligands for imaging and therapy. J. Nucl. Med. 2017;58:67S–76S.
[4] Fragomeni R.A.S., Amir T., Sheikhbahaei S., Harvey S.C., Javadi M.S., Solnes L.B., Kiess A.P., Allaf M.E., Pomper M.G., Gorin M.A., et al. Imaging of nonprostate cancers using PSMA-targeted radiotracers: Rationale, current state of the field, and a call to arms. J. Nucl. Med. 2018;59:871–877.
[5] Siva S., Udovicich C., Tran B., Zargar H., Murphy D.G., Hofman M.S. Expanding the role of small-molecule PSMA ligands beyond PET staging of prostate cancer. Nat. Rev. Urol. 2020;17:107–118.
[6] Chen, W.-J. et al. (2021) Regulatory roles of six transmembrane epithelial antigen of the prostate family members in the occurrence and development of malignant tumors. Front. Cell Dev. Biol. 9, 752426
[7] Oosterheert, W. and Gros, P. (2020) Cryo-electron micros copy structure and potential enzymatic function of human six-transmembrane epithelial antigen of the prostate 1 (STEAP1). J. Biol. Chem. 295, 9502–9512
[8] Singh, Rohit, and Jon Amund Kyte. “STEAP1: a promising target in prostate cancer therapy.” Trends in cancer vol. 11,8 (2025): 722-725.
[9] Moreaux, J. et al. (2012) STEAP1 is overexpressed in can cers: a promising therapeutic target. Biochem. Biophys. Res. Commun. 429, 148–155
[10] Gomes, I.M. et al. (2014) STEAP1 is overexpressed in prostate cancer and prostatic intraepithelial neoplasia le sions, and it is positively associated with Gleason score. Urol. Oncol. 32, 53.e23–59
[11] Bhatia, V. et al. (2023) Targeting advanced prostate cancer with STEAP1 chimeric antigen receptor T cell and tumor localized IL-12 immunotherapy. Nat. Commun. 14, 2041
[12] Shen F,Smith R,McDevitt T, et al. Human kallikrein 2: A novel lineage-specific surface target in prostate cancer.[J]. Clinical cancer research,2025.
[13] Boixareu, Cristina et al. “Targeting the tumour cell surface in advanced prostate cancer.” Nature reviews. Urology vol. 22,9 (2025): 569-589.
