哺乳動物機(jī)體是一個精密運(yùn)轉(zhuǎn)的網(wǎng)絡(luò),各器官協(xié)同調(diào)節(jié)循環(huán)代謝物的生成與消耗,共同維系生命穩(wěn)態(tài)。器官間通過代謝物進(jìn)行動態(tài)對話,當(dāng)葡萄糖、膽固醇等關(guān)鍵代謝物的平衡被打破,便有可能引發(fā)心臟代謝疾病(CMD),累及多個器官的功能。然而如致病因素(如西方飲食或慢性高膽固醇血癥)如何干擾這一復(fù)雜的代謝網(wǎng)絡(luò)并最終促進(jìn)CMD,仍是亟待破解的謎題。
在CMD的研究過程中,傳統(tǒng)組學(xué)技術(shù)雖提供了寶貴的靜態(tài)分子圖譜,卻難以捕捉器官代謝活動的動態(tài)過程。隨著質(zhì)譜技術(shù)的重大突破,動靜脈(AV)代謝梯度(代謝組學(xué))分析有望突破此局限,該方法通過計(jì)算動靜脈濃度差可直接量化器官的代謝物凈產(chǎn)出(Δ>0)或消耗(Δ<0),有望成為解析器官代謝活動的關(guān)鍵利器。
基于此,2025年5月,加州大學(xué)Cholsoon Jang研究團(tuán)隊(duì)在Cell上發(fā)表了題為“Cross-organ metabolite production and consumption in healthy and atherogenic conditions”的研究論文,通過對LDLR(低密度脂蛋白受體)缺陷豬模型進(jìn)行多器官AV代謝組學(xué)分析,系統(tǒng)解析了不同飲食和病理?xiàng)l件下的全局代謝物產(chǎn)生與消耗圖譜。此外,該研究首次揭示出西方飲食會誘導(dǎo)肝外器官異常釋放膽汁酸,且這一現(xiàn)象在LDLR缺陷豬中顯著加劇,為深入理解CMD的病理機(jī)制提供了新的關(guān)鍵線索。
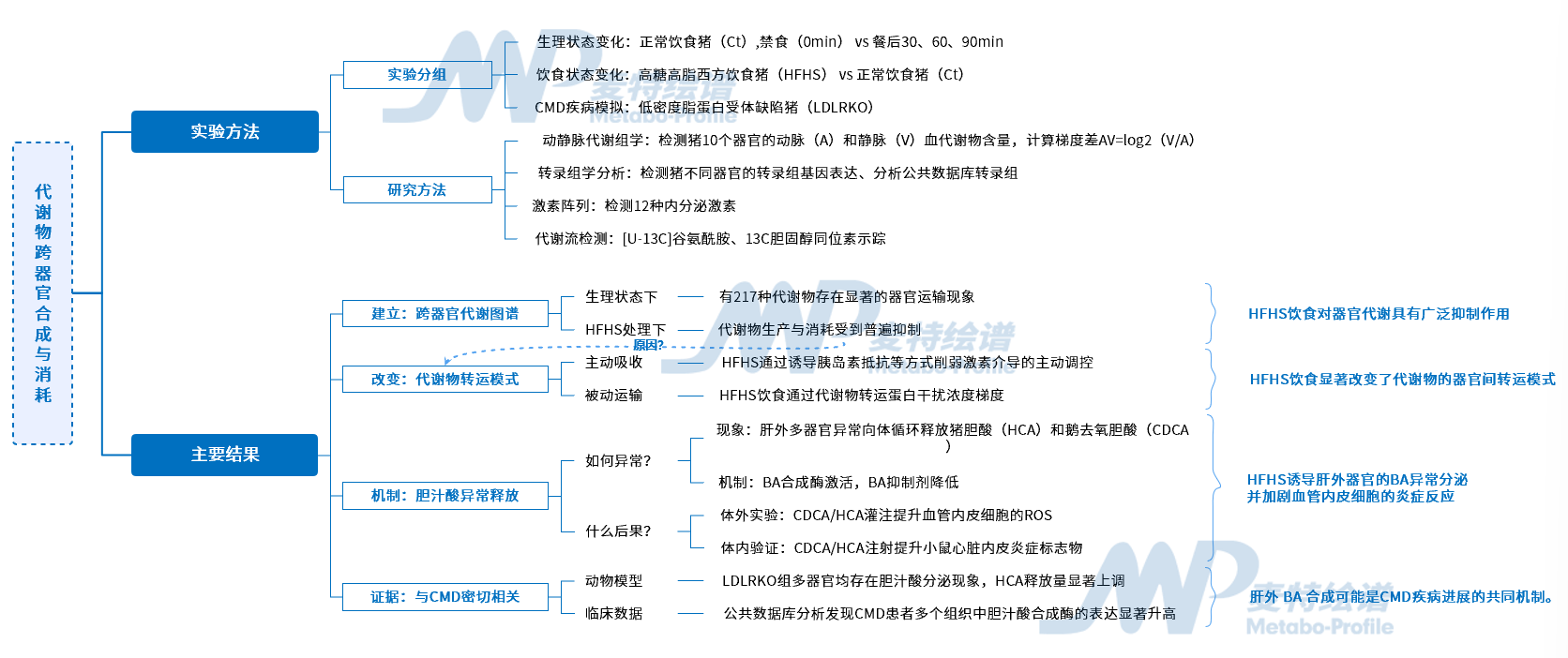
技術(shù)路線圖
研究結(jié)果
1. 禁食/喂養(yǎng)對器官代謝的基礎(chǔ)影響
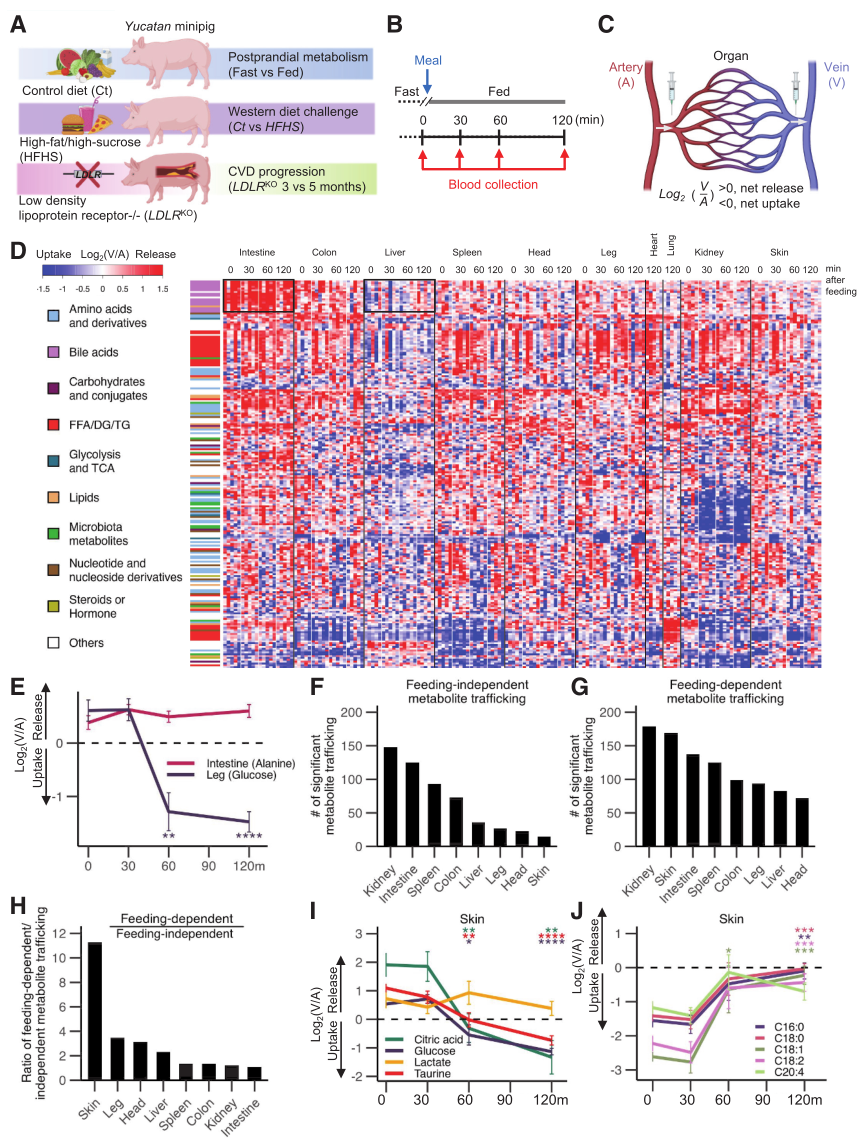
首先通過動靜脈(AV)代謝組學(xué)分析,研究者在10個器官的4個時(shí)間點(diǎn)(禁食及喂養(yǎng)后 30、60、120分鐘)跟蹤了1305種循環(huán)代謝物,其中217種在特定器官或時(shí)間點(diǎn)存在顯著轉(zhuǎn)運(yùn)差異。進(jìn)一步分析顯示,540例代謝事件不依賴食物攝入,如腸道持續(xù)釋放丙氨酸、腎臟攝取氨基酸,主要富集于腹腔內(nèi)臟器官;958例事件依賴喂養(yǎng),如腿部肌肉餐后葡萄糖攝取,以腎臟和皮膚最為敏感,這些提示了餐后組織重塑的代謝需求。
圖1. 禁食和進(jìn)食對器官特異性代謝物運(yùn)輸?shù)挠绊?/p>
2. 西方飲食(HFHS)對代謝網(wǎng)絡(luò)的系統(tǒng)性抑制
鑒于西方飲食與心臟代謝疾病的明確因果關(guān)聯(lián),研究者進(jìn)一步探究了高脂/高蔗糖(HFHS)飲食對器官代謝物生成與消耗的影響。結(jié)果表明,2周HFHS飲食誘導(dǎo)下,豬的體重、胰島素水平及HOMA-IR顯著升高,動脈血脂質(zhì)、核苷酸和膽汁酸水平異常,但空腹血糖、呼吸頻率等無明顯變化。AV梯度測量顯示,相比于正常飲食的對照組(Ct),HFHS組中1368種代謝物的器官生產(chǎn)與消耗普遍減弱,喂養(yǎng)依賴性事件數(shù)量減少。以葡萄糖為例,Ct組腿部肌肉餐后|Δlog?V/A|為1.9~2.1,而HFHS組僅0.1~0.2,反映胰島素抵抗導(dǎo)致的葡萄糖攝取障礙。類似缺陷也存在于皮膚、腦等器官,同時(shí)肝臟糖異生抑制能力受損。整體而言,HFHS組78%的代謝物|Δlog?V/A|<1.0,遠(yuǎn)高于Ct組的29%,證實(shí)其缺陷對器官代謝的廣泛抑制。
圖2. 西方飲食喂養(yǎng)對器官特異性代謝物運(yùn)輸?shù)挠绊?/p>
3. 代謝物生產(chǎn)位點(diǎn)的重分配與調(diào)控機(jī)制
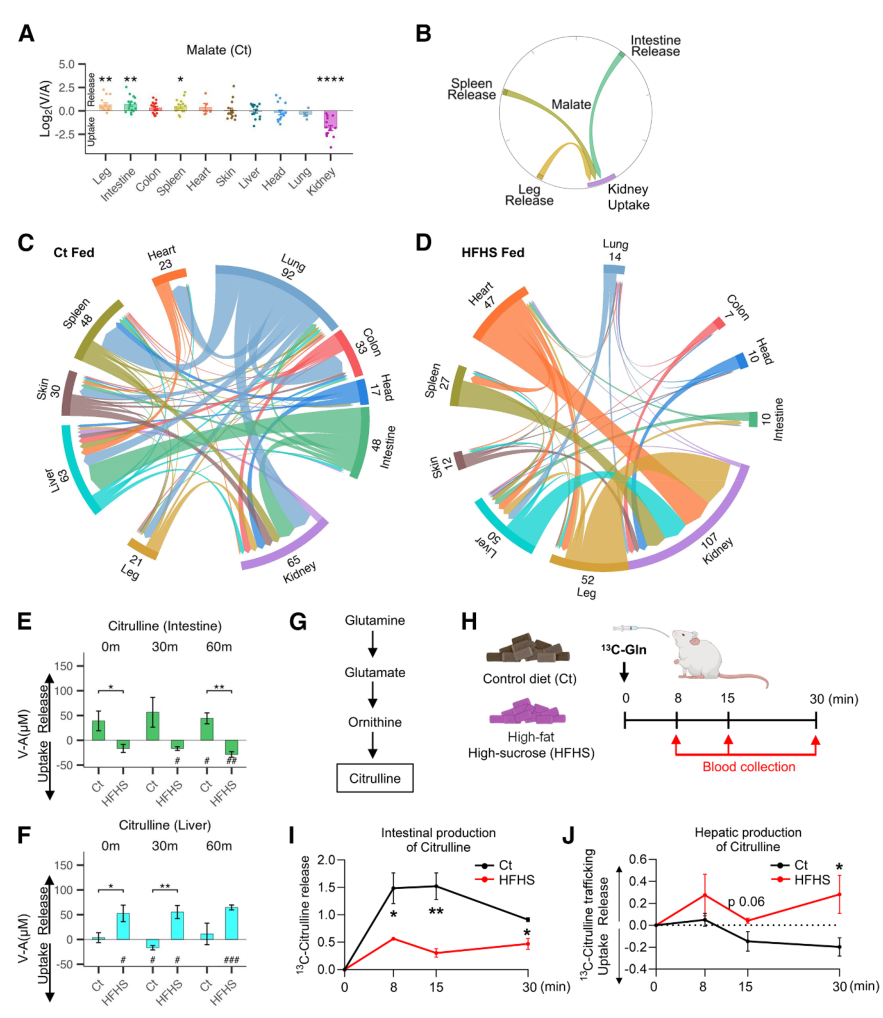
接下來對每種代謝物進(jìn)行統(tǒng)計(jì)分析,確定其顯著釋放或吸收的器官,繪制循環(huán)代謝物的主要來源與目標(biāo)的器官圖譜。AV數(shù)據(jù)顯示,HFHS飲食顯著改變了代謝物的器官間轉(zhuǎn)運(yùn)模式,以瓜氨酸為例,Ct組中該物質(zhì)主要由腸道生產(chǎn),而HFHS組則轉(zhuǎn)向肝臟,小鼠的[U-13C]谷氨酰胺代謝流結(jié)果驗(yàn)證了這一切換,伴隨體重增加和胰島素抵抗等表型的改變。
圖3. 西方飲食對器官之間代謝物運(yùn)轉(zhuǎn)的影響
在機(jī)制方面,研究者揭示了HFHS飲食通過雙重機(jī)制破壞器官代謝調(diào)控:
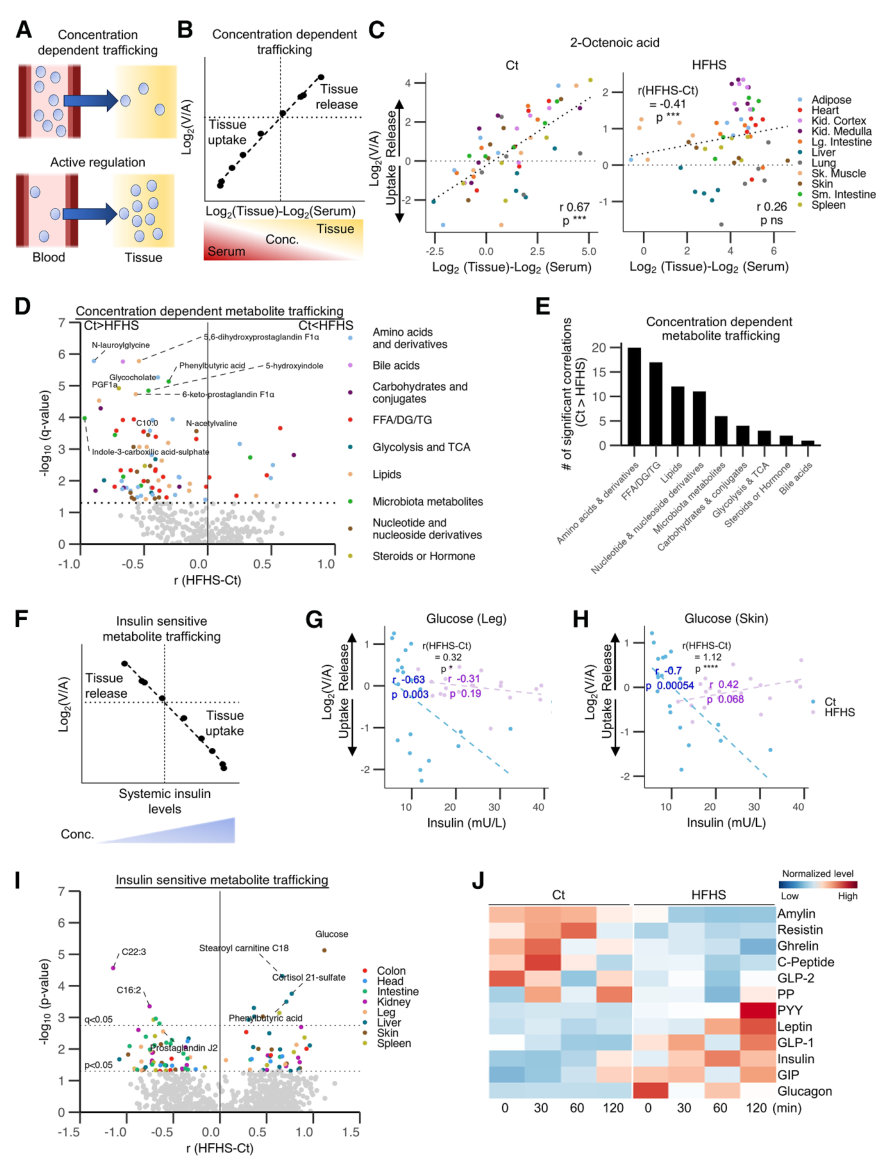
被動運(yùn)輸:這種物質(zhì)運(yùn)輸由濃度梯度介導(dǎo),即物質(zhì)會從高濃度區(qū)域流向低濃度區(qū)域。因此首先通過相關(guān)性分析,篩選出229種代謝物在Ct組的轉(zhuǎn)運(yùn)與組織-血液的濃度梯度顯著正相關(guān),即它們的轉(zhuǎn)運(yùn)由濃度梯度驅(qū)動,其中包含以2-辛烯酸為代表的多種有機(jī)酸;而在HFHS組中,該相關(guān)性普遍減弱,轉(zhuǎn)錄組分析顯示對應(yīng)的代謝物轉(zhuǎn)運(yùn)蛋白表達(dá)異常。
主動運(yùn)輸:這是一種逆濃度梯度的物質(zhì)運(yùn)輸方式,往往受到激素的調(diào)節(jié)。以機(jī)體血糖調(diào)節(jié)為例,細(xì)胞在胰島素的誘導(dǎo)下主動攝取葡萄糖,從而降低血糖濃度。在Ct組中,胰島素水平與腿部和皮膚的葡萄糖攝取強(qiáng)相關(guān),而在HFHS組中由于胰島素抵抗,這種相關(guān)性消失。
圖4. 通過濃度梯度或激素調(diào)節(jié)進(jìn)行代謝物運(yùn)輸
總之,HFHS飲食一方面干擾濃度梯度驅(qū)動的被動運(yùn)輸,另一方面通過誘導(dǎo)胰島素抵抗等方式削弱激素介導(dǎo)的主動調(diào)控,最終導(dǎo)致器官代謝物生成與消耗的整體紊亂。
4. 肝外器官膽汁酸的異常釋放及病理作用
盡管HFHS飲食普遍抑制器官的代謝物生成與消耗,但研究者也發(fā)現(xiàn)酰基肉堿和膽汁酸等膽固醇衍生物的生成顯著增強(qiáng)。在Ct組中,膽汁酸的釋放與攝取符合經(jīng)典的肝腸循環(huán)模式,而在HFHS組中,心、肺等多器官異常向體循環(huán)釋放豬膽酸(HCA)和鵝去氧膽酸(CDCA),致系統(tǒng)血中BA 水平升高。機(jī)制方式,首先通過全器官轉(zhuǎn)錄組測序發(fā)現(xiàn),相較于Ct組,HFHS組的BA合成酶(CYP7A1、CYP27A1 等)表達(dá)上調(diào),而BA抑制劑(FGF19)的水平降低3倍,說明膽固醇向膽汁酸的轉(zhuǎn)化增強(qiáng),或?yàn)镠FHS下機(jī)體為緩解循環(huán)膽固醇升高的代償機(jī)制。
在代謝紊亂和心血管疾病患者中,循環(huán)膽汁酸水平長期呈現(xiàn)異常升高狀態(tài),且血液膽汁酸濃度與脂肪性肝炎及冠狀動脈狹窄的嚴(yán)重程度呈正相關(guān),基于此,研究者推測具有細(xì)胞毒性的膽汁酸可能對血管內(nèi)皮細(xì)胞(ECs)產(chǎn)生損害,體外實(shí)驗(yàn)中,CDCA/HCA的微流控灌注可顯著提升ECs的ROS生成和單核細(xì)胞粘附;體內(nèi)實(shí)驗(yàn)中,CDCA/HCA的1:1輸注使小鼠心臟中的內(nèi)皮炎癥標(biāo)志物Vcam-1和Icam-1的表達(dá)顯著增加,其作用程度與陽性對照脂多糖(LPS)相當(dāng)。以上結(jié)果證實(shí)BA可觸發(fā)血管炎癥。
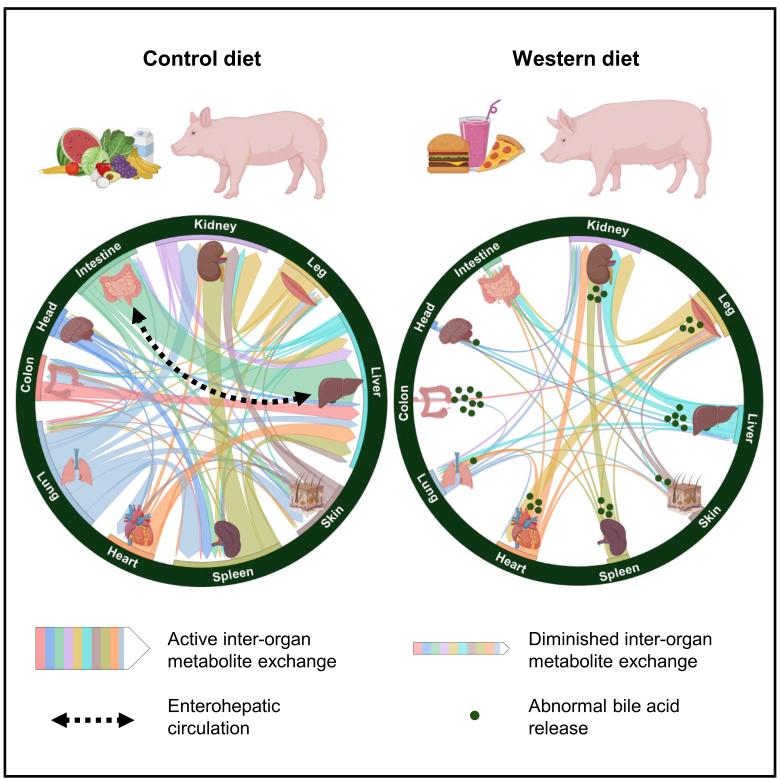
圖5. HFHS飲食導(dǎo)致多個器官異常膽汁酸釋放
5. LDLR缺陷豬與人類CMD患者的肝外BA合成證據(jù)
在當(dāng)前的診療實(shí)踐與臨床研究中,CMD患者循環(huán)膽汁酸水平升高通常被歸因于肝臟來源,而其他器官的潛在貢獻(xiàn)尚未得到充分考量。因此,研究者利用LDLR缺陷(LDLRKO)豬模型,結(jié)合3-5個月的致動脈粥樣硬化飲食干預(yù)(高脂高糖+1%膽固醇),成功模擬了人類代謝性心肌病(CMD)的核心病理特征,包括高膽固醇血癥、冠狀動脈粥樣硬化等。與HFHS組相似,LDLRKO組的AV檢測結(jié)果顯示多器官均存在膽汁酸分泌現(xiàn)象,且HCA的釋放量顯著高于HFHS組。此外,LDLRKO組的FGF19水平較HFHS組更低,提示FGF19水平下降可能是驅(qū)動血液膽汁酸升高的關(guān)鍵機(jī)制。最后通過分析人類轉(zhuǎn)錄組數(shù)據(jù)集,發(fā)現(xiàn)在CMD患者多個組織中膽汁酸合成酶的表達(dá)顯著升高,提示肝外BA合成可能是CMD疾病進(jìn)展的共同機(jī)制。
圖6. LDLRKO模型豬CMD患者肝外器官BA合成的研究
全文總結(jié)
本研究采用動靜脈代謝組學(xué)、組織轉(zhuǎn)錄組學(xué)及多激素檢測平臺,系統(tǒng)解析了豬在禁食/進(jìn)食狀態(tài)、西式飲食誘導(dǎo)(HFHS)及低密度脂蛋白受體缺陷(LDLRKO)相關(guān)心血管疾病進(jìn)展過程中的跨器官代謝動態(tài)。通過整合關(guān)鍵代謝物在10種主要代謝器官的攝取/釋放通量數(shù)據(jù),構(gòu)建了進(jìn)食依賴性與非依賴性代謝物交換的時(shí)空圖譜。研究揭示:
(1)多器官存在進(jìn)食狀態(tài)特異性代謝物交換模式
(2)西式飲食通過重塑代謝物濃度梯度及干擾FGF19/FGF21-FXR信號軸,破壞器官間代謝協(xié)同
(3)LDLR缺陷與西式飲食協(xié)同誘導(dǎo)肝外器官(如心臟、骨骼肌)膽汁酸(BA)異常分泌,并通過激活血管內(nèi)皮炎癥通路加劇動脈粥樣硬化
本研究首次闡明了病理狀態(tài)下器官間代謝干擾的層級網(wǎng)絡(luò),為飲食-遺傳交互作用驅(qū)動心臟代謝疾病的機(jī)制研究提供了系統(tǒng)性資源。
參考文獻(xiàn)
Bae H, Jung S, Le J, et al . Cross-organ metabolite production and consumption in healthy and atherogenic conditions. Cell. 2025
請掃描二維碼閱讀原文
繪譜幫你測
麥特繪譜公司的經(jīng)典膽汁酸產(chǎn)品已協(xié)助數(shù)千家合作單位開展肝病、腸病、心血管疾病、糖尿病、肥胖、衰老、腫瘤/癌癥、畜牧動物、中藥等領(lǐng)域功能研究,已發(fā)表項(xiàng)目文章100+篇,其中大于10分的50+篇,涵蓋Cell Metabolism, Nature Metabolism, Nature Communications, Nature Aging, Advanced Science, Microbiome, Science Advances等期刊。近期公司的原研新品【膽汁酸全新修飾譜】檢測項(xiàng)目重磅發(fā)布,有望助力臨床醫(yī)生和科研人員深入挖掘新型修飾膽汁酸的巨大臨床功能價(jià)值,助您的成果更上一層樓,圓夢頂刊!