【答疑解惑】類器官培養(yǎng)100問-血管共培養(yǎng)篇
類器官是由成體干細(xì)胞或多能干細(xì)胞誘導(dǎo)分化并經(jīng)體外3D環(huán)境培養(yǎng)的細(xì)胞團(tuán),具備主要組織或器官的三維結(jié)構(gòu)與生理功能。然而,大部分的類器官缺乏血管網(wǎng)絡(luò)的支持,這限制了其形態(tài)大小和發(fā)育狀態(tài),導(dǎo)致無法完全模擬人體內(nèi)真實(shí)的組織器官。血管化問題是在類器官研究領(lǐng)域中的一個重要挑戰(zhàn)。
血管化類器官構(gòu)建的主要挑戰(zhàn)在于如何有效地形成和維持血管網(wǎng)絡(luò),以確保類器官內(nèi)部細(xì)胞的營養(yǎng)供應(yīng)和代謝廢物排出。血管化過程涉及復(fù)雜的生物學(xué)機(jī)制,包括血管發(fā)生和血管生成等,這些過程需要精確的調(diào)控和適當(dāng)?shù)呐囵B(yǎng)條件。其中,類器官/血管共培養(yǎng)是實(shí)現(xiàn)類器官血管化的一種重要方法。為此,小編針對類器官/血管共培養(yǎng)體系的細(xì)胞來源、培養(yǎng)方式、培養(yǎng)條件的優(yōu)化、共培后類器官的功能鑒定及定位等常見問題進(jìn)行了匯總整理,歡迎感興趣的老師一起交流討論!
Q1:為了彌補(bǔ)單一類器官在應(yīng)用上的不足,目前我們可以選擇哪些共培養(yǎng)模型?
A1:
1、免疫微環(huán)境共培養(yǎng)(包括T、NK、CAF等免疫微環(huán)境中的各類細(xì)胞);
2、血管共培養(yǎng);
3、間充質(zhì)細(xì)胞共培養(yǎng);
4、神經(jīng)網(wǎng)絡(luò)共培養(yǎng);
5、不同種類的類器官共培養(yǎng);
6、作為感染模型共培養(yǎng)(如:病毒、細(xì)菌等共培養(yǎng))。
Q2:當(dāng)我們需要做體外類器官血管化培養(yǎng)時,可以選用哪些來源的細(xì)胞作為類器官中“血管”的部分?
A2:
1、內(nèi)皮細(xì)胞。Takebe等人【1】將iPSC衍生的肝內(nèi)胚層、人臍靜脈內(nèi)皮細(xì)胞(HUVECs)和人骨髓間充質(zhì)干細(xì)胞(MSCs)接種在Matrigel中,培育出了血管化的肝芽(LBs);
2、干細(xì)胞。如:iPSC、ESC可以分化為血管內(nèi)皮細(xì)胞或血管類器官;
3、類器官共分化。通過誘導(dǎo)人多能干細(xì)胞同時向血管譜系和特定類器官譜系分化,以產(chǎn)生具有血管樣結(jié)構(gòu)的類器官【2】。
Q3:類器官與血管共培養(yǎng)有哪些方面的應(yīng)用?
A3:
1、血管系統(tǒng)發(fā)揮著運(yùn)輸營養(yǎng)物質(zhì)、氧氣、代謝廢物等重要作用,在缺乏可灌注的血管系統(tǒng)模型中,類器官僅依靠被動擴(kuò)散來交換營養(yǎng)物質(zhì)、氧氣和代謝廢物,如果尺寸過大,會逐漸導(dǎo)致類器官的核心壞死【3】;
2、使用這些血管類器官來模擬疾病進(jìn)程中的血管病變。如:通過構(gòu)建干細(xì)胞誘導(dǎo)分化(iPSC)的血管類器官模型,可以用于阿爾茨海默病、心血管疾病、傷口愈合、中風(fēng)、癌癥和糖尿病等一系列血管相關(guān)疾病的病因和治療方法研究【4】;
3、作為抑制血管生成藥物的效果評價模型。如:靶向血管內(nèi)皮生長因子/血管內(nèi)皮生長因子受體的藥物正在用于治療耐藥和轉(zhuǎn)移性結(jié)直腸癌的研究【5】;
4、作為特定的研究模型。如:血管類器官(BVOs)可以重現(xiàn)發(fā)育過程中血管的結(jié)構(gòu)和功能,并且BVOs浸潤腦類器官從而形成血腦屏障(BBB)模型【6】。
Q4:類器官的血管共培養(yǎng)有哪些方式?
A4:
1、使用內(nèi)皮細(xì)胞包裹類器官共培養(yǎng)。如:將人內(nèi)皮細(xì)胞嵌入基質(zhì)膠中,并在其中添加早期類器官(如圖1)。隨著時間的流逝,這會導(dǎo)致人類內(nèi)皮細(xì)胞自組裝成類器官外圍的毛細(xì)血管并侵入形成血管網(wǎng)絡(luò)。當(dāng)然這種方式可以在類器官的外圍形成明顯的血管網(wǎng)絡(luò),但在類器官中心的血管網(wǎng)絡(luò)形成較少【7】;
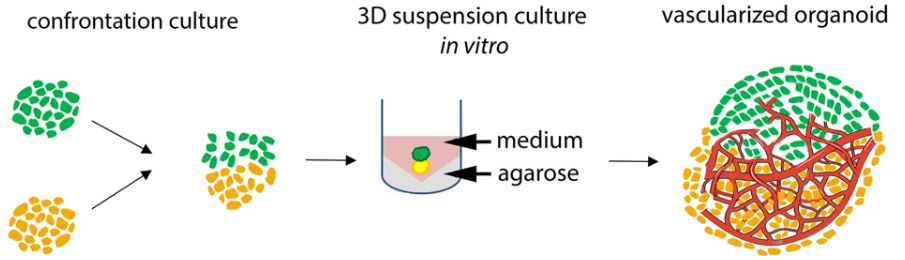
圖1. 內(nèi)皮細(xì)胞包裹類器官共培養(yǎng)流程示意圖【7】
2、干細(xì)胞與血管內(nèi)皮細(xì)胞均勻混合后共培養(yǎng)。如:將hESCs或iPSCs與人臍靜脈內(nèi)皮細(xì)胞(HUVECs)共培養(yǎng),定向誘導(dǎo)其分化為血管化的腦類器官(如圖2)。免疫熒光染色結(jié)果表明,HUVECs在腦類器官中相互連接,并形成具有通透能力的復(fù)雜血管系統(tǒng),該血管系統(tǒng)可以在腦類器官中可穩(wěn)定存在200天以上【8】;
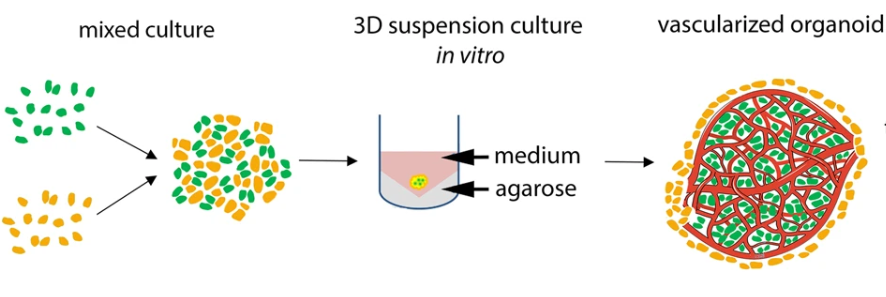
圖2. 干細(xì)胞與血管內(nèi)皮細(xì)胞均勻混合后共培養(yǎng)流程示意圖【7】
3、誘導(dǎo)自發(fā)血管化。如:通過動態(tài)調(diào)節(jié)WNT信號通路,控制近端腎小球和遠(yuǎn)端腎小管的比例,調(diào)節(jié)近端足細(xì)胞釋放血管內(nèi)皮生長因子A(VEGFA)的水平,進(jìn)而可誘導(dǎo)血管化的腎臟類器官分化形成【9】;
4、移植到體內(nèi)形成血管結(jié)構(gòu)。如:在體外將人胚胎干細(xì)胞(hESC)誘導(dǎo)分化為腦類器官后,直接移植入免疫缺陷小鼠軟腦膜血管上。移植的類器官繼續(xù)進(jìn)行分化和成熟,并與小鼠腦組織進(jìn)行了很好的整合,雙光子掃描成像結(jié)果顯示小鼠血管侵入移植物并生長延伸,血管內(nèi)血流活躍,移植物類器官功能性血管網(wǎng)絡(luò)發(fā)展良好【10】。
Q5:有哪些細(xì)胞因子/小分子可以促使干細(xì)胞向血管分化?
A5:干細(xì)胞在分化過程中,受不同的信號通路調(diào)控。那么激活/抑制特定的通路就要通過添加不同的細(xì)胞因子/小分子來實(shí)現(xiàn)。
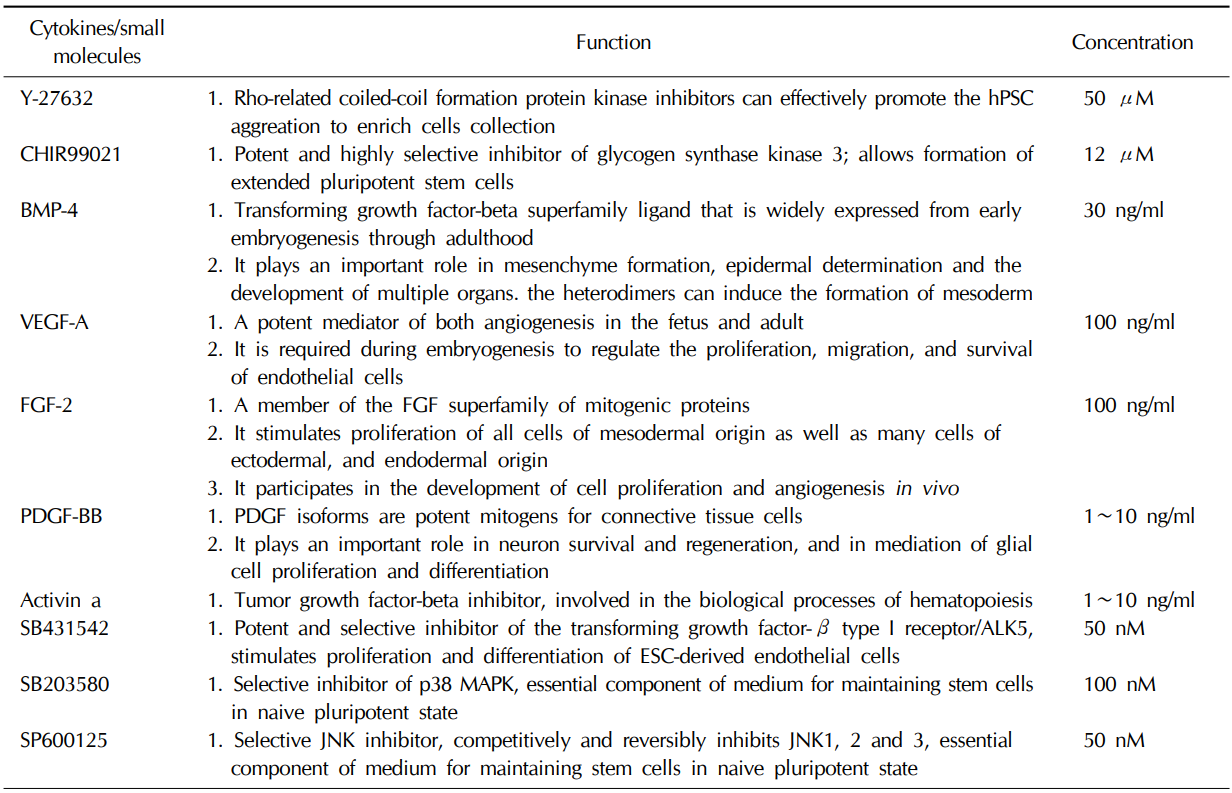
下表總結(jié)了血管分化途徑中所需的細(xì)胞因子/小分子,以及在分化過程中行使的功能【11】。
表1. 血管類器官培養(yǎng)中所需的細(xì)胞因子和小分子【11】
Q6:血管化后的類器官有哪些可檢測的特征和功能?
A6:
1、具有血管的一些表型特征,如:在含有凝膠的3D培養(yǎng)體系下,血管內(nèi)皮細(xì)胞可以自發(fā)形成血管網(wǎng)絡(luò);能夠表達(dá)內(nèi)皮細(xì)胞(CD31)、周細(xì)胞(PDGFR-β)、血管基底膜(Col IV)等相應(yīng)的血管特征標(biāo)志物(如圖3);
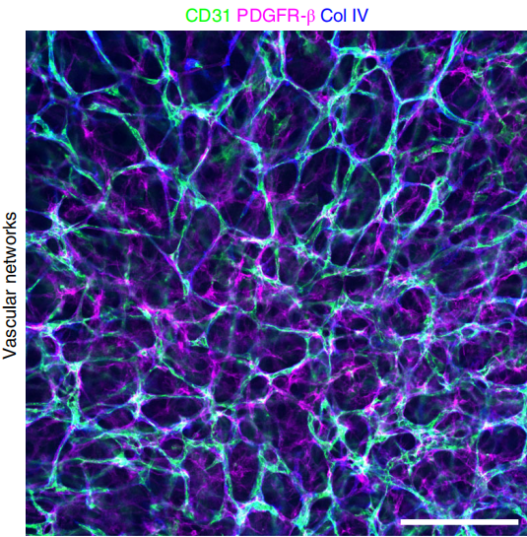
圖3. 從人多能干細(xì)胞分化出來的血管網(wǎng)絡(luò),和血管類器官的特征標(biāo)志物【12】
2、能夠分泌多種因子,調(diào)節(jié)目的細(xì)胞的發(fā)育成熟,如:與單獨(dú)培養(yǎng)的腦類器官相比,血管化的腦類器官中神經(jīng)元更成熟【8】;
3、具有一定的可灌注功能,如:向血管化的類器官中灌注FITC-葡聚糖,通過檢測類器官內(nèi)部的FITC信號,確定血管是否具有可灌注的功能【13】;
4、與未血管化的類器官相比,能夠更好地維持類器官的長時間生長,凋亡信號更低【14】;
5、與某些類器官共培養(yǎng)時能夠執(zhí)行功能,如:與腦類器官共培養(yǎng)可以形成血腦屏障;
6、在體內(nèi)移植類器官過程中,血管系統(tǒng)可以募集宿主ECs來重建功能性血管系統(tǒng),并促進(jìn)血液流入移植物,提高移植物的存活率【8】;
Q7:在類器官血管化的模型中,如何有效地定位血管?
A7:
1、如果需要實(shí)時觀察血管的生成情況,可以將內(nèi)皮細(xì)胞預(yù)先進(jìn)行熒光標(biāo)記,在培養(yǎng)過程中可以在熒光顯微鏡下觀察血管結(jié)構(gòu)【15】;
2、由于內(nèi)皮細(xì)胞在凝膠培養(yǎng)體系中易成管,因此可以在培養(yǎng)過程中使用熒光標(biāo)記的液體灌注,在熒光顯微鏡下可以觀察到清晰的血管結(jié)構(gòu)【16】;
3、可以將培養(yǎng)物固定后,通過免疫熒光鑒定出血管內(nèi)皮細(xì)胞的位置。
Q8:和單一類器官培養(yǎng)體系相比,類器官-血管這種共培養(yǎng)的體系需要如何調(diào)整?
A8:通常是兩種培養(yǎng)基按照1:1(v/v)混合,便于維持兩種模型的生長。當(dāng)然這并不一定是最優(yōu)的培養(yǎng)體系,如果有需要可以進(jìn)行不同配比和其他體系的優(yōu)化。
Q9:不同組織的血管化模型是一致的嗎?
A9:不是的,由于身體的每個組織都有自己獨(dú)特的結(jié)構(gòu)、細(xì)胞組成和功能,那么我們構(gòu)建的血管化類器官也要匹配對應(yīng)組織的特性,這些差異主要包括不同的血管網(wǎng)絡(luò)結(jié)構(gòu)、內(nèi)皮細(xì)胞表型等特征。例如:肌肉、脂肪或血腦屏障等組織中的ECs可以是“連續(xù)的”,細(xì)胞與細(xì)胞之間緊密地連接在一起,限制了通透性;而在一些內(nèi)分泌組織中,ECs可以是“不連續(xù)的”,細(xì)胞之間有間隙,可以允許更大的分子進(jìn)行交換【17】。
Q10:可以實(shí)現(xiàn)不同類型的類器官共培養(yǎng)嗎?
A10:已有研究通過將肝臟和胰島類器官進(jìn)行共培養(yǎng),構(gòu)建了2型糖尿病(T2DM)疾病模型(如圖4)【18】,這種多類器官系統(tǒng)可以在生理和病理?xiàng)l件下體外模擬肝-胰島軸,為今后 T2DM 發(fā)病機(jī)制研究和藥物開發(fā)提供了獨(dú)特的研究平臺。
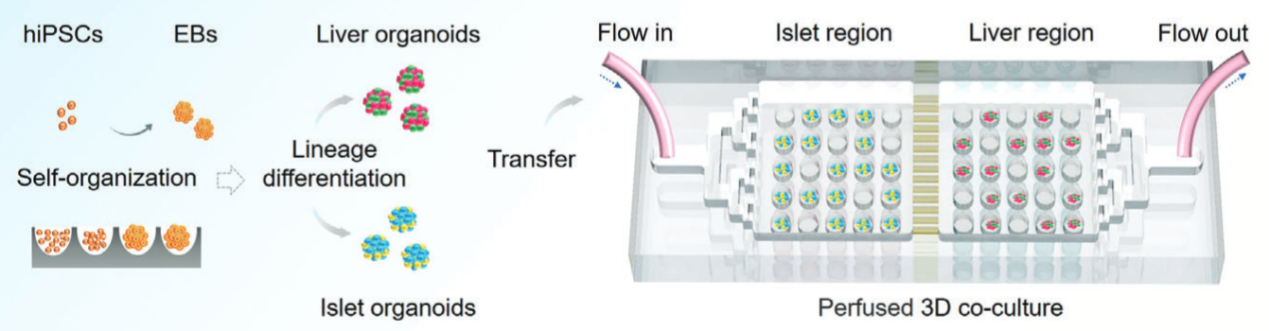
圖4. 在微孔設(shè)備中共培養(yǎng)肝臟和胰島類器官【18】
Takebe等人利用hPSC的三維分化方法產(chǎn)生多內(nèi)胚層結(jié)構(gòu)域,在前腸-中腸邊界形成了視黃酸依賴的肝膽胰臟器官結(jié)構(gòu),在體外實(shí)現(xiàn)了人肝-膽-胰(hepato-biliary-pancreatic, HBP)類器官的共培養(yǎng)【19】。
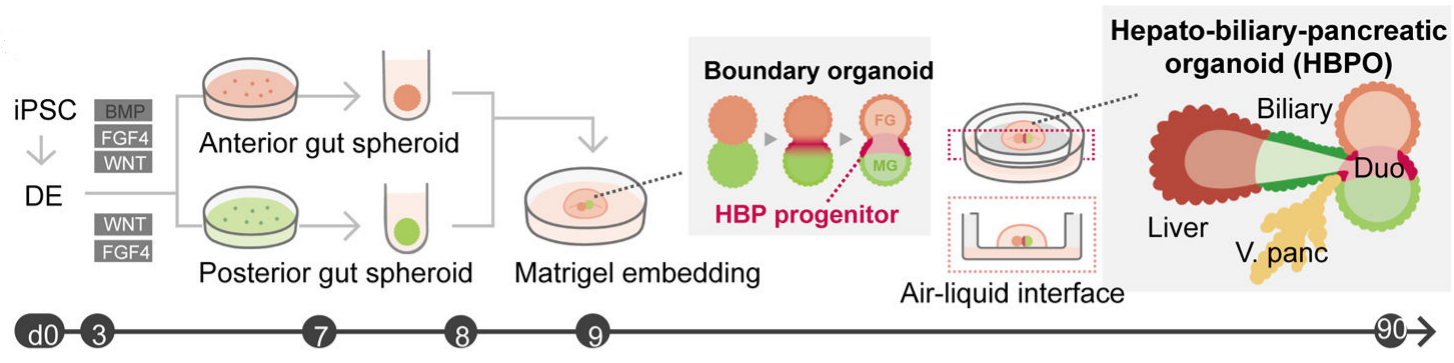
圖5. hPSC誘導(dǎo)分化為HBP類器官的原理圖【19】
近岸蛋白依靠專業(yè)的研發(fā)團(tuán)隊(duì),精心打造類器官驗(yàn)證平臺,致力于為廣大類器官客戶提供經(jīng)驗(yàn)證、高活性、可信任的類器官培養(yǎng)產(chǎn)品。近岸蛋白可提供自主研發(fā)生產(chǎn)的30余種類器官培養(yǎng)相關(guān)細(xì)胞因子,如Activin A、BMP-4、Wnt3a、R-Spondin、Noggin、EGF、FGFs等高活性、高穩(wěn)定性細(xì)胞因子,以及一系列類器官培養(yǎng)基,涵蓋腸癌、肺癌、肝癌、乳腺癌、胰腺癌、腎癌、卵巢癌等腫瘤類器官以及正常肝/肺類器官完全培養(yǎng)基,經(jīng)過類器官培養(yǎng)驗(yàn)證,專為類器官培養(yǎng)開發(fā),產(chǎn)品適用性高,已廣泛應(yīng)用于企業(yè)和科研院所,讓您的類器官培養(yǎng)更可控!
類器官培養(yǎng)細(xì)胞因子產(chǎn)品
|
類器官培養(yǎng)類型 |
相關(guān)因子 |
|
胃類器官 |
Activin A、BMP-4、EGF、FGF-4、FGF-10、Noggin、 R-spondin 1、Wnt3a
|
|
腸類器官 |
Activin A、BMP-4、EGF、FGF-4、Noggin、R-spondin 1、Wnt3a |
|
肝類器官 |
Activin A、BMP-4、BMP-7、FGF-7、FGF-10、FGF-19、HGF、OSM、R-Spondin 1 |
|
肺類器官 |
Activin A、FGF-4、FGF-7、FGF-10、Noggin、SHH、Wnt3a |
|
前列腺類器官 |
EGF、FGF-10、Noggin、R-spondin 1、Wnt-3a |
|
腦類器官 |
BDNF、EGF、FGF basic、GDNF、NT-3 |
|
內(nèi)耳類器官 |
BMP-4、FGF basic |
|
視網(wǎng)膜類器官 |
SHH、Wnt-3a |
|
乳腺類器官 |
EGF、FGF basic、FGF-7、FGF-10、Heregulinβ-1、Noggin、R-Spondin 1、R-Spondin 3、Wnt-3a |
|
腎臟類器官 |
BMP-2、BMP-4、BMP-7、FGF basic、FGF-9、Activin A、FGF-7、GDNF、R-Spondin 1 |
|
心臟類器官 |
Activin A、BMP-4、FGF basic、TGF-beta 1、Transferrin |
|
血管類器官 |
BMP-4、FGF basic、VEGF |
類器官培養(yǎng)基產(chǎn)品
|
目錄號 |
產(chǎn)品名稱 |
|
OCMHC01 |
Intestinal Cancer(腸癌)Organoid Culture Medium |
|
OCMHC02 |
Renal Cancer(腎癌)Organoid Culture Medium |
|
OCMHC03 |
Brain Glioma(腦膠質(zhì)瘤)Organoid Culture Medium |
|
OCMHC04 |
Liver Cancer(肝癌)Organoid Culture Medium |
|
OCMHC05 |
Lung Cancer(肺癌)Organoid Culture Medium |
|
OCMHC06 |
Breast Cancer(乳腺癌)Organoid Culture Medium |
|
OCMHC07 |
Gastric Cancer(胃癌) Organoid Culture Medium |
|
OCMHC08 |
Pancreatic Cancer(胰腺癌)Organoid Culture Medium |
|
OCMHC09 |
Esophageal cancer(食管癌)Organoid Culture Medium |
|
OCMHC10 |
Cervical carcinoma(宮頸癌)Organoid Culture Medium |
|
OCMHC11 |
Thyroid carcinoma(甲狀腺癌) Organoid Culture Medium |
|
OCMHC12 |
Prostatic cancer(前列腺癌) Organoid Culture Medium |
|
OCMHC13 |
Bladder Cancer(膀胱癌) Organoid Culture Medium |
|
OCMHC14 |
Ovarian Cancer (卵巢癌)Organoid Culture Medium |
|
OCMMN01 |
Mouse Intestinal (小鼠小腸)Organoid Culture Medium |
|
OCMMN02 |
Mouse Colonic (小鼠結(jié)腸)Organoid Culture Medium |
|
OCMHN01 |
Liver Organoid (肝擴(kuò)增)Expansion Medium |
|
OCMHN02 |
Liver Organoid (肝分化) Differentiation Medium |
|
OCMHN03 |
Lung Organoid (肺擴(kuò)增) Culture Medium |
參考文獻(xiàn)
【1】Takebe, T. et al. (2013). Vascularized and functional human liver from an iPSC-derived organ bud transplant. Nature, 499(7459), 481-484.
【2】Cui, K. et al. (2023). Engineering placenta‐like organoids containing endogenous vascular cells from human‐induced pluripotent stem cells. Bioengineering & Translational Medicine, 8(1), e10390.
【3】Pham, M. T. et al. (2018). Generation of human vascularized brain organoids. Neuroreport, 29(7), 588-593.
【4】Wimmer, R. A. et al. (2019). Human blood vessel organoids as a model of diabetic vasculopathy. Nature, 565(7740), 505-510.
【5】Al Bitar, S. et al. (2023). Molecular mechanisms targeting drug-resistance and metastasis in colorectal cancer: Updates and beyond. World Journal of Gastroenterology, 29(9), 1395.
【6】Ahn, Y. et al. (2021). Human blood vessel organoids penetrate human cerebral organoids and form a vessel-like system. Cells, 10(8), 2036.
【7】Wörsdörfer, P. et al. (2019). Generation of complex human organoid models including vascular networks by incorporation of mesodermal progenitor cells. Scientific reports, 9(1), 15663.
【8】Shi, Y. et al. (2020). Vascularized human cortical organoids (vOrganoids) model cortical development in vivo. PLoS biology, 18(5), e3000705.
【9】Low, J. H. et al. (2019). Generation of human PSC-derived kidney organoids with patterned nephron segments and a de novo vascular network. Cell stem cell, 25(3), 373-387.
【10】Mansour, A. A. et al. (2018). An in vivo model of functional and vascularized human brain organoids. Nature biotechnology, 36(5), 432-441.
【11】Yu, J. (2021). Vascularized organoids: a more complete model. International Journal of Stem Cells, 14(2), 127.
【12】Wimmer, R. A. et al. (2019). Generation of blood vessel organoids from human pluripotent stem cells. Nature protocols, 14(11), 3082-3100.
【13】Frenkel, N. et al. (2021). Long-lived human lymphatic endothelial cells to study lymphatic biology and Lymphatic Vessel/Tumor Coculture in a 3D Microfluidic Model. ACS Biomaterials Science & Engineering, 7(7), 3030-3042.
【14】Cakir, B. et al. (2019). Engineering of human brain organoids with a functional vascular-like system. Nature methods, 16(11), 1169-1175.
【15】Rajasekar, S. et al. (2020). IFlowPlate—A customized 384‐well plate for the culture of perfusable vascularized colon organoids. Advanced materials, 32(46), 2002974.
【16】Bonanini, F. et al. (2022). In vitro grafting of hepatic spheroids and organoids on a microfluidic vascular bed. Angiogenesis, 25(4), 455-470.
【17】Strobel, H. A. et al. (2023). Vascularized tissue organoids. Bioengineering, 10(2), 124.
【18】Tao, T. et al. (2022). Microengineered multi‐organoid system from hiPSCs to recapitulate human liver‐islet axis in normal and type 2 diabetes. Advanced Science, 9(5), 2103495.
【19】Koike, H., et al. (2019). Modelling human hepato-biliary-pancreatic organogenesis from the foregut–midgut boundary. Nature, 574(7776), 112-116.
