
在基因傳遞中,載體在DNA(親水,帶負(fù)電)通過(guò)細(xì)胞膜(疏水,帶負(fù)電)的過(guò)程中是必不可少的。此外,治療效率還取決于DNA有效地遞送到靶部位。由于系統(tǒng)中存在許多傳遞障礙,如細(xì)胞內(nèi)攝取、內(nèi)體逃逸、DNA釋放和核攝取等,以及細(xì)胞外屏障,如避免顆粒清除機(jī)制、靶向特定組織和/或感興趣的細(xì)胞、保護(hù)DNA免受降解等,因此開發(fā)一種高效且生物相容性好的基因傳遞系統(tǒng)非常重要。到目前為止,基因傳遞系統(tǒng)可分為兩大類,即病毒轉(zhuǎn)導(dǎo)系統(tǒng)和非病毒轉(zhuǎn)染系統(tǒng)。盡管病毒可用于基因傳遞,但其攜帶的DNA體積大、裝載能力低、大規(guī)模制造、質(zhì)量控制成本、免疫原性和潛在的致癌性等缺點(diǎn)限制了病毒載體在基因傳遞中的應(yīng)用。
因此,研究人員已將注意力轉(zhuǎn)向開發(fā)非病毒載體,作為傳遞基因的替代載體。非病毒傳遞系統(tǒng)有幾個(gè)明顯的優(yōu)點(diǎn),包括易于制備,適于聚合物性質(zhì)的合成操作, 細(xì)胞或組織靶向性,低免疫原性和致癌性,無(wú)病毒重組,不受攜帶DNA大小的限制,制造成本低。此外,非病毒載體由于其大小、電荷和結(jié)構(gòu)修飾載體的優(yōu)點(diǎn), 可以很容易地將遺傳物質(zhì)傳遞到靶細(xì)胞。
其中,納米材料是基因傳遞的理想材料,因?yàn)槠湮锢硇再|(zhì)使其適合于特定的功能。無(wú)機(jī)納米材料因其易于功能化、獨(dú)特的電學(xué)和光學(xué)特性、生物相容性以及低細(xì)胞毒性而備受追捧。磁性納米顆粒、金納米顆粒、量子點(diǎn)和碳納米管是常用的無(wú)機(jī)材料,用于傳遞基因。
磁性納米顆粒
磁感染是一種基于磁性納米顆粒(MNPs)與基因載體關(guān)聯(lián)的程序,可以在磁場(chǎng)存在下增強(qiáng)基因轉(zhuǎn)移。它最初是由Christian Plank和他的同事開發(fā)的,他們通過(guò)使用MNPs-DNA復(fù)合物或MNPs病毒載體復(fù)合物在細(xì)胞培養(yǎng)和體內(nèi)轉(zhuǎn)移基因。過(guò)程很簡(jiǎn)單:將MNPs-DNA復(fù)合物添加到貼壁細(xì)胞的培養(yǎng)物中,并將磁鐵靠近燒瓶或平板的底部,將磁性復(fù)合物吸引到底部,在那里它們與細(xì)胞密切接觸并被物理內(nèi)化,對(duì)內(nèi)吞攝取機(jī)制沒(méi)有任何特殊的磁力影響。在體內(nèi),在靶部位添加磁場(chǎng)會(huì)增加轉(zhuǎn)染量,并將治療基因靶向到體內(nèi)的特定器官/位置。一般來(lái)說(shuō),我們通過(guò)靜脈注射帶有治療基因的顆粒,并在靶部位施加高梯度的外部磁鐵來(lái)捕獲顆粒。一旦被捕獲,這些顆粒就會(huì)被滯留在目標(biāo)部位,然后被組織吸收。
金納米粒子
金納米顆粒(AuNPs)是一種穩(wěn)定、均勻、具有生物相容性的金屬納米顆粒,具有獨(dú)特的電子結(jié)構(gòu)、尺寸相關(guān)的強(qiáng)度顯示、高度可調(diào)的電子、磁性和光電子特性, 使其成為基因傳遞的理想選擇。此外,AuNPs的軟表面化學(xué)性質(zhì)使它們能夠與各種生物分子和配體進(jìn)行定制。例如,Klibanov等人將~2 kDa 聚乙烯亞胺(PEI)鏈共價(jià)連接到AuNPs上,將質(zhì)粒DNA載體傳遞到哺乳動(dòng)物細(xì)胞中。他們發(fā)現(xiàn),最有效的偶聯(lián)物在質(zhì)粒DNA傳遞方面的效率是未經(jīng)修飾的PEI對(duì)偶物的12倍(圖1)。AuNPs的另一個(gè)重要特征是其金屬核心構(gòu)建塊。這種結(jié)構(gòu)為治療材料提供了堅(jiān)實(shí)的支撐,使這些材料即使在無(wú)限稀釋后也能保持穩(wěn)定。
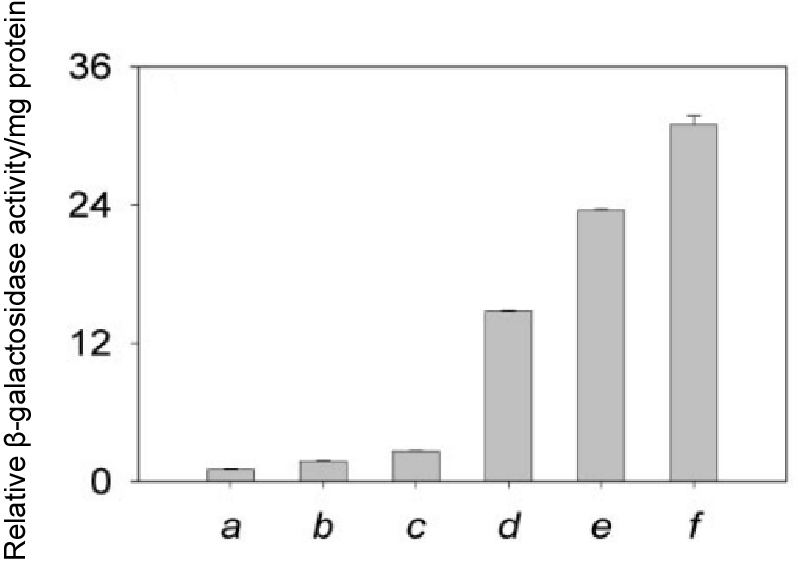
圖 1:在不同N/P比下,COS-7細(xì)胞培養(yǎng)中β-gal基因在血清存在下由PEI2(圖 a-c)和PEI2 - gnpii(圖 d- f)介導(dǎo)的表達(dá)程度。對(duì)于a,d,N/P=90; 對(duì)于b,e, N/P=120;對(duì)于c,f,N/P=150。
量子點(diǎn)
量子點(diǎn)(QD)是基于半導(dǎo)體的單分散納米晶體,可以通過(guò)膠體或等離子體合成機(jī)制等不同方法制備。由于其光學(xué)和電學(xué)性質(zhì),量子點(diǎn)是一種有吸引力的無(wú)機(jī)材料。量子點(diǎn)的大小與它們的吸收和基因傳遞效率直接相關(guān)。例如,Yang等人通過(guò)在單個(gè)點(diǎn)上涂覆PEI合成了多個(gè)QD(MQD)束。這些MQD結(jié)合編碼增強(qiáng)型綠色熒光蛋白(pEGFP)的質(zhì)粒DNA分子(pDNA),然后有效地將該pDNA傳遞到人間充質(zhì)干細(xì)胞(hMSCs)中。他們發(fā)現(xiàn),在幾個(gè)不同大小的QD中,QD655 是覆蓋PEI/pDNA的最大QD,轉(zhuǎn)染效率最高。QD655的熒光強(qiáng)度比使用QD525 的結(jié)果高60%(圖 2)。這表明使用量子點(diǎn)進(jìn)行基因傳遞是針對(duì)難以穿透的干細(xì)胞的另一種有吸引力的方法。
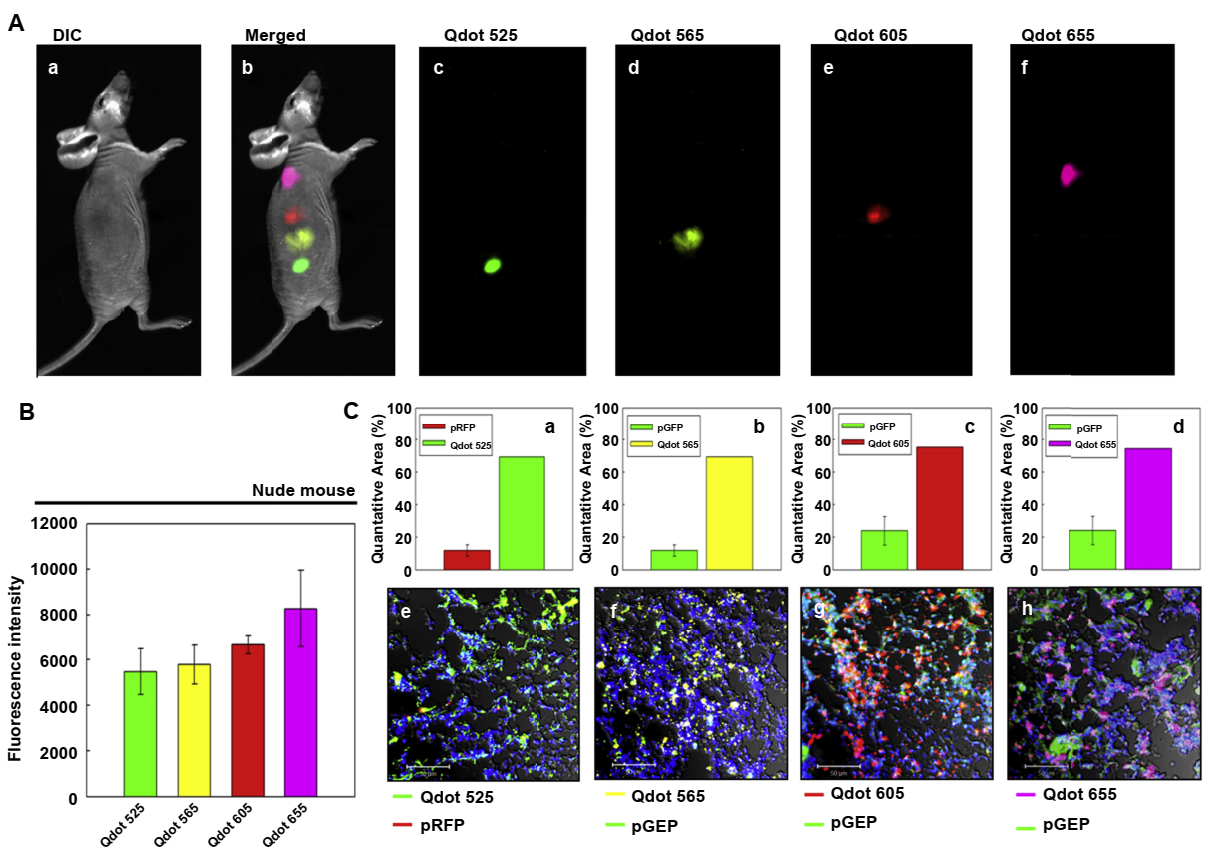
圖 2:多個(gè)QD捆綁NPs轉(zhuǎn)染hMSCs的裸鼠體內(nèi)生物成像。(A)皮下注射多個(gè)
QD捆綁NPs轉(zhuǎn)染hMSCs的小鼠體內(nèi)光學(xué)成像:a)對(duì)照組,b)合并圖像,c- f)移植區(qū)域圖像,c)多個(gè)QD525捆綁NPs,d)多個(gè)QD565捆綁NPs,e)多個(gè)QD605捆綁NPs,f)多個(gè)QD655捆綁NPs與pDNA復(fù)合物;(B)(A)中熒光信號(hào)的定量;(C)多個(gè)QD捆綁NPs轉(zhuǎn)染hMSCs移植區(qū)熒光信號(hào)(a-d)和共聚焦熒光圖像(e-h)的定量:多個(gè)QD525捆綁NPs(a和e),多個(gè)QD565捆綁NPs(b和f),多個(gè)QD605捆綁NPs(c和g),多個(gè)QD655捆綁NPs處理組(d和h)。
碳納米管
考慮到缺乏對(duì)內(nèi)源性酶的穩(wěn)定性,較差的藥代動(dòng)力學(xué)特征,以及固有的無(wú)法橫過(guò)質(zhì)膜的能力,它對(duì)核酸在體內(nèi)的治療遞送是一個(gè)挑戰(zhàn)。碳納米管(Carbon nanotubes,CNTs)已被廣泛應(yīng)用,包括用于基因治療的核酸遞送。CNTs需要對(duì)其外表面進(jìn)行化學(xué)調(diào)整,以便在各種應(yīng)用中最大限度地發(fā)揮其獨(dú)特的性能。CNTs 具有獨(dú)特的長(zhǎng)徑比,是化學(xué)功能化策略和生物相容性的理想模板,這使其成為分子轉(zhuǎn)運(yùn)系統(tǒng)的有希望的候選者。此外,經(jīng)過(guò)表面功能化后,CNTs在水介質(zhì)中的溶解度增加, 在體內(nèi)和體外的生物相容性和傳遞核酸的傾向都得到改善。因此,具有表面修飾的CNTs是一系列核酸的理想遞送系統(tǒng)。Munk等人評(píng)估了羧酸功能化多壁碳納米管(COOH-MWCNTs)的細(xì)胞毒性及其將編碼綠色熒光蛋白基因的質(zhì)粒 DNA傳遞到牛原代成纖維細(xì)胞的用途。流式細(xì)胞術(shù)細(xì)胞活力結(jié)果顯示低濃度COOH-MWCNTs 的無(wú)毒性。拉曼光譜的頻移表明質(zhì)粒DNA與納米材料相連。熒光成像、流式細(xì)胞術(shù)和PCR分析證實(shí)COOH-MWCNT成功將pDNA 導(dǎo)入原代成纖維細(xì)胞。結(jié)果表明,COOH-MWCNTs是將DNA遞送到難以轉(zhuǎn)染的原代牛細(xì)胞的有吸引力的替代方案。
參考文獻(xiàn)
1.KC, R. B., Thapa, B., & Bhattarai, N. (2014). Gold nanoparticle-based gene delivery: promises and challenges.?Nanotechnology Reviews, 3(3), 269-280.?https://doi.org/10.1515/ntrev-2013-0026
2.Majidi, S., Zeinali Sehrig, F., Samiei, M., Milani, M., Abbasi, E., Dadashzadeh, K., & Akbarzadeh, A. (2016). Magnetic nanoparticles: Applications in gene delivery and gene therapy.?Artificial cells, nanomedicine, and biotechnology, 44(4), 1186-1193.?https://doi.org/10.3109/21691401.2015.1014093
3.Prabu, S. L., Suriyaprakash, T. N. K., & Thirumurugan, R. (2017). Medicated nanoparticle for gene delivery. In Advanced Technology for Delivering Therapeutics. IntechOpen.?http:/1dx.doi.org/10.5772/65709
4.Thomas, M., & Klibanov, A. M. (2003). Conjugation to gold nanoparticles enhances polyethylenimine's transfer of plasmid DNA into mammalian cells.?Proceedings of the National Academy of Sciences, 100(16), 9138-9143.?https://doi.org/10.1073/pnas.1233634100
5.Bates, K., & Kostarelos, K. (2013). Carbon nanotubes as vectors for gene therapy: past achievements, present challenges and future goals.?Advanced drug delivery reviews, 65(15), 2023-2033.?https://doi.org/10.1016/j.addr.2013.10.003
6.Riley, M. K., & Vermerris, W. (2017). Recent advances in nanomaterials for gene delivery—a review.?Nanomaterials, 7(5), 94.?https://doi.org/10.3390/nano7050094
7.Yang, H. N., Park, J. S., Jeon, S. Y., Park, W., Na, K., & Park, K. H. (2014). The effect of quantum dot size and poly (ethylenimine) coating on the efficiency of gene delivery into human mesenchymal stem cells.?Biomaterials, 35(29), 8439-8449.?https://doi.org/10.1016/j.biomaterials.2014.06.024
8.Munk, M., Zanette, R. D. S. S., de Almeida Camargo, L. S., de Souza, N. L. G. D., de Almeida, C. G., Gern, J. C., ... & de Mello Brand?o, H. (2017). Using carbon nanotubes to deliver genes to hard-to-transfect mammalian primary fibroblast cells.?Biomedical Physics & Engineering Express, 3(4), 045002.?https://iopscience.iop.org/article/10.1088/2057-1976/aa7927/meta
阿拉丁提供相關(guān)產(chǎn)品,產(chǎn)品詳情請(qǐng)見阿拉丁官網(wǎng):Nanoparticle-Based Gene Delivery (aladdin-e.com)
