原發(fā)性硬化性膽管炎(PSC)是一種免疫介導(dǎo)的膽汁淤積性肝病,目前尚無(wú)有效藥物治療,約有70%的PSC患者同時(shí)罹患炎癥性腸病(IBD),提示腸肝共病。目前,已有大量研究證實(shí),TH17細(xì)胞及其分泌的IL-17A是PSC和IBD共同的關(guān)鍵致病因素:患者體內(nèi)TH17比例升高,可轉(zhuǎn)分化為更具破壞力的“TH17”,從而加劇腸黏膜屏障損傷與炎癥。24-去甲熊去氧膽酸(NorUDCA)是一種已進(jìn)入III期臨床的新型膽汁酸,已在PSC患者中顯示改善膽汁淤積的療效;在之前的研究中,發(fā)現(xiàn)NorUDCA可以通過(guò)抑制mTORC1信號(hào)重塑CD8?T細(xì)胞代謝。考慮到mTORC1也是TH17分化與功能的核心調(diào)控節(jié)點(diǎn),作者推測(cè)NorUDCA可能具有調(diào)節(jié)TH17致病性并緩解腸道炎癥的潛力。基于此,來(lái)自維也納醫(yī)科大學(xué)等單位的研究人員在Gut期刊上發(fā)表了一篇題為“24-Nor-ursodeoxycholic acid improves intestinal inflammation by targeting TH17 pathogenicity and transdifferentiation”的研究論文,圍繞“NorUDCA通過(guò)調(diào)控TH17細(xì)胞致病性及轉(zhuǎn)分化改善腸道炎癥”的核心命題,采用“體內(nèi)模型驗(yàn)證→機(jī)制解析→轉(zhuǎn)化驗(yàn)證”的技術(shù)路線,系統(tǒng)探究了NorUDCA的作用及分子機(jī)制。

技術(shù)路線圖
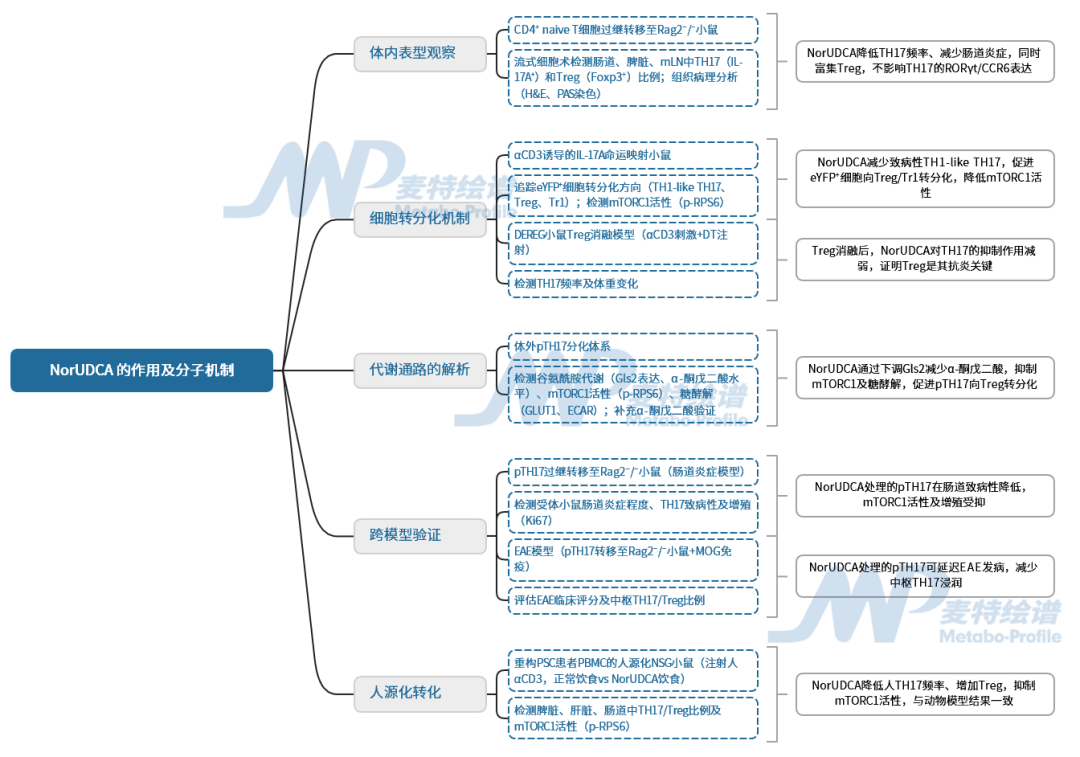
研究結(jié)果
1、體內(nèi)表型觀察
體內(nèi)表型觀察通過(guò)CD4+初始T細(xì)胞過(guò)繼轉(zhuǎn)移模型開(kāi)展。研究將CD4+初始T細(xì)胞轉(zhuǎn)移到Rag2?/?小鼠,分“標(biāo)準(zhǔn)飼料組”和“0.5% NorUDCA”飼料組,8周后做檢測(cè)。檢測(cè)結(jié)果顯示,NorUDCA組的血清膽汁酸升高,mLN、脾臟縮小,結(jié)腸更長(zhǎng);腸道白細(xì)胞浸潤(rùn)減少,結(jié)構(gòu)和黏液屏障保留;腸道及淋巴器官中TH17頻率降低、Treg升高,但Treg絕對(duì)數(shù)不變;TH17的RORγt和CCR6表達(dá)未受影響。表明NorUDCA可通過(guò)調(diào)節(jié)TH17和Treg比例減輕腸道炎癥,這個(gè)過(guò)程不影響TH17分化或遷移。
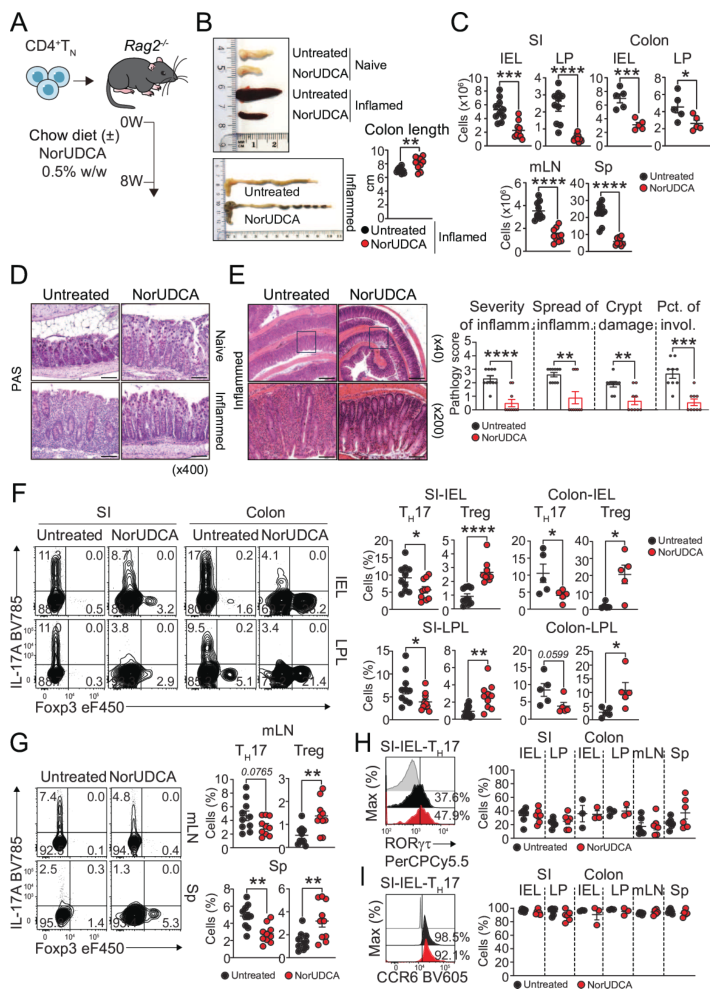
圖1. NorUDCA在CD4+初始T細(xì)胞過(guò)繼轉(zhuǎn)移模型中降低多組織TH17頻率并富集Treg
2、細(xì)胞轉(zhuǎn)分化機(jī)制研究
細(xì)胞轉(zhuǎn)分化部分通過(guò)兩個(gè)模型探究NorUDCA對(duì)TH17細(xì)胞命運(yùn)的調(diào)控。首先是αCD3誘導(dǎo)的IL-17A命運(yùn)映射小鼠模型(IL-17ACreR26R-eYFP),腹腔注射αCD3后,小鼠分食“標(biāo)準(zhǔn)飼料”或“NorUDCA飼料”,100小時(shí)后檢測(cè)。檢測(cè)結(jié)果顯示,NorUDCA減輕腸道水腫和淋巴細(xì)胞浸潤(rùn),降低效應(yīng)TH17(IL-17A+eYFP+)及總eYFP+細(xì)胞頻率,減少致病性TH1樣TH17(IL-17A+IFN-γ+)生成,同時(shí)提高Tr1細(xì)胞(CD49b+Lag3+)和Treg比例,eYFP+細(xì)胞IL-10表達(dá)增加。且NorUDCA誘導(dǎo)的Treg源自exTH17細(xì)胞和未表達(dá)IL-17A的CD4+T細(xì)胞,eYFP+細(xì)胞mTORC1活性(p-RPS6)受抑。
另一個(gè)是DEREG小鼠Treg消融模型,αCD3刺激后注射白喉毒素耗竭Treg,發(fā)現(xiàn)NorUDCA對(duì)TH17的抑制作用減弱,體重丟失更嚴(yán)重。綜上,NorUDCA可抑制TH17向致病性表型轉(zhuǎn)分化,促進(jìn)其向抗炎性Treg/Tr1轉(zhuǎn)化,且Treg誘導(dǎo)是其抗炎的關(guān)鍵機(jī)制。
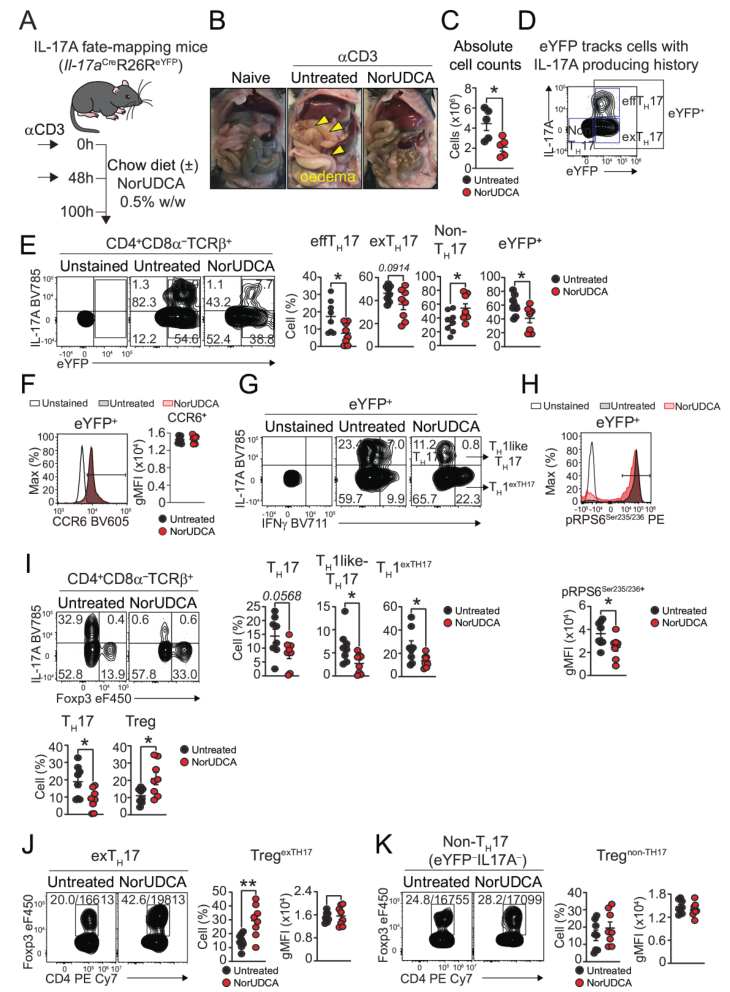
圖2. 在αCD3模型中,NorUDCA靶向體內(nèi)TH17致病性及轉(zhuǎn)分化
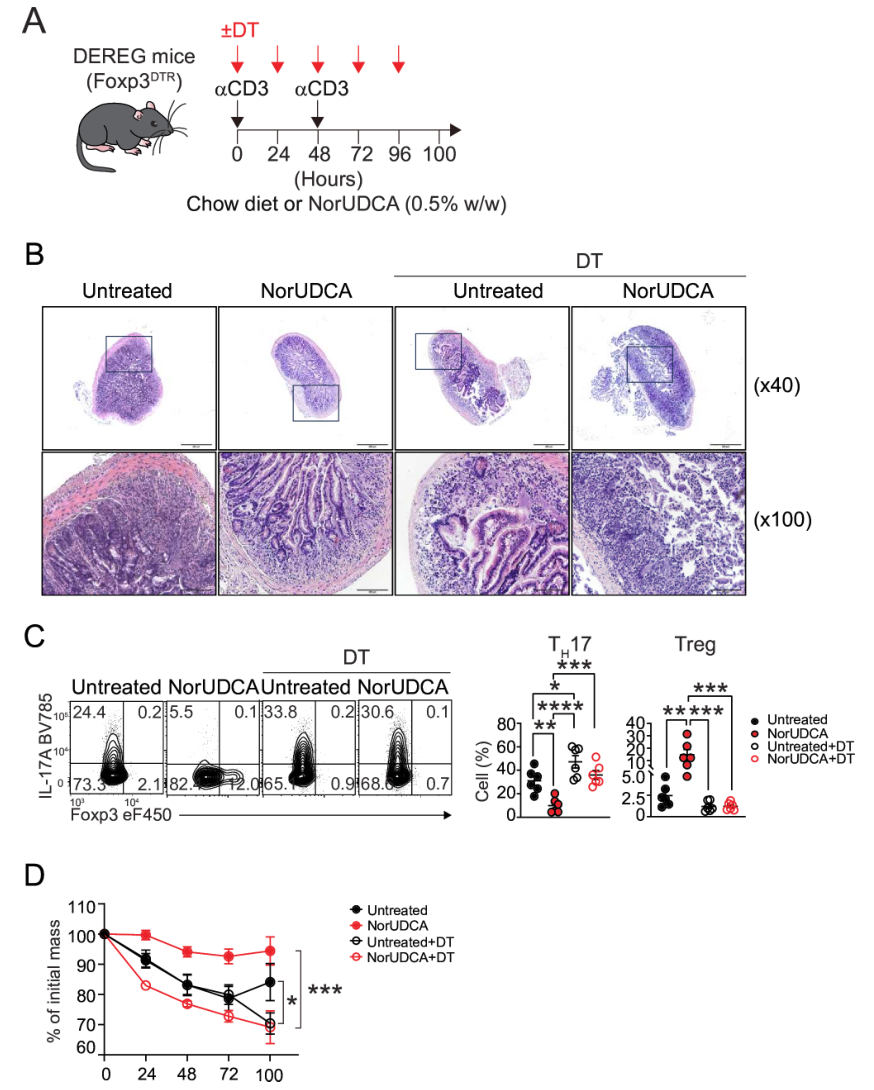
圖3. Treg誘導(dǎo)是NorUDCA在體內(nèi)限制TH17致病性的關(guān)鍵
3、代謝通路解析
代謝通路解析部分以體外致病性TH17(pTH17)分化體系為核心模型,深入探究NorUDCA通過(guò)代謝調(diào)控影響細(xì)胞命運(yùn)的分子機(jī)制。實(shí)驗(yàn)以小鼠CD4+初始T細(xì)胞為起始材料,在體外誘導(dǎo)其分化為pTH17細(xì)胞,設(shè)置NorUDCA處理組與對(duì)照組,結(jié)合多組學(xué)、靶向代謝組學(xué)、代謝物檢測(cè)及功能驗(yàn)證實(shí)驗(yàn)展開(kāi)分析。
結(jié)果顯示,NorUDCA主要通過(guò)靶向“谷氨酰胺-mTORC1-糖酵解”軸調(diào)控細(xì)胞命運(yùn):其一,抑制谷氨酰胺代謝,下調(diào)谷氨酰胺酶Gls2的表達(dá),減少谷氨酰胺向谷氨酸的轉(zhuǎn)化及α-酮戊二酸的生成,而谷氨酰胺轉(zhuǎn)運(yùn)體ASCT2的表達(dá)未受影響,說(shuō)明其主要作用于代謝過(guò)程而非攝取環(huán)節(jié);其二,抑制mTORC1活性,通過(guò)降低下游靶蛋白磷酸化RPS6的水平,減弱該信號(hào)通路的激活;其三,抑制糖酵解,下調(diào)糖酵解關(guān)鍵調(diào)控因子Hif1α和c-Myc,減少葡萄糖轉(zhuǎn)運(yùn)體GLUT1的表達(dá),降低葡萄糖攝取能力(通過(guò)2-NBDG熒光標(biāo)記檢測(cè)),并降低細(xì)胞外酸化率(ECAR),表明糖酵解活性受抑。
同時(shí),NorUDCA可促進(jìn)pTH17向功能性Treg轉(zhuǎn)化,短期處理即可減少pTH17的IL-17A分泌,提高Foxp3+Treg的比例,且這些Treg能有效抑制pTH17的增殖。補(bǔ)充細(xì)胞可通透的α-酮戊二酸可逆轉(zhuǎn)上述效應(yīng),恢復(fù)mTORC1活性、GLUT1表達(dá)及IL-17A分泌,進(jìn)一步證實(shí)谷氨酰胺-mTORC1-糖酵解軸是NorUDCA調(diào)控pTH17與Treg細(xì)胞命運(yùn)平衡的關(guān)鍵靶點(diǎn)。
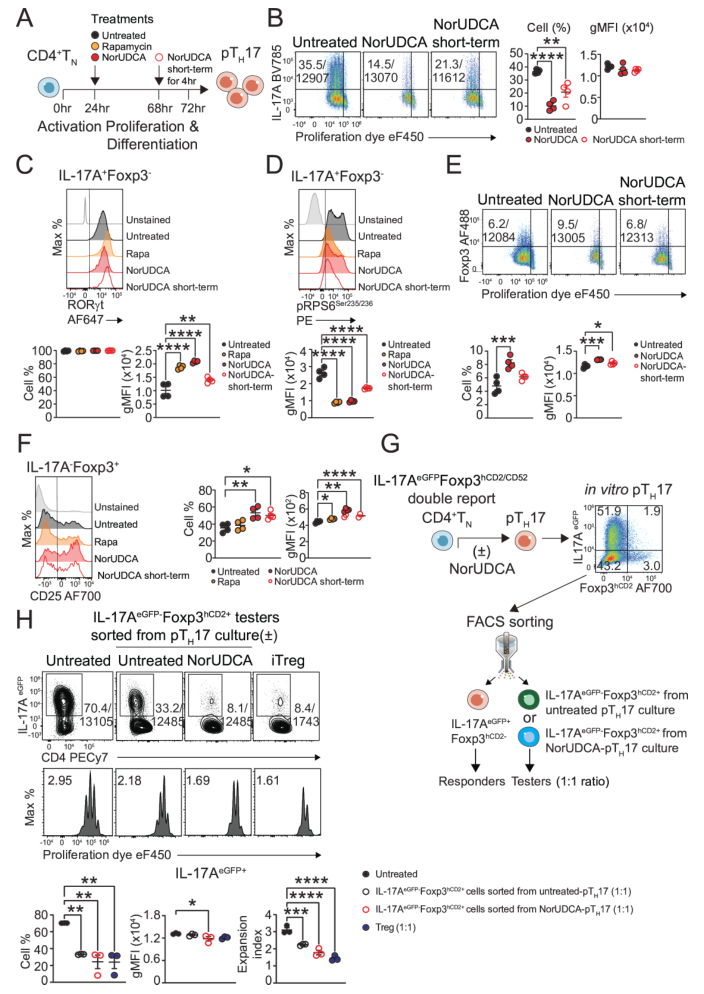
圖4. NorUDCA在體外抑制致病性TH17分化并促進(jìn)功能性抑制性Treg生成
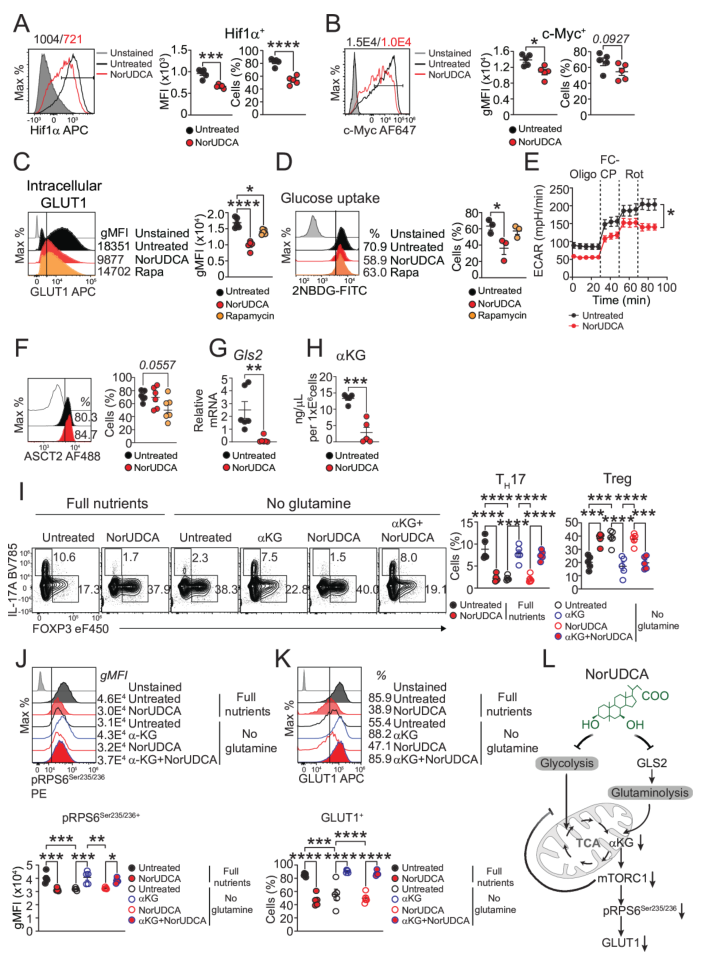
圖5. NorUDCA通過(guò)限制谷氨酰胺代謝抑制pTH17細(xì)胞中mTORC1激活及糖酵解
4、跨模型驗(yàn)證
跨模型驗(yàn)證通過(guò)兩種過(guò)繼轉(zhuǎn)移模型驗(yàn)證NorUDCA對(duì)致病性TH17(pTH17)的調(diào)控作用。首先是腸道炎癥模型:將體外誘導(dǎo)的pTH17經(jīng)NorUDCA短期處理后,轉(zhuǎn)移至Rag2?/?小鼠,4周后發(fā)現(xiàn),處理組小鼠腸道水腫減輕,腸道上皮內(nèi)TH17頻率降低、Treg頻率升高,且TH17的mTORC1活性(p-RPS6)和增殖能力(Ki67)受抑,CCR6表達(dá)未變(排除遷移影響)。
其次是實(shí)驗(yàn)性自身免疫性腦脊髓炎(EAE)模型:將TCR2D2pTH17經(jīng)NorUDCA處理后轉(zhuǎn)移至Rag2?/?小鼠并誘導(dǎo)EAE,結(jié)果顯示處理組疾病發(fā)作延遲、癥狀減輕,中樞神經(jīng)系統(tǒng)中TH17減少、Treg增加,TH17的Ki67表達(dá)降低,遷移標(biāo)志物CCR6、CXCR3未受影響。綜上,NorUDCA短期處理可通過(guò)T細(xì)胞內(nèi)在機(jī)制,長(zhǎng)期抑制pTH17在腸道及中樞的致病性,為其跨組織抗炎作用提供依據(jù)。
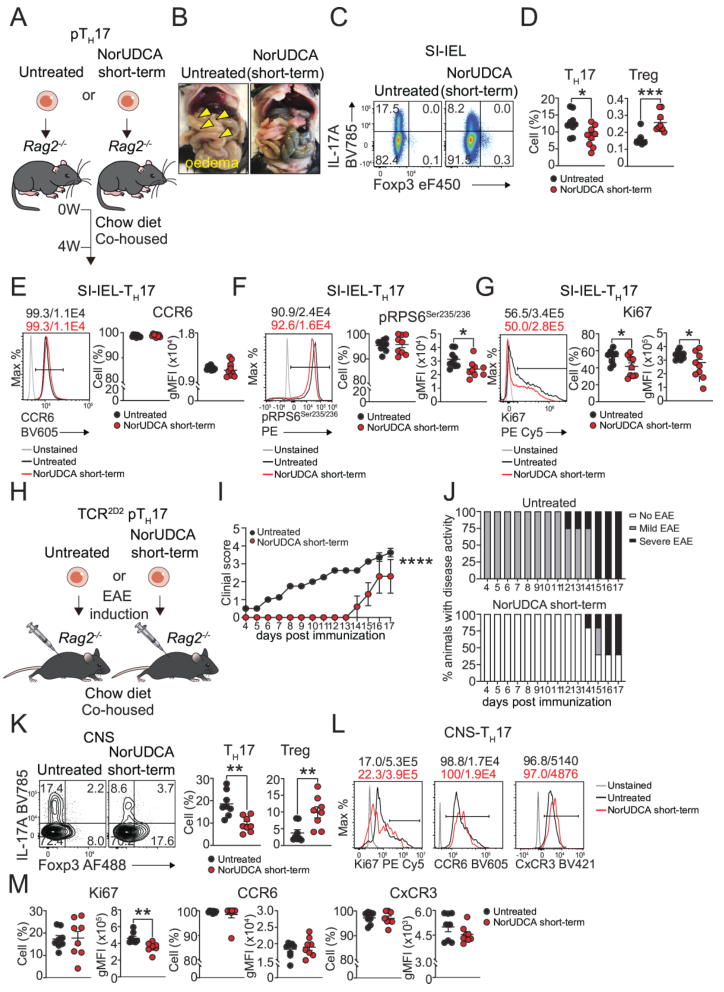
圖6. 經(jīng)NorUDCA短期處理的pTH17細(xì)胞在體內(nèi)轉(zhuǎn)移后致病性及增殖能力降低
5、人源化轉(zhuǎn)化
人源化轉(zhuǎn)化研究采用重構(gòu)PSC患者PBMC的人源化NSG小鼠模型。小鼠接受人αCD3抗體刺激后,分食“標(biāo)準(zhǔn)飼料”或“NorUDCA飼料”。結(jié)果顯示,NorUDCA組腸道水腫減輕,脾臟、肝臟及腸道的免疫細(xì)胞浸潤(rùn)減少。流式檢測(cè)發(fā)現(xiàn),其脾臟、肝臟、小腸和結(jié)腸中TH17頻率降低,Treg頻率升高,且TH17的mTORC1活性(p-RPS6)和增殖能力(Ki67)受抑。該結(jié)果與動(dòng)物模型一致,證實(shí)NorUDCA可抑制人TH17炎癥,為臨床應(yīng)用提供依據(jù)。
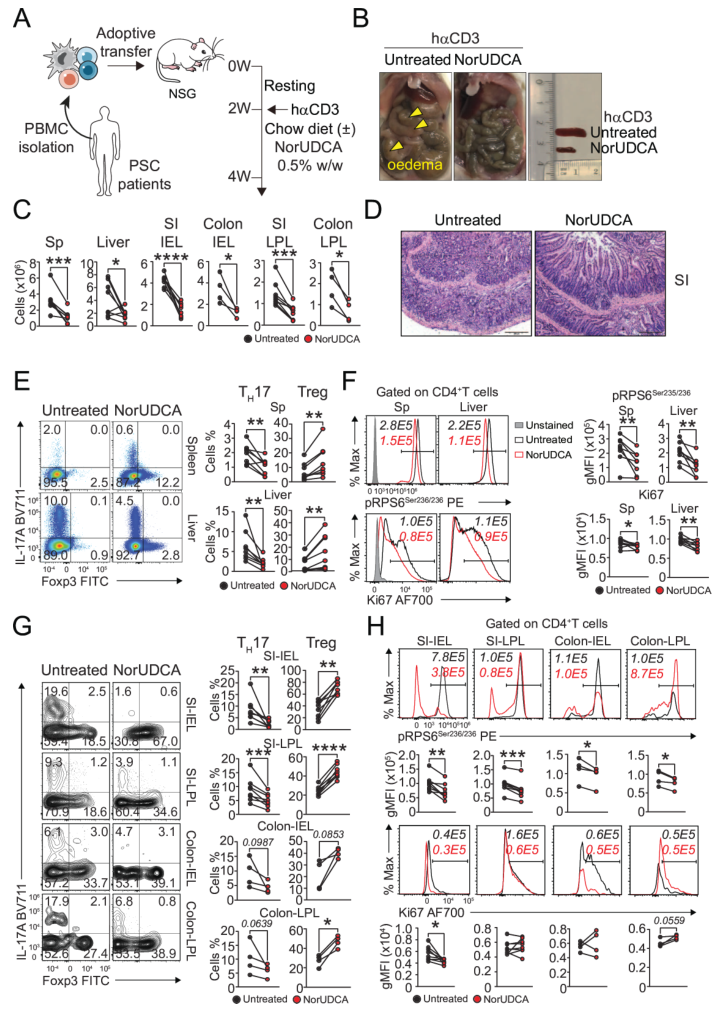
圖7. 在重構(gòu)PSC患者PBMC的人源化NSG模型中,NorUDCA抑制TH17炎癥
研究結(jié)論
本研究成功搭建起小鼠實(shí)驗(yàn)與臨床應(yīng)用的橋梁,證實(shí)了 NorUDCA 能夠糾正原發(fā)性硬化性膽管炎(PSC)患者膽管細(xì)胞中存在的系統(tǒng)性 T 細(xì)胞相關(guān)異常。雖然NorUDCA 早已在部分肝病治療中嶄露頭角,此次研究更讓我們看到它的新可能 —— 未來(lái)或許能為 PSC 相關(guān)腸道炎癥的治療開(kāi)辟全新方向。
參考文獻(xiàn)
24-Nor-ursodeoxycholic acid improves intestinal inflammation by targeting TH17 pathogenicity and transdifferentiation. Gut. 2025
繪譜幫你測(cè)
經(jīng)歷了千百年的相持后,我們終于看到了戰(zhàn)勝貧困的曙光。勝利在向我們招手,更加美好的未來(lái)需要我們共同創(chuàng)造。麥特繪譜開(kāi)創(chuàng)性地搭建了醫(yī)學(xué)領(lǐng)域高端代謝組學(xué)技術(shù)平臺(tái),覆蓋了非靶向-全定量-代謝流等全方位的高端醫(yī)學(xué)代謝組解決方案,同時(shí)全面布局微生物組學(xué)、轉(zhuǎn)錄組學(xué)和蛋白質(zhì)組學(xué)等多組學(xué)技術(shù)服務(wù),已成為全球多組學(xué)研究者的優(yōu)選合作伙伴。麥特繪譜已為數(shù)百家三甲醫(yī)院、科研院所和企業(yè)提供多組學(xué)一站式整體解決方案,協(xié)助客戶與合作伙伴發(fā)表SCI文章600+篇,累計(jì)影響因子6000+,平均IF>10,涵蓋Cell, Science, Nature, Cancer Cell, Signal Trans-duction and Targeted Therapy, Nature Biotechnology, Cell Metabolism等權(quán)威期刊。
