腦白質(zhì)損傷指中樞神經(jīng)系統(tǒng)中一個(gè)或多個(gè)區(qū)域軸突、少突膠質(zhì)細(xì)胞和髓鞘的進(jìn)行性變性。隨著人口老齡化,中老年人群中腦白質(zhì)損傷的發(fā)生率逐步增加。研究表明,腦白質(zhì)損傷與認(rèn)知功能障礙高度相關(guān),尤其是工作記憶的下降。因此,腦白質(zhì)損傷也被認(rèn)為是認(rèn)知障礙一級(jí)預(yù)防和癡呆二級(jí)預(yù)防的治療靶點(diǎn)。而慢性腦缺血是腦白質(zhì)損傷的主要原因,腦小血管病及頸動(dòng)脈狹窄等多種腦大血管病變和腦小血管病變均會(huì)引起白質(zhì)損傷。鑒于損傷過程的復(fù)雜性,目前尚無有效的臨床治療方案。因此,針對(duì)慢性缺血性腦白質(zhì)損傷的治療是亟待研究的新領(lǐng)域。

近日,來自南京大學(xué)醫(yī)學(xué)院附屬鼓樓醫(yī)院的徐運(yùn)團(tuán)隊(duì)在Advanced Science上在線發(fā)表了題為“Optogenetic Stimulation of mPFC Alleviates White Matter Injury-Related Cognitive Decline after Chronic Ischemia through Adaptive Myelination”的工作。團(tuán)隊(duì)基于“適應(yīng)性髓鞘形成”理論,提出了治療慢性缺血性腦白質(zhì)損傷的新策略,揭示了神經(jīng)活性調(diào)控在腦白質(zhì)損傷及相關(guān)認(rèn)知障礙中的治療潛力。
研究思路及方法
1.適應(yīng)性髓鞘形成
神經(jīng)元和髓鞘之間存在著密切的聯(lián)系。近年來研究表明,神經(jīng)元活性能夠影響少突系細(xì)胞的譜系進(jìn)展并調(diào)控髓鞘形成,即適應(yīng)性髓鞘形成。然而,目前適應(yīng)性髓鞘形成相關(guān)的研究多見于發(fā)育和急性脫髓鞘疾病,在慢性腦缺血中,增加神經(jīng)元活性能否促進(jìn)腦白質(zhì)修復(fù)目前仍不清楚。
2.激活BCAS小鼠內(nèi)側(cè)前額葉皮層谷氨酸能神經(jīng)元改善工作記憶
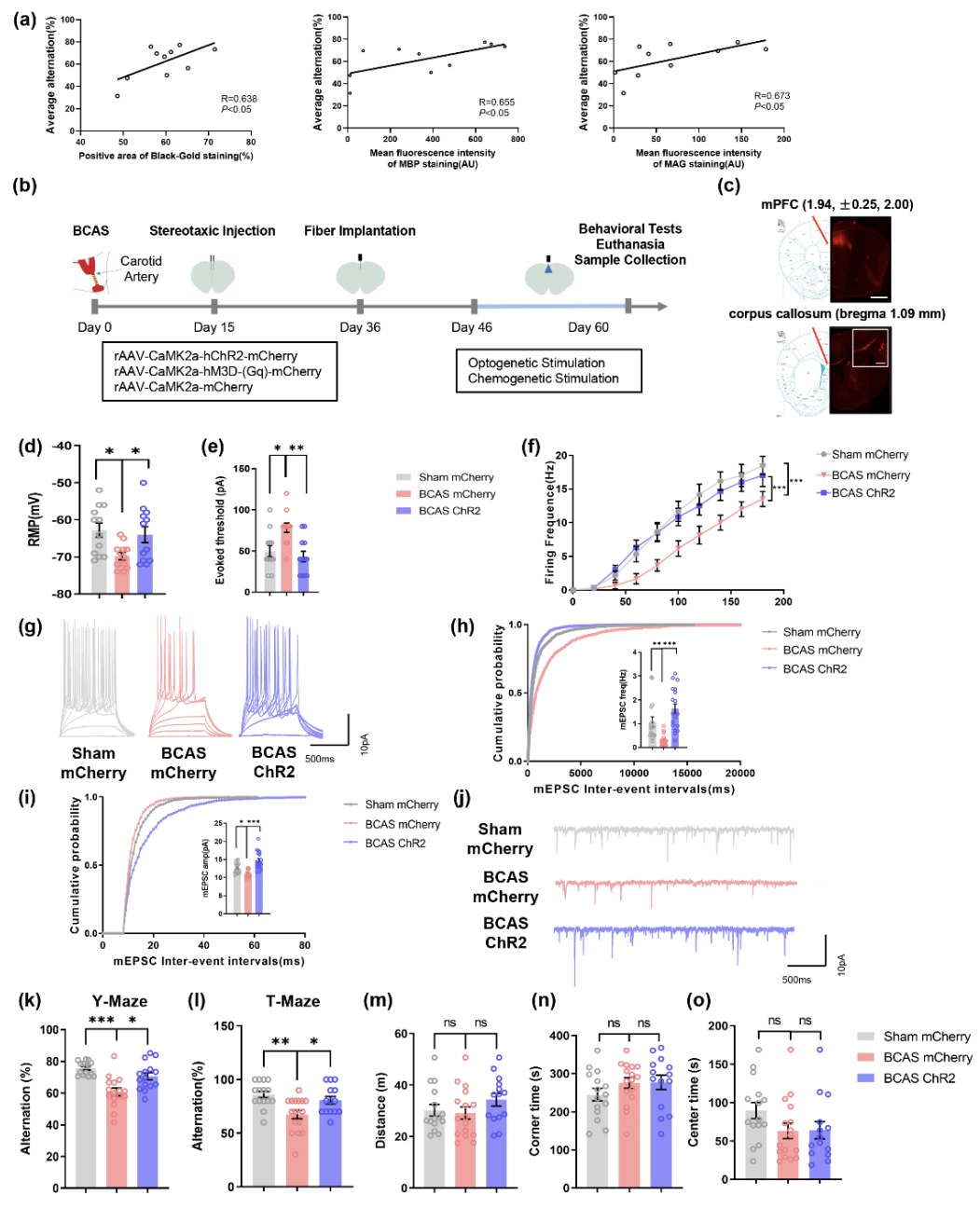
我們采用野生型(WT)小鼠制備雙側(cè)頸動(dòng)脈狹窄(BCAS)模型發(fā)現(xiàn),造模后2個(gè)月小鼠出現(xiàn)認(rèn)知功能障礙及白質(zhì)損傷,且認(rèn)知功能下降程度與白質(zhì)損傷程度呈正相關(guān)。隨后,通過病毒示蹤技術(shù),我們發(fā)現(xiàn)小鼠內(nèi)側(cè)前額葉皮層(mPFC)谷氨酸能神經(jīng)元發(fā)出的神經(jīng)纖維投射經(jīng)過胼胝體。
基于此,我們利用光遺傳學(xué)及化學(xué)遺傳學(xué)技術(shù)調(diào)控BCAS小鼠mPFC谷氨酸能神經(jīng)元的活性。在BCAS模型46天后,對(duì)目的神經(jīng)元進(jìn)行連續(xù)15天的刺激。電生理檢測(cè)結(jié)果顯示,相比于假手術(shù)(Sham)小鼠,BCAS小鼠mPFC谷氨酸能神經(jīng)元活性降低,而光/化學(xué)遺傳學(xué)刺激提高了BCAS小鼠mPFC谷氨酸能神經(jīng)元活性。采用Y迷宮和T迷宮對(duì)工作記憶進(jìn)行檢測(cè),發(fā)現(xiàn)BCAS后小鼠工作記憶出現(xiàn)障礙,而激活mPFC谷氨酸能神經(jīng)元顯著改善BCAS小鼠工作記憶。此外,曠場(chǎng)實(shí)驗(yàn)表明,BCAS造模及光/化學(xué)遺傳學(xué)刺激不影響小鼠的情緒及運(yùn)動(dòng)功能。
3.激活BCAS小鼠mPFC谷氨酸能神經(jīng)元改善腦白質(zhì)損傷
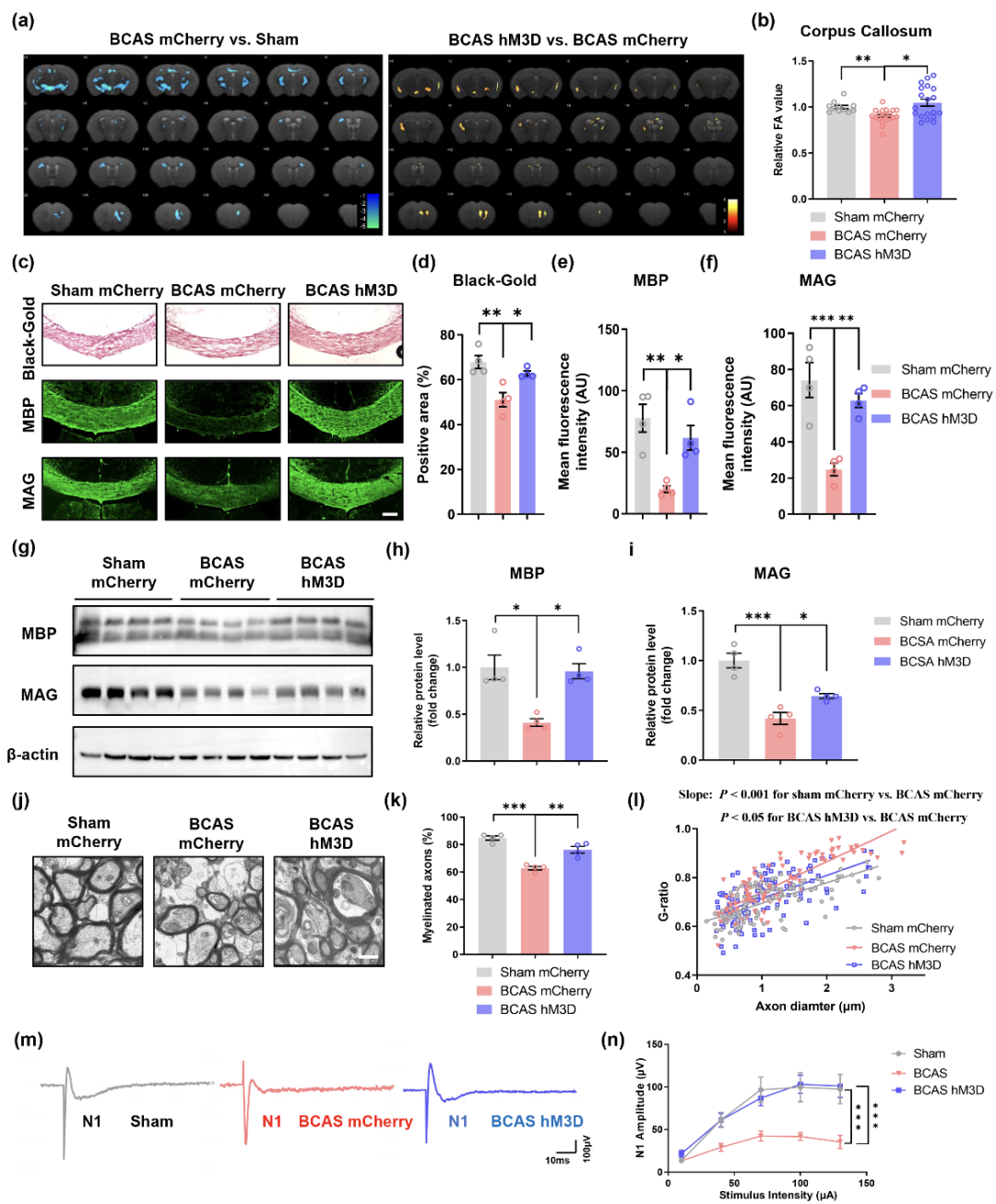
隨后,我們分別采用黑金染色、免疫熒光和Western blot技術(shù)檢測(cè)胼胝體區(qū)域的白質(zhì)完整性,發(fā)現(xiàn)相較于Sham小鼠,BCAS小鼠出現(xiàn)白質(zhì)損傷,神經(jīng)元的激活則改善了BCAS小鼠的脫髓鞘病變。利用透射電鏡檢測(cè)胼胝體區(qū)域髓鞘厚度,發(fā)現(xiàn)神經(jīng)元活性的提升改善了慢性腦缺血引起的髓鞘厚度減低。采用磁共振成像檢測(cè),發(fā)現(xiàn)BCAS造模后小鼠胼胝體區(qū)域各向異性分?jǐn)?shù)(FA)降低,化學(xué)遺傳學(xué)刺激提高了BCAS小鼠的FA值。通過胼胝體復(fù)合動(dòng)作電位檢測(cè)發(fā)現(xiàn),化學(xué)遺傳學(xué)刺激改善了BCAS小鼠的軸突傳導(dǎo)速率損傷。
4.激活BCAS小鼠mPFC谷氨酸能神經(jīng)元促進(jìn)少突膠質(zhì)前體細(xì)胞分化
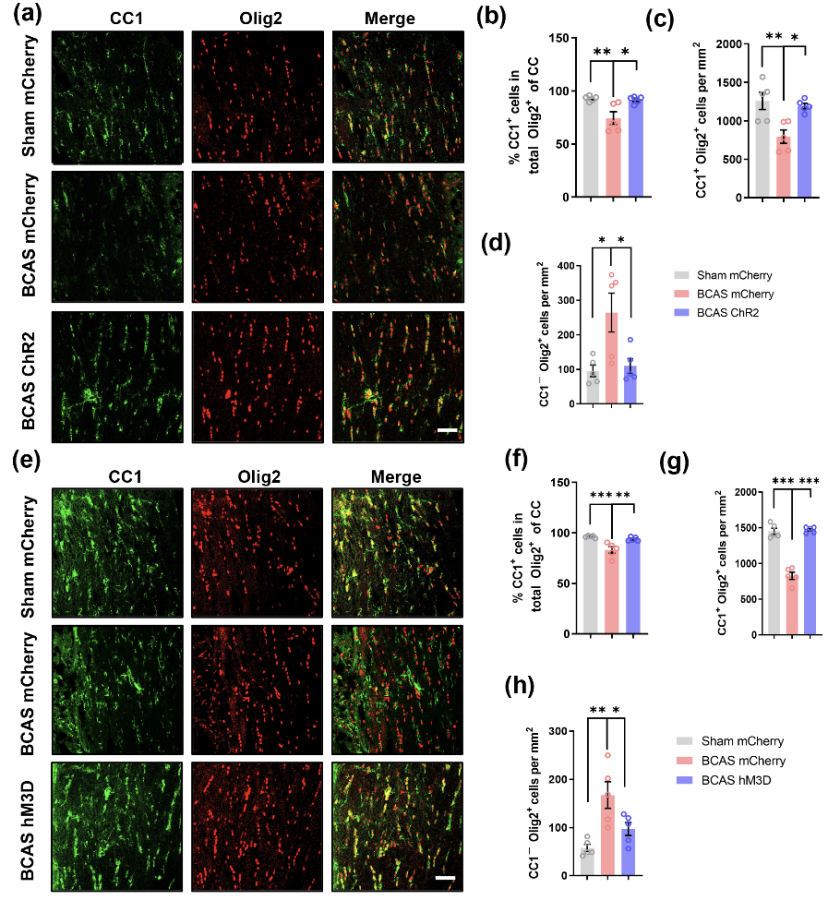
為了進(jìn)一步研究腦白質(zhì)改善與少突膠質(zhì)細(xì)胞譜系進(jìn)展的關(guān)系,利用免疫熒光技術(shù)分別標(biāo)記少突系細(xì)胞、少突膠質(zhì)細(xì)胞(OLs)及少突膠質(zhì)前體細(xì)胞(OPCs)。發(fā)現(xiàn)相較于Sham小鼠,BCAS小鼠胼胝體區(qū)域OLs的數(shù)量及其在少突系細(xì)胞中的占比均減少,少突膠質(zhì)前體細(xì)胞的數(shù)量增加。神經(jīng)元激活后OLs的數(shù)量及其在少突系細(xì)胞中的占比增加。
5.激活BCAS小鼠mPFC谷氨酸能神經(jīng)元上調(diào)Wnt2的表達(dá)
為了進(jìn)一步探究mPFC谷氨酸能神經(jīng)元激活改善腦白質(zhì)損傷的潛在機(jī)制,我們采用基于微陣列的基因組學(xué)分析對(duì)BCAS小鼠及光刺激后BCAS小鼠的mPFC組織進(jìn)行檢測(cè)。結(jié)合相關(guān)數(shù)據(jù)庫篩選神經(jīng)元激活后差異表達(dá)且翻譯產(chǎn)物為神經(jīng)元特異性分泌型蛋白的基因,利用qPCR驗(yàn)證發(fā)現(xiàn)Wnt2是顯著變化的基因。同樣的,化學(xué)遺傳學(xué)刺激后BCAS小鼠mPFC組織中Wnt2的表達(dá)上升。對(duì)Wnt2的細(xì)胞來源驗(yàn)證表明Wnt2在皮層神經(jīng)元中高表達(dá)。利用免疫熒光檢測(cè)Wnt2在神經(jīng)元中的表達(dá)及分布,發(fā)現(xiàn)激活mPFC谷氨酸能神經(jīng)元后,激活神經(jīng)元中的Wnt2表達(dá)顯著上調(diào),且胼胝體區(qū)域神經(jīng)元軸突Wnt2的表達(dá)亦上升。

6.過表達(dá)Wnt2改善BCAS小鼠的腦白質(zhì)損傷及工作記憶障礙
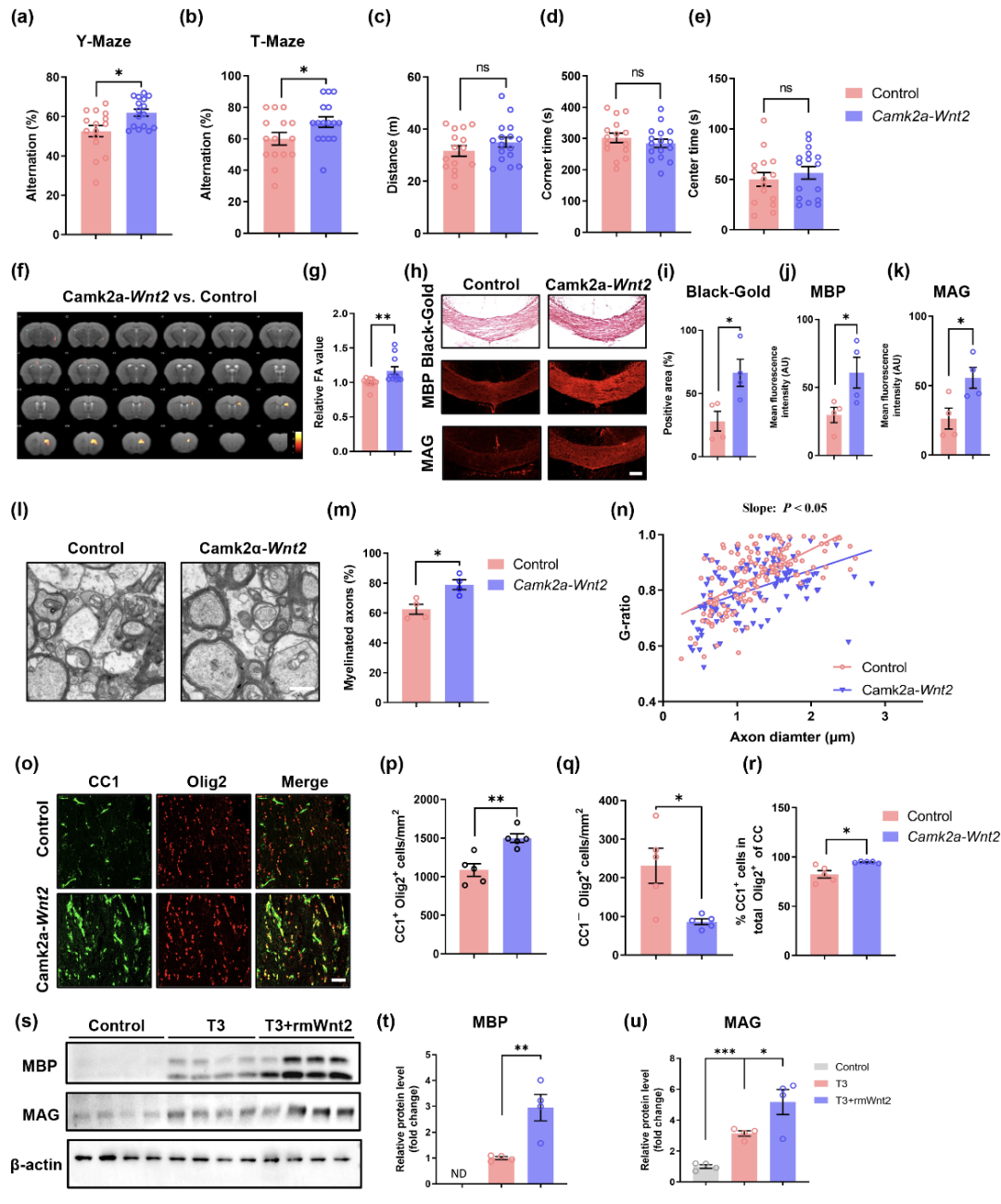
為了進(jìn)一步探究mPFC谷氨酸能神經(jīng)元中Wnt2的作用,通過注射腺相關(guān)病毒,在mPFC谷氨酸能神經(jīng)元中過表達(dá)Wnt2。通過行為學(xué)測(cè)試,發(fā)現(xiàn)Wnt2過表達(dá)改善了BCAS小鼠的工作記憶并且不影響小鼠的情緒及運(yùn)動(dòng)能力。利用磁共振成像檢測(cè),發(fā)現(xiàn)Wnt2過表達(dá)后BCAS小鼠胼胝體區(qū)域FA值上升。分別采用黑金染色和免疫熒光檢測(cè)胼胝體處的白質(zhì)完整性,發(fā)現(xiàn)Wnt2過表達(dá)改善了慢性腦缺血引起的髓鞘損傷。利用透射電鏡檢測(cè)胼胝體處髓鞘厚度,發(fā)現(xiàn)相比較于BCAS小鼠,Wnt2過表后BCAS小鼠髓鞘厚度增加。此外,通過體內(nèi)外實(shí)驗(yàn)也進(jìn)一步證實(shí)Wnt2能夠促進(jìn)OPC向少突膠質(zhì)細(xì)胞進(jìn)一步分化。
研究總結(jié)
在此項(xiàng)研究中,我們發(fā)現(xiàn)慢性腦缺血模型小鼠存在認(rèn)知功能下降與腦白質(zhì)損傷,其內(nèi)側(cè)前額葉皮層(mPFC)向胼胝體發(fā)出神經(jīng)纖維投射。運(yùn)用光/化學(xué)遺傳學(xué)手段激活小鼠mPFC谷氨酸能神經(jīng)元促進(jìn)了胼胝體區(qū)域白質(zhì)修復(fù)并改善了工作記憶。機(jī)制方面,谷氨酸能神經(jīng)元激活上調(diào)Wnt2的表達(dá),其通過促進(jìn)少突膠質(zhì)前體細(xì)胞的分化以改善腦白質(zhì)損傷。本研究揭示了神經(jīng)調(diào)控在改善腦白質(zhì)損傷及相關(guān)認(rèn)知障礙中的治療潛力。
吉?jiǎng)P助力
本文Wnt2過表達(dá)病毒由吉?jiǎng)P基因提供,助力高水平科學(xué)研究。

公眾號(hào)底部菜單欄【新功能】上線!
病毒實(shí)驗(yàn)幫
免費(fèi)在線學(xué)習(xí)《國自然熱點(diǎn)研究》、《數(shù)據(jù)庫及軟件操作教程》
一鍵下載《病毒使用手冊(cè)》、《高分文獻(xiàn)》
還有不定時(shí)的送新書、抽獎(jiǎng)活動(dòng),趕緊來掃碼關(guān)注一波吧
作者簡(jiǎn)介
南京大學(xué)醫(yī)學(xué)院附屬鼓樓醫(yī)院徐運(yùn)教授、劉品一博士為該論文的通訊作者,鄧世佶博士生、舒姝博士、翟利利博士為論文共同第一作者。
