新冠疫情后,疫苗開發(fā)迎來了變革期。在2024-2025這一關(guān)鍵節(jié)點(diǎn),全球疫苗產(chǎn)業(yè)在傳統(tǒng)平臺優(yōu)化與新型平臺迭代上同步加速。整體疫苗開發(fā)正朝著“通用化、可及化、智能化”方向邁進(jìn)。
在此行業(yè)快速擴(kuò)充的關(guān)口,我們嘗試對2024-2025期間,新型疫苗及傳統(tǒng)疫苗的突破性進(jìn)展進(jìn)行了整體梳理,尤其是已經(jīng)邁入臨床轉(zhuǎn)化或商業(yè)化階段的高價(jià)值項(xiàng)目,力圖以全球性的眼光,觀察未來疫苗行業(yè)的騰飛新方向。
一、新型疫苗平臺快速迭代
2024-2025年間,新型疫苗技術(shù)迎來了加速應(yīng)用與產(chǎn)業(yè)化突破。在2024-2025年間,國內(nèi)RNA疫苗(mRNA/circRNA/saRNA)獲批臨床項(xiàng)目近20項(xiàng),進(jìn)入“多病種切入”“版本更新”階段。重組亞單位疫苗及病毒樣顆粒(VLP)平臺也通過配方更新、佐劑與結(jié)構(gòu)設(shè)計(jì)等,繼續(xù)在監(jiān)管與覆蓋能力上取得實(shí)質(zhì)性進(jìn)展。
RNA疫苗(mRNA/circRNA/saRNA)
2024年5月1日—University of Florida(UF Health Cancer Center)團(tuán)隊(duì)發(fā)布其mRNA疫苗用于腦瘤(glioblastoma)治療的初步人體研究成果[1]。該團(tuán)隊(duì)開發(fā)了一種基于mRNA的腫瘤疫苗(使用患者自身腫瘤細(xì)胞信息+復(fù)雜遞送機(jī)制)并在成人患者中觀察到“在48小時(shí)內(nèi)使腫瘤從免疫冷態(tài)變?yōu)槊庖邿釕B(tài)”的免疫反應(yīng)。對mRNA平臺而言,它標(biāo)志著mRNA疫苗不僅限于傳染病防控,還可用于復(fù)雜腫瘤免疫治療,體現(xiàn)平臺通用性的突破。也說明mRNA的遞送和免疫激活機(jī)制正被重大改進(jìn)。
對于circRNA而言,最大的突破性進(jìn)展莫過于連續(xù)三個(gè)項(xiàng)目進(jìn)入臨床階段,原研單位均來自中國。轉(zhuǎn)錄本生物放射性口干癥的臨床項(xiàng)目于2024年10月份獲批,環(huán)碼生物用于治療缺血性心臟病環(huán)狀RNA項(xiàng)目于2025年1月獲批臨床,圓因生物環(huán)狀RNA藥物TI-0093注射液于2025年8月獲臨床試驗(yàn)?zāi)驹S可,該項(xiàng)目用于治療HPV16陽性的晚期復(fù)發(fā)或轉(zhuǎn)移性實(shí)體瘤。臨床項(xiàng)目的增多意味著在逐漸突破工藝的同時(shí),質(zhì)量研究也開始逐步完善。
相較于circRNA,saRNA進(jìn)展更快,2023年11月,日本厚生勞動省批準(zhǔn)了CSL與Arcturus therapeutics聯(lián)合開發(fā)的自復(fù)制RNA(saRNA)新冠疫苗:ARCT-154(一款saRNA-LNP凍干制劑),是第一個(gè)獲批上市的saRNA疫苗。2025年9月份,美國公司Replicate Bioscience公布了其狂犬病saRNA臨床項(xiàng)目RBI-4000的8個(gè)月耐久性分析數(shù)據(jù),在0.1–10 μg劑量方案下,在受試者中可在最長8個(gè)月仍檢測到中和抗體,且用多種衰減模型比較顯示其抗體半衰期與/或耐久性與傳統(tǒng)滅活疫苗相當(dāng)或更優(yōu)[2]。證明了RNA平臺向“更低劑量(成本)、更廣覆蓋”方向的可行性,是RNA平臺從“短期應(yīng)急”向“長期常規(guī)”轉(zhuǎn)變的關(guān)鍵里程碑。
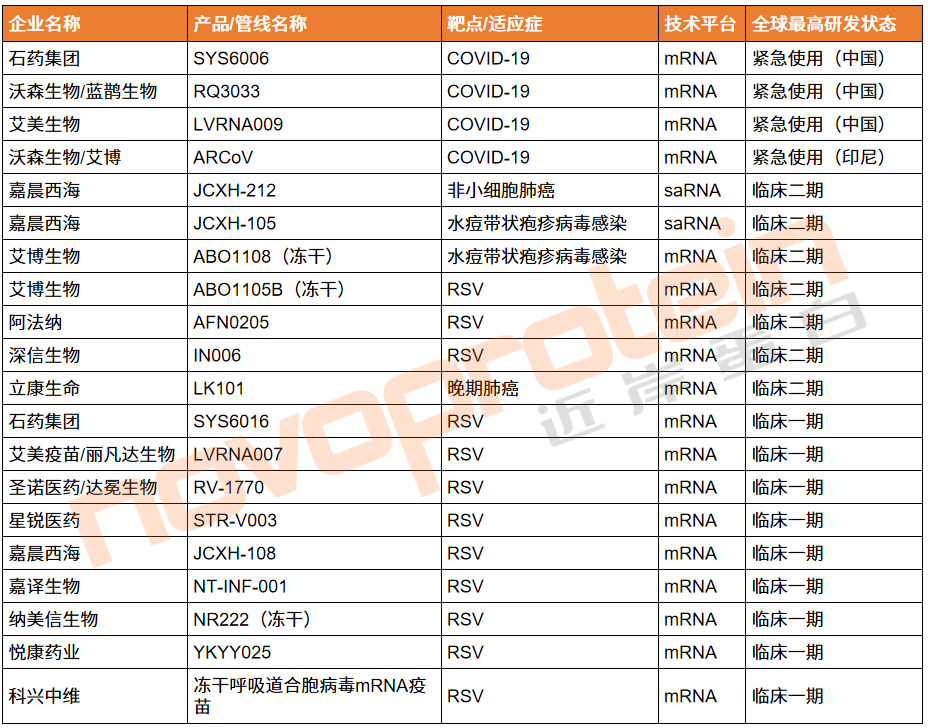
表1、截至目前國內(nèi)獲批緊急使用或進(jìn)入臨床的mRNA疫苗
(部分清單,novoprotein整理)
亞單位/重組蛋白疫苗
2024年8月30日,Novavax(公司)獲得美國FDA對其更新配方蛋白/佐劑COVID-19疫苗的緊急使用授權(quán)(EUA)[3]。是蛋白/佐劑平臺在法規(guī)層面被再次認(rèn)可為主流抗 SARS-CoV-2的可用選項(xiàng),表明蛋白疫苗(非mRNA)仍具快速迭代并被監(jiān)管接受的能力。
2024年9月4日,Vaxcyte公司宣布其31價(jià)肺炎球菌結(jié)合疫苗(VAX-31)在一項(xiàng)針對1015名50歲及以上健康成人的1/2期臨床試驗(yàn)中取得了積極結(jié)果,并決定推進(jìn)至更高3期臨床[4]。代表多價(jià)蛋白/結(jié)合疫苗通過擴(kuò)大覆蓋血清型(價(jià)型擴(kuò)展)直接提升公共衛(wèi)生價(jià)值,代表結(jié)合疫苗在覆蓋率的競爭力上取得實(shí)質(zhì)進(jìn)展。
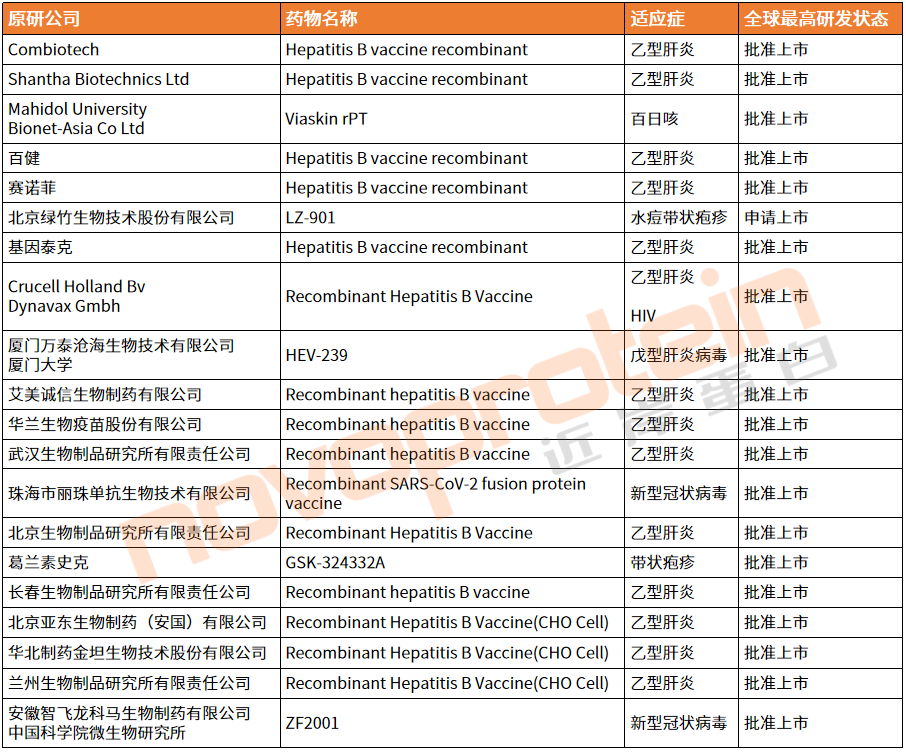
表2、截至目前進(jìn)入商業(yè)化階段的亞單位/重組蛋白疫苗
(部分清單,novoprotein整理)
病毒樣顆粒疫苗(VLP)
VLP在2024–2025年的真正突破是由臨床成功轉(zhuǎn)向監(jiān)管批準(zhǔn)與商業(yè)化上市,實(shí)現(xiàn)質(zhì)的飛躍。
2025年3月18日,Bavarian Nordic(公司)推出并在美歐獲批商業(yè)化其VLP-based Chikungunya疫苗VIMKUNYA™用于12歲以上人群,并啟動2-11歲兒童的第III期試驗(yàn)[5]。這是第一個(gè)以VLP技術(shù)在成人/青少年中獲準(zhǔn)并商業(yè)化的針對新興病原體(Chikungunya)的疫苗,把VLP從“臨床候選/研究”階段推進(jìn)到使用階段,證明其在安全性與免疫原性上既能滿足監(jiān)管要求又具備商業(yè)化條件。
2024年2月19日,阿斯利康以11億美元金額完成了對Icosavax公司的收購,并推進(jìn) IVX-A12(RSV+hMPV組合蛋白VLP疫苗)至臨床中后期[6]。II期數(shù)據(jù)表明,IVX-A12在接種疫苗一個(gè)月后可引發(fā)針對RSV和hMPV強(qiáng)大免疫應(yīng)答,該疫苗已進(jìn)入到III期臨床。大型制藥公司對VLP平臺的并購與推進(jìn)說明VLP已被視為可產(chǎn)業(yè)化、可規(guī)模生產(chǎn)且商業(yè)價(jià)值明確的平臺。對行業(yè)來說,意味著資本與產(chǎn)能將加速VLP的廣泛應(yīng)用。
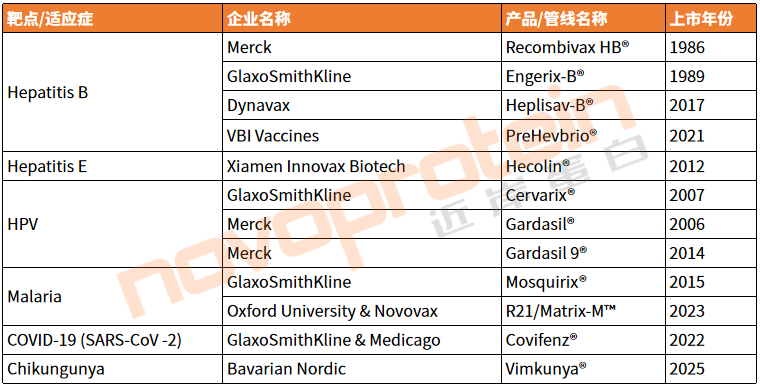
表3、截至目前進(jìn)入商業(yè)化階段的VLP疫苗
(novoprotein整理,如有錯(cuò)漏,歡迎指正)
二、傳統(tǒng)疫苗平臺的精進(jìn)
在2024-2025年間,傳統(tǒng)疫苗平臺(如減毒/滅活/病毒載體等)雖然相較于新型疫苗平臺顯得“穩(wěn)重”,但同樣在給藥方式、靶點(diǎn)拓展、特殊人群應(yīng)用、監(jiān)管規(guī)范化等方面有所突破,顯著強(qiáng)化了作為“疫苗產(chǎn)業(yè)基本盤”的角色。下面列出幾個(gè)突破性進(jìn)展:
給藥方式創(chuàng)新
2024年4月15日,牛津大學(xué)公布了通過氣溶膠方式給予減毒版Tuberculosis疫苗(BCG疫苗)的一項(xiàng)人體挑戰(zhàn)模型研究[7],研究中將BCG通過噴霧方式進(jìn)入肺部,研究其在近似自然感染途徑下的安全性與耐受性。這一研究強(qiáng)調(diào)傳統(tǒng)減毒疫苗不僅在經(jīng)典的“肌肉/皮下注射”路徑上可靠,而且通過更接近病原自然侵入途徑(肺部噴霧)進(jìn)行的給藥方式研究,代表了傳統(tǒng)平臺在“給藥方式”與免疫原性增強(qiáng)上的改進(jìn)。
靶點(diǎn)拓展
2024年9月10日,法國Valneva公司在《Journal of Travel Medicine》雜志上發(fā)表其基孔肯雅熱減毒活疫苗VLA1553(IXCHIQ®)相關(guān)數(shù)據(jù)[8],隨后該款疫苗成為第一款獲得FDA批準(zhǔn)的基孔肯雅熱減毒病毒疫苗用于成人免疫。標(biāo)志著減毒病毒疫苗平臺在全球公共衛(wèi)生病原體(蚊媒病毒)中的應(yīng)用擴(kuò)展,從傳統(tǒng)的減毒疫苗(如麻疹、風(fēng)疹)走向新的病毒類型,從而強(qiáng)化了減毒平臺在“新病原/少有疫苗”領(lǐng)域中的價(jià)值。
免疫受損人群應(yīng)用
2025年6月11日,由康希諾生物與中國軍事醫(yī)學(xué)科學(xué)院生物工程研究所共同研究的腺病毒5型載體的新冠疫苗(Ad5nCoV)在HIV感染者(PLWH)人群中進(jìn)行研究,顯示安全且免疫反應(yīng)持續(xù)至少一年[9]。表明腺病毒載體平臺正在擴(kuò)展至免疫受損人群的應(yīng)用,這加強(qiáng)了其在“高風(fēng)險(xiǎn)群體疫苗策略”中的地位。
監(jiān)管規(guī)范化
2024年12月20日,中國國家藥典委員會發(fā)布新版《多糖結(jié)合疫苗質(zhì)量控制技術(shù)指南(征求意見稿)》,涉及多糖結(jié)合疫苗中“偶聯(lián)工藝”“純化工藝”“載體蛋白選擇”等[10]。該指南的發(fā)布體現(xiàn)監(jiān)管層面對多糖-蛋白結(jié)合疫苗平臺的進(jìn)一步規(guī)范與推動,意味著該平臺進(jìn)一步規(guī)范化。
未來,無論是新型疫苗還是傳統(tǒng)疫苗,技術(shù)趨勢都將持續(xù)向多病種覆蓋與多平臺融合發(fā)展。人工智能的快速進(jìn)步,為疫苗從抗原設(shè)計(jì)、結(jié)構(gòu)優(yōu)化到免疫效果預(yù)測提高了研發(fā)效率。隨著多技術(shù)平臺的疫苗項(xiàng)目不斷實(shí)現(xiàn)從早期研究到臨床驗(yàn)證,再到商業(yè)化落地的突破,意味著在面對快速變異的病原體與潛在大流行時(shí),人類將具備更敏捷的響應(yīng)能力、更高的制造靈活性以及更可持續(xù)的免疫保障體系。這不僅代表疫苗研發(fā)范式的革新,也預(yù)示著疫苗產(chǎn)業(yè)正邁入一個(gè)以智能化、模塊化的新階段。
近岸蛋白加速新型疫苗療法的研究開發(fā)與轉(zhuǎn)化應(yīng)用
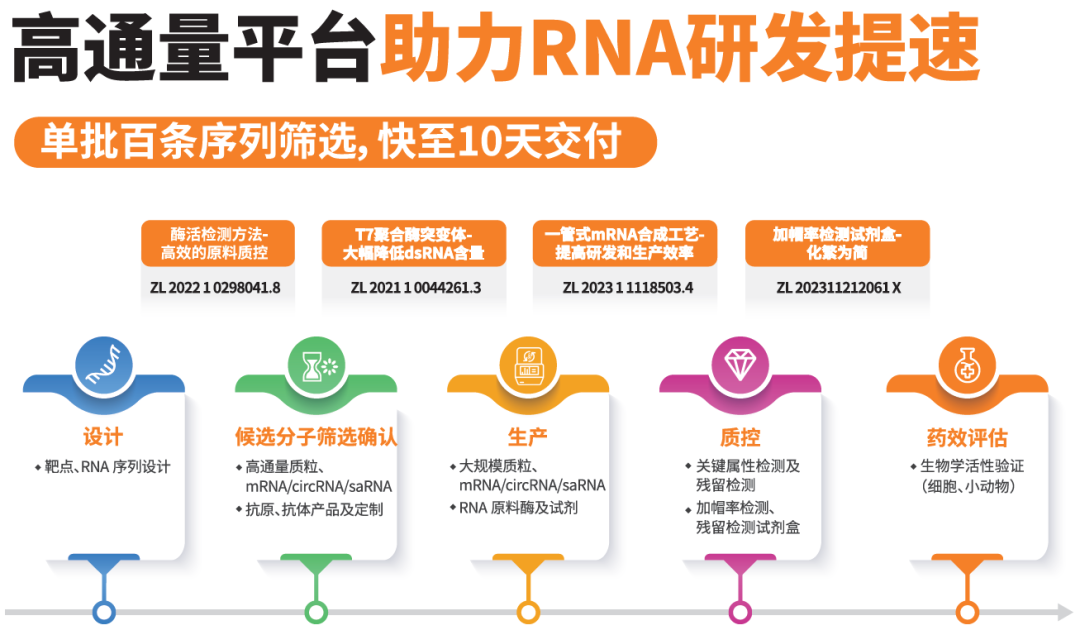
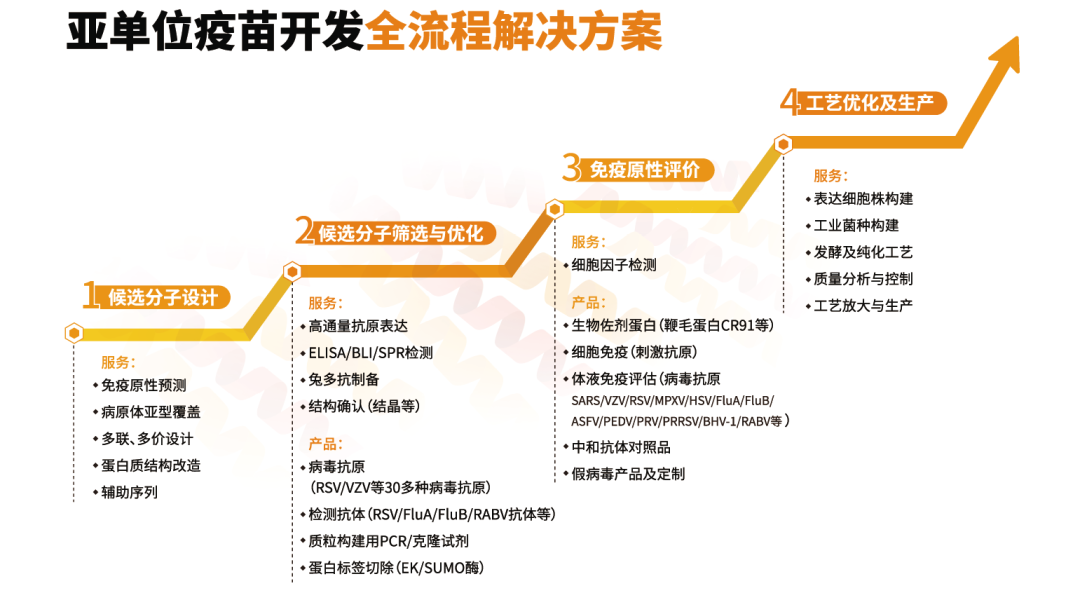
近岸蛋白提供新型疫苗研發(fā)過程中的全流程解決方案,涵蓋RNA疫苗、亞單位疫苗、VLP疫苗多核心技術(shù)平臺,具備從抗原設(shè)計(jì)、候選分子篩選、工藝建立,到質(zhì)量控制與評價(jià)的能力,團(tuán)隊(duì)成員擁有多年人用與獸用疫苗開發(fā)經(jīng)驗(yàn)。

11月14-16日,2025中國疫苗行業(yè)協(xié)會學(xué)術(shù)年會在福建廈門召開,本次大會將有中國疫苗行業(yè)各研究院所、高等院校、藥物研發(fā)與生產(chǎn)企業(yè)等行業(yè)專家展開深入交流,設(shè)置了多個(gè)分會場主題。近岸蛋白誠邀您在廈門國際會議展覽中心,B12展位進(jìn)行交流。
RNA疫苗方面,近岸蛋白支持mRNA、circRNA、saRNA多種技術(shù)開發(fā)路線,覆蓋從候選分子序列優(yōu)化、通量篩選與生物學(xué)評估等過程服務(wù),擁有GMP級T7 RNA聚合酶、加帽酶等關(guān)鍵原料,并完成全套產(chǎn)品FDA DMF備案,已助力20余家客戶完成中美IND申報(bào)。
在亞單位疫苗開發(fā)中,近岸蛋白擁有計(jì)算機(jī)輔助抗原結(jié)構(gòu)設(shè)計(jì)與蛋白分析改造能力,支持通過大腸桿菌、酵母、真核、昆蟲多表達(dá)系統(tǒng)匹配小規(guī)模到放大生產(chǎn)。VLP疫苗表達(dá)體系具備高效自組裝能力,獨(dú)立開發(fā)生產(chǎn)工藝具備高純度高均一性特點(diǎn)。
參考文獻(xiàn)
[1] UF-developed mRNA vaccine triggers fierce immune response to fight malignant brain tumor. UF Health Cancer Institute
[2] Christian J. Maine, Gaelle Picarda, Shigeki J. Miyake-Stoner et al. Durability of next-generation self-replicating RNA vaccine RBI-4000: a phase 1, randomized open label clinical trial. Nature. Published 2025 Sep 24.
[3] FDA Authorizes Updated Novavax COVID-19 Vaccine to Better Protect Against Currently Circulating Variants. U.S.FOOD&DRUG官網(wǎng)
[4] Summary of VAX-31 Adult 50+ Phase 1/2 Study Topline Data Findings. Vaxcyte官網(wǎng)
[5] Bavarian Nordic官網(wǎng)
[6] AstraZeneca官網(wǎng)
[7] Breakthrough aerosol human infection model gives hope for future tuberculosis vaccine development. University of Oxford News.
[8] Lin H Chen, Andrea Fritzer, Romana Hochreiter et al. From bench to clinic: the development of VLA1553/IXCHIQ, a live-attenuated chikungunya vaccine. Journal of Travel Medicine. Published 2024 Sep 10.
[9] Pedro Cahn, Luis Barreto, Maria Ines FigueroaImmune et al. response induced by the recombinant novel coronavirus vaccine (Adenovirus type 5 vector) (Ad5-nCoV) in persons living with HIV (PLWH). Plos One. Published 2025 Jun 11.
[10] 中國食品藥品國際交流中心官網(wǎng)
