作為新興技術(shù),mRNA疫苗通過(guò)脂質(zhì)納米顆粒(LNP)將mRNA導(dǎo)入體內(nèi)表達(dá)抗原蛋白,從而刺激機(jī)體產(chǎn)生特異性免疫反應(yīng)。新冠肺炎疫情(COVID-19)爆發(fā)后,針對(duì)性的mRNA疫苗在多種疫苗類型中脫穎而出。與此同時(shí),諸如自復(fù)制mRNA和circRNA等新型路線也逐漸走入大眾視野,隨著資本的大量涌入,circRNA技術(shù)迅速發(fā)展起來(lái)。
circRNA分子呈共價(jià)閉合環(huán)狀結(jié)構(gòu),不含5’-Cap和3’-polyA結(jié)構(gòu),不易被RNase降解,具有較高的穩(wěn)定性,因而大大延長(zhǎng)了其半衰期,從而達(dá)到低劑量長(zhǎng)時(shí)效的目的。此外circRNA因?yàn)椴恍枰揎椇塑蘸图用奔游驳炔僮鳎赃€有相對(duì)簡(jiǎn)單的生產(chǎn)工藝優(yōu)勢(shì)。與mRNA相同,前期線性RNA的獲得均來(lái)組線性化質(zhì)粒的體外轉(zhuǎn)錄,而后根據(jù)其環(huán)化工藝的不同,circRNA的人工制備大致分為三個(gè)類型:I型內(nèi)含子自剪切、Ⅱ型內(nèi)含子自剪切和T4 RNA連接酶。大致流程如下:

在環(huán)化結(jié)束后,需要通過(guò)系列純化手段對(duì)circRNA進(jìn)行高純度回收,由于不同環(huán)化方式的效率差異,RNase R的引入,有效去除未環(huán)化的線性RNA,從而達(dá)到純化circRNA的目的。RNase R來(lái)源于大腸桿菌RNR超家族,是一種鎂離子依賴性的3'—5'核糖核酸外切酶,可從3'—5'方向?qū)NA逐步切割成二核苷酸和三核苷酸。RNase R幾乎能夠消化所有線性的RNA,但不易消化環(huán)狀RNA、套索結(jié)構(gòu)RNA和3'端突出少于7個(gè)核苷酸的短雙鏈RNA分子。通常用來(lái)消化線性RNA以富集circRNA或套索結(jié)構(gòu)RNA。近岸蛋白經(jīng)過(guò)系列驗(yàn)證,重磅推出高活性GMP級(jí)RNase R(目錄號(hào):GMP-E224)。GMP級(jí)產(chǎn)品采用藥用規(guī)格原輔料生產(chǎn),嚴(yán)格控制宿主核酸殘留污染,符合GMP規(guī)范的產(chǎn)品生產(chǎn)與質(zhì)量管理規(guī)程,保障生產(chǎn)過(guò)程及所有原輔料可追溯。
質(zhì)量控制

應(yīng)用實(shí)例
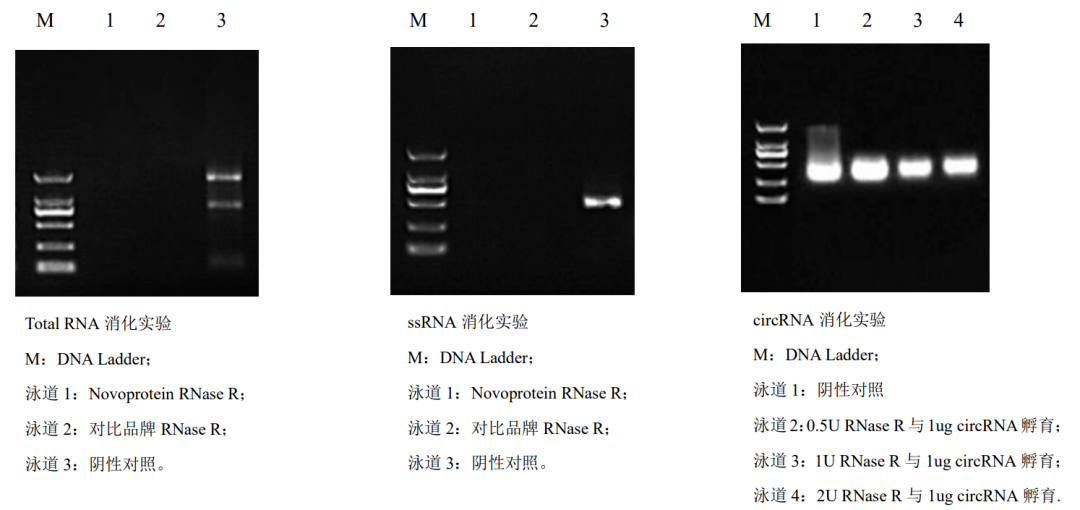
RNase R針對(duì)Total RNA、ssRNA及circRNA的消化實(shí)驗(yàn),實(shí)驗(yàn)證明, RNase R可以消化絕大部分的總 RNA樣品,完全消化ssRNA樣品,對(duì)circRNA樣品起到良好的純化效果。
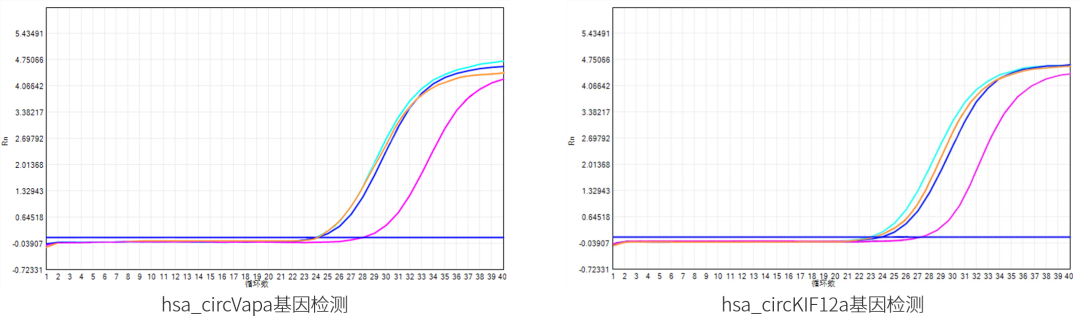
為了進(jìn)一步驗(yàn)證RNase R對(duì)環(huán)狀RNA無(wú)酶切作用,利用qPCR方式檢測(cè)經(jīng)RNase R(藍(lán)色:近岸蛋白;綠色:對(duì)照品牌)消化后的總RNA樣品中hsa_circKIF12a和hsa_circVapa基因的豐度變化,結(jié)果顯示,與陰性組(橙色)相同,兩個(gè)基因的豐度基本沒有變化,而經(jīng)RNase A(粉色)消化的樣品中基因豐度明顯下降,表明環(huán)狀RNA耐受RNase R的消化。
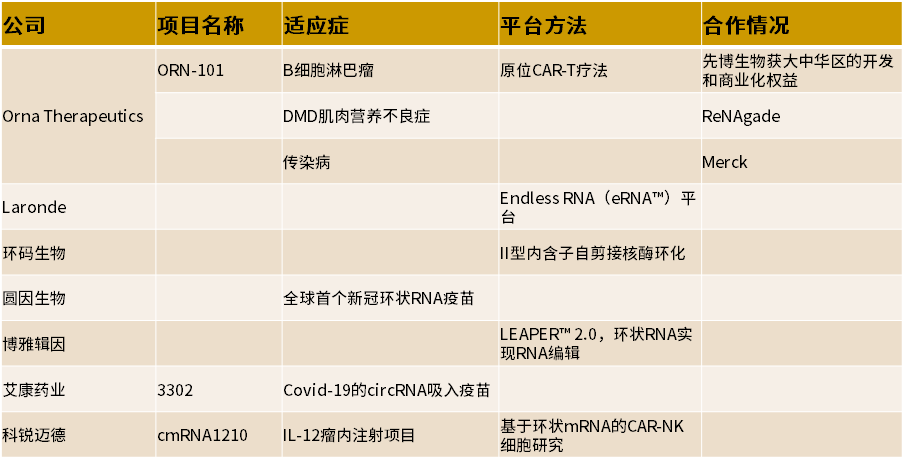
隨著序列設(shè)計(jì)的不斷優(yōu)化,環(huán)化工藝的進(jìn)一步探索,伴隨circRNA的各項(xiàng)技術(shù)壁壘也將會(huì)逐步打破。國(guó)外以O(shè)RNA Therapeutics和Laronde為代表,國(guó)內(nèi)環(huán)碼生物、科銳邁德、圓因生物等公司先后成立布局circRNA,越來(lái)越多的研發(fā)管線來(lái)滿足臨床治療需求,circRNA未來(lái)可期。
相關(guān)產(chǎn)品:
