前言
腎臟疾病是全球性健康問題,影響著眾多人群。近年來,基于人類多能干細(xì)胞(hPSC)的腎臟類器官技術(shù)為腎臟研究帶來了新的希望,但仍存在空間模式化不足、成熟度低等問題,限制了其在疾病建模和再生醫(yī)學(xué)中的應(yīng)用。
腎臟由超過30種不同類型的細(xì)胞組成,這些細(xì)胞在腎臟的連續(xù)管狀網(wǎng)絡(luò)中分化并執(zhí)行多種生理功能。具體而言,生理條件下,腎臟的形成依賴于幾種腎祖細(xì)胞之間的相互作用,其中SIX2+腎祖細(xì)胞(NPCs)和WNT11+輸尿管祖細(xì)胞(UPCs)的相互作用是腎臟發(fā)育的基礎(chǔ)。NPCs生成腎單位,而UPCs分化形成收集管(CD)網(wǎng)絡(luò)。盡管已有研究嘗試通過混合不同類型的腎祖細(xì)胞來生成類器官,但這些結(jié)構(gòu)仍然缺乏成熟的腎臟功能。因此,開發(fā)具有復(fù)雜空間模式化和成熟功能的腎臟類器官模型是當(dāng)前研究的重點。
2025年9月17日,南加州大學(xué)李中偉及合作團(tuán)隊在期刊Cell Stem Cell發(fā)表論文“Spatially patterned kidney assembloids recapitulate progenitor self-assembly and enable high-fidelity in vivo disease modeling”,成功開發(fā)出一種空間模式化的腎臟組裝體(KPAs),能夠在體外乃至體內(nèi)重現(xiàn)腎臟前體細(xì)胞的自組織過程,形成與天然腎臟高度相似的結(jié)構(gòu)和功能。移植體內(nèi)后,KPAs可與小鼠的血液循環(huán)系統(tǒng)無縫對接并繼續(xù)生長、發(fā)育并形成具有功能的腎臟結(jié)構(gòu),表現(xiàn)出良好的血管化和尿液生成能力。這不僅解決了類器官長期停留在“半成熟狀態(tài)”的難題,也首次為復(fù)雜腎病的高保真建模提供了切實可行的平臺。

01 從類器官到“組裝體”
現(xiàn)有的腎臟類器官模型大多依賴單一前體細(xì)胞群體,比如利用SIX2陽性的腎單位前體細(xì)胞(NPCs)生成腎單位,或通過尿管芽前體細(xì)胞(UPCs)發(fā)育出集合管網(wǎng)絡(luò)。雖然這些模型揭示了腎臟發(fā)育的局部過程,但由于缺乏不同前體細(xì)胞之間的相互作用,它們始終無法形成真正成熟的空間格局。李中偉團(tuán)隊抓住了一個關(guān)鍵:在胚胎發(fā)育中,腎臟的復(fù)雜結(jié)構(gòu)源自不同前體細(xì)胞群體的互作——NPCs生成腎單位,UPCs形成集合管,間質(zhì)祖細(xì)胞(IPCs)和血管祖細(xì)胞(VPC)則提供支持。研究者推測,只有將這些多種前體細(xì)胞以接近天然的方式匯聚,才能觸發(fā)真正的“自組裝”過程。
在此基礎(chǔ)上,團(tuán)隊提出了“腎臟組裝體”的概念。不同于傳統(tǒng)的類器官單一分化,組裝體通過將人類多能干細(xì)胞衍生的iNPCs與iUPCs在優(yōu)化的培養(yǎng)體系中共培養(yǎng),誘導(dǎo)它們自發(fā)組織成具有空間分區(qū)的腎臟微型結(jié)構(gòu)。這種策略相當(dāng)于在培養(yǎng)皿中重現(xiàn)了胚胎腎臟發(fā)育的“對話邏輯”,讓細(xì)胞自己找到屬于它們的“位置”。
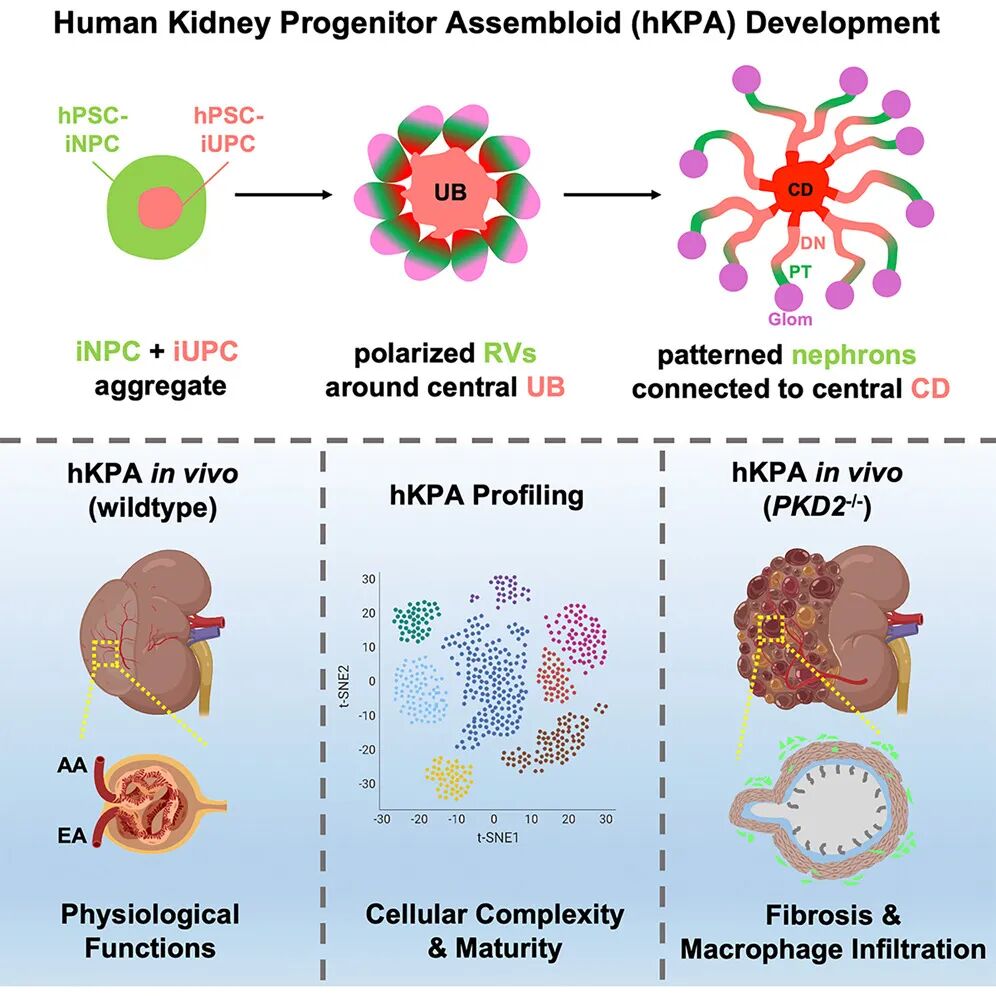
02 實驗設(shè)計:從小鼠到人類
研究首先在小鼠體系中進(jìn)行驗證。通過改良的“v2培養(yǎng)基”,小鼠NPCs與UPCs能夠在三周左右的時間里自發(fā)形成包含約150個腎單位的三維結(jié)構(gòu),即小鼠KPA(mKPA)。所有腎單位不僅展現(xiàn)出近曲小管、亨利袢、遠(yuǎn)曲小管等分段特征,還能與中央集合管網(wǎng)絡(luò)相連,形成類似天然腎臟的連續(xù)管道。尤其值得注意的是,類器官中展現(xiàn)出了典型的維生素D代謝、促紅細(xì)胞生成素分泌等內(nèi)分泌功能,這些都是此前人類腎臟類器官無法實現(xiàn)的生理特征。
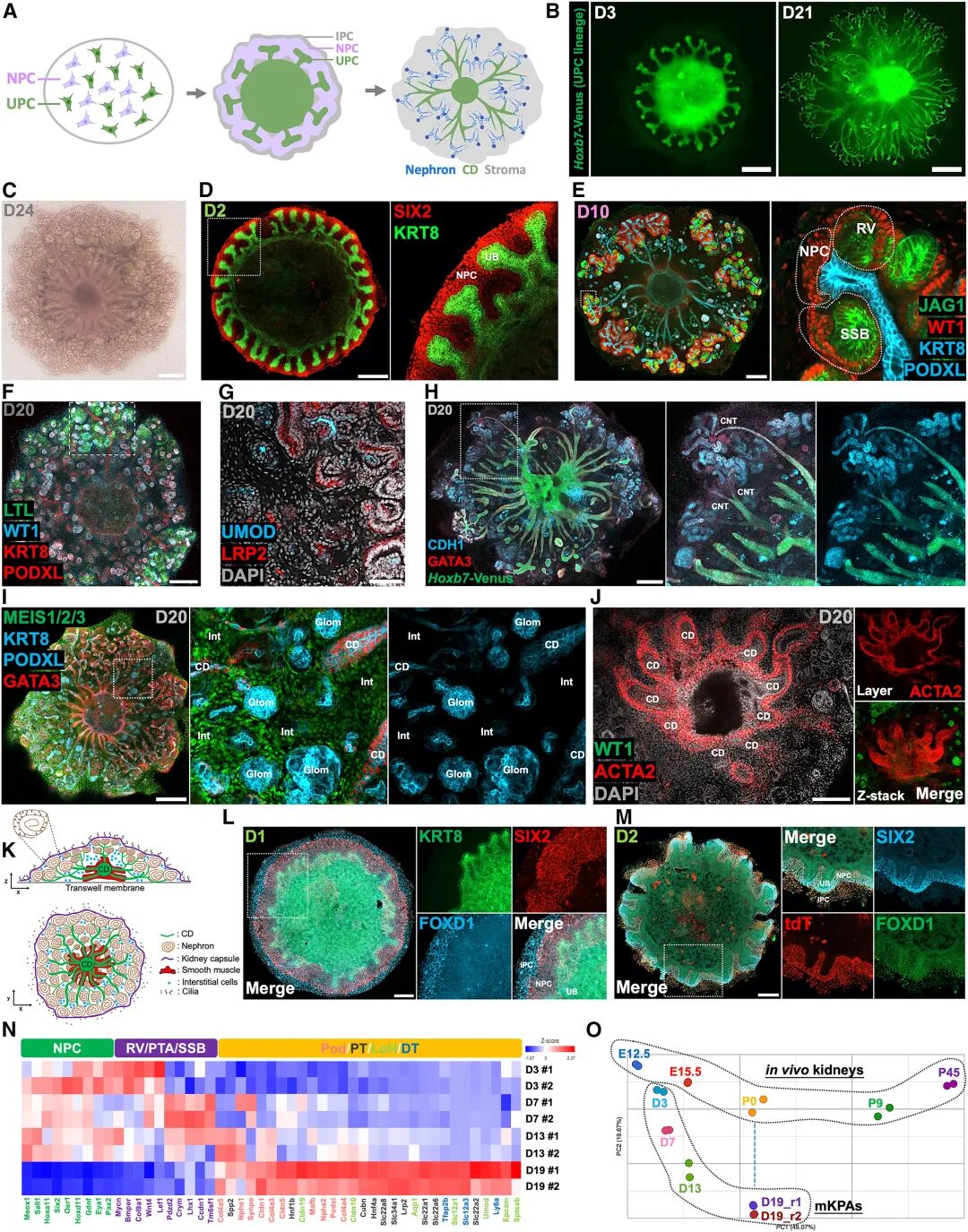
圖 :由可擴(kuò)展的 NPC 和 UPC 組裝成 小鼠KPA(mKPA)
在人類體系中,研究團(tuán)隊進(jìn)一步建立了“v3培養(yǎng)基”(在v2基礎(chǔ)上縮短了FGF9的處理時間,并添加了激素氫化可的松21-半琥珀酸酯(HCHS)和A83-01),并在其中成功組裝了空間模式化的人源腎臟組裝體(hKPAs)。這些hKPAs同樣形成了極化的腎泡,逐步分化為分節(jié)的腎單位,并與中央集合管對接。此外,尤其值得注意的是,該培養(yǎng)方案具有高度可重復(fù)性,在多個iPSC系中均能建立。
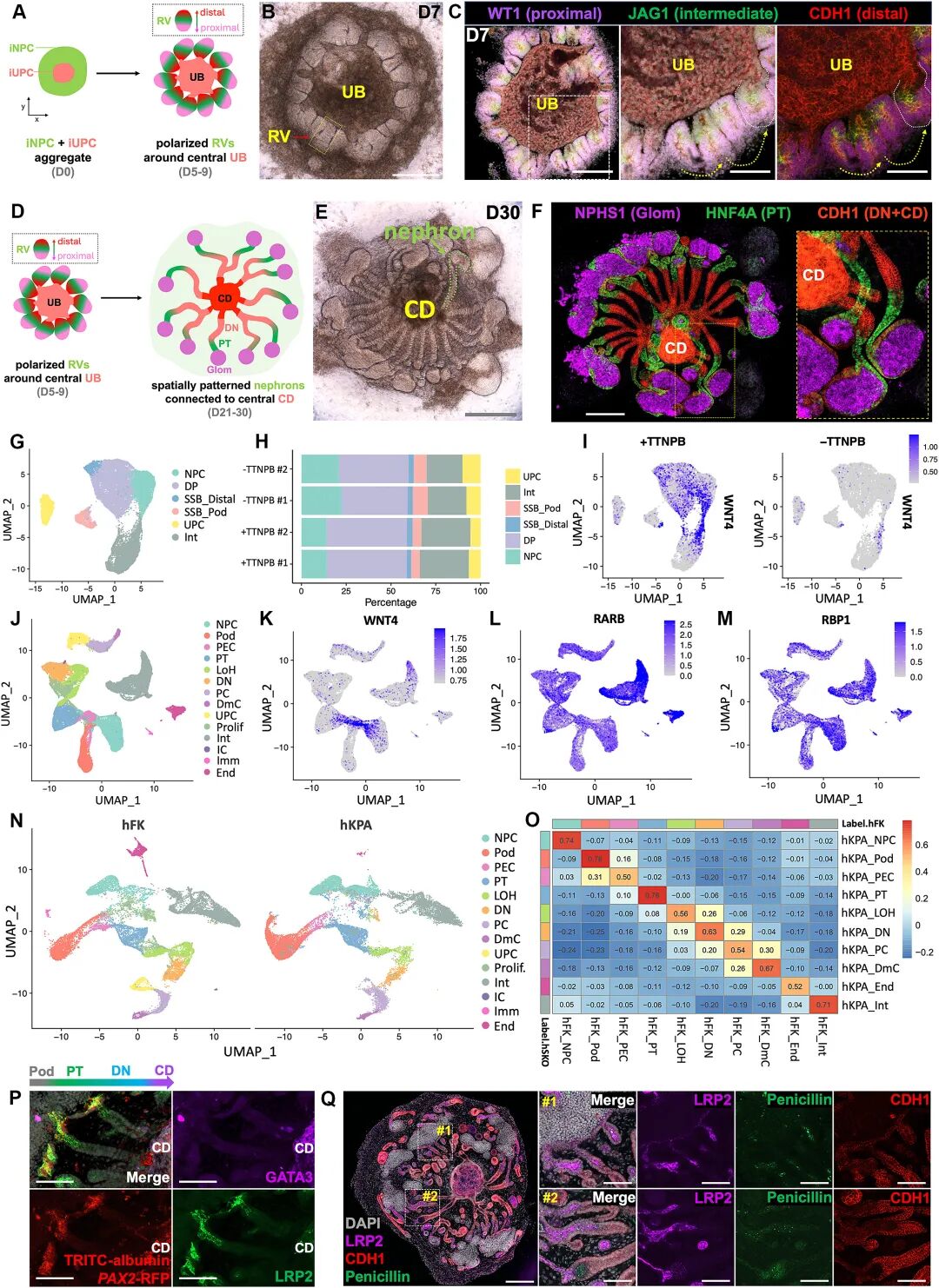
圖:iNPC 和 iUPC 的空間模式化 hKPA 組裝
03 核心突破:空間格局與功能成熟
通過單細(xì)胞組學(xué)和多組學(xué)聯(lián)合分析,研究團(tuán)隊證實,這些組裝體在轉(zhuǎn)錄譜和染色質(zhì)開放狀態(tài)上都高度接近新生鼠腎臟和17周的人類胎兒腎臟。
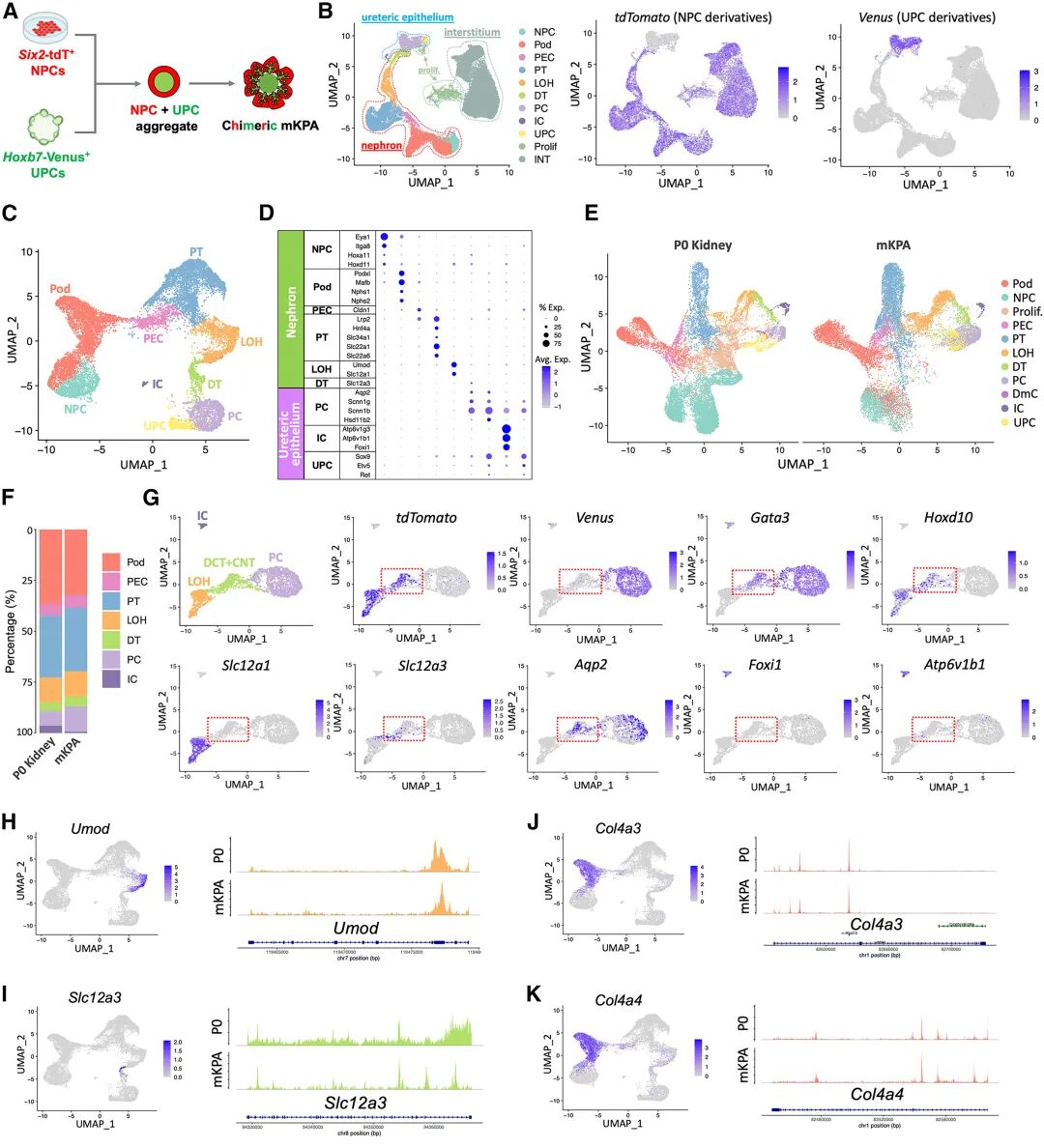
圖:mKPAs 的單細(xì)胞多組學(xué)分析
相比傳統(tǒng)類器官,KPAs不僅包含集合管細(xì)胞類型,還在代謝通路上表現(xiàn)出更強的氧化磷酸化能力,提示能量代謝向成熟腎小管靠攏。移植到小鼠體內(nèi)后,hKPAs表現(xiàn)出進(jìn)一步的成熟,形成了人源性血管、間質(zhì)和腎小球結(jié)構(gòu),展現(xiàn)了真正的灌注和濾過功能。
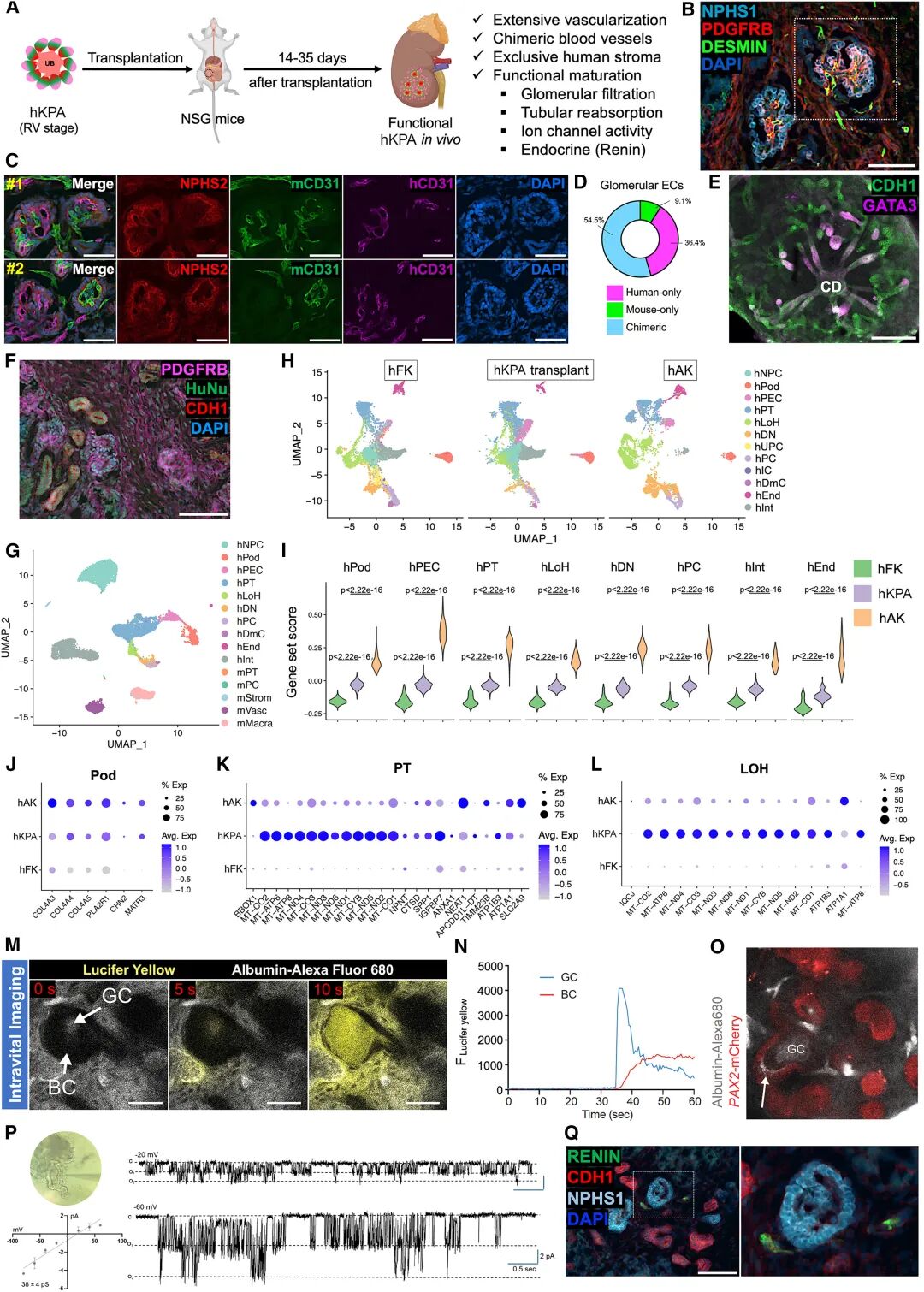
圖:體內(nèi)移植后功能性hKPA的生成
這種成熟度的提升帶來了關(guān)鍵意義:它不僅僅是“結(jié)構(gòu)像”,更是“功能像”。過去的腎臟類器官常被詬病停留在胚胎早期,無法模擬成人期疾病。而KPAs在體內(nèi)環(huán)境中展現(xiàn)的功能,使其成為一個能夠跨越“發(fā)育—疾病—再生”全鏈條的研究平臺。
04 疾病建模:ADPKD的高保真復(fù)現(xiàn)
為了驗證平臺的應(yīng)用潛力,研究團(tuán)隊選擇了最常見的遺傳性腎病——常染色體顯性多囊腎病(ADPKD)。結(jié)果顯示,基因編輯后(PKD2-/- hKPAs)的組裝體不僅在兩個月內(nèi)生長至接近宿主腎臟的體積,還出現(xiàn)了典型的囊性結(jié)構(gòu),囊液中肌酐和尿素濃度顯著升高,與患者表現(xiàn)高度一致。更重要的是,PKD2-/- hKPAs中觀察到囊上皮極性的喪失、周圍基質(zhì)細(xì)胞的纖維化以及巨噬細(xì)胞浸潤,這些復(fù)雜的細(xì)胞間互作是現(xiàn)有體外類器官模型完全無法再現(xiàn)的。
單細(xì)胞測序進(jìn)一步揭示了PKD2-/- hKPAs中關(guān)鍵致病通路的激活,包括cAMP、PI3K/AKT、mTOR以及Wnt信號,同時氧化磷酸化水平顯著下降。這些分子特征與患者樣本高度吻合,為闡釋疾病機(jī)制和尋找潛在靶點提供了窗口。
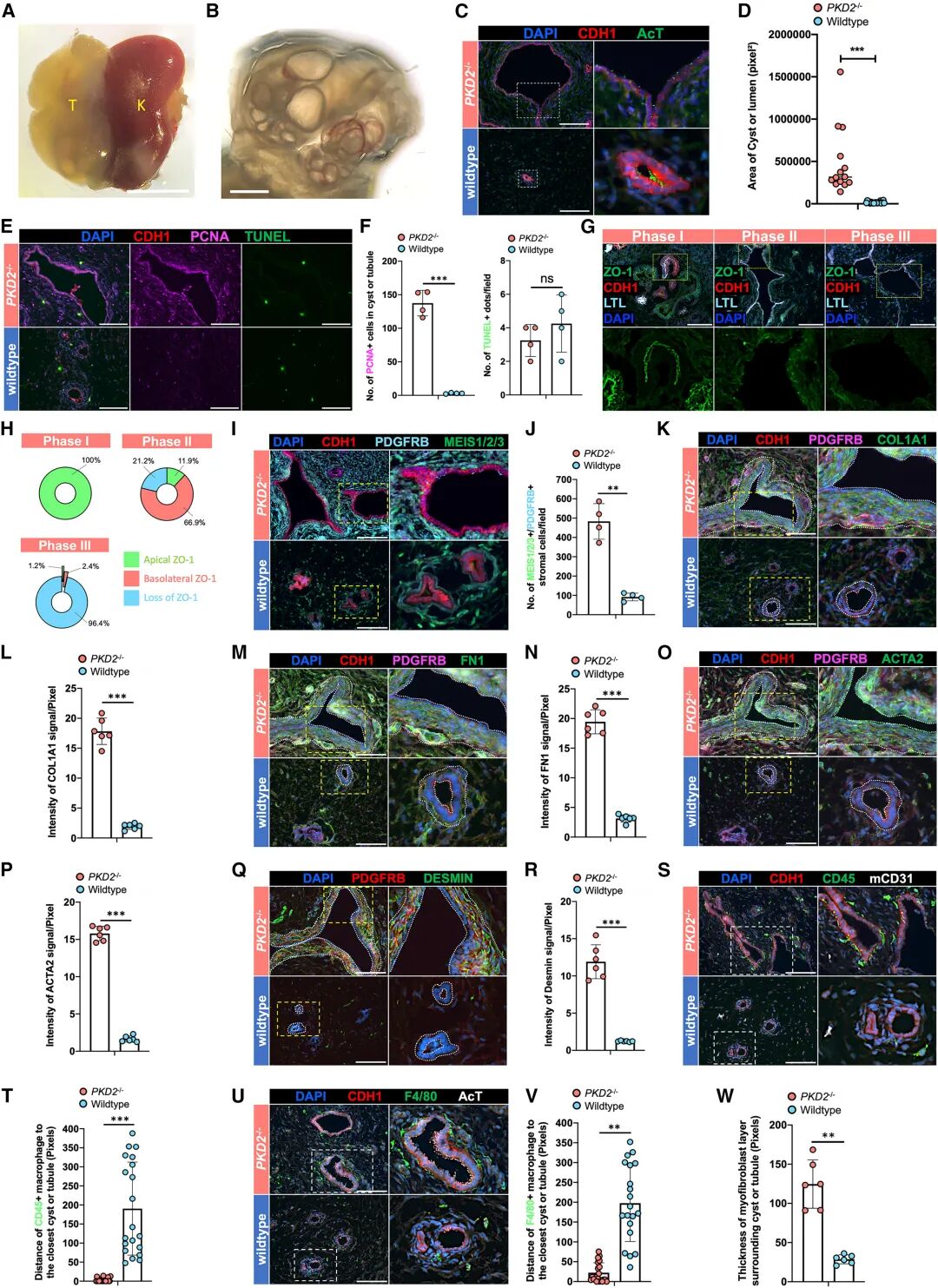
圖:人類 ADPKD 與PKD2−/− hKPA的高保真體內(nèi)模型
05 總結(jié)
本研究重要性在于,它為腎臟疾病研究打開了全新的可能性。空間模式化的組裝體不僅能真實反映復(fù)雜疾病的進(jìn)展過程,也能成為藥物篩選和療效預(yù)測的高保真平臺。在再生醫(yī)學(xué)領(lǐng)域,這種策略更為人造腎臟的構(gòu)建提供了堅實基礎(chǔ)。通過不斷優(yōu)化培養(yǎng)體系與前體細(xì)胞的互作模式,未來或許能夠在實驗室中生成具備完整功能的腎臟,用于替代衰竭的器官。
近岸蛋白相關(guān)產(chǎn)品
近岸蛋白提供多種類器官體外培養(yǎng)全方案,包括基質(zhì)膠、培養(yǎng)基、相關(guān)細(xì)胞因子等:
經(jīng)類器官培養(yǎng)驗證的完全培養(yǎng)基
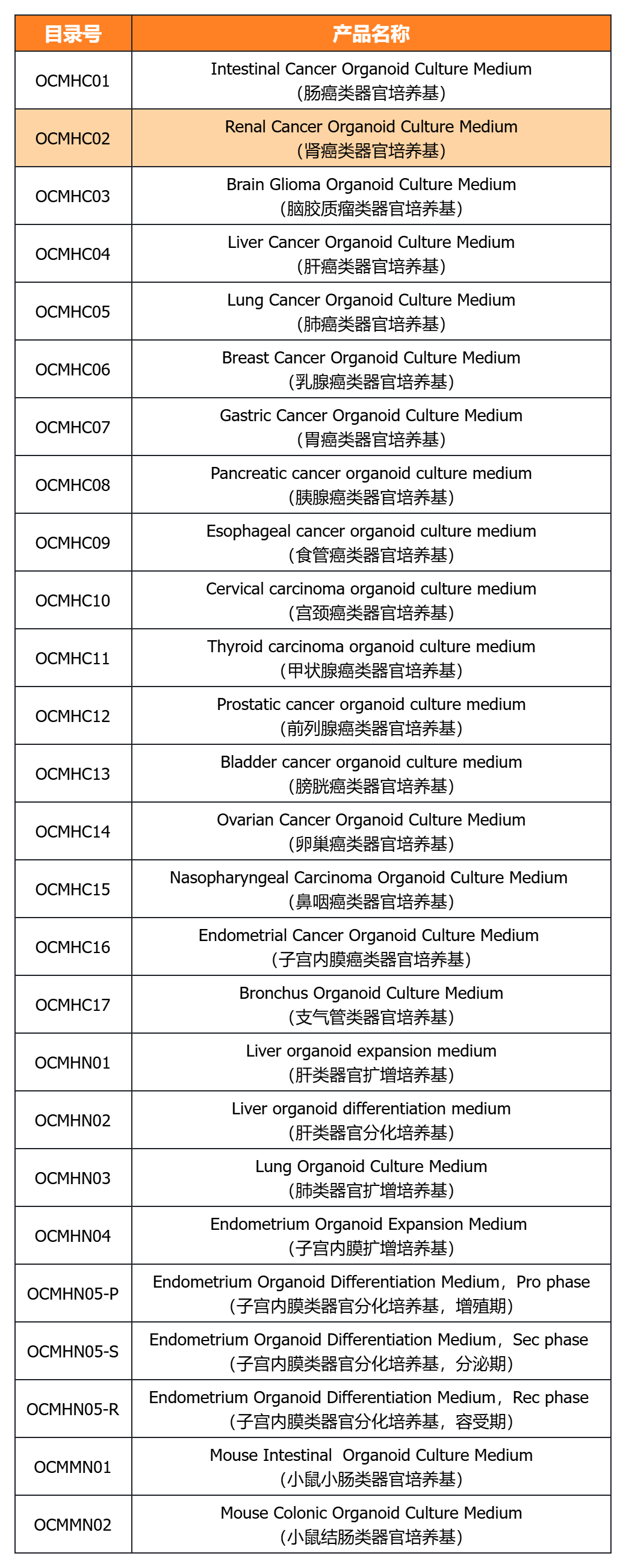
經(jīng)類器官培養(yǎng)驗證的細(xì)胞因子
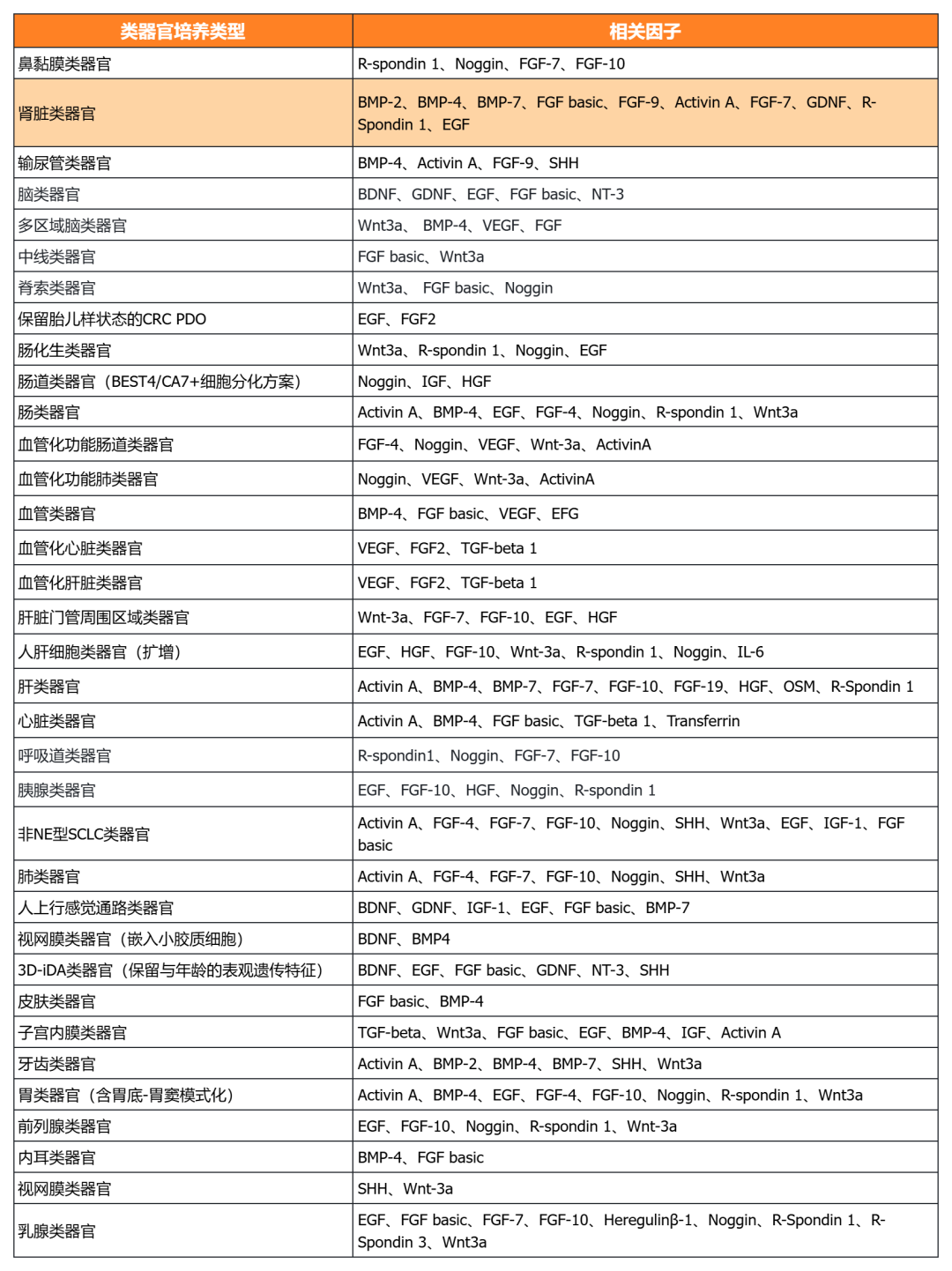
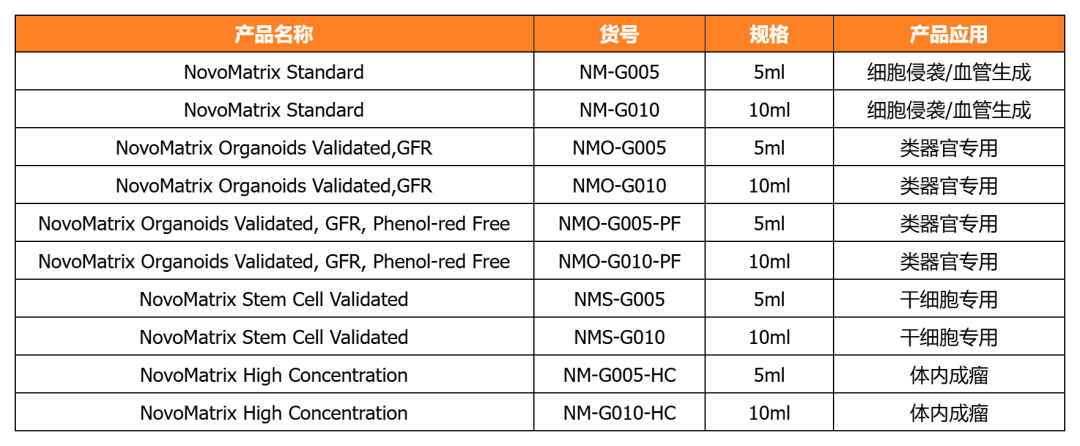
NovoMatrix 基質(zhì)膠
參考資料
Huang B, Medina P, He J, et al. Spatially patterned kidney assembloids recapitulate progenitor self-assembly and enable high-fidelity in vivo disease modeling. Cell Stem Cell. Published online September 17, 2025. doi:10.1016/j.stem.2025.08.013
