
編者按
轉(zhuǎn)化生長(zhǎng)因子β(TGF-β)是分泌型二聚體細(xì)胞因子多功能家族的原型成員,TGF-β信號(hào)通路的每一步都受到精確控制,并與其他信號(hào)通路串?dāng)_。上皮-間充質(zhì)轉(zhuǎn)化(EMT)是一種動(dòng)態(tài)且可逆的形態(tài)過程,是胚胎發(fā)育[1](Nakajima等人,2000)和傷口愈合[2](Barriere等人,2015)過程中的瞬時(shí)和可逆的關(guān)鍵過程。此外,它在病理過程中起著重要作用,特別是在癌癥進(jìn)展和纖維化中[3-4](Zeisberg等人,2007;Derynck&Weinberg,2019年)。TGF-β是EMT的有效誘導(dǎo)劑[5](Derynck等人,2014)。鞘糖脂(GSL)是在細(xì)胞膜中發(fā)現(xiàn)的主要一類糖脂。
今天,我們特別關(guān)注一項(xiàng)2022年12月由荷蘭萊頓大學(xué)醫(yī)學(xué)中心蛋白質(zhì)組學(xué)和代謝組學(xué)中心研究團(tuán)隊(duì)在EMBO J(IF=11.4)上發(fā)表的研究成果,該研究構(gòu)建了斑馬魚異種移植模型,并利用小鼠正常乳腺上皮NMuMG細(xì)胞和人肺上皮腺癌A549細(xì)胞,通過分析糖組學(xué)平臺(tái)研究GSLs在TGF-β誘導(dǎo)的EMT中的改變和作用,結(jié)果表明,通過失活糖基轉(zhuǎn)移酶UGCG來抑制GSL表達(dá)可促進(jìn)TGF-β信號(hào)傳導(dǎo)和TGF-β誘導(dǎo)的EMT;在TGF誘導(dǎo)的EMT期間,這兩種細(xì)胞系中的GSLsβ顯著降低,催化A系列神經(jīng)節(jié)苷脂合成的ST3GAL5抑制了TGF-β信號(hào)轉(zhuǎn)導(dǎo)反應(yīng)。這些神經(jīng)節(jié)苷脂被發(fā)現(xiàn)可以確定TβRI在脂筏中的定位并控制其泛素化和周轉(zhuǎn)。值得注意的是,研究者發(fā)現(xiàn)ST3GAL5在肺癌組織中的表達(dá)水平遠(yuǎn)低于在鄰近正常組織中的表達(dá)水平,并且其表達(dá)與肺癌患者的良好預(yù)后相關(guān)。
文章題目
ST3GAL5‐catalyzed gangliosides inhibit TGF‐β‐induced epithelial‐mesenchymal transition via TβRI degradation
雜志:EMBO JOURNALEMBO J(IF=11.4)
發(fā)表時(shí)間:2022.12.12
作者:Jing Zhang, Tao Zhang, Peter ten Dijke等
單位:荷蘭萊頓大學(xué)醫(yī)學(xué)中心蛋白質(zhì)組學(xué)和代謝組學(xué)中心等
01、研究結(jié)果
1. TGF‐β抑制NMuMG和A549‐VIM-RFP細(xì)胞中神經(jīng)節(jié)苷脂的表達(dá)
為了研究TGF-β誘導(dǎo)的接受EMT的細(xì)胞中GSL-聚糖的變化,研究者們選擇了兩種具有顯著TGF-β誘導(dǎo)的EMT反應(yīng)的成熟細(xì)胞模型,即NMuMG(Zhang等人,2020a)和A549-波形蛋白(VIM)-紅色熒光蛋白(RFP)細(xì)胞系(Wang等人,2020)。
結(jié)果顯示,在TGF-β刺激的A549-VIM-RFP細(xì)胞中觀察到GSLs的絕對(duì)豐度大幅下降,用TGF-β刺激NMuMG和A549-VIM-RFP細(xì)胞可顯著降低ST3GAL5蛋白表達(dá)。此外,TGF-β降低了NMuMG細(xì)胞中B4galnt1、B5galt6和St3gal5的基因表達(dá)水平,這些必需酶催化神經(jīng)節(jié)苷脂的形成。
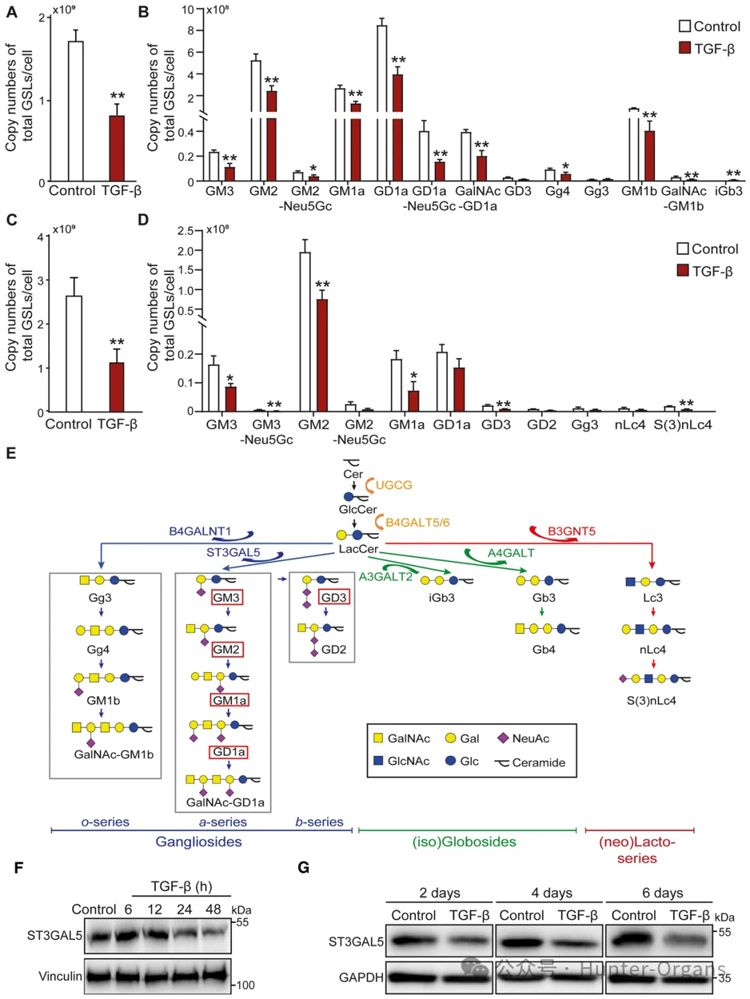
圖1
2. UGCG敲除導(dǎo)致NMuMG細(xì)胞中TGF-β信號(hào)轉(zhuǎn)導(dǎo)和TGF-β誘導(dǎo)的EMT的增強(qiáng)
糖基轉(zhuǎn)移酶UGCG是啟動(dòng)復(fù)雜GSL結(jié)構(gòu)合成途徑的第一種酶,為了研究GSLs在TGF-β信號(hào)傳導(dǎo)中的作用,研究者通過基因編輯生成UgcgNMuMG敲除(KO)細(xì)胞,進(jìn)行UGCG酶活性測(cè)定、CTB和FACS分析、糖組分析和單個(gè)GSL絕對(duì)豐度的定量分析、RNA測(cè)序(RNA-seq)、基因集富集分析(GSEA)證實(shí)了UGCG介導(dǎo)TGF-β信號(hào)傳導(dǎo)抑制的假設(shè)。
隨后,研究者檢查了Ugcg耗竭對(duì)NMuMG細(xì)胞中TGF-β誘導(dǎo)的反應(yīng)和EMT標(biāo)志物表達(dá)水平的影響。結(jié)果進(jìn)一步驗(yàn)證了TGF-β誘導(dǎo)EMT增強(qiáng)。EMT的激活可以使細(xì)胞遷移能力增強(qiáng)。因此,研究者進(jìn)一步研究了NMuMG細(xì)胞中UgcgKO的基礎(chǔ)遷移率。與對(duì)照細(xì)胞相比,具有Ugcg耗竭的NMuMG細(xì)胞顯示出遷移增強(qiáng)。綜上所述,UGCG是NMuMG細(xì)胞中TGF-β/SMAD信號(hào)轉(zhuǎn)導(dǎo)和EMT的關(guān)鍵抑制劑。
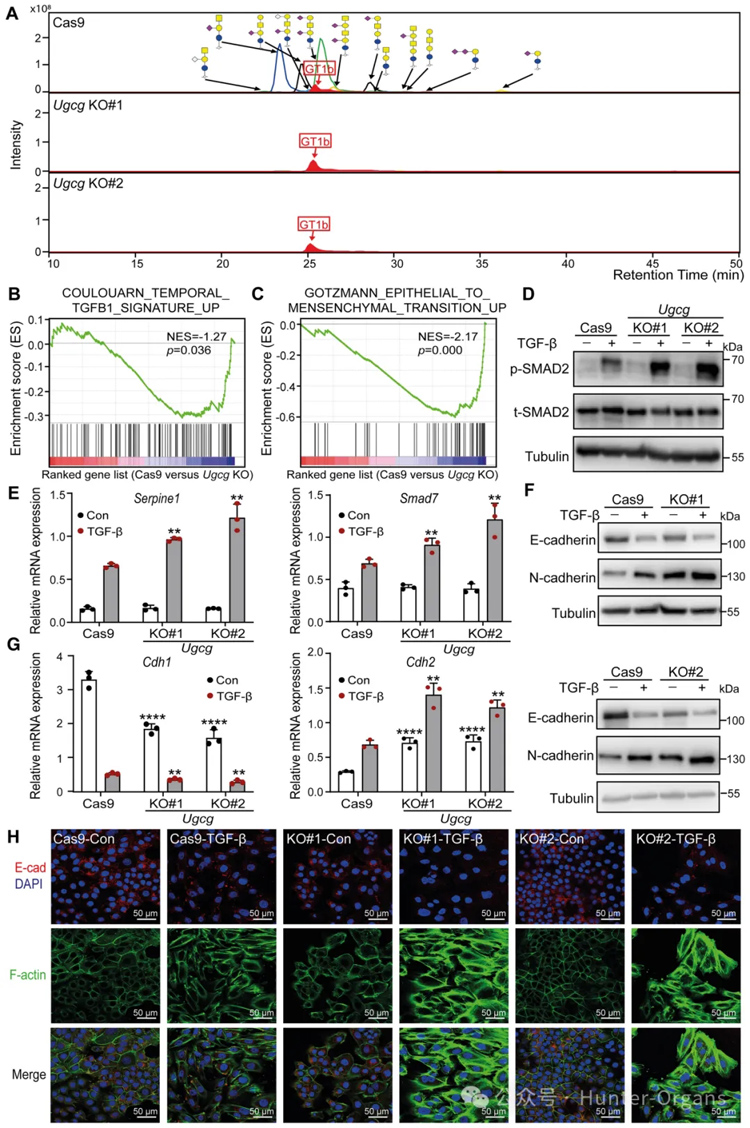
圖2
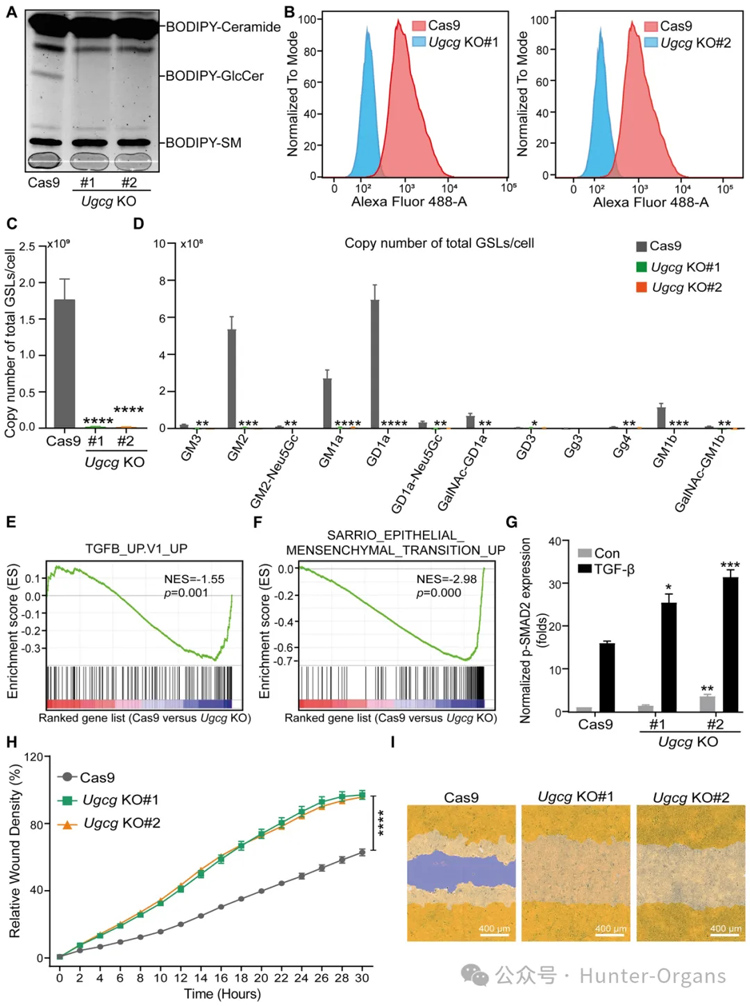
圖3
3. Eliglustat是一種UGCG活性抑制劑,可促進(jìn)TGF-β信號(hào)傳導(dǎo)、TGFβ誘導(dǎo)的EMT、細(xì)胞遷移、外滲和早期轉(zhuǎn)移性生長(zhǎng)
研究者們通過通過使用FACS分析測(cè)量GM1表達(dá)來證實(shí)eliglustat作為UGCG抑制劑的有效性;qRT-PCR分析證實(shí),eliglustat通過增加TGF-β靶基因(包括SMAD7、SERPINE1和CCN2)的表達(dá)水平來促進(jìn)TGF-β信號(hào)轉(zhuǎn)導(dǎo);通過RFP標(biāo)記的波形蛋白表達(dá)的動(dòng)態(tài)增加和F-肌動(dòng)蛋白形成的增強(qiáng),進(jìn)一步證實(shí)了eliglustat介導(dǎo)的TGF-β誘導(dǎo)的EMT的促進(jìn);通過劃痕測(cè)定證明eliglustat處理增強(qiáng)了基礎(chǔ)和TGF-β誘導(dǎo)的細(xì)胞遷移。
此外,添加SB505124完全阻斷了eliglustat誘導(dǎo)的細(xì)胞遷移促進(jìn),表明eliglustat誘導(dǎo)的細(xì)胞遷移需要TβRI信號(hào)傳導(dǎo)。基于此,研究者使用斑馬魚異種移植模型系統(tǒng)研究了eliglustat對(duì)A549細(xì)胞外滲的影響;通過尾靜脈將A549-Luc細(xì)胞注射到裸鼠體內(nèi),研究了eliglustat對(duì)A549-Luc細(xì)胞轉(zhuǎn)移能力的影響。數(shù)據(jù)表明,UGCG和UGCG定義的GSL抑制小鼠上皮NMuMG細(xì)胞和人肺癌A549細(xì)胞中的TGF-β信號(hào)傳導(dǎo)和EMT,以及A549細(xì)胞的遷移、外滲和轉(zhuǎn)移。
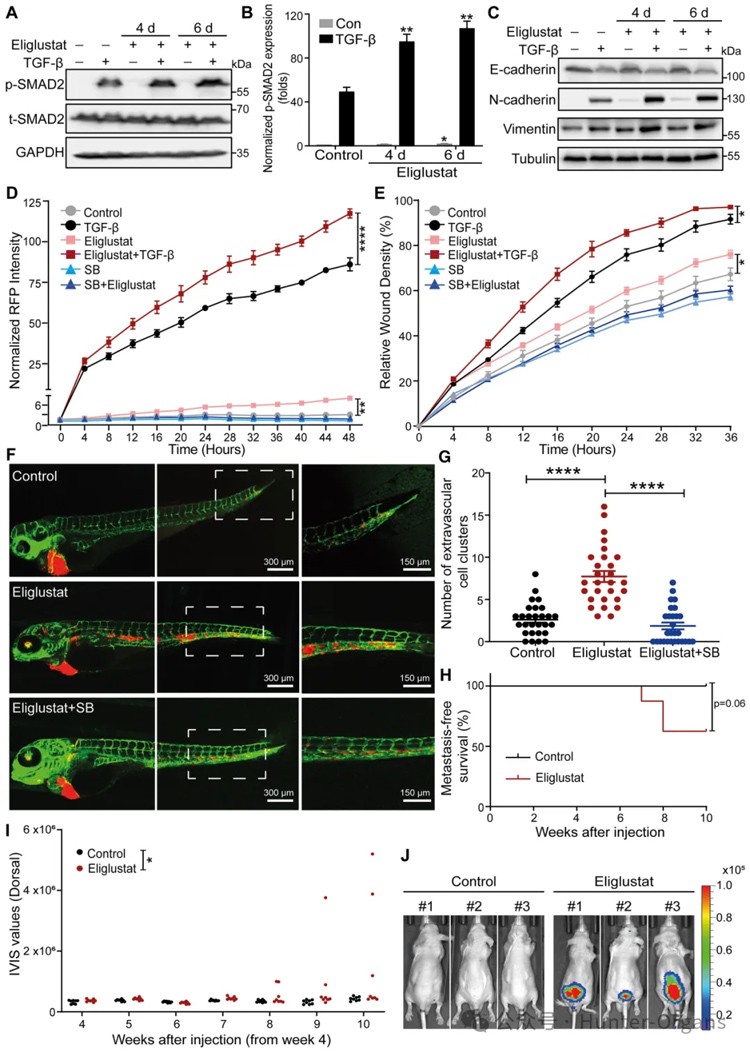
圖4

圖5
4. 抑制GSL生物合成可降低TβRI在脂筏中的定位,保護(hù)TβRI免受泛素化并增加其穩(wěn)定性
鞘糖脂被發(fā)現(xiàn)可以通過促進(jìn)脂筏或小窩膜中膜錨定分子之間的橫向相互作用來影響信號(hào)轉(zhuǎn)導(dǎo),為研究GSLs控制TGF-β受體信號(hào)轉(zhuǎn)導(dǎo)和TGF-β-receptor誘導(dǎo)的EMT機(jī)制,研究者通過免疫印跡分析,專門檢查細(xì)胞表面TβRI池,可觀察到用eliglustat處理的A549-VIM-RFP細(xì)胞中的細(xì)胞表面TβRI水平顯著增加。因此,研究者研究了抑制GSL合成是否會(huì)影響TβRI在質(zhì)膜中脂筏和非脂筏微結(jié)構(gòu)域之間的分配,結(jié)果顯示GSL生物合成減少會(huì)降低脂筏組分中的TβRI水平。
此外,研究者研究了eliglustat對(duì)TβRI泛素化的影響、eliglustat在調(diào)節(jié)TβRI穩(wěn)定性中的作用,這些結(jié)果表明,從機(jī)制上講,GSL誘導(dǎo)的TGF-β信號(hào)轉(zhuǎn)導(dǎo)抑制是由于有利于TβRI在脂筏中的定位而引起的,從而觸發(fā)其泛素化和隨后的降解。
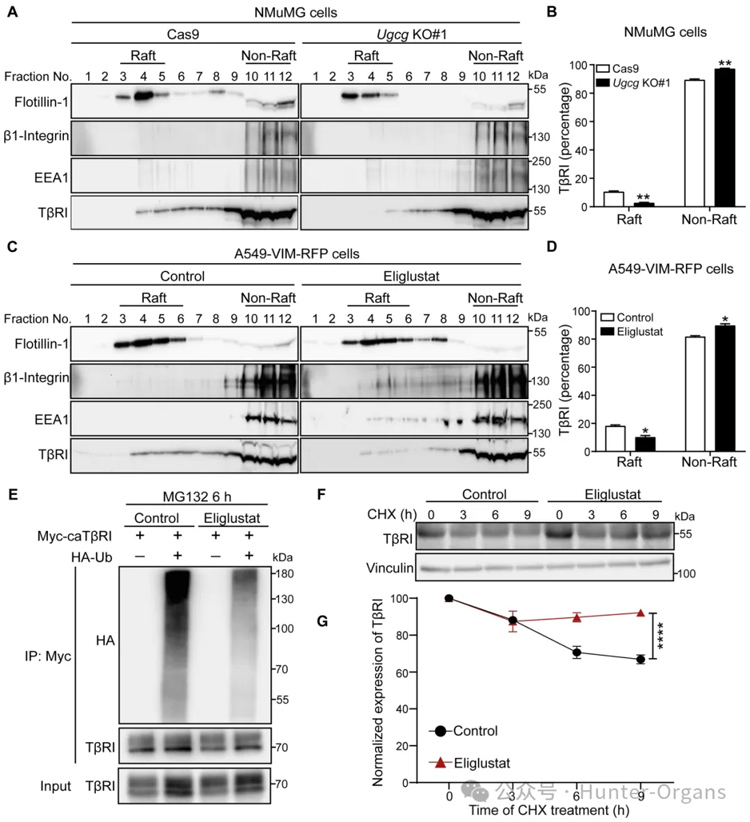
圖6
5. ST3GAL5介導(dǎo)的A系列神經(jīng)節(jié)苷脂生物合成抑制TGFβ信號(hào)傳導(dǎo)和TGFβ誘導(dǎo)的EMT
使用PGCnano-LC-ESI-MS/MS對(duì)缺乏ST3GAL5或B4GALNT1的細(xì)胞進(jìn)行糖組分析證實(shí)了這兩種酶產(chǎn)生的特定神經(jīng)節(jié)苷脂產(chǎn)物的大幅減少。ST3GAL5敲低細(xì)胞的GM3、GM2和GM1a顯著降低,與TGF-β處理后的結(jié)果一致。然而,B4GALNT1敲除導(dǎo)致總GSL水平與TGF-β對(duì)神經(jīng)節(jié)苷脂水平的影響非常不同。
接下來,研究者研究了ST3GAL5和B4GALNT1敲低對(duì)A549細(xì)胞中TGF-β信號(hào)傳導(dǎo)和EMT的影響。結(jié)果證明ST3GAL5的異位表達(dá)通過下調(diào)TGF-β誘導(dǎo)的SMAD2磷酸化和SMAD3依賴性CAGA-GFP報(bào)告基因活性,以及降低TGF-β/SMAD靶基因的轉(zhuǎn)錄水平來抑制TGF-β信號(hào)通路。TGF-β誘導(dǎo)的EMT也被ST3GAL5過表達(dá)所抑制。所有這些結(jié)果都表明,ST3GAL5而非B4GALNT是TGF-β信號(hào)傳導(dǎo)和TGF-β誘導(dǎo)的EMT的關(guān)鍵參與者。
ST3GAL5催化LacCer轉(zhuǎn)化為GM3,GM3是前體神經(jīng)節(jié)苷脂,用于延伸和進(jìn)一步支化反應(yīng),產(chǎn)生a系列神經(jīng)節(jié)苷脂以及b系列神經(jīng)節(jié)苷脂。兩種類型的神經(jīng)節(jié)苷脂在NMuMG和A549細(xì)胞中均高表達(dá)。接下來,研究者研究了添加外源性神經(jīng)節(jié)苷脂對(duì)TGF-β信號(hào)轉(zhuǎn)導(dǎo)的影響,發(fā)現(xiàn)a系列神經(jīng)節(jié)苷脂處理后的兩種細(xì)胞對(duì)TGF-β誘導(dǎo)的SMAD3依賴性CAGA-GFP報(bào)告基因活性表現(xiàn)出顯著抑制,而b系列神經(jīng)節(jié)苷脂處理的細(xì)胞與對(duì)照細(xì)胞相比沒有變化。此外,a系列神經(jīng)節(jié)苷脂的外源添加消除了TGF-β誘導(dǎo)的間充質(zhì)標(biāo)志物的表達(dá),TGF-β誘導(dǎo)的RFP標(biāo)記波形蛋白表達(dá)的促進(jìn)。此外,在用外源性a系列神經(jīng)節(jié)苷脂刺激后,A549-VIM-RFP細(xì)胞在TGF-β處理后表現(xiàn)出比對(duì)照細(xì)胞更少的F-肌動(dòng)蛋白形成。綜上所述,ST3GAL5合成的a系列神經(jīng)節(jié)苷脂在TGF-β信號(hào)傳導(dǎo)和TGF-β誘導(dǎo)的EMT中起關(guān)鍵作用。
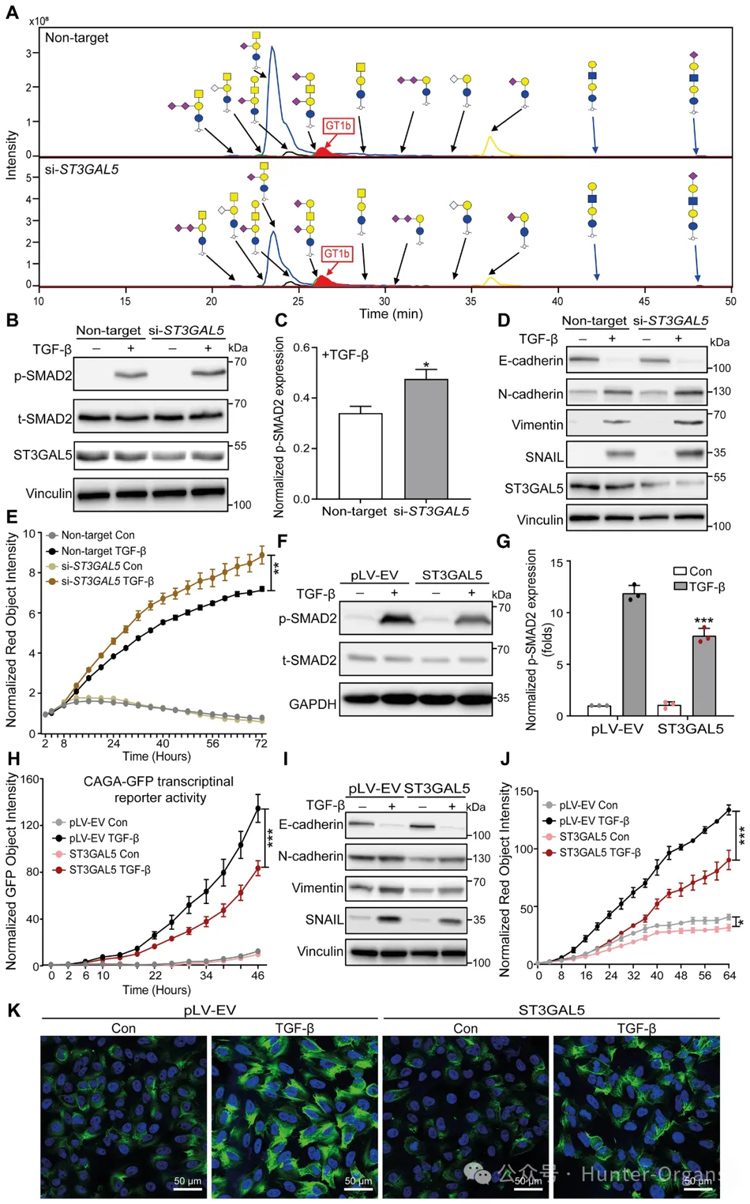
圖7

圖8
6. ST3GAL5促進(jìn)SMAD7-SMURF2誘導(dǎo)的泛素化和TβRI降解
接下來,研究者研究了ST3GAL5誘導(dǎo)TGF-β信號(hào)傳導(dǎo)抑制的機(jī)制。由于MDA-MB-231細(xì)胞中的內(nèi)源性TβRI水平遠(yuǎn)高于NMuMG細(xì)胞和A549細(xì)胞,因此使用MDA-MB-231細(xì)胞系來研究神經(jīng)節(jié)苷脂對(duì)TβRI泛素化的影響。研究者觀察到,將外源性a系列神經(jīng)節(jié)苷脂(GM1a、GM2或GM3)添加到感染HA-Ub慢病毒的MDA-MB-231細(xì)胞中可促進(jìn)TβRI的泛素化。
此外,GM3誘導(dǎo)的TβRI泛素化增加因SMURF2的敲低而減弱,表明該E3連接酶參與TβRI的泛素化。定量結(jié)果顯示,GM3處理顯著降低了TβRI在細(xì)胞表面的表達(dá),并且通過添加蛋白酶體抑制劑MG132或溶酶體抑制劑BafA1減弱了這種作用,表明GM3誘導(dǎo)的TβRI降解是通過蛋白酶體和溶酶體途徑介導(dǎo)的。這些結(jié)果表明,ST3GAL5催化的a系列神經(jīng)節(jié)苷脂通過降低細(xì)胞表面表達(dá)和TβRI的穩(wěn)定性來減輕TGF-β信號(hào)轉(zhuǎn)導(dǎo)反應(yīng)并增加SMURF2誘導(dǎo)的TβRI泛素化。
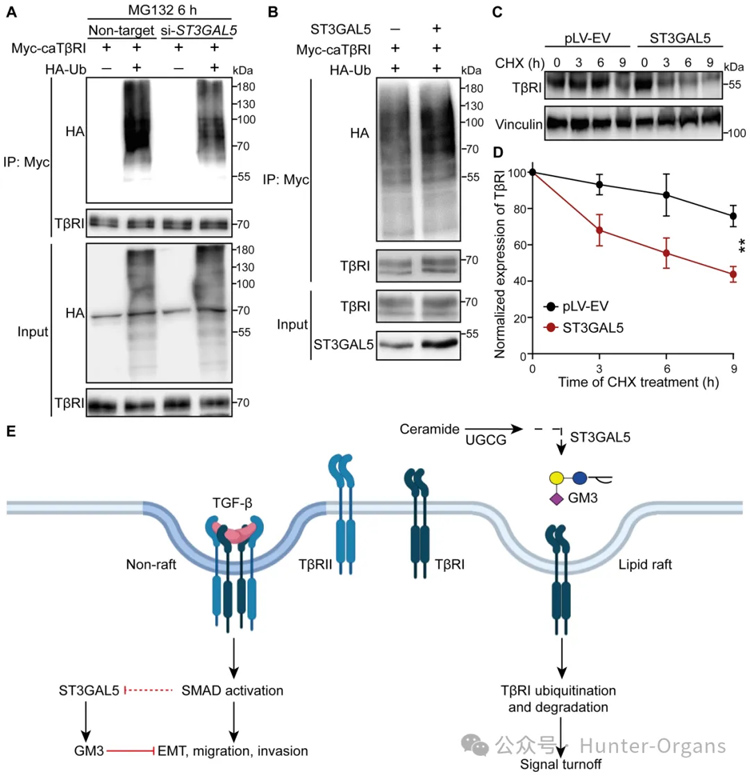
圖9
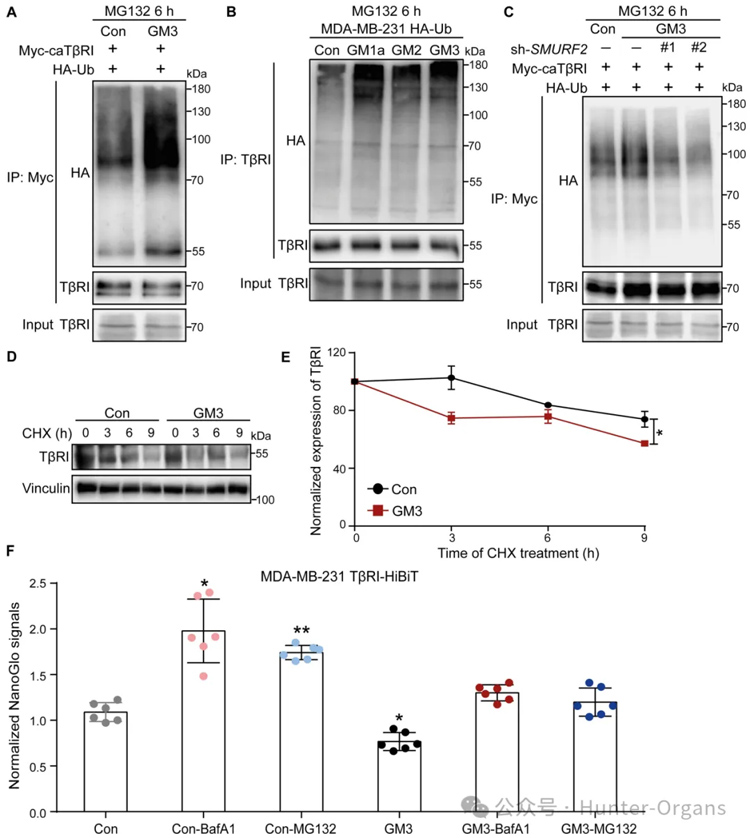
圖10
7. ST3GAL5的異位表達(dá)抑制A549細(xì)胞遷移、侵襲和轉(zhuǎn)移性生長(zhǎng),并與肺癌的良好預(yù)后有關(guān)
為了研究ST3GAL5和通過其催化活性在A549細(xì)胞遷移中產(chǎn)生的神經(jīng)節(jié)苷脂的功能,研究者使用siRNA介導(dǎo)的ST3GAL5敲低或轉(zhuǎn)染對(duì)照siRNA對(duì)A549細(xì)胞進(jìn)行了劃痕測(cè)定。ST3GAL5的過表達(dá)顯著抑制了TGF-β誘導(dǎo)的遷移。此外,添加GM1a、GM2或GM3會(huì)降低A549-VIM-RFP細(xì)胞在TGF-β刺激下的遷移能力。接下來,研究者分析了肺癌A549細(xì)胞中ST3GAL5錯(cuò)誤表達(dá)對(duì)斑馬魚異種移植模型外滲的影響。將ST3GAL5耗竭或過表達(dá)的mCherry表達(dá)A549細(xì)胞注射到斑馬魚胚胎中,注射后4天計(jì)數(shù)血管外簇。在注射ST3GAL5敲低A549細(xì)胞的斑馬魚胚胎組中觀察到更多的血管間細(xì)胞簇。ST3GAL5的異位表達(dá)強(qiáng)烈抑制了斑馬魚模型中A549細(xì)胞的外滲。然后,研究者使用注射有或沒有ST3GAL5過表達(dá)的A549-Luc細(xì)胞的5周齡BALB/cnu/nu小鼠來研究ST3GAL5對(duì)細(xì)胞轉(zhuǎn)移生長(zhǎng)能力的影響。結(jié)果與其在體外和斑馬魚異種移植模型中的發(fā)現(xiàn)一致,即在注射ST3GAL5過表達(dá)A549-Luc細(xì)胞的小鼠中檢測(cè)到初始細(xì)胞轉(zhuǎn)移的時(shí)間晚于注射A549-Luc對(duì)照細(xì)胞的小鼠。此外,ST3GAL5的異位表達(dá)抑制了循環(huán)A549細(xì)胞的早期轉(zhuǎn)移。
接下來,鑒于ST3GAL5在調(diào)節(jié)細(xì)胞遷移和侵襲中的關(guān)鍵作用,研究者研究了ST3GAL5是否可能是早期肺癌的相關(guān)生物標(biāo)志物。使用982名肺癌患者的公開隊(duì)列,我們發(fā)現(xiàn)ST3GAL5的低表達(dá)與首次進(jìn)展前的生存預(yù)后不良有關(guān)。此外,研究者通過使用ST3GAL5特異性抗體進(jìn)行免疫組織化學(xué)(IHC)染色,檢查了組織微陣列中ST3GAL5蛋白水平,該陣列包含來自50名患者的150個(gè)肺癌組織和相鄰表型正常組織。與癌癥組織相比,ST3GAL5在鄰近的正常組織中高表達(dá)。總之,這些結(jié)果表明,ST3GAL5表達(dá)抑制細(xì)胞遷移、侵襲和轉(zhuǎn)移,并且與肺癌的良好預(yù)后相關(guān)。
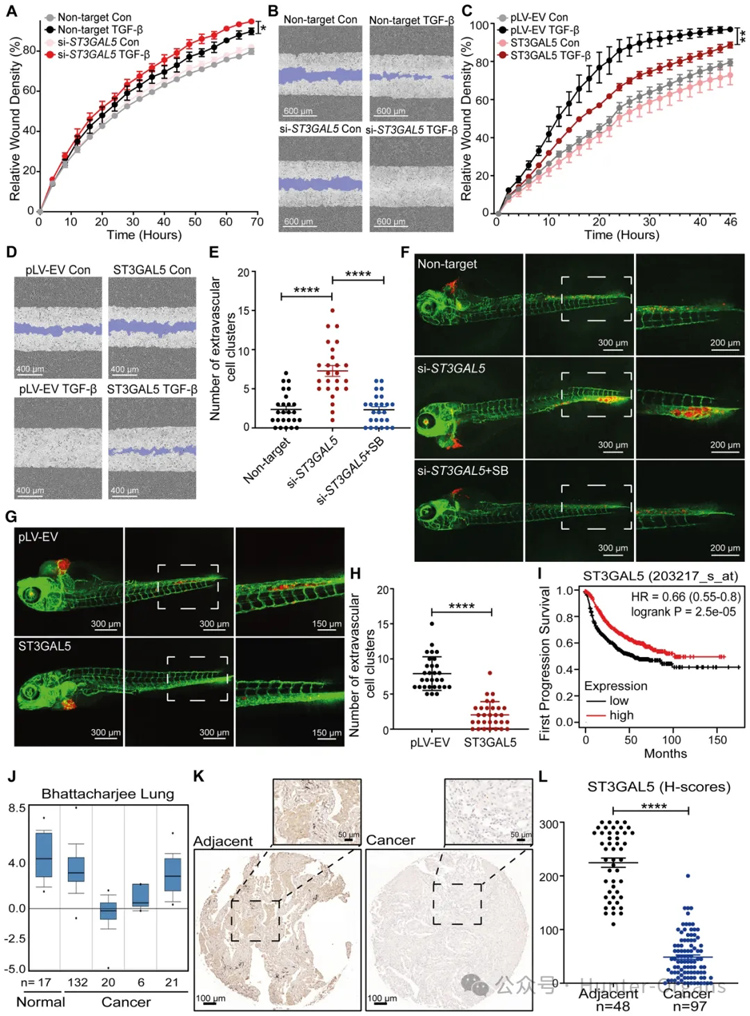
圖11
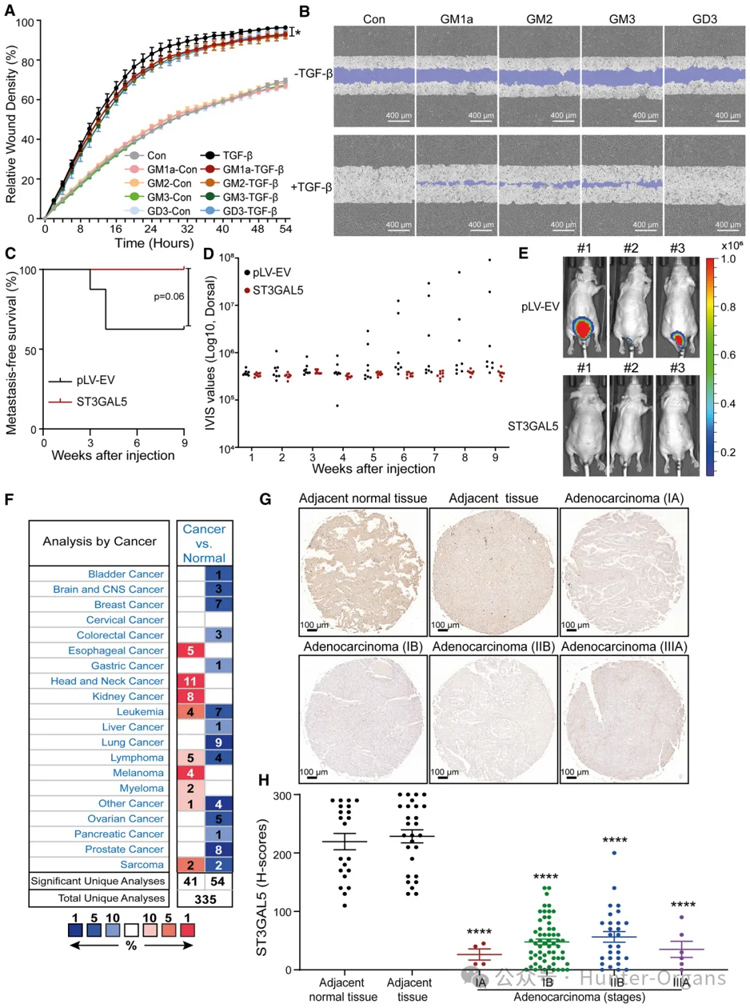
圖12
作為健康美麗產(chǎn)業(yè)CRO服務(wù)開拓者與引領(lǐng)者、斑馬魚生物技術(shù)的全球領(lǐng)導(dǎo)者,環(huán)特生物搭建了“斑馬魚、類器官、哺乳動(dòng)物、人體”四位一體的綜合技術(shù)服務(wù)體系,開展健康美麗CRO服務(wù)、科研服務(wù)、智慧實(shí)驗(yàn)室搭建三大業(yè)務(wù)。目前,環(huán)特已建立200多種斑馬魚模型及腦類器官、心臟類器官及各種腫瘤類器官培養(yǎng)平臺(tái),歡迎有需要的讀者垂詢!
