
編者按
為什么年輕人傷口愈合快,老年人卻容易久久不愈?為什么斑馬魚能再生肢體和心臟,而人類卻不行?隨著年齡增長,身體的“自我修復”能力不斷下降,這背后究竟發生了什么?
最近,一項發表在Theranostics(IF13.3)上的研究成果利用斑馬魚早衰(SAZ) 模型及基因編輯技術,揭開了衰老導致組織再生能力下降的關鍵機制,并給出了一種令人意外的干預策略——原來,不是干細胞不行了,而是“清潔工”巨噬細胞出bug了,衰老會通過改變巨噬細胞的代謝適應和極化、吞噬作用等功能來抑制組織再生。只要早期促進糖酵解,就能讓衰老個體的組織再生能力“起死回生”。
01、研究亮點
通過斑馬魚基因編輯技術敲降 terfa(TRF2)基因,成功構建斑馬魚早衰(SAZ)模型,并首次揭示巨噬細胞在衰老引起的再生障礙中的核心作用;
發現衰老會加速斑馬魚巨噬細胞功能受損,衰老導致巨噬細胞在再生早期無法正常上調 ldha 表達和糖酵解代謝,從而損害其促炎極化和吞噬功能;
發現乳酸代謝是再生關鍵節點,通過LDHA/B抑制劑Galloflavin可以完全阻斷寡霉素的拯救效應,直接證實乳酸生成在巨噬細胞介導的再生過程中的必要性;
通過斑馬魚、異種共生實驗和細胞分選、小鼠實驗等多層次揭示了衰老導致的巨噬細胞功能異常是再生能力下降的核心原因,發現巨噬細胞是衰老影響組織再生的關鍵。
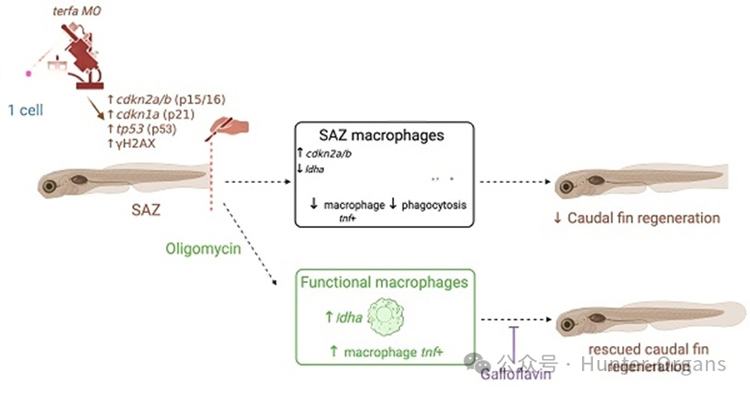
圖1
02、主要研究成果
1. 構建斑馬魚早衰(SAZ)模型
terfa 基因編碼的蛋白TRF2是保護染色體末端“端粒”的關鍵分子。研究人員通過斑馬魚基因編輯技術敲降terfa(TRF2)基因,成功建立了具有衰老特征但早期發育正常的斑馬魚早衰(SAZ)模型。敲低terfa基因后,斑馬魚呈現出典型的衰老特征:DNA 損傷標志 γH2AX 顯著增多;衰老標志物cdkn2a/b、cdkn1a、tp53基因及衰老相關分泌表型因子IL-6、MMP9 表達上調,同時出現再生能力顯著下降。但這些早衰斑馬魚的尾鰭發育和游動能力完全正常,它們只是“老”了,而不是發育畸形。
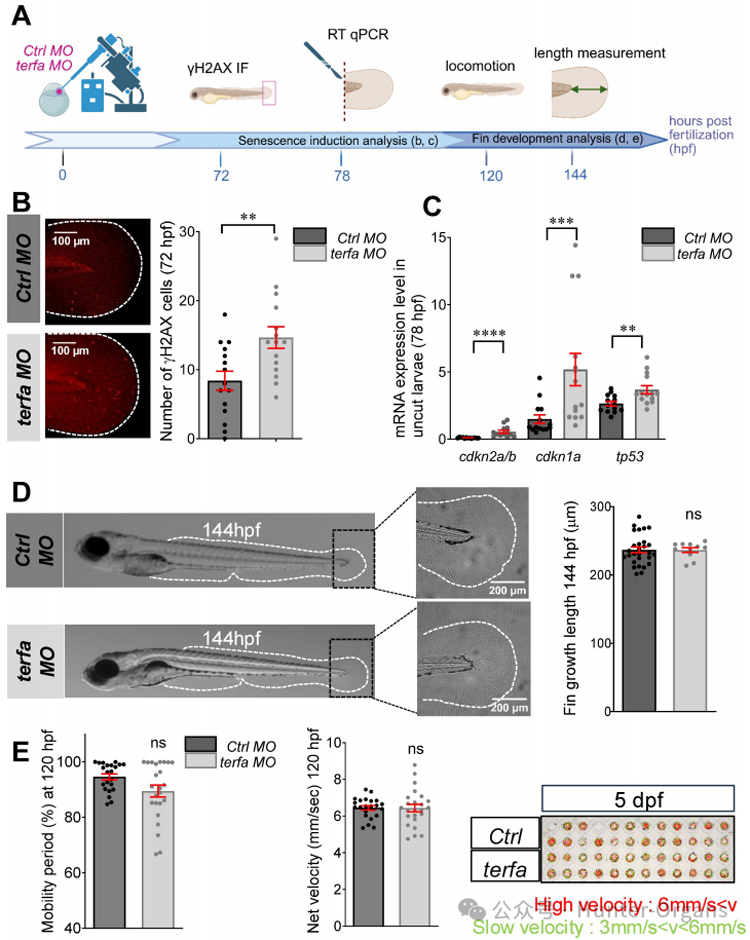
圖2
2. 斑馬魚早衰SAZ模型再生能力受損
斑馬魚是組織再生研究的重要模型生物,正常斑馬魚在尾鰭切除后,72 小時內就能長回接近原來的長度和面積。然而,當研究人員剪掉早衰斑馬魚的尾鰭后,發現斑馬魚的再生能力被嚴重抑制,表現為再生長度減少約30-40%,再生面積明顯縮小;lin28表達降低,胚基形成受阻;增殖細胞標記物pH3陽性細胞數量顯著減少。這表明,斑馬魚早衰SAZ模型的再生能力確實受到了損害,且與細胞周期停滯和增殖能力下降有關。
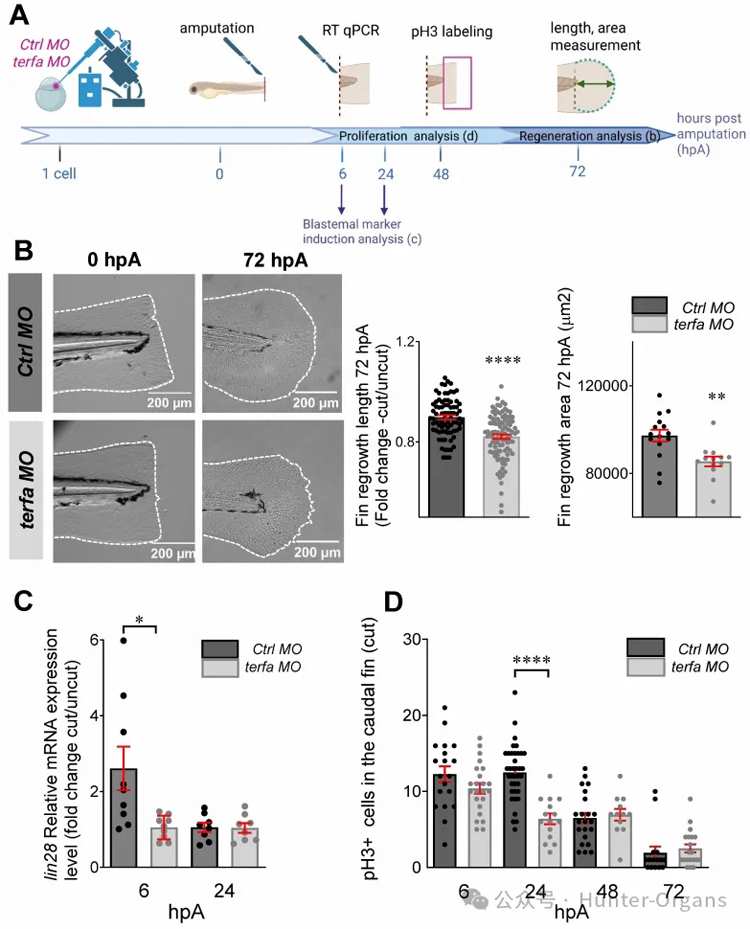
圖3
3. 早衰斑馬魚的巨噬細胞響應遲緩且偏向抗炎
那么,衰老究竟是通過哪些細胞、哪些分子機制來抑制組織再生的?研究人員通過異種共生實驗,把早衰魚和正常魚“縫合”在一起,共享血液循環,讓早衰斑馬魚獲得正常的巨噬細胞,結果,早衰斑馬魚的尾鰭再生能力被完全恢復。這表明,衰老相關的循環因素,特別是衰老的巨噬細胞參與了組織再生能力的下降。
分離并純化對照組和SAZ組的巨噬細胞,SAZ組的巨噬細胞內衰老標志物cdkn2a/b的表達水平顯著高于對照組的巨噬細胞。這表明,在SAZ模型中,巨噬細胞本身確實表現出更高的衰老特征,揭示了衰老不僅影響其他細胞類型,也直接作用于關鍵的免疫細胞——巨噬細胞。
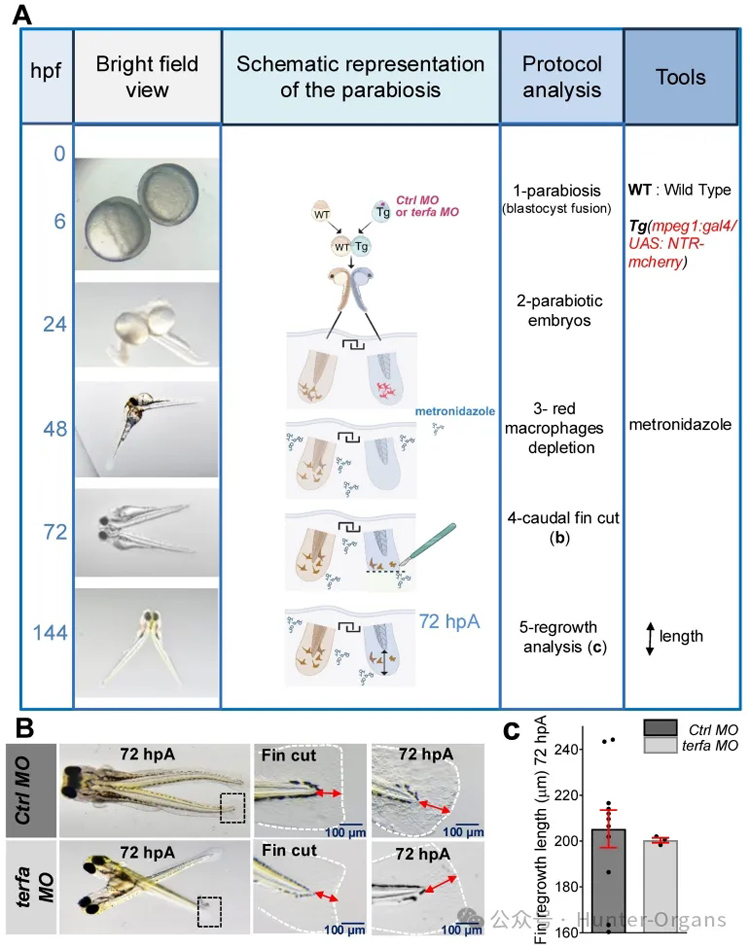
圖4
隨后,研究人員利用轉基因斑馬魚,實時追蹤斑馬魚尾鰭切除后不同時間點傷口處的巨噬細胞募集情況、TNFα+比例等免疫反應。結果令人驚訝,兩種品系的巨噬細胞都能迅速募集到傷口,但SAZ組衰老斑馬魚傷口處的TNFα+巨噬細胞的比例在再生早期(6h和24h)顯著低于對照組。表達TNFα的促炎性巨噬細胞數量顯著減少,同時,巨噬細胞的吞噬功能也受到損害,巨噬細胞吞噬脂質體和細胞碎片的能力顯著下降。因此,SAZ巨噬細胞雖然能到達傷口,但其向關鍵的促炎表型(TNFa+)的極化能力受損,尤其是在再生早期。
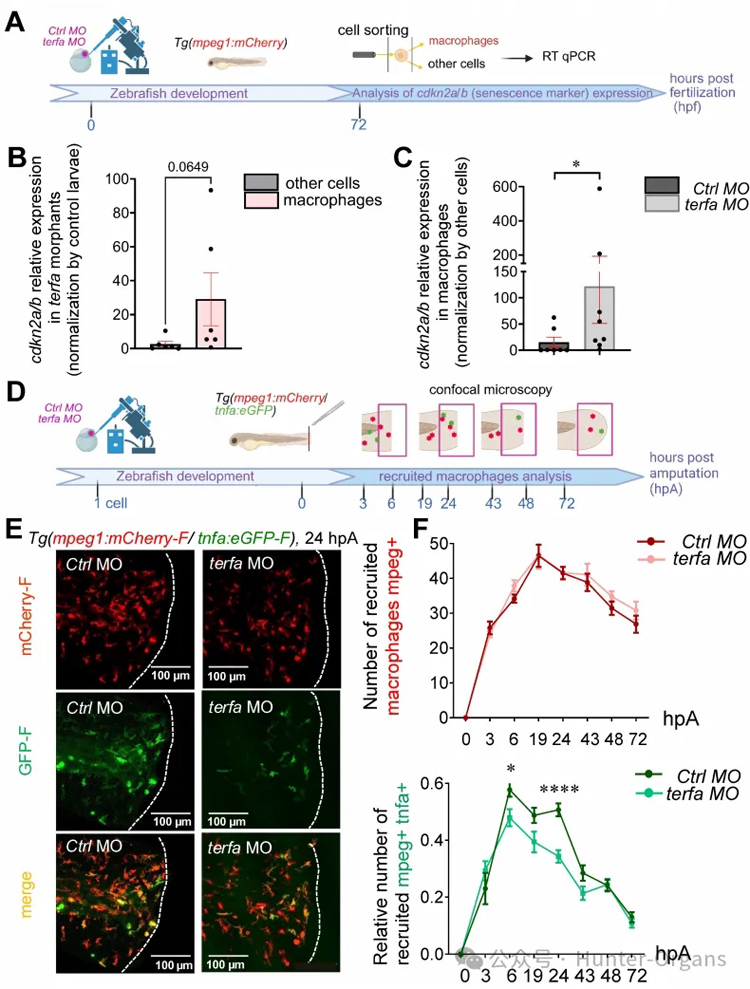
圖5
4. SAZ巨噬細胞的糖酵解能力,可以使組織再生能力回歸
為什么早衰斑馬魚的巨噬細胞功能會失常?研究人員把目光投向了“代謝”。巨噬細胞在傷口早期需要快速切換到糖酵解模式來獲取能量,挽救SAZ模型中受損的巨噬細胞炎癥反應和再生能力。但研究人員從早衰斑馬魚中分離出巨噬細胞后,發現一個關鍵基因ldha(乳酸脫氫酶 A)的表達大幅下降。ldha負責將丙酮酸轉化為乳酸,是糖酵解的最后一個關鍵酶。在再生早期(24 hPA),從衰老加速斑馬魚分離的巨噬細胞中 ldha mRNA 水平顯著低于對照組,而其他糖酵解酶eno3、pdbh則無明顯變化。
研究人員又用一種能間接促進糖酵解的化合物寡霉素處理早衰斑馬魚,發現寡霉素處理使衰老的斑馬魚ldha 表達、TNFα+ 巨噬細胞數量和再生長度/面積均恢復至正常水平,但全程寡霉素處理反而抑制對照組再生,這表明短暫促糖酵解恢復再生能力。需要注意的是,僅在再生早期(尾鰭切除前后各6小時)短暫促進糖酵解,即可完全恢復衰老個體的再生能力,而如果全程持續給藥,持續進行干預反而會抑制正常斑馬魚的再生。
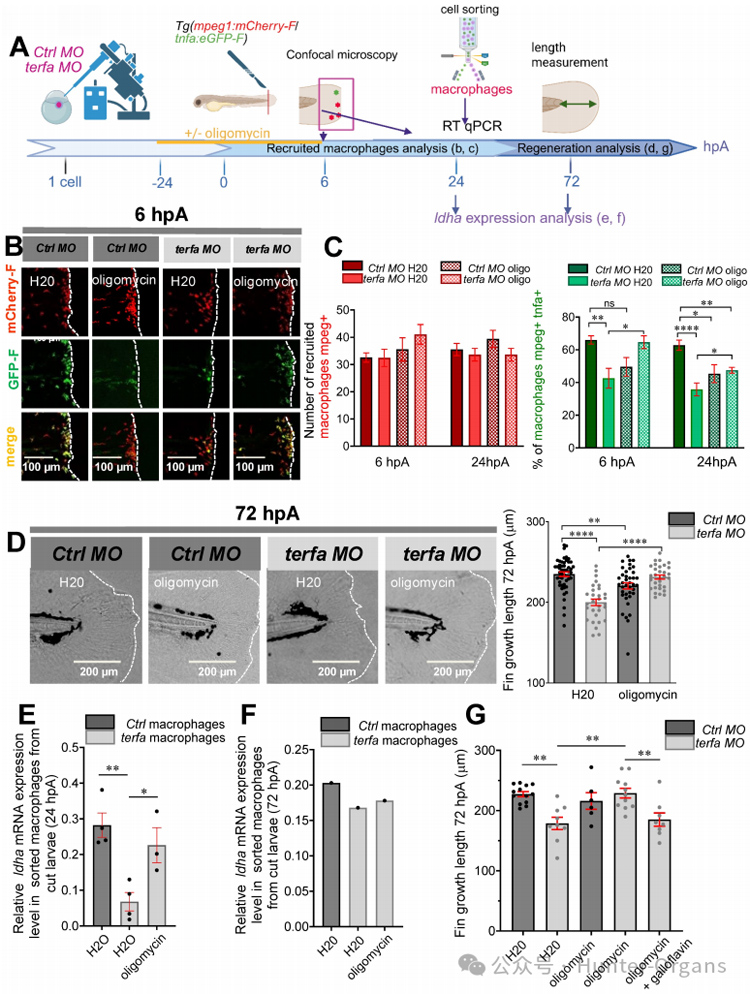
圖6
為了驗證是LDHA/乳酸通路在起作用,研究人員聯合使用了寡霉素與LDHA/B 特異性抑制劑Galloflavin,發現Galloflavin完全阻斷了寡霉素對組織再生的拯救效果,證實了寡霉素之所以能挽救SAZ的再生能力,是因為它通過上調1dha表達,增強了巨噬細胞的乳酸代謝能力。抑制乳酸代謝即可阻斷這一效應。乳酸不僅僅是代謝廢物,更是巨噬細胞執行促再生活性的關鍵節點和信號分子。
6. 哺乳動物實驗驗證巨噬細胞吞噬功能缺陷的普遍性
為了進一步驗證巨噬細胞吞噬功能缺陷是否是terfa敲低的直接結果,隨后,研究人員又在小鼠 RAW264.7巨噬細胞中敲低了terfa同源基因,發現在脂多糖(LPS)+干擾素IFNγ激活后,顯著增強了對照組巨噬細胞的吞噬能力,但在terfa敲低組,即使經過激活,吞噬能力也沒有顯著提升。因此,terfa敲低確實會損害巨噬細胞的吞噬潛力,且這種效應不局限于斑馬魚,小鼠巨噬細胞同樣會受影響。
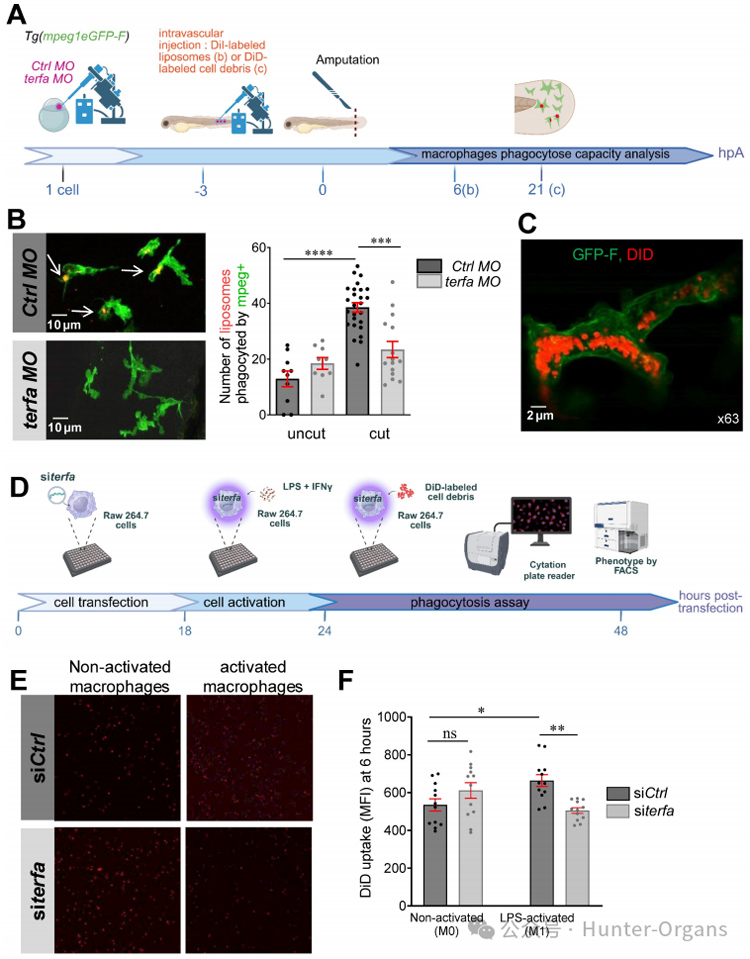
圖7
近年來,環特生物自主建立了以斑馬魚、細胞、類器官、哺乳動物、皮膚外植體和人體臨床為特色的多維生物技術解決方案,構建了斑馬魚早衰、自閉癥、抑郁癥、焦慮癥等200多種疾病模型,為疾病機制研究、尋找潛在治療策略提供了寶貴工具。歡迎有需要的客戶垂詢!
03、編者點評
本研究首次在斑馬魚早衰(SAZ)模型中,揭示了巨噬細胞代謝重編程在衰老相關再生障礙中的核心作用,發現衰老導致巨噬細胞在再生早期無法正常上調 ldha 表達和糖酵解代謝,從而損害其促炎極化和吞噬功能,并將衰老對再生的負面影響,精確到一種免疫細胞的一個代謝節點——巨噬細胞的 LDHA/乳酸通路,為改善老年人傷口愈合提供了新方向:局部、短暫地提升乳酸生成,或許能促進慢性難愈創面的修復。
作為健康美麗產業CRO服務開拓者與引領者、斑馬魚生物技術的全球領導者,環特生物基于多維生物技術服務體系,開展健康美麗CRO服務、科研服務、智慧實驗室搭建三大業務,歡迎來電咨詢——173 6453 1293遲先生!
參考文獻:
Barthelaix A, et al. Disrupted macrophage metabolic adaptation and function drive senescence-induced decline in vertebrate regeneration. Theranostics 2025; 15(15):7308-7326.
