肺癌是全球癌癥相關死亡的主要原因之一,其中肺腺癌(LUAD)是NSCLC最常見的組織學亞型。大多數(shù)LUAD患者在診斷時已處于晚期并伴有轉(zhuǎn)移,這也是導致高死亡率的主要原因。
既往研究從基因、表觀遺傳等腫瘤細胞自身角度研究轉(zhuǎn)移原因,但對腫瘤周圍環(huán)境中的“外部勢力”,比如微生物群的作用了解不多。近來研究發(fā)現(xiàn)腫瘤組織里也存在微生物,它們可能通過代謝產(chǎn)物或與免疫細胞互動影響腫瘤行為。不過,肺里的微生物如何影響肺腺癌轉(zhuǎn)移,具體機制還亟待揭開。
2025年7月,北京大學腫瘤醫(yī)院研究團隊在Cell Host & Microbe(IF=18.7)上在線發(fā)表了題為“Lactate production by tumor-resident Staphylococcus promotes metastatic colonization in lung adenocarcinoma”的研究文章,通過多組學分析,揭示了腫瘤內(nèi)駐留的葡萄球菌(Staphylococcus)通過分泌乳酸激活腫瘤細胞中的MCT1-假缺氧-NDRG1軸,從而增強腫瘤細胞的轉(zhuǎn)移能力。此外,抑制MCT1可以顯著減弱葡萄球菌的促轉(zhuǎn)移作用,為LUAD的治療提供了新的潛在靶點。(麥特繪譜提供Q300全定量代謝組學檢測服務)
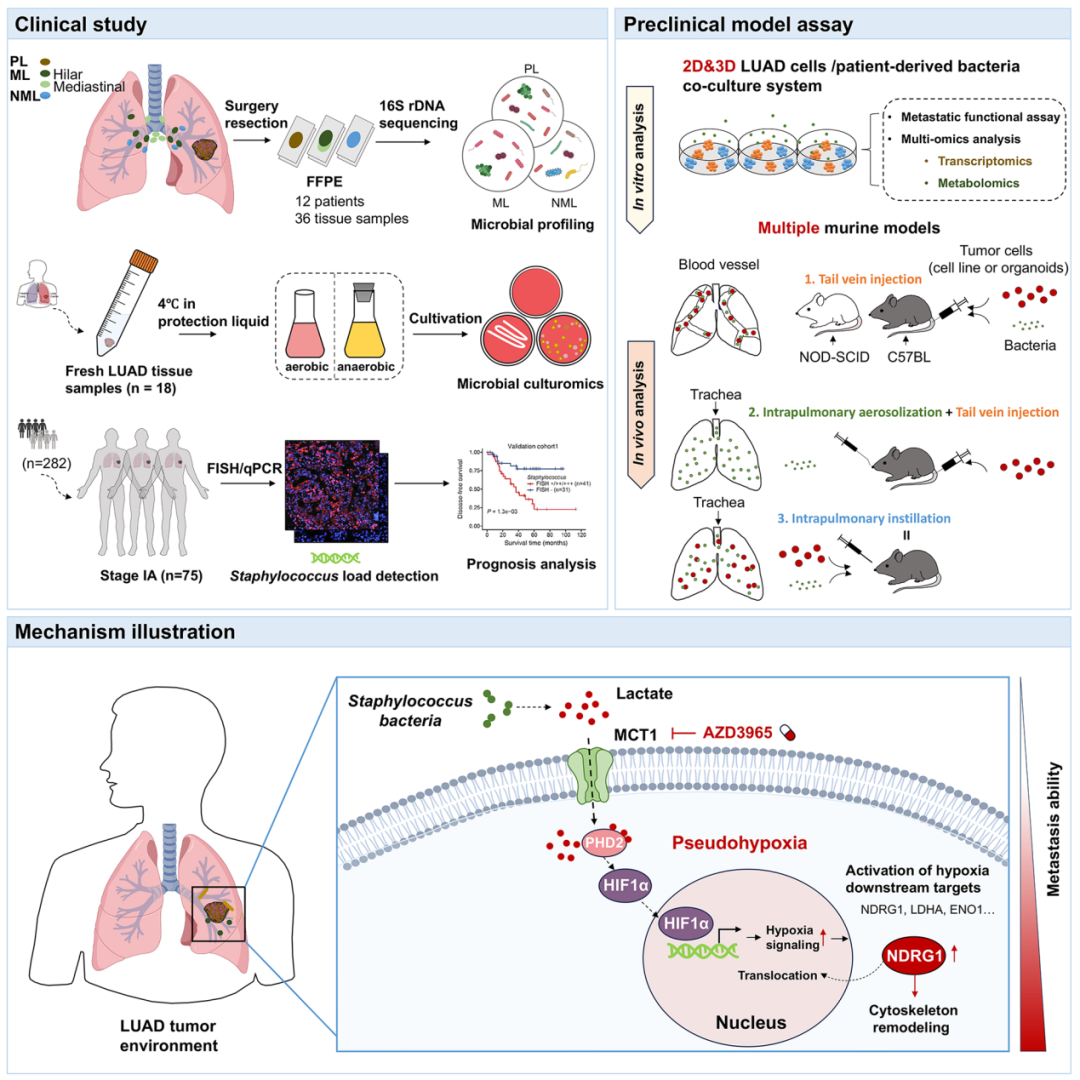
一、研究思路
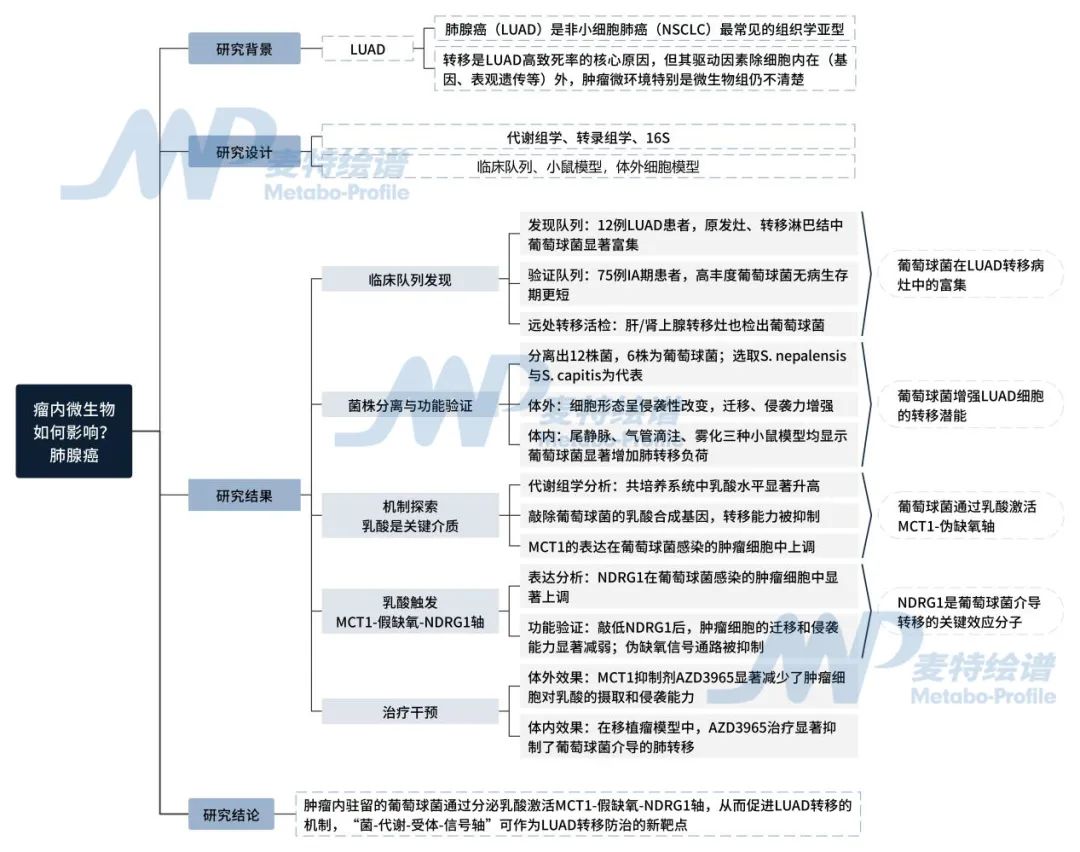
圖1. 研究思路圖
二、研究結果
1. 葡萄球菌富集與LUAD轉(zhuǎn)移密切相關
研究對12例LUAD患者的原發(fā)腫瘤(PL)、轉(zhuǎn)移淋巴結(ML)和非轉(zhuǎn)移淋巴結(NML)樣本進行 16S rRNA測序,發(fā)現(xiàn)葡萄球菌在PL和ML中顯著富集,而在NML中豐度較低,且其豐度與患者復發(fā)風險升高相關(疾病無進展生存率降低)。進一步對10例遠處轉(zhuǎn)移患者的樣本分析顯示,葡萄球菌在原發(fā)灶和轉(zhuǎn)移灶(如腎上腺、肝臟)中均被檢測到,證實其與LUAD轉(zhuǎn)移緊密相關。
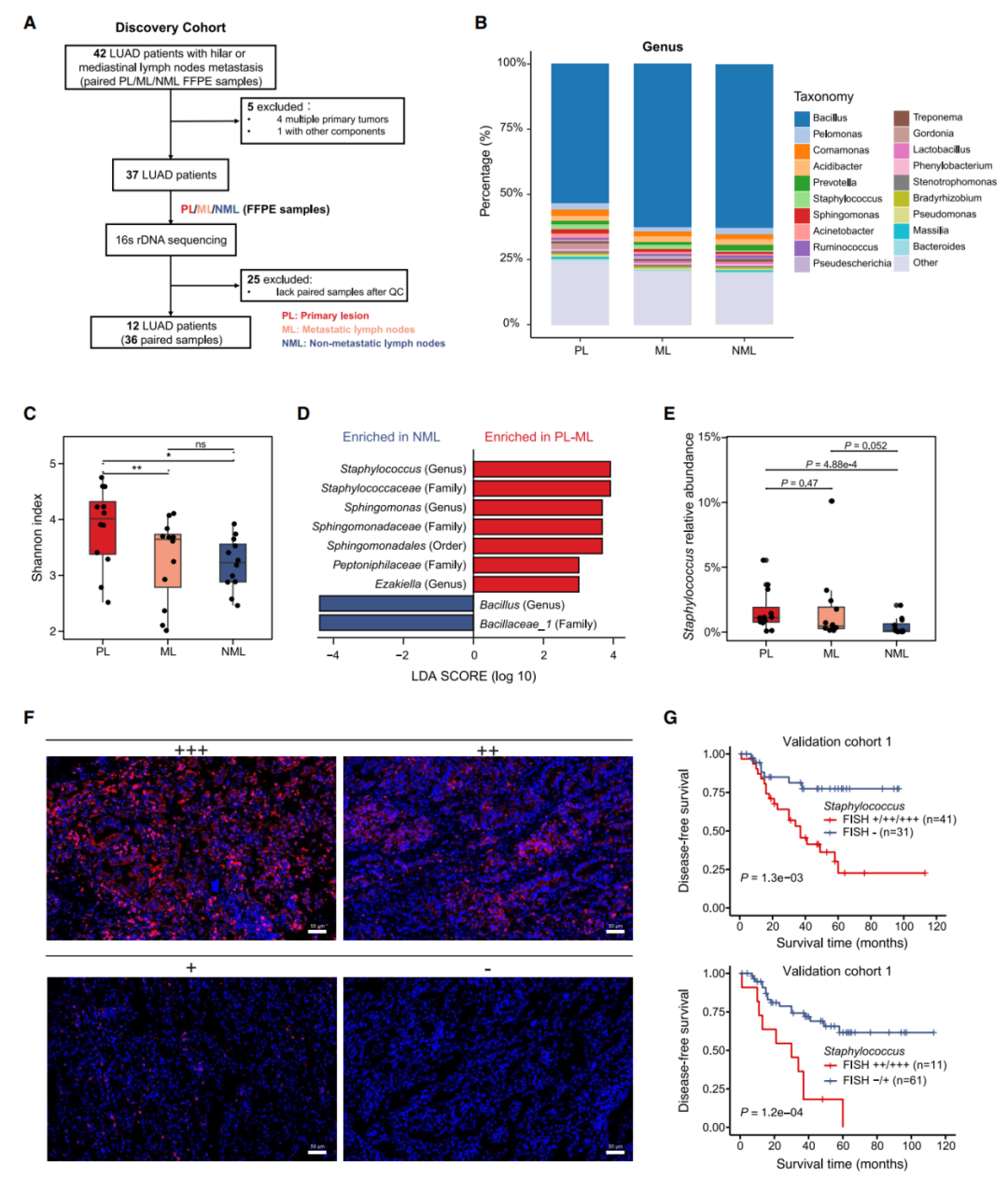
圖2. 高豐度葡萄球菌與LUAD轉(zhuǎn)移相關
2. 葡萄球菌增強LUAD細胞的轉(zhuǎn)移潛能
從LUAD患者樣本中分離出12株細菌(6 株為葡萄球菌),其中S. nepalensis和S. capitis在體外實驗中表現(xiàn)出最強的促轉(zhuǎn)移能力:與這兩種細菌共培養(yǎng)或暴露于其條件培養(yǎng)基后,LUAD細胞( A549)的遷移、侵襲能力顯著增強,細胞骨架重組(絲狀肌動蛋白重排)并形成侵襲偽足,上皮-間質(zhì)轉(zhuǎn)化(EMT)相關蛋白(波形蛋白 VIM、SNAI1)表達上調(diào)。體內(nèi)實驗中,經(jīng)尾靜脈注射感染這兩種葡萄球菌的LLC細胞(小鼠肺癌細胞)在C57BL小鼠中形成更多肺轉(zhuǎn)移灶,肺內(nèi)霧化+尾靜脈注射及肺內(nèi)滴注策略都證實葡萄球菌能增加轉(zhuǎn)移負荷。
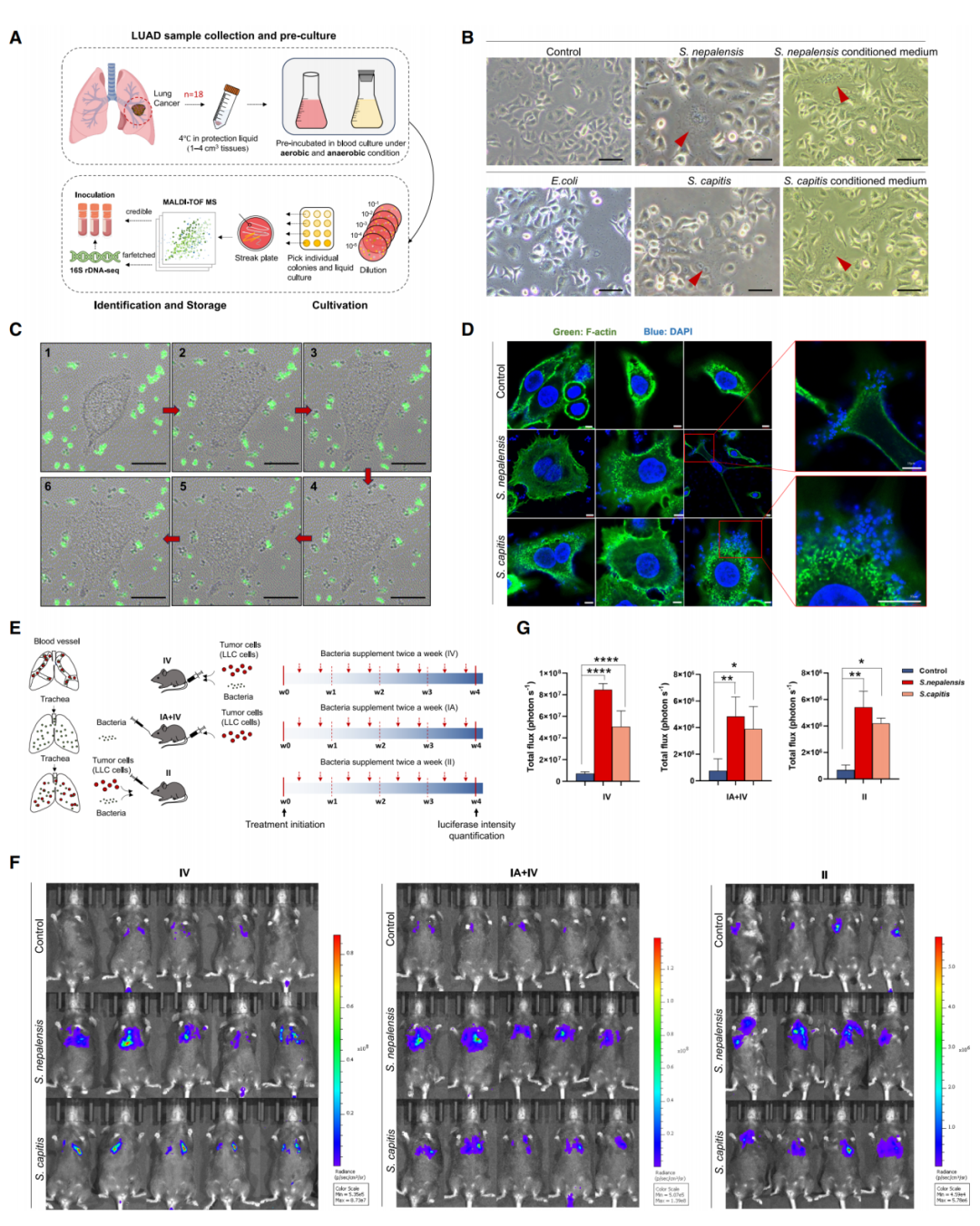
圖3. 人源性葡萄球菌誘導的LUAD細胞形態(tài)學改變及轉(zhuǎn)移潛能的增強
3. 葡萄球菌感染誘導LUAD細胞特定轉(zhuǎn)錄組特征
對患者來源類器官(LCO_5、LCO_6)與葡萄球菌共培養(yǎng)后的 RNA 測序顯示,缺氧通路是最顯著的上調(diào)通路,即使在常氧條件下,腫瘤細胞也表現(xiàn)出 “假缺氧” 表型(類似缺氧的基因表達特征)。此外,糖酵解、TNF信號通路及細菌感染相關通路TLR、NF-κB、IL-17信號等也被激活。差異基因分析發(fā)現(xiàn),轉(zhuǎn)移相關基因(NDRG1、CCL20、VIM等)和侵襲偽足相關基因(TKS5、NCK1)顯著上調(diào),且72個持續(xù)上調(diào)的基因(包括4個缺氧特征基因)被定義為 “葡萄球菌感染特征”,該特征集與多種癌癥(包括LUAD)患者的不良預后相關。
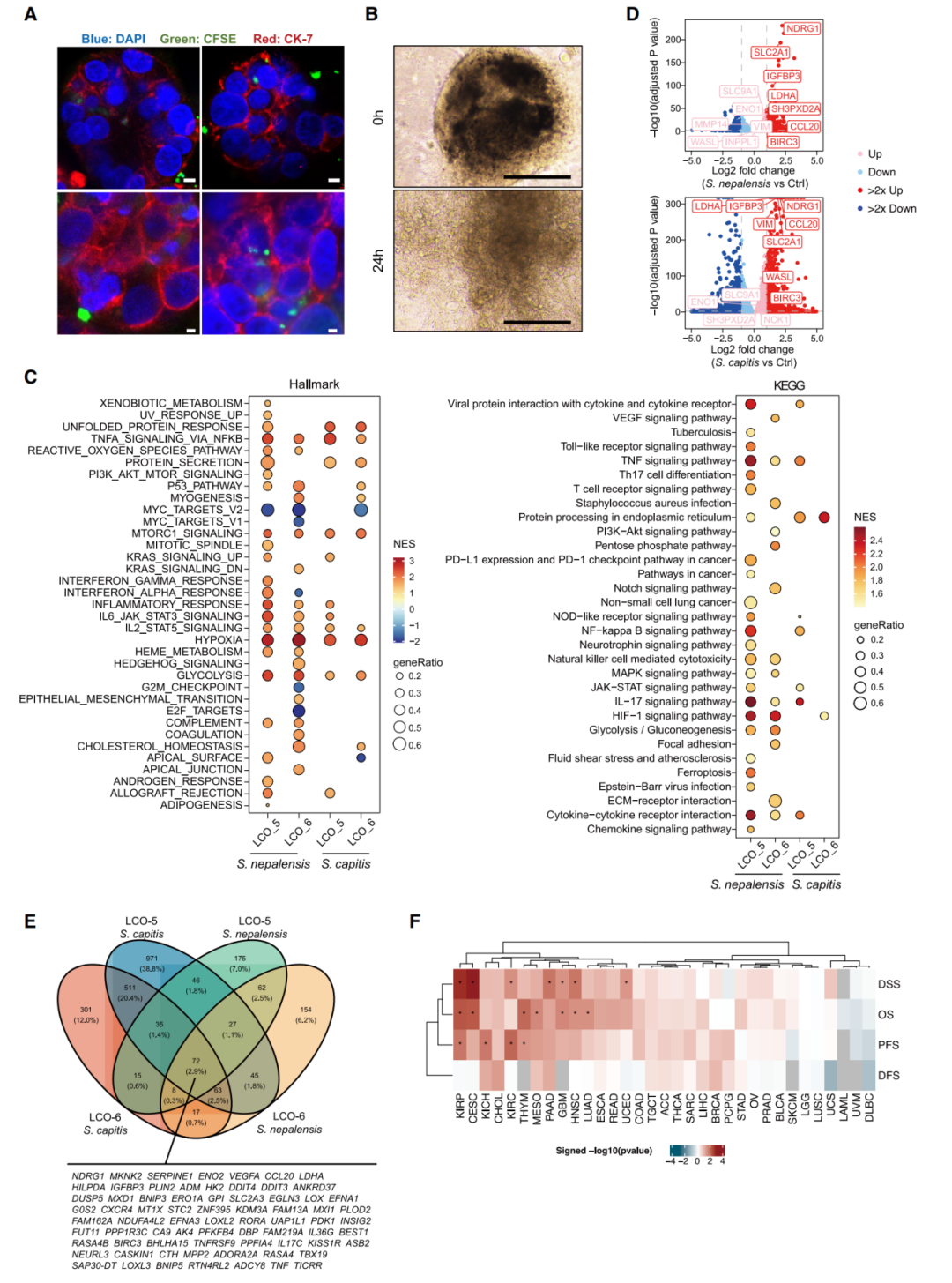
圖4. 葡萄球菌感染導致LUAD細胞特異性轉(zhuǎn)錄組學特征
4. 葡萄球菌分泌的乳酸激活MCT1-假缺氧軸促進LUAD轉(zhuǎn)移
代謝組學分析顯示,與葡萄球菌共培養(yǎng)的類器官培養(yǎng)基中乳酸等有機酸水平顯著升高,且培養(yǎng)基pH降低。構建S. capitis突變株Δddh/ldh(無法產(chǎn)生D-和L-乳酸),與A549細胞共培養(yǎng),發(fā)現(xiàn)其侵入性偽足形成減少,遷移和侵襲能力減弱,轉(zhuǎn)移和缺氧相關蛋白上調(diào)程度降低;在NOD/SCID小鼠異種移植模型中,Δddh/ldh感染導致的肺轉(zhuǎn)移顯著減少。RNA-seq和Western blotting結果表明,與葡萄球菌共培養(yǎng)后,LUAD類器官中MCT1(Monocarboxylate transporter 1,由SLC16A1編碼) 表達顯著上調(diào),伴隨缺氧相關蛋白(HIF1α, LDHA, ENO1, NDRG1)和轉(zhuǎn)移相關蛋白VIM的上調(diào),表明MCT1上調(diào)促進乳酸攝取,導致細胞內(nèi)乳酸積累,進而觸發(fā)缺氧誘導因子,激活假缺氧信號。
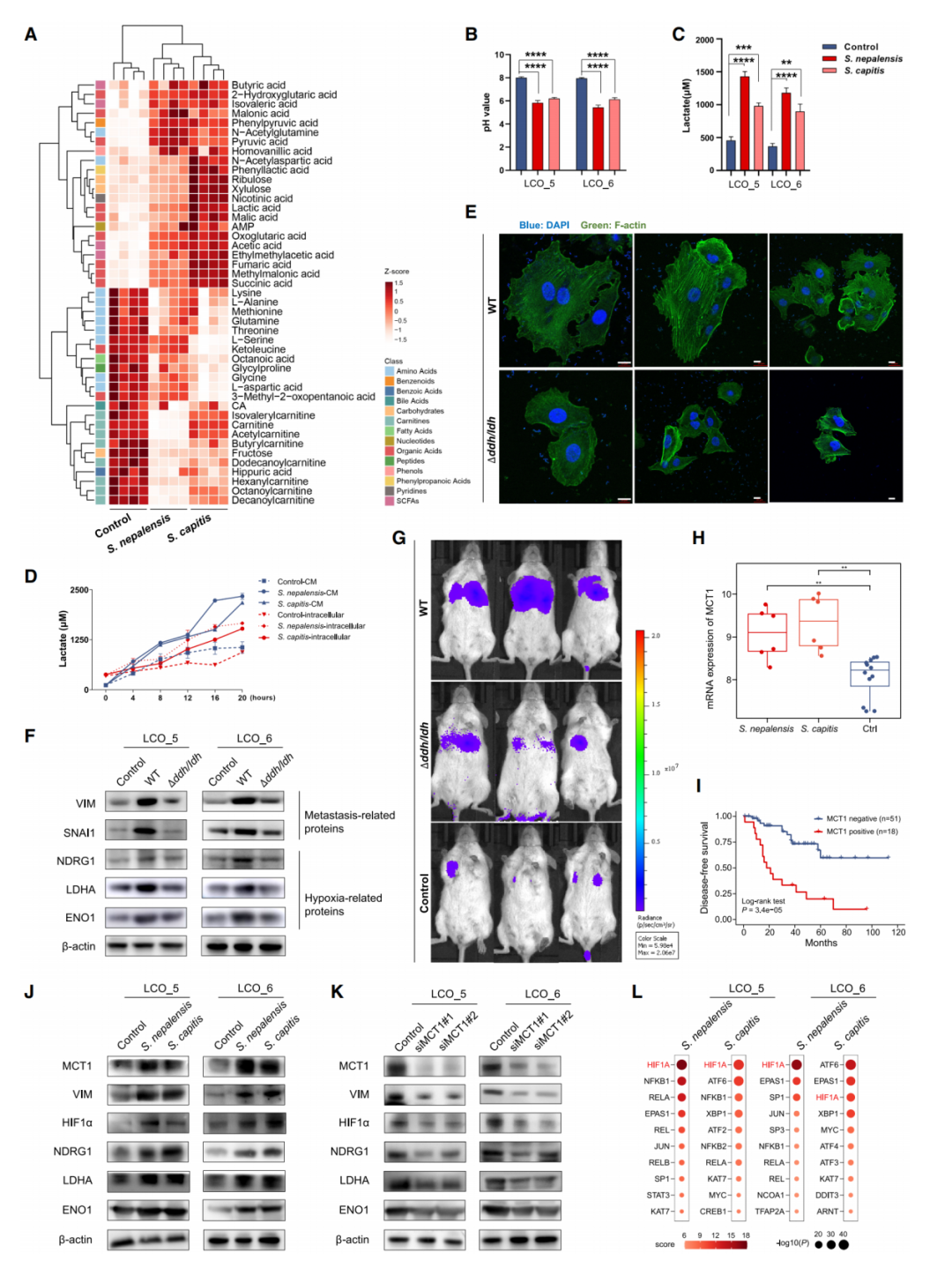
圖5. 乳酸激活MCT1-假缺氧軸促進LUAD轉(zhuǎn)移
5. NDRG1是葡萄球菌介導的假缺氧和轉(zhuǎn)移的關鍵效應因子
在葡萄球菌誘導的差異基因中,NDRG1(N-myc下游調(diào)控基因1)上調(diào)最顯著,其高表達與LUAD患者不良預后相關,且在腫瘤分期晚期的表達水平高于早期。敲除NDRG1后,葡萄球菌誘導的腫瘤細胞遷移、侵襲能力顯著減弱,缺氧通路和EMT通路激活被抑制,且體內(nèi)轉(zhuǎn)移負荷降低。此外,葡萄球菌感染可誘導NDRG1向細胞核遷移,推測其通過激活轉(zhuǎn)移相關基因(如SNAI1、VIM)的轉(zhuǎn)錄發(fā)揮作用。
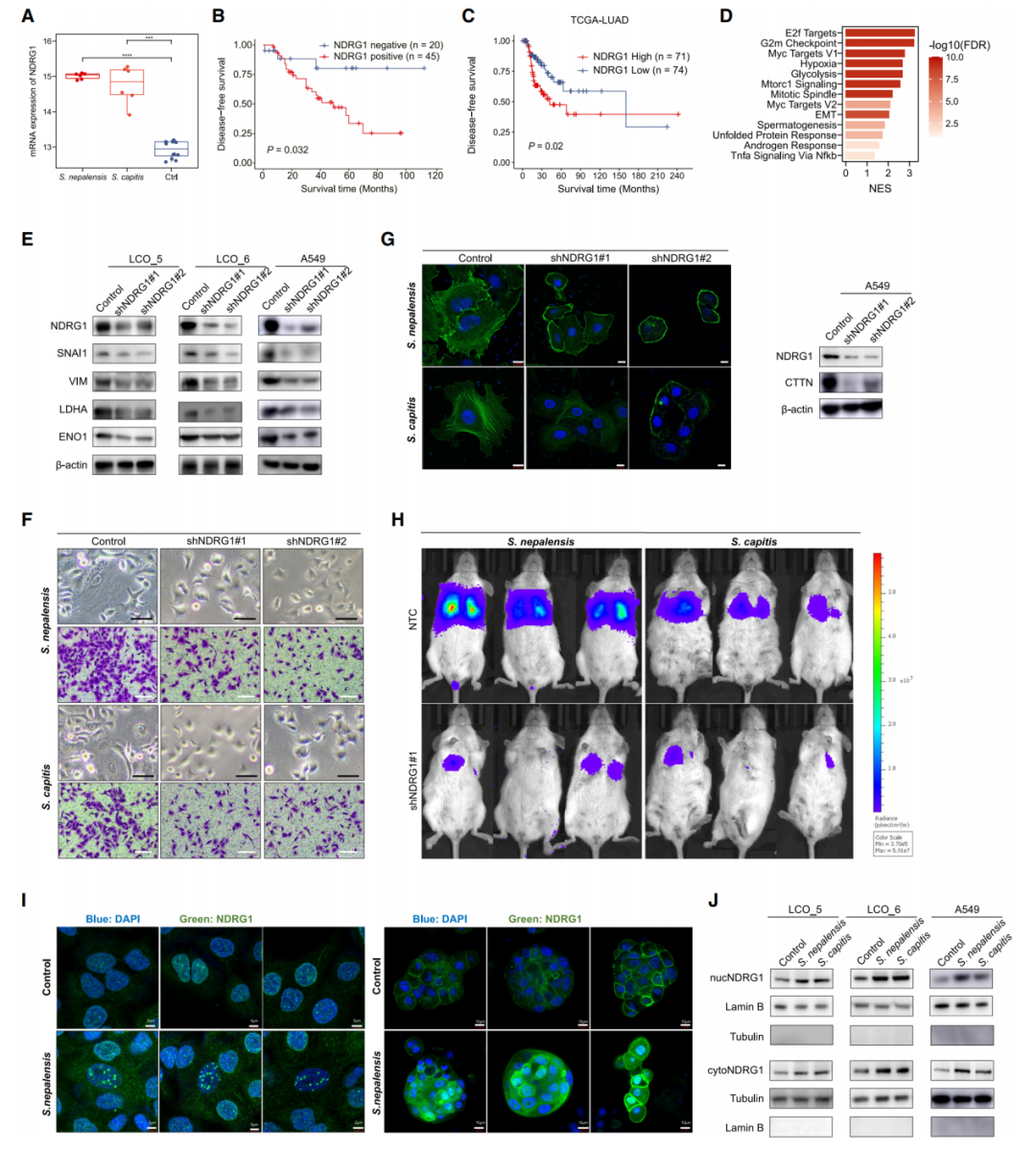
圖6. NDRG1在葡萄球菌誘導的假缺氧和轉(zhuǎn)移中的關鍵作用
6. 抑制MCT1可減弱葡萄球菌的促轉(zhuǎn)移作用
使用MCT1抑制劑AZD3965處理后,葡萄球菌感染的LUAD細胞內(nèi)乳酸攝取減少,侵襲能力和VIM表達被抑制。體內(nèi)實驗中,AZD3965顯著減少S. nepalensis和S. capitis誘導的肺轉(zhuǎn)移灶數(shù)量,且轉(zhuǎn)移灶中MCT1和NDRG1的表達水平降低。
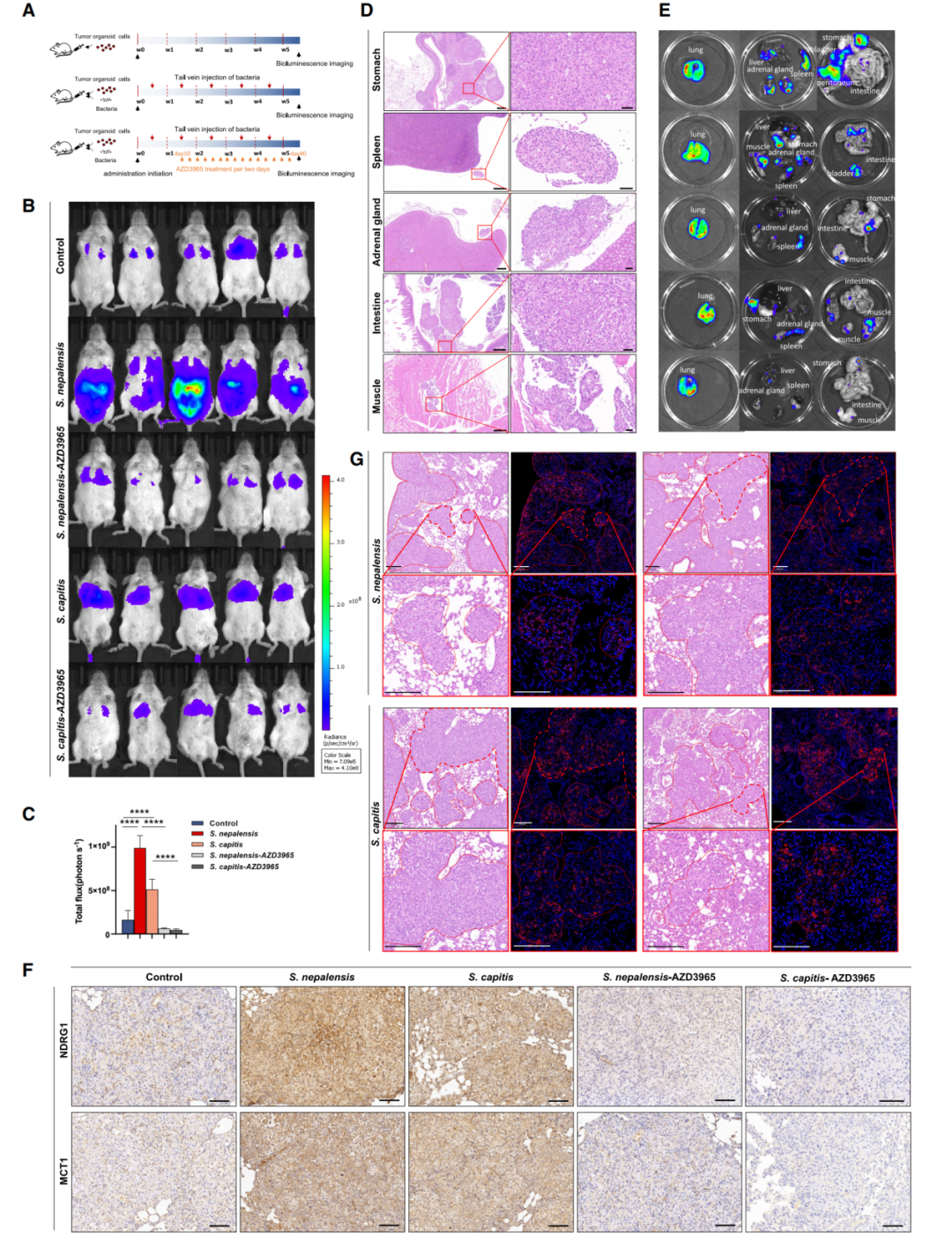
圖7. 抑制MCT1減弱葡萄球菌感染的促轉(zhuǎn)移潛力
三、研究結論
本研究證實,腫瘤駐留葡萄球菌通過分泌乳酸,激活宿主腫瘤細胞的MCT1-假缺氧-NDRG1軸,促進LUAD轉(zhuǎn)移;抑制MCT1可有效減弱其促轉(zhuǎn)移作用,為LUAD的治療提供了 “靶向微生物下游分子” 的新策略。
參考文獻
Lactate production by tumor-resident Staphylococcus promotes metastatic colonization in lung adenocarcinoma. Cell Host & Microbe. 2025
繪譜幫你測
本研究通過全定量代謝組學技術(麥特繪譜提供)對腫瘤類器官中的代謝物進行測定和分析,發(fā)現(xiàn)乳酸是介導腫瘤轉(zhuǎn)移的關鍵介質(zhì),乳酸水平的升高與腫瘤細胞的轉(zhuǎn)移能力增強呈現(xiàn)明顯的正相關性,為深入探究肺腺癌轉(zhuǎn)移的分子機制提供了重要突破口。麥特繪譜開創(chuàng)性地搭建了醫(yī)學領域高端代謝組學技術平臺,覆蓋了非靶向-全定量-代謝流等全方位的高端醫(yī)學代謝組解決方案,同時全面布局微生物組學、轉(zhuǎn)錄組學和蛋白質(zhì)組學等多組學技術服務,已成為全球多組學研究者的優(yōu)選合作伙伴。麥特繪譜已為數(shù)百家三甲醫(yī)院、科研院所和企業(yè)提供多組學一站式整體解決方案,協(xié)助客戶與合作伙伴發(fā)表SCI文章600+篇,累計影響因子6000+,平均IF>10,涵蓋Cell, Science, Nature, Cancer Cell, Signal Trans-duction and Targeted Therapy, Nature Biotechnology, Cell Metabolism等權威期刊。
