將兩個(gè)蛋白或者多肽以肽鍵進(jìn)行連接,表達(dá)出的蛋白即融合蛋白。融合蛋白的概念在細(xì)胞生物學(xué)研究以及大分子藥物研究領(lǐng)域有著重要的應(yīng)用。
常見的融合蛋白包括,目的蛋白融合標(biāo)簽蛋白,融合熒光蛋白,以及兩個(gè)不同蛋白的融合。那么這些融合蛋白的具體作用是什么呢,又有哪些需要注意的點(diǎn)呢?
在目的蛋白上融合一段小的標(biāo)簽是目前常見的構(gòu)建方案,我們先逐一介紹這種構(gòu)建的優(yōu)勢(shì)。
■ A. 便于使用wb和免疫熒光檢測(cè)外源基因的表達(dá)
對(duì)于一些基因,尤其是本底表達(dá)非常低的蛋白,在過表達(dá)之后,我們一般僅需要通過wb或者免疫熒光確認(rèn)其表達(dá)即可。在融合標(biāo)簽蛋白后我們僅需要使用標(biāo)簽蛋白的抗體進(jìn)行檢測(cè)即可。
如此有兩個(gè)主要優(yōu)勢(shì):其一,不同的目的蛋白均可以融合相同的標(biāo)簽蛋白,因此實(shí)驗(yàn)室只需要準(zhǔn)備一種標(biāo)簽蛋白的抗體即可檢測(cè)多個(gè)蛋白,節(jié)省很多的實(shí)驗(yàn)經(jīng)費(fèi)。其二,有相當(dāng)部分蛋白沒有商業(yè)化抗體或者抗體特異性不好,會(huì)導(dǎo)致后續(xù)結(jié)果非常難看,而標(biāo)簽抗體是目前非常成熟的抗體,可以極大地避免出現(xiàn)該問題。
■ B.用于Co-IP或者ChIP實(shí)驗(yàn)
為了檢測(cè)目的蛋白和另外一個(gè)蛋白有相互作用,一般我們會(huì)通過Co-[LS1] IP實(shí)驗(yàn)來驗(yàn)證。但是對(duì)于部分蛋白,并沒有商業(yè)化的抗體,或者已有的抗體特異性很差。此時(shí),可以通過在目的蛋白上融合一個(gè)標(biāo)簽蛋白,利用標(biāo)簽蛋白來進(jìn)行IP實(shí)驗(yàn)。類似的,很多的ChIP實(shí)驗(yàn)也可以采用相同的策略,因?yàn)镃hIP級(jí)別的抗體相對(duì)也是較少的。常用的標(biāo)簽包括flag,HA,his,myc,V5等,分子量大小都在1-2kd以內(nèi)。
因此標(biāo)簽是我們尋找蛋白相互作用結(jié)構(gòu)域或者功能域的重要工具。常規(guī)的,我們將一個(gè)蛋白按照結(jié)構(gòu)分成N端,C端和中心區(qū)域core(圖1)。例如,蛋白A和另外一個(gè)蛋白B有相互作用,為了確定蛋白A的哪個(gè)結(jié)構(gòu)域參與了該相互作用過程,可以按照?qǐng)D1構(gòu)建蛋白A的不同截短體,通過Co-IP分析不同截?cái)囿w和蛋白B的相互作用來確定。
比如后續(xù)實(shí)驗(yàn)全長(zhǎng)和N端以及ΔC端能夠拉下來蛋白B,其它截短體不行,就說明是N端的結(jié)構(gòu)域參與了這個(gè)結(jié)合過程。由于這些不同的截?cái)囿w的抗原表位沒有同源區(qū),只能使用標(biāo)簽抗體來進(jìn)行IP實(shí)驗(yàn)。
■ C. 蛋白純化
除了上面介紹的標(biāo)簽,還有一類用于做蛋白純化的標(biāo)簽,主要包括GST和his。GST標(biāo)簽大小26kd左右,可以提高重組蛋白的穩(wěn)定性,在絕大多數(shù)情況下,GST標(biāo)簽蛋白是完全可溶的。GST標(biāo)簽蛋白可以在溫和、非變形的條件下洗脫,因此保留了蛋白的抗原性和生物活性。
如果要去除GST標(biāo)簽,可以在GST和目的蛋白中間添加特異性蛋白酶切位點(diǎn),通過相應(yīng)的蛋白酶切除GST。但由于GST標(biāo)簽較大,有可能對(duì)融合蛋白的結(jié)構(gòu)或者功能造成影響。相比GST標(biāo)簽,his標(biāo)簽的分子量非常小,不到1kd,蛋白純化完之后可以不需切除此標(biāo)簽,也很少對(duì)蛋白產(chǎn)生功能影響。
圖 1 截短體構(gòu)建
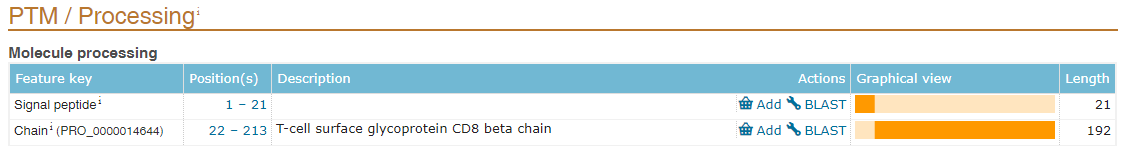
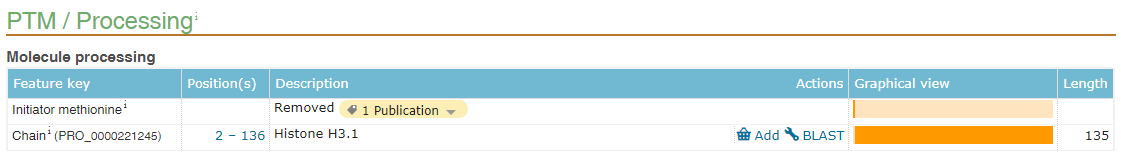
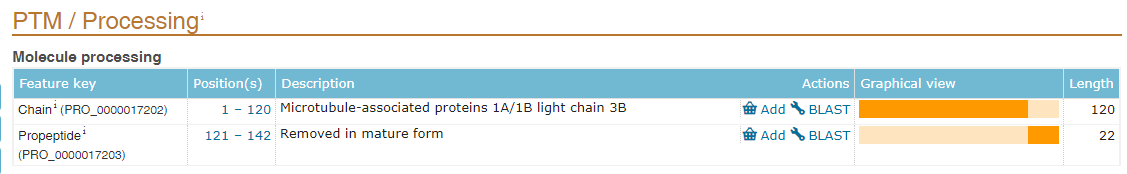
不管是用于wb,IP或者是蛋白純化,在構(gòu)建標(biāo)簽的時(shí)候,需要考慮標(biāo)簽添加的位置,即N端或者C端。N端有信號(hào)肽的蛋白,由于在蛋白轉(zhuǎn)運(yùn)后,信號(hào)肽(signal peptide)將被切除(圖2),所以這類蛋白我們一般將標(biāo)簽構(gòu)建在C端,或者構(gòu)建在N端信號(hào)肽之后。N端有甲硫氨酸切除的蛋白一般也采用這種構(gòu)建方式,如組蛋白H3(圖3)。另外,部分蛋白還存在前體肽(propeptide),在成熟后也將被切除(圖4),所以構(gòu)建標(biāo)簽時(shí)也要避免構(gòu)建到被切除的肽段上。可以在uniprotKB數(shù)據(jù)庫查詢自己構(gòu)建的蛋白是否包含信號(hào)肽或者前體肽,或者切除甲硫氨酸。
確定蛋白定位對(duì)于研究其功能有著重要的啟示。通過將一個(gè)待研究蛋白和GFP或者RFP等熒光蛋白進(jìn)行融合,后續(xù)通過觀察熒光的定位,就能夠知曉目的蛋白的位置。其具體應(yīng)用包括但不限于以下實(shí)驗(yàn)?zāi)康模?/span>第一, 不確定目的蛋白的細(xì)胞定位,通過融合熒光蛋白進(jìn)行確認(rèn);
第二, 用于確認(rèn)某個(gè)結(jié)構(gòu)域或者修飾位點(diǎn)是否影響目的蛋白定位;例如,構(gòu)建野生型蛋白融合熒光蛋白后觀察蛋白定位于細(xì)胞核;同時(shí)構(gòu)建缺失某個(gè)結(jié)構(gòu)域或者突變某個(gè)修飾位點(diǎn)的突變蛋白融合熒光蛋白,觀察其蛋白定位是否發(fā)生變化;
第三, 觀察某個(gè)干預(yù)過程是否導(dǎo)致影響蛋白定位發(fā)生變化,例如調(diào)控其他基因表達(dá),或者小分子化合物處理等。
除此以外,熒光蛋白融合目的基因的構(gòu)建方式還可以用于區(qū)分內(nèi)源蛋白和外源蛋白達(dá)量,因?yàn)镚FP大小在26kd左右。過表達(dá)融合蛋白后,使用目的蛋白的抗體進(jìn)行wb,一般可以雜出兩條明顯的條帶,通過對(duì)比條帶的亮度,可以區(qū)分內(nèi)外源的表達(dá)比例。而如果使用前面介紹的各種標(biāo)簽,由于其分子量很小,分子量在50kd上的蛋白一般就很難跑出兩條條帶。
熒光蛋白在融合目的基因時(shí)也需要考慮是融合在N端或者C端,具體考慮內(nèi)容和標(biāo)簽蛋白融合時(shí)一致。
對(duì)于融合熒光蛋白,建議在構(gòu)建時(shí)在目的基因和熒光蛋白中間添加連接肽linker[LS1] ,吉?jiǎng)P基因在構(gòu)建這類蛋白時(shí)一般會(huì)添加柔性連接肽,具體內(nèi)容見后續(xù)內(nèi)容介紹。同時(shí),部分融合熒光蛋白可能出現(xiàn)融合后熒光極弱甚至沒有熒光的情況,這可能是融合蛋白內(nèi)部相互作用影響了熒光蛋白的正確構(gòu)象,此時(shí)可以考慮更換熒光蛋白的位置,如從N端換到C端。還可以考慮更換不同的連接肽序列,尤其是是剛性連接肽進(jìn)行嘗試。
原則上講,所有融合蛋白在構(gòu)建的時(shí)候,都可以添加linker連接肽。通過研究天然的、具有多個(gè)結(jié)構(gòu)域的蛋白,研究者發(fā)現(xiàn)了天然連接肽的多種特性。在該基礎(chǔ)上,研究者設(shè)計(jì)了多種人工的連接肽,分成兩大類,分別是柔性連接肽(flexible linker)和剛性連接肽(rigid linker)。
柔性連接肽用于連接需要有一定活動(dòng)性和相互作用的兩個(gè)蛋白或者多肽(圖5)。柔性連接肽通常包含小的氨基酸,非極性的如Gly,極性的如Ser和Thr。這些尺寸更小的氨基酸提供了連接肽的靈活性,允許被連接的兩個(gè)蛋白具有一定的活動(dòng)性。并且,添加Ser和Thr可以使得連接肽和水分子形成氫鍵,賦予連接肽在水溶液中的穩(wěn)定性,從而減少連接肽和前后兩個(gè)蛋白的相互作用。
目前最主要的柔性連接肽由Gly和Ser殘基組成(“GS”linker)。其中使用最廣泛的柔性連接肽的序列為(Gly-Gly-Gly-Gly-Ser)n。通過調(diào)整n的數(shù)值(重復(fù)數(shù)),該GS連接肽的長(zhǎng)度可以得到改變,從而可以最優(yōu)地分離兩個(gè)兩個(gè)連接的蛋白,或使其可以相互作用。除了GS柔性連接肽以外,還有一些其它的柔性連接肽,如KESGSVSSEQLAQFRSLD,EGKSSGSGSESKST,(Gly)8,GSAGSAAGSGEF等。
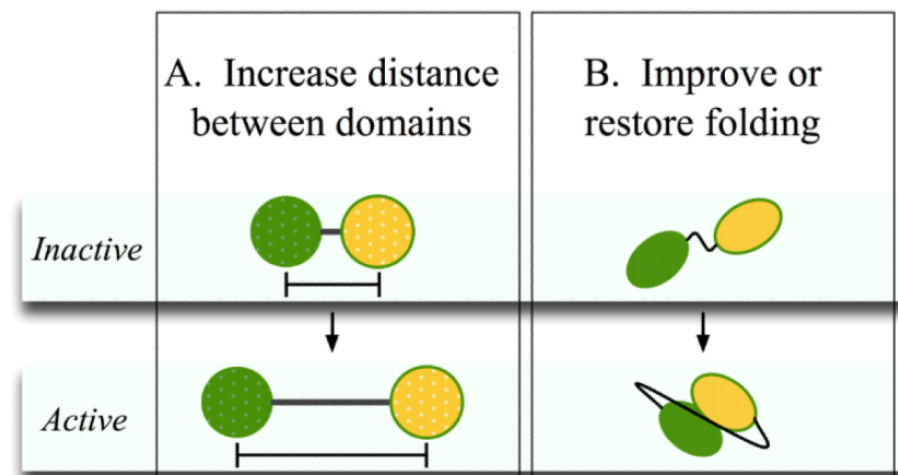
雖然柔性連接肽具有很多的優(yōu)點(diǎn),但是顯而易見的,缺乏剛性是其一個(gè)很大的限制。有文章報(bào)導(dǎo)了柔性連接肽導(dǎo)致融合蛋白表達(dá)下降或者生物活性喪失。這很可能是由于柔性連接肽不能將兩個(gè)蛋白充分地分離,導(dǎo)致其產(chǎn)生了相互作用,進(jìn)而影響融合蛋白的穩(wěn)定性或者生物活性。在這種條件下,剛性連接肽,可以被用于完全隔絕兩個(gè)連接的蛋白,維持他們獨(dú)立的功能(圖5)。
Figure 5 剛性連接肽和柔性連接肽發(fā)揮功能示意圖
α螺旋結(jié)構(gòu)肽段內(nèi)部會(huì)形成氫鍵和緊密的結(jié)構(gòu),因此同時(shí)具有穩(wěn)定性和剛性。利用(EAAAK)n形成成的α螺旋的剛性連接肽被廣泛應(yīng)用于許多融合蛋白的構(gòu)建。可以看到很多剛性連接肽都采用了α螺旋,典型的如A(EAAAK)nA,或者(H4)2連接肽(A(EAAAK)4ALEA(EAAAK)4A)。
除了α螺旋外,還有一類剛性連接肽是富含Pro的氨基酸序列,Pro可以賦予連接肽極強(qiáng)的構(gòu)象約束。序列為(XP)n,X可以是任意氨基酸,優(yōu)先選擇Ala,Lys,Glu。需要注意的是,如果兩個(gè)連接的蛋白需要一定的相互作用的話,不建議使用剛性連接肽。并且,可能存在部分特例,兩個(gè)蛋白并不需要相互作用,但使用柔性連接肽的表達(dá)效果優(yōu)于剛性連接肽的情況。其具體的原因可能還需要進(jìn)一步地探究。
通過今天的介紹,大家是否對(duì)融合蛋白有了更多的認(rèn)識(shí)呢?如果大家有相關(guān)產(chǎn)品的需求,歡迎聯(lián)系吉?jiǎng)P基因進(jìn)行交流或者訂購!

更多精彩好文請(qǐng)掃碼關(guān)注病毒實(shí)驗(yàn)幫
IF:31.37 少吃就不會(huì)胖了......嗎?
(2024-02-05T00:00 瀏覽數(shù):75004)
多巴胺總讓人感覺愉悅?新研究發(fā)現(xiàn)多巴胺也引起回避行為
(2024-02-05T00:00 瀏覽數(shù):63334)
高效感染造血干細(xì)胞利器——嵌合型腺病毒載體Ad5/F35
(2024-02-05T00:00 瀏覽數(shù):66773)
分子燈籠,傳遞在黑夜中的微光
(2024-02-05T00:00 瀏覽數(shù):62342)
用條形碼文庫病毒輕松給細(xì)胞打上條形碼
(2024-02-04T00:00 瀏覽數(shù):65580)
Science新作:篩選關(guān)鍵神經(jīng)元,逆轉(zhuǎn)完全性截癱
(2024-02-04T00:00 瀏覽數(shù):72707)
Nat Commun:沈陽藥科大學(xué)與新加坡國立大學(xué)報(bào)道新型多價(jià)IL-15遞送策略
(暫無發(fā)布時(shí)間 瀏覽數(shù):61677)
貓咪是我的家人,我才不舍得給她做絕育手術(shù)呢!AAV來為您解憂
(暫無發(fā)布時(shí)間 瀏覽數(shù):70694)
一閃一閃亮晶晶 選好熒光很要緊
(暫無發(fā)布時(shí)間 瀏覽數(shù):76993)
【硬核】外周對(duì)中樞的神經(jīng)環(huán)路示蹤策略
(暫無發(fā)布時(shí)間 瀏覽數(shù):76746)