
反應(yīng)
TEMPO(2,2,6,6-四甲基哌啶-1-氧自由基)及其衍生物是在有機氧化反應(yīng)中用作催化劑的穩(wěn)定硝酰自由基。TEMPO由Lebedev和Kazarnovskii于1960年首次發(fā)現(xiàn)。TEMPO穩(wěn)定的自由基性質(zhì)是由于其自身存在龐大的取代基,這阻礙了自由基與其他分子的發(fā)生反應(yīng)。[1]
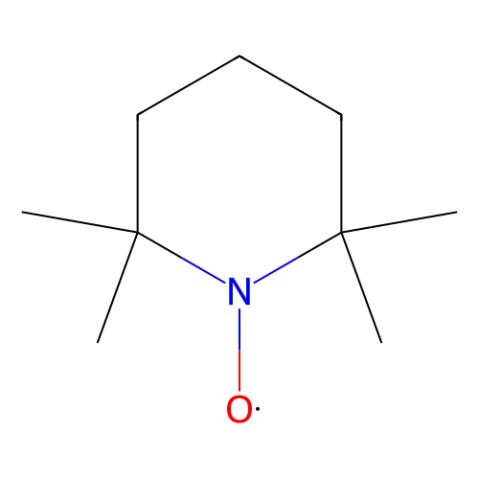
?
圖1.TEMPO(2,2,6,6-四甲基哌啶-1-氧自由基)
?
TEMPO及其衍生物主要應(yīng)用于伯醇和仲醇的氧化反應(yīng)。TEMPO不僅在有機溶劑中具有良好的溶解性,在水性介質(zhì)中溶解性也同樣優(yōu)異。[1] 此外,TEMPO還可以與各種用于水性介質(zhì)中氧化的再氧化劑(如次氯酸鹽)和用于有機介質(zhì)中氧化的Cu/O2一起使用。[2]?在水性介質(zhì)內(nèi),TEMPO可被同一化學(xué)計量的氧化劑(次氯酸鈉)氧化并生成亞硝基鎓陽離子,作為醇氧化過程中實際的氧化劑。在醇的氧化過程中,亞硝基鎓陽離子被還原為羥胺,羥胺再通過合適的氧化劑被氧化回亞硝基鎓陽離子,以完成催化循環(huán)。次氯酸鹽作為主氧化劑,溴化物作為助催化劑。[2]
?

圖2.TEMPO催化下的醇氧化機理[2]
TEMPO(2,2,6,6-四甲基哌啶-1-氧自由基)及其衍生物也可作為催化劑參與其他氧化反應(yīng)。它們是高選擇性氧化催化劑重金屬試劑的高性價比替代品,可催化反應(yīng)涉及碳-碳鍵、碳-氧鍵、碳-氧雙鍵、碳-氮鍵和碳氮雙鍵的形成。[3]
應(yīng)用
TEMPO催化氧化反應(yīng)已應(yīng)用于以下領(lǐng)域:
1,4-氨基-2,2,6,6-四甲基哌啶-1-氧自由基(4-氨基-TEMPO)催化下的氧化反應(yīng)可用于制備細胞松蘿酸,并可通過尺寸排阻色譜與多角度激光散射檢測器聯(lián)用(SEC-MALS)聯(lián)用進行分析。[4]
2,與TEMPO相比,2-氮雜金剛烷N-氧基(AZADO)和1-甲基-2-氮雜金剛烷-N-氧基(1-Me-AZAADO)在可將各種空間位阻醇轉(zhuǎn)化為相應(yīng)的羰基化合物的應(yīng)用方面表現(xiàn)出優(yōu)異的催化能力。[5]
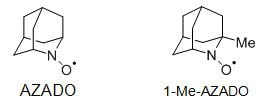
圖3.2-氮雜金剛烷N-氧基(AZADO)和1-甲基-2-氮雜金剛烷-N-氧基(1-Me-AZAADO)
1,TEMPO可用于催化氧化再生纖維素(粘膠人造絲)。TEMPO可將人造絲中的C6伯羥基氧化為羧基,使得產(chǎn)物具有水溶性。[6]
2,TEMPO衍生物由于可將極性物質(zhì)(如羥基或酯基)接枝到聚合物上,現(xiàn)已應(yīng)用于聚合后改性過程。4-羥基-TEMPO(HO-TEMPO)和4-苯甲酰氧基-TEMPO(BzO-TEMPO)可作為官能化試劑應(yīng)用于聚[乙烯-共-(1-辛烯)]的高效官能化。其可通過硝酰自由基與以碳-中心的自由基(如大分子自由基)的快速偶聯(lián),對極性官能團進行接枝。[7]
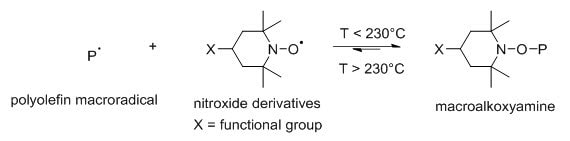
圖4.?硝酰衍生物和大分子自由基反應(yīng)
1,氮氧自由基衍生物與大分子自由基之間的偶聯(lián)反應(yīng)。[2]
2,TEMPO、Ce(IV)和NaNO2三者組成的催化體系現(xiàn)已應(yīng)用于不同醇的選擇性氧化反應(yīng)。在該反應(yīng)中醇氧化后生成的相應(yīng)醛和酮產(chǎn)率45.5–98.0%。[8]
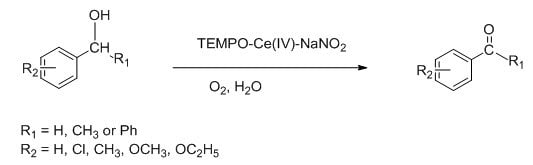
圖5.?TEMPO-Ce(IV)-NANO2
1,在TEMPO 催化下,可將黃原膠通過區(qū)域選擇性氧化合成黃原酸鈉鹽。通過2,2′-二苯基-1-苦基肼(DPPH)和羥基自由基的反應(yīng)進程可用于評估黃嘌呤的抗氧化活性。[9]
2,有報告稱,通過4-乙酰氨基-TEMPO/NaClO/NaClO2催化熱凝膠多糖氧化,實現(xiàn)了純(1→3)-β-聚葡萄糖醛酸鈉鹽的制備。[10]
3,通過監(jiān)測 TEMPO催化下原始纖維素的氧化程度,從而實現(xiàn)了從棗椰樹制備納米纖維素 (NFC)這一反應(yīng)的優(yōu)化。[11]
近期研究和趨勢
1,已開發(fā)出在儲能材料領(lǐng)域具有重要應(yīng)用前景的穩(wěn)定氮氧自由基有機聚合物材料。[12]?
2,Cu/TEMPO催化劑體系在二醇的好氧氧化內(nèi)酯化反應(yīng)中具有高效和高選擇性的優(yōu)勢。[13]
3,在漆酶(生物催化劑)和TEMPO或4-氨基-TEMPO(介質(zhì))的催化條件下,可通過纖維素納米纖維(CNFs)的化學(xué)-酶促修飾引入表面活性醛基。[14]
4,在固體-固體2,2,6,6-四甲基-1-哌啶氧基(TEMPO)存在下,二苯甲醇電解轉(zhuǎn)化為二苯甲酮。[15]
5,通過使用TEMPO替代昂貴的過渡金屬催化劑作為電活性有機催化劑對醇進行環(huán)保電化學(xué)氧化。該電催化系統(tǒng)已被用作各種醇的快速、簡單、選擇性和無廢物的氧化方案。[16]
6,可磁分離的有機催化劑(Fe3O4@SiO2–TEMPO)在無金屬和無鹵素條件下。可對5-羥甲基糠醛(5-HMF)有氧氧化為2,5-二甲酰呋喃(DFF),且該反應(yīng)具有高度選擇性。[17]
7,目前已經(jīng)制備了TEMPO氧化的魔芋葡甘露聚糖(OKGM)聚合物組成的凝膠微球光響應(yīng)傳遞系統(tǒng)。[18]
8,(bpy)CuI/TEMPO/NMI催化劑體系(bpy=2,2′-聯(lián)吡啶,TEMPO=2,2,6,6-四甲基-甲基哌啶-N-氧基,NMI=N-甲基咪唑)在芐基和脂族醇的快速和高選擇性氧化中得以應(yīng)用。該反應(yīng)中使用的“(bpy)CuI/TEMPO”催化劑體系以MeCN溶劑和5 mol% [Cu(MeCN)4](OTf)、5 mol% bpy、5 mol% TEMPO和10 mol%NMI組成。其中芐醇的氧化速度快于脂肪醇(環(huán)己醇)。[19]
上述氧化的方案如下所示(圖6):
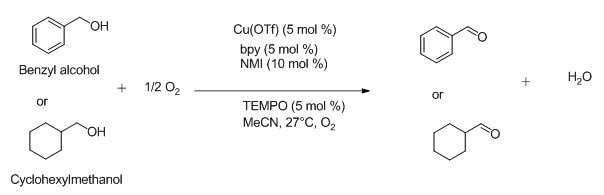
圖6.氧化反應(yīng)
參考文獻
1.費爾南德斯MJF,佐藤H. 2011。溶劑對(2,2,6,6-四甲基哌啶-1-基)氧基(TEMPO)的影響:RISM-SCF-SEDD研究。理論化學(xué)學(xué)報130(2-3):299-304。https://doi.org/10.1007/s00214-011-0976-y
2.基里奇一世, 納吉 J, 卡爾格 H, 帕伊 G. 1999.環(huán)保工藝中的多孔材料。第一屆國際經(jīng)濟經(jīng)濟管理會議記錄;03 9月 1999;埃格爾(匈牙利)
3.周志, 劉琪. 2014.TEMPO及其衍生物:合成和應(yīng)用。COC。18(4):459-474.https://doi.org/10.2174/13852728113176660151
4.柴田I,柳澤M,齋藤T,磯谷A.2006。通過TEMPO介導(dǎo)的氧化從再生纖維素制備的纖維素醛酸的SEC-MALS分析。纖維素。13(1):73-80.https://doi.org/10.1007/s10570-005-9021-4
5.澀谷M,富澤M,鈴木I,巖淵Y.2006。2-氮雜金剛烷N-氧基(AZADO)和1-Me-AZADO:用于醇氧化的高效有機催化劑。J. Am. Chem. Soc..128(26):8412-8413.https://doi.org/10.1021/ja0620336
6.柴田I,磯谷A.2003。10(4):335-341.https://doi.org/10.1023/a:1027330409470
7.帕薩利亞 E, 科艾 S, 西科尼亞 F, 夏爾代利 F. 2014.聚烯烴功能化的一些最新進展。波利姆。國際..63(1):12-21.https://doi.org/10.1002/pi.4598
8.閆瑩, 童旭, 王珂, 白曉. 2014.通過含TEMPO的催化系統(tǒng)對水性介質(zhì)中的醇進行高效和選擇性好氧氧化。催化通訊。43112-115.?https://doi.org/10.1016/j.catcom.2013.09.022
9.德拉特雷 C, 皮埃爾 G, 加達林 C, 特拉奇亞 M, 埃爾布塔赫法蒂 R, 磯蓋 A, 米肖 P. 2015.從TEMPO介導(dǎo)的黃原膠氧化中獲得的聚葡萄糖醛酸鈉鹽的抗氧化活性。碳水化合物聚合物。11634-41.?https://doi.org/10.1016/j.carbpol.2014.04.054
10.渡邊E,田村N,齋藤T,羽生N,磯谷A.2014.通過用4-乙酰氨基-TEMPO催化氧化制備完全C6-羧化的庫德蘭。碳水化合物聚合物。10074-79.?https://doi.org/10.1016/j.carbpol.2012.11.094
11.貝那穆 K, 杜弗雷斯內(nèi) A, 馬格寧 A, 莫爾塔 G, 卡達米 H. 2014.通過改變TEMPO介導(dǎo)的氧化時間來控制棕櫚樹納米原纖化纖維素的大小和粘彈性。碳水化合物聚合物。9974-83.?https://doi.org/10.1016/j.carbpol.2013.08.032
12.休斯BK,布勞內(nèi)克華盛頓,弗格森AJ,肯珀TW,拉森RE,熱內(nèi)特T.2014。通過穩(wěn)定的含硝化自由基的大分子淬滅苝熒光團。物理化學(xué)雜志B. 118(43):12541-12548.https://doi.org/10.1021/jp506240j
13.謝旭, 斯塔爾 SS. 2015.高效選擇性的Cu/硝基催化二醇有氧氧化內(nèi)酯化方法。J. Am. Chem. Soc..137(11):3767-3770.https://doi.org/10.1021/jacs.5b01036
14.Jauovec D, Vogrini R, Kokol V. 2015.使用漆酶/ TEMPO介導(dǎo)的氧化將醛基與羧基引入纖維素納米纖維。碳水化合物聚合物。11674-85.?https://doi.org/10.1016/j.carbpol.2014.03.014
15.卡盧扎 D, J?nsson-Niedziólka M, Ahn SD, Owen RE, Jones MD, Marken F. 2015.二苯基甲醇到二苯甲酮的固-固-固EC TEMPO-電催化轉(zhuǎn)化。J 固態(tài)電化學(xué)。19(5):1277-1283.https://doi.org/10.1007/s10008-014-2722-6
16.Karimi B, Rafiee M, Alizadeh S, Vali H. 新型電生成TEMPO官能化MCM-41修飾電極上醇的環(huán)保電催化氧化.綠色化學(xué)..17(2):991-1000.https://doi.org/10.1039/c4gc01303d
17.卡里米 B, 米爾扎伊 HM, 法爾漢吉 E. 2014.Fe3O4@SiO2-TEMPO作為一種磁性可回收催化劑,用于在無金屬和無鹵條件下將5-羥甲基糠醛高選擇性好氧氧化成2,5-二甲酰基呋喃。化學(xué)貓化學(xué).6(3):758-762.https://doi.org/10.1002/cctc.201301081
18.陳旭, 王淑, 陸敏, 陳瑩, 趙玲, 李文, 袁琪, 諾德文, 李彥. 2014.光響應(yīng)性TEMPO氧化魔芋葡甘露聚糖微球的形成和表征。生物大分子。15(6):2166-2171.https://doi.org/10.1021/bm500327m
19.胡佛JM,賴蘭BL,斯塔爾SS.2013。銅(I)/TEMPO催化好氧酒精氧化的機理.J. Am. Chem. Soc..135(6):2357-2367.https://doi.org/10.1021/ja3117203
阿拉丁提供相關(guān)產(chǎn)品,詳情請見阿拉丁官網(wǎng):TEMPO 催化氧化 (aladdin-e.com)
