近年來(lái),隨著全球各大藥企在新藥研發(fā)中持續(xù)投入,大量新藥進(jìn)入臨床階段,多家國(guó)內(nèi)外的制藥企業(yè)將更多的資源投入技術(shù)研發(fā),致力于實(shí)現(xiàn)關(guān)鍵性突破,打造具有差異化的管線。
差異化管線布局關(guān)鍵在于靶點(diǎn)選擇,人類(lèi)蛋白質(zhì)組中具有藥物開(kāi)發(fā)的潛在靶標(biāo)約有6000多種為膜蛋白。其中結(jié)構(gòu)復(fù)雜的多次跨膜蛋白(Multipass transmembrane protein)包括GPCRs、離子通道和轉(zhuǎn)運(yùn)蛋白等。這些完整結(jié)構(gòu)的多次跨膜蛋白具有重要的功能,從運(yùn)輸?shù)叫盘?hào)轉(zhuǎn)導(dǎo)與諸多疾病的發(fā)生緊密相關(guān)。在小分子的上市藥物中,有超過(guò)50%的靶點(diǎn)為多次跨膜蛋白;市面上大部分作用于多次跨膜蛋白的現(xiàn)有藥物都有各自的不足,例如同族多次跨膜蛋白中的配體結(jié)合口袋相對(duì)相似,藥物缺乏較好的特異性;亦或是它們參與許多不同的信號(hào)通路而產(chǎn)生的不良影響,這些信號(hào)通路(離子通道和轉(zhuǎn)運(yùn)體)可能對(duì)整體細(xì)胞平衡條件產(chǎn)生強(qiáng)烈影響。這些不足會(huì)導(dǎo)致藥物安全性堪憂、副作用過(guò)強(qiáng)。多次跨膜蛋白靶點(diǎn)相關(guān)的疾病需開(kāi)發(fā)針對(duì)特定構(gòu)象或信號(hào)通路的治療方法,獲得具有更高親和力、特異性的藥物,單克隆抗體(mAb)靶向多次跨膜蛋白是實(shí)現(xiàn)靶向選擇的一種有效方法。
在過(guò)去生物藥研發(fā)歷程中,多次跨膜靶點(diǎn)大多數(shù)被定義為難成藥或不可成藥的靶點(diǎn),猶如“高嶺之花”觸不可及。近年來(lái)隨著對(duì)多次跨膜蛋白認(rèn)知的逐步深入及技術(shù)的迭代更新,更多的靶點(diǎn)開(kāi)始褪去神秘的面紗,逐漸走入行業(yè)的視野。由于存在多個(gè)跨膜結(jié)構(gòu)域(TMDs),這可能導(dǎo)致表達(dá)和純化過(guò)程中的不穩(wěn)定性和聚集,多次跨膜蛋白靶向藥物開(kāi)發(fā)最大的挑戰(zhàn)在于其構(gòu)象的復(fù)雜程度。對(duì)于靶向藥物研發(fā)而言,獲取保持天然構(gòu)象與活性的靶蛋白是至關(guān)重要的環(huán)節(jié),因此,迫切需要?jiǎng)?chuàng)新技術(shù)來(lái)突破多次跨膜蛋白靶點(diǎn)面臨的“抗體開(kāi)發(fā)難題”。
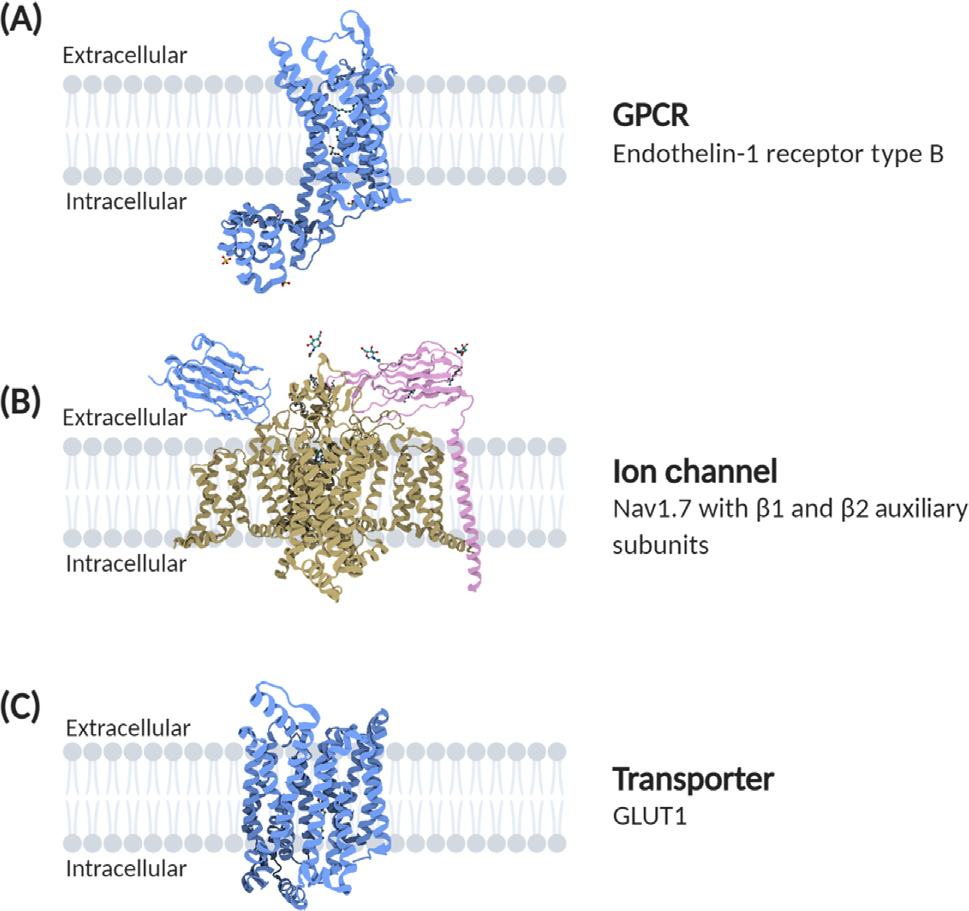
圖1. 多次跨膜蛋白的經(jīng)典結(jié)構(gòu)[1]
“抗體開(kāi)發(fā)難題”,我們能做什么?
近岸蛋白自主研發(fā)3000+藥物靶蛋白,覆蓋多個(gè)疾病領(lǐng)域,擁有550個(gè)物種超過(guò)24000個(gè)重組蛋白開(kāi)發(fā)經(jīng)驗(yàn),產(chǎn)品類(lèi)型豐富,涵蓋多種屬、多標(biāo)簽、生物素化以及特定位點(diǎn)突變體蛋白等,應(yīng)用于動(dòng)物免疫、抗體藥物篩選評(píng)估、質(zhì)量放行等藥物研發(fā)環(huán)節(jié)。
在過(guò)去的幾年內(nèi),近岸蛋白對(duì)多次跨膜靶點(diǎn)進(jìn)行深度開(kāi)發(fā),持續(xù)強(qiáng)化,新增了多個(gè)多次跨膜靶點(diǎn)產(chǎn)品,公司的多次跨膜蛋白等困難靶點(diǎn)開(kāi)發(fā)技術(shù),解決了跨膜蛋白表達(dá)量低、穩(wěn)定性差、溶解度低及難純化等難題,產(chǎn)品類(lèi)型多樣,開(kāi)發(fā)技術(shù)包含類(lèi)病毒粒子(VLP)、去垢劑及mRNA等形式。
NovoiSMART®技術(shù)平臺(tái)
NovoiSMART®(Novo Immunize and Screen antibody of Multipass trAnsmembRane proTein)是由近岸蛋白基于豐富的蛋白質(zhì)和抗體開(kāi)發(fā)經(jīng)驗(yàn),針對(duì)結(jié)構(gòu)復(fù)雜的多次跨膜蛋白抗體開(kāi)發(fā)難的現(xiàn)狀,推出的綜合性的技術(shù)平臺(tái),可提供多次跨膜靶點(diǎn)抗體開(kāi)發(fā)整體解決方案。NovoiSMART®技術(shù)平臺(tái)結(jié)合多策略抗體發(fā)現(xiàn)技術(shù)、人源化親和力成熟等技術(shù),已完成120多個(gè)靶標(biāo)抗體藥物候選分子篩選及驗(yàn)證,其中多個(gè)候選分子已完成商業(yè)轉(zhuǎn)讓。NovoiSMART®技術(shù)平臺(tái)能夠滿足復(fù)雜靶點(diǎn)及各類(lèi)藥物開(kāi)發(fā)的不同需求。
案例
一、GPRC5D表位多樣性抗體篩選
GPRC5D即G蛋白偶聯(lián)受體C組5成員D(G protein-coupled receptor, class C, group 5, member D),它是G蛋白偶聯(lián)受體(GPCRs)家族的成員之一。
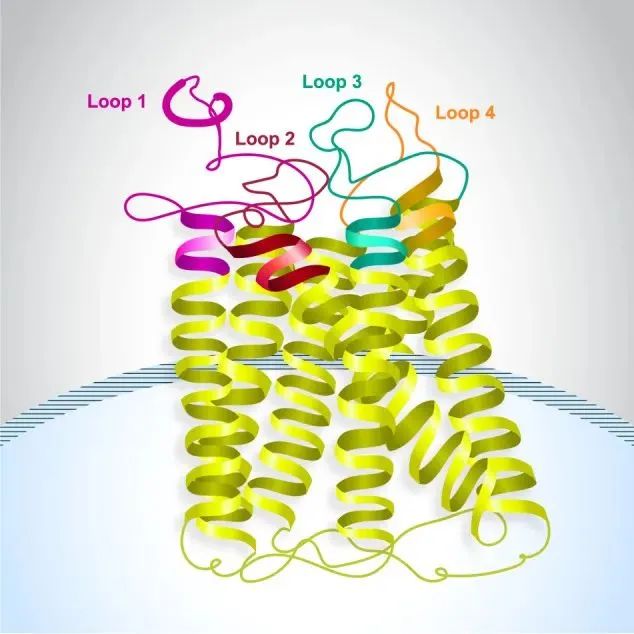
圖2.GPRC5D結(jié)構(gòu)[2]
GPRC5D在細(xì)胞膜表面穩(wěn)定表達(dá)、不會(huì)脫落,且在除毛囊以外的正常細(xì)胞中不表達(dá),僅在多發(fā)性骨髓瘤細(xì)胞中顯著上升表達(dá)。由于MM遺傳和表型的異質(zhì)性,每一種抗原都不是由MM細(xì)胞或漿細(xì)胞直接表達(dá)的,靶點(diǎn)脫落和抗原丟失是引起腫瘤逃逸和MM復(fù)發(fā)難治的重要原因。靶向GPRC5D的免疫療法可以抑制腫瘤逃逸,它的表達(dá)不受 BCMA丟失的影響,因此使用這種治療性抗體可以治療抗BCMA療法治療失敗或BCMA低表達(dá)或不表達(dá)的患者。
GPRC5D具有4個(gè)胞外結(jié)構(gòu)域(ECD),篩選結(jié)合不同抗原結(jié)構(gòu)域和不同抗原表位的抗體并開(kāi)發(fā)成藥,可以有效的避免抗原丟失或者突變引起的藥效降低或者耐藥,增強(qiáng)藥物的長(zhǎng)期持久性嚴(yán)守MM最后一道治療防線。近岸蛋白通過(guò)NovoiSMART®技術(shù)平臺(tái),對(duì)篩選獲得的候選分子進(jìn)一步進(jìn)行表位檢測(cè)。使用GPRC5A的胞外序列對(duì)GPRC5D的4個(gè)胞外結(jié)構(gòu)域 ECD進(jìn)行突變替換,并命名1-4(對(duì)應(yīng)圖2結(jié)構(gòu)的Loop1-4的替換)。結(jié)果如圖3和圖4顯示,成功篩選出表位多樣的GPRC5D候選分子。基于此類(lèi),對(duì)于部分耐藥靶標(biāo),NovoiSMART®技術(shù)平臺(tái)可以為您提供更優(yōu)的選擇!
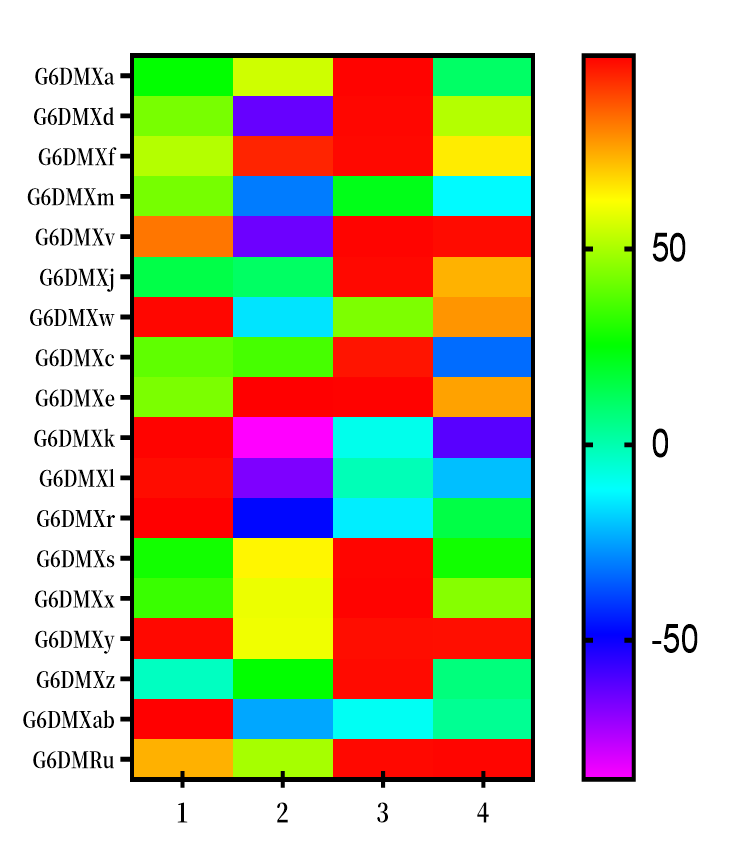
圖3.流式檢測(cè)相較野生型的MFI下降比例熱圖
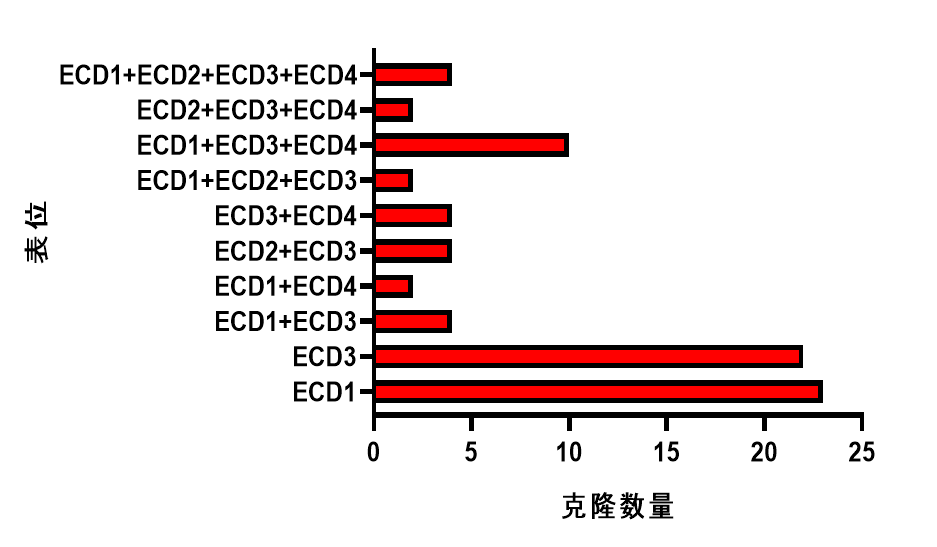
圖4.GPRC5D抗體表位多樣性統(tǒng)計(jì)
二、CLDN6高特異性抗體篩選
Claudin6 (CLDN6) 是一個(gè)四次跨膜蛋白,具有一個(gè)短的細(xì)胞質(zhì)N端和一個(gè)C端細(xì)胞質(zhì)結(jié)構(gòu)域,兩個(gè)胞外結(jié)構(gòu)域(ECL1較大,ECL2較小),以及一個(gè)短的胞內(nèi)環(huán)。ECL1和羧基末端的PDZ結(jié)合基序( PBM )是CLDNs的典型結(jié)構(gòu)域。
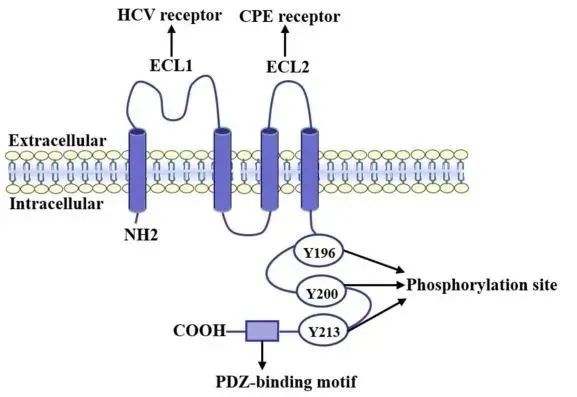
圖5.CLDN6結(jié)構(gòu)圖[3]
CLDN6和同家族的CLDN9具有高度同源性,其胞外區(qū)的氨基酸序列只有三處不同。但二者的表達(dá)卻并非完全相同,CLDN6在卵巢癌、子宮肉瘤和睪丸癌中高表達(dá),在其它組織中表達(dá)極低。同家族的CLDN9在卵巢癌、膽管癌、睪丸癌等癌癥中高表達(dá),但在其它組織中也有不同程度的表達(dá)。在藥物開(kāi)發(fā)中,對(duì)家族龐大的靶蛋白來(lái)說(shuō),不同的適應(yīng)癥涉及不同的靶點(diǎn)設(shè)計(jì)及藥物類(lèi)型,其所需要的特異性要求也不同。近岸蛋白通過(guò)NovoiSMART®技術(shù)平臺(tái),針對(duì)CLDN6和CLDN9分別進(jìn)行免疫篩選,結(jié)果如圖6所示,CLDN6候選分子與CLDN6陽(yáng)性細(xì)胞特異性結(jié)合,與CLDN9陽(yáng)性細(xì)胞基本無(wú)非特異性結(jié)合;圖7的CLDN9候選分子也顯示出與CLDN9陽(yáng)性細(xì)胞的特異性結(jié)合,與CLDN6陽(yáng)性細(xì)胞基本無(wú)非特異結(jié)合。盡管CLDN6和CLDN9序列與結(jié)構(gòu)高度相似,但NovoiSMART®技術(shù)平臺(tái)可以精準(zhǔn)篩選出具有高度特異性與功能活性的候選分子。對(duì)于諸多家族蛋白眾多,且同源性較高的藥物靶標(biāo)開(kāi)發(fā),NovoiSMART®技術(shù)平臺(tái)可以更快速精準(zhǔn)地為您保駕護(hù)航!
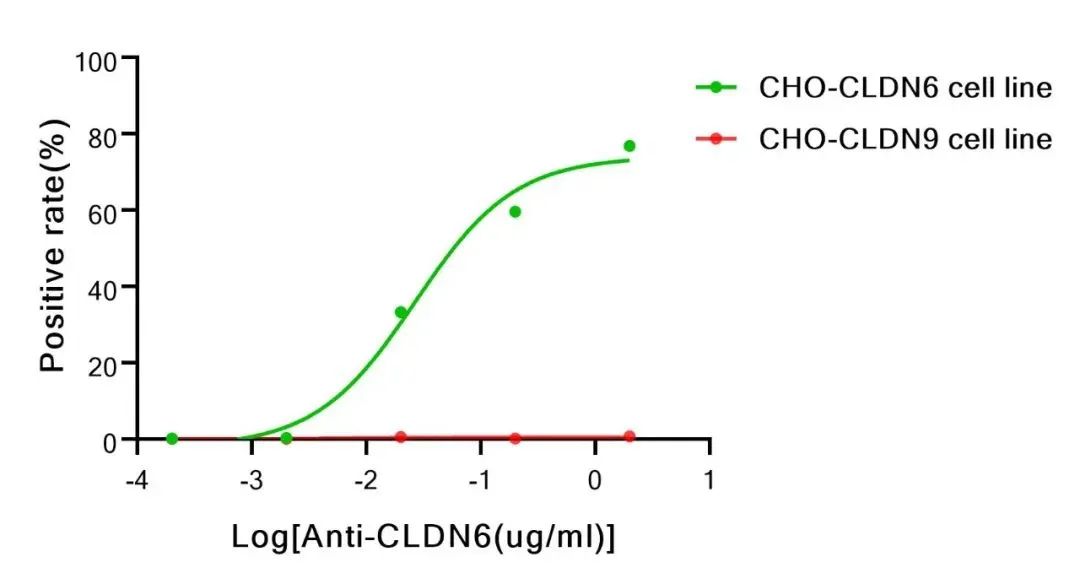
圖6. 抗體特異性結(jié)合CLDN6陽(yáng)性細(xì)胞
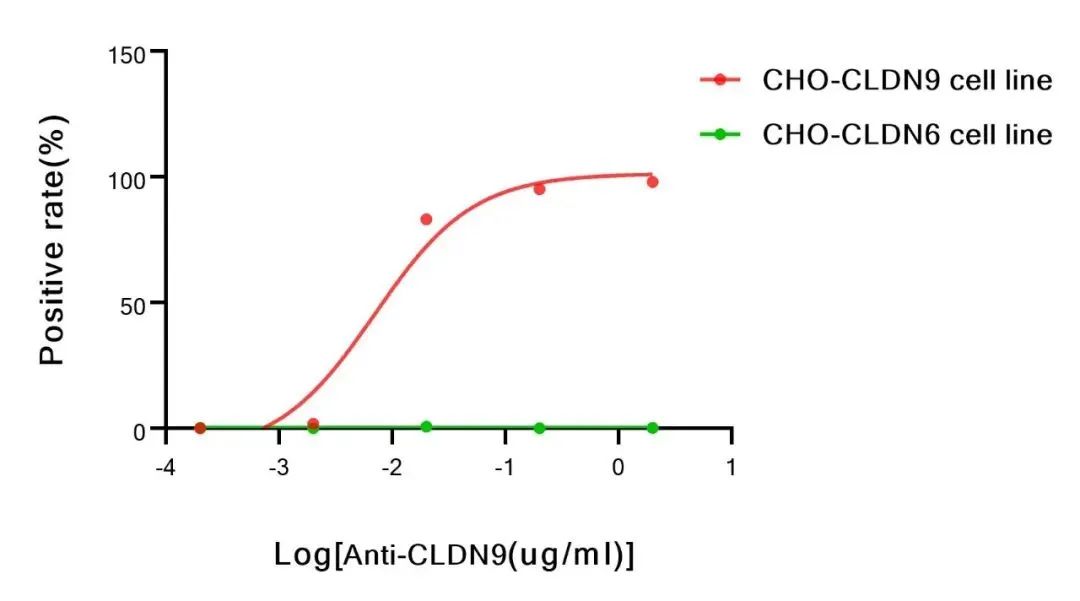
圖7. 抗體特異性結(jié)合CLDN9陽(yáng)性細(xì)胞
近岸蛋白已開(kāi)發(fā)多次跨膜靶點(diǎn)(部分)展示
| 靶點(diǎn)名稱(chēng) | 靶點(diǎn)描述 |
| GPRC5D | GPCR家族,七次跨膜蛋白, 可用于多發(fā)性骨髓瘤治療 |
| Claudin 18.2 | 四次跨膜蛋白,與Claudin 18.1同源性高,可用于胃癌、食道癌、胰腺癌等疾病治療 |
| Claudin 6 | 四次跨膜蛋白,與Claudin 9同源性高,可用于卵巢癌、子宮內(nèi)膜癌等多種疾病治療 |
| NaPi2b | 離子通道蛋白,八次跨膜蛋白,可用于非小細(xì)胞肺癌、卵巢癌等疾病治療 |
| CCR7 | GPCR家族,七次跨膜蛋白, 可用于非霍奇金淋巴瘤、慢性淋巴細(xì)胞白血病等疾病治療 |
| SCN9A | 離子通道蛋白,二十四次跨膜蛋白,可用于慢性疼痛、神經(jīng)痛、骨關(guān)節(jié)炎等疾病治療 |
參考文獻(xiàn)
[1] Gulezian E, Crivello C, Bednenko J, Zafra C, Zhang Y, Colussi P, Hussain S. Membrane protein production and formulation for drug discovery. Trends Pharmacol Sci. 2021 Aug;42(8):657-674. doi: 10.1016/j.tips.2021.05.006. PMID: 34270922.
[2] Rodriguez-Otero P, van de Donk NWCJ, Pillarisetti K, Cornax I, Vishwamitra D, Gray K, Hilder B, Tolbert J, Renaud T, Masterson T, Heuck C, Kane C, Verona R, Moreau P, Bahlis N, Chari A. GPRC5D as a novel target for the treatment of multiple myeloma: a narrative review. Blood Cancer J. 2024 Feb 2;14(1):24. doi: 10.1038/s41408-023-00966-9. Erratum in: Blood Cancer J. 2024 Mar 6;14(1):40. doi: 10.1038/s41408-024-01018-6. PMID: 38307865; PMCID: PMC10837198.
[3] Qu H, Jin Q, Quan C. CLDN6: From Traditional Barrier Function to Emerging Roles in Cancers. Int J Mol Sci. 2021 Dec 14;22(24):13416. doi: 10.3390/ijms222413416. PMID: 34948213; PMCID: PMC8705207.
