導 語
腫瘤轉移是癌癥治療的最大挑戰之一,而細胞侵襲實驗是研究癌細胞遷移能力的“黃金標準”!如何利用基質膠精準構建體外侵襲模型?實驗關鍵步驟與試劑如何選擇?翌圣生物本期技術專欄為您揭曉答案!
PART.01
細胞侵襲實驗
細胞侵襲實驗通過模擬癌細胞穿透基底膜的過程,評估其遷移與侵襲能力,廣泛應用于抗腫瘤藥物篩選、轉移機制研究及靶向治療開發。實驗中,基質膠(如翌圣生物Ceturegel®基質膠)作為基底膜替代物,為細胞提供三維微環境,結合Transwell小室形成物理屏障,通過量化穿透基質的細胞數評估侵襲性。
實驗優勢:
? 高靈敏度:可檢測微量藥物對侵襲的抑制作用
? 可視化強:通過染色直接觀察侵襲細胞
? 適用性廣:支持多種腫瘤細胞
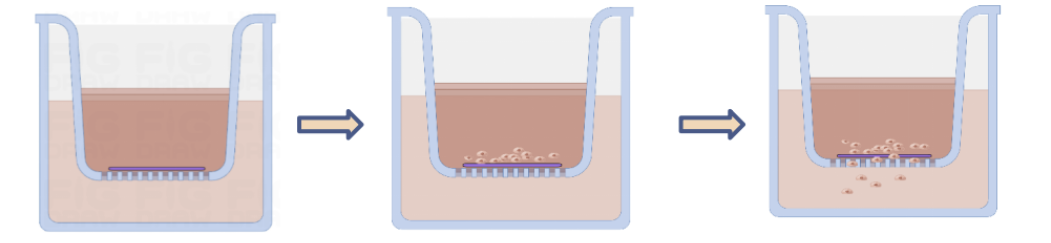
圖1.細胞侵襲實驗過程
PART.02
實驗步驟
首先將拿到的Ceturegel®基質膠凍融后按照原液1:8稀釋(終濃度不要超過3 mg/mL)來包被Transwell小室底部膜的上室面,置37℃、30 min - 8 h使基質膠聚合成凝膠,使用前用無血清培養基進行基底膜水化30 min。
將細胞饑餓12 - 24 h以去除血清的影響。
消化細胞,終止消化后離心棄去培養液并用PBS洗1 - 2次,用含無血清培養基重懸調整細胞密度至4×104~5×105個/mL 。。
取細胞懸液100 μL加入Transwell小室。
在24孔板下室加入600 μL含20%FBS培養基,添加時要避免下層培養液和小室間產生氣泡,產生氣泡易使下層培養液的趨化作用減弱甚至消失。
培養細胞:常規培養12 - 48 h(時間主要依癌細胞侵襲能力而定)。
取出Transwell小室,棄去孔中培養液,用不含鈣的PBS清洗2遍,4%多聚甲醛固定10 - 30 min,將小室適當風干。
使用0.1%結晶紫染色5 - 20 min,用棉簽輕輕擦掉上層未遷移細胞,用PBS洗3遍于顯微鏡下隨即5個視野觀察細胞,記數。
PART.03
實驗結果
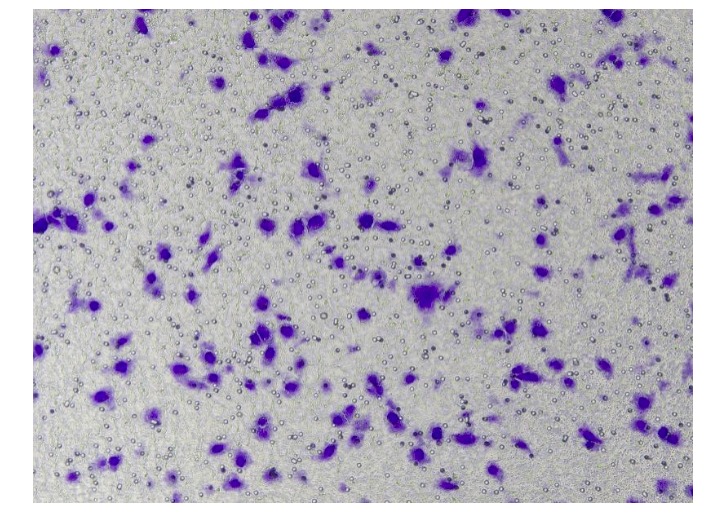
圖2.細胞侵襲后經結晶紫染色的結果
PART.04
常見問題及解答
細胞不轉移?
QA
①細胞侵襲轉移能力比較弱。
②基質膠濃度不佳鋪的太厚,需要做預實驗摸索。
③細胞給的量少可嘗試增加細胞數量。
④細胞沒有用PBS洗1-2 遍,用胰酶消化后,必須將含血清的培養基洗去。
⑤細胞的活性太差,活性不好的細胞做侵襲實驗難度較大。
染色后細胞分布不均一?
QA
①小室未平衡放置于孔板中。
②細胞懸液加入時局部過多。
③小室有傾斜或晃動。
④小室本身滲透膜不平。
PART.05
產品詳情
|
產品名稱 |
貨號 |
規格 |
|
Ceturegel® Matrix LDEV-Free基質膠 |
40183ES |
1.5 mL/5 mL/10 mL |
|
PerfCell™ Trypsin (0.25%), phenol red胰酶溶液(0.25%),含酚紅 |
40126ES |
100 mL |
|
Fetal Bovine Serum Gold 胎牛血清(特級) |
40130ES |
50 mL/500 mL |
|
PBS(1×)細胞培養級 |
41403ES |
500 mL |
|
0.5%結晶紫染色液 Crystal Violet Stain Solution |
60506ES |
100 mL |
|
24孔細胞小室,PC膜,8μm,滅菌,TC處理 |
84052ES |
12個/板 |
|
24孔細胞小室,PET膜,8μm,滅菌,TC處理 |
84051ES |
12個/板 |
