腫瘤壞死因子(TNF)通路是一個高度依賴蛋白質(zhì)磷酸化調(diào)控的重要的促炎信號通路。臨床上,靶向TNF在治療炎癥方面非常成功,但抗炎療法可能會引起嚴(yán)重的副作用。由于TNF相關(guān)磷酸化調(diào)控網(wǎng)絡(luò)未得以全面剖析,因此亟需更系統(tǒng)的方法深入了解其中激酶、磷酸酶、底物關(guān)系及其信號轉(zhuǎn)導(dǎo)動力學(xué)變化,為藥物干預(yù)提供靶點(diǎn),幫助更精確地控制疾病。 今年10月,蛋白組學(xué)領(lǐng)軍大牛Matthias Mann教授團(tuán)隊(duì)在Nature Communications上發(fā)表了題為 “Phosphoproteome profiling uncovers a key role for CDKs in TNF signaling”的論文,利用高深度的DIA磷酸化蛋白質(zhì)組學(xué)深入解析了TNF下游的信號轉(zhuǎn)導(dǎo)變化,從功能上探討了TNF及其誘導(dǎo)的細(xì)胞死亡中蛋白磷酸化變化,并揭示了CDK激酶在其中的關(guān)鍵調(diào)控作用,為抗炎治療等提供潛在藥物干預(yù)靶點(diǎn)。 技術(shù)路線 步驟1:通過DIA磷酸化組學(xué),比較TNF處理不同時間磷酸化水平的變化; 步驟2:抑制關(guān)鍵激酶并揭示激酶和底物的關(guān)系; 步驟3:分離細(xì)胞膜、細(xì)胞核和細(xì)胞質(zhì),通過組學(xué)研究TNF誘導(dǎo)的磷酸化引起的蛋白易位; 步驟4:研究TNF誘導(dǎo)的細(xì)胞死亡中蛋白和磷酸化水平的變化; 步驟5:抑制CDK激酶,通過蛋白組學(xué)研究CDK的作用。 研究結(jié)果 1. TNF誘導(dǎo)磷酸化水平隨時間變化,可區(qū)分早期和晚期信號轉(zhuǎn)導(dǎo)活動 為系統(tǒng)描繪TNF相關(guān)磷酸化變化網(wǎng)絡(luò),對TNF處理不同時間后U937細(xì)胞進(jìn)行DIA磷酸化蛋白質(zhì)組學(xué)分析,共鑒定到28,000條高可信度的磷酸化肽段。結(jié)果顯示,磷酸化水平在處理3min后顯著上調(diào),15min達(dá)到峰值,大多數(shù)在60min后恢復(fù)到基線水平(圖1d,e,f)。進(jìn)一步分析表明,許多參與NF-κB、模式識別信號通路為瞬時變化修飾蛋白,少數(shù)轉(zhuǎn)錄相關(guān)蛋白為較為持久修飾蛋白,其磷酸化在TNF刺激后60分鐘仍保持上調(diào) (圖1f)。綜上,可根據(jù)蛋白磷酸化變化時序區(qū)分早期(5分鐘)、中期(15分鐘)、晚期(60分鐘)信號活動。 圖1 TNF調(diào)控下不同時間的磷酸化信號活動 2. TNF刺激下的激酶-底物關(guān)系分析 為進(jìn)一步揭示激酶-底物關(guān)系,使用特定抑制劑去抑制關(guān)鍵激酶活性,并進(jìn)行磷酸化組學(xué)分析。結(jié)果表明,對于通過激活NF-κB等上游通路的激酶而言,如TAK1,其活性抑制后幾乎消除了TNF相關(guān)的磷酸化變化(圖2c)。相反,抑制下游激酶如IKK1/2、p38、MEK1/2和JNK則不能完全消除TNF作用(圖2c)。進(jìn)一步在STRING網(wǎng)絡(luò)中分析激酶與底物關(guān)系,發(fā)現(xiàn)在TNF刺激下磷酸化的蛋白質(zhì)并未與其他磷酸化蛋白緊密相關(guān) (圖2d)。同時,有些蛋白不受TAK1抑制影響,但受到IKK1/2抑制的強(qiáng)烈影響(圖2e),表明IKK1/2發(fā)揮了一些不依賴于TAK1活性的功能。總之,該分析全面揭示了TNF刺激下的激酶與底物關(guān)系。 圖2 TNF刺激下的激酶-底物關(guān)系 3. TNF相關(guān)磷酸化引發(fā)蛋白質(zhì)重新定位 TNF相關(guān)磷酸化變化依賴于激酶及其底物的重新定位。為了分析該現(xiàn)象,比較TNF處理后,細(xì)胞膜、細(xì)胞核和細(xì)胞質(zhì)中的蛋白及磷酸化變化,從而評估蛋白質(zhì)定位變化 (圖3a)。結(jié)果顯示,NF-κB通路、轉(zhuǎn)錄相關(guān)蛋白質(zhì)等很多蛋白質(zhì)發(fā)生定位變化(圖3d,e, f)。富集分析顯示,RIG-I通路、RNA加工體組裝的蛋白質(zhì)在膜上發(fā)生磷酸化變化,而模式識別受體信號通路和細(xì)胞遷移通路中的磷酸化在細(xì)胞質(zhì)基質(zhì)中發(fā)生變化(圖3h),且其中多數(shù)能被TAK1抑制劑阻礙,暗示其受細(xì)胞質(zhì)中TAK1 活性調(diào)控(圖3g)。 圖3 TNF誘導(dǎo)的磷酸化影響TAK1下游信號通路成員的定位變化 4. TNF誘導(dǎo)的細(xì)胞死亡觸發(fā)強(qiáng)烈的RNA加工響應(yīng)和CDK激活 為分析TNF誘導(dǎo)細(xì)胞死亡中關(guān)鍵調(diào)控的磷酸化蛋白,對TNF處理的U937細(xì)胞添加細(xì)胞凋亡和壞死抑制劑(SM、IDN-6556)誘導(dǎo)細(xì)胞死亡,并進(jìn)行磷酸化組學(xué)分析 (圖4b)。結(jié)果表明,RNA剪接和mRNA加工的蛋白磷酸化在凋亡過程中顯著上調(diào)(圖4c)。進(jìn)一步分析及驗(yàn)證發(fā)現(xiàn),該過程受到細(xì)胞周期蛋白依賴激酶CDKs的磷酸化變化調(diào)控,CDKs通過調(diào)節(jié)RNA聚合酶II活性來調(diào)節(jié)轉(zhuǎn)錄過程, 其中,CDK9 T354位點(diǎn)的磷酸化在TNF處理后上調(diào)9倍(圖4c-i)。 圖4 TNF誘導(dǎo)的細(xì)胞死亡導(dǎo)致強(qiáng)烈的RNA加工響應(yīng)及CDK激活 5. TNF靶基因的轉(zhuǎn)錄依賴于CDK激酶活性 TNF能誘導(dǎo)廣泛的靶基因轉(zhuǎn)錄表達(dá),而上述分析中已發(fā)現(xiàn)CDKs通過調(diào)節(jié)RNA聚合酶II活性調(diào)控轉(zhuǎn)錄。為進(jìn)一步解析CDKs活性變化是否影響TNF誘導(dǎo)的靶基因表達(dá)。采用不同CDKs抑制劑處理TNF刺激的U937細(xì)胞,并進(jìn)行蛋白質(zhì)組分析,發(fā)現(xiàn)CDK激酶活性抑制后幾乎消除了TNF誘導(dǎo)的蛋白質(zhì)表達(dá)變化(圖5a-5b)。隨后,又驗(yàn)證了相關(guān)靶基因CCL2 (MCP1)和CXCL10 (IP10)mRNA水平變化,發(fā)現(xiàn)同樣下調(diào)(圖5d),說明該過程確實(shí)發(fā)生在轉(zhuǎn)錄水平上。綜上表明,CDKs激酶活性變化調(diào)控TNF靶基因的轉(zhuǎn)錄。 小結(jié) 中科優(yōu)品推薦 磷酸化修飾是生物體內(nèi)最普遍的一種修飾,研究方法眾多,【中科新生命】可提供4D-labelfree、TMT、DIA多種技術(shù)方法的磷酸化組學(xué)檢測。其中DIA磷酸化可實(shí)現(xiàn)超高深度的檢測,覆蓋度及準(zhǔn)確性都有顯著提升。歡迎感興趣的老師前來咨詢。

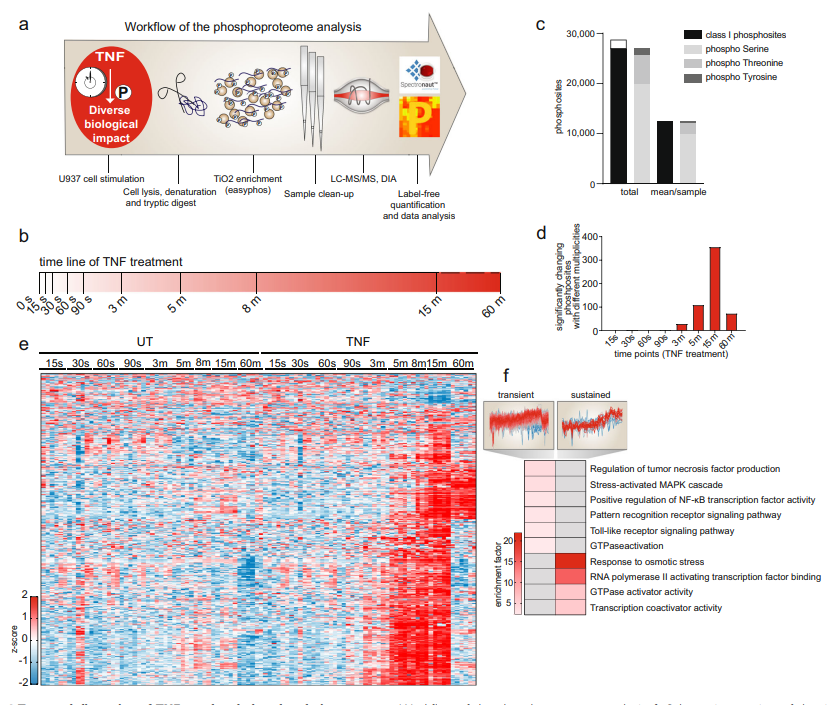
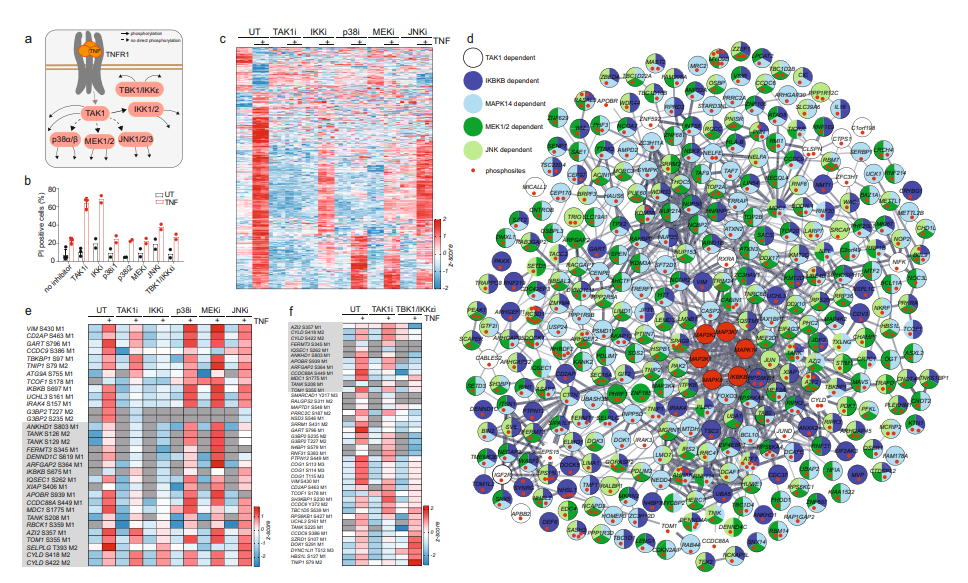
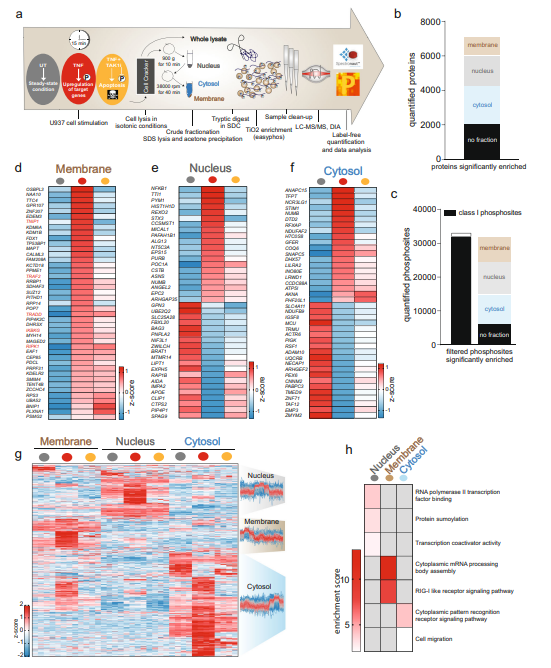
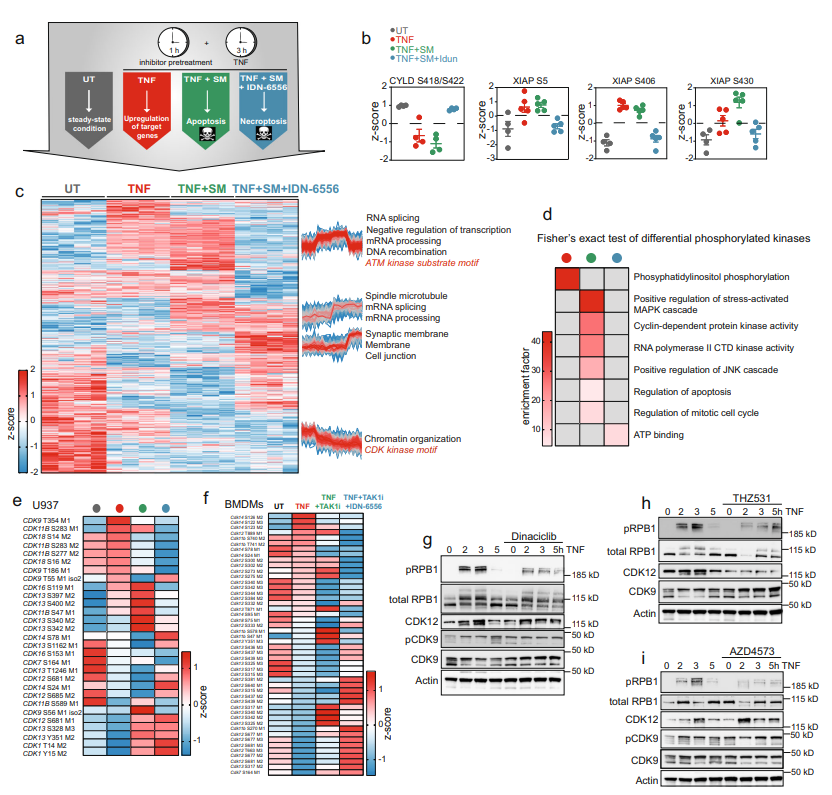
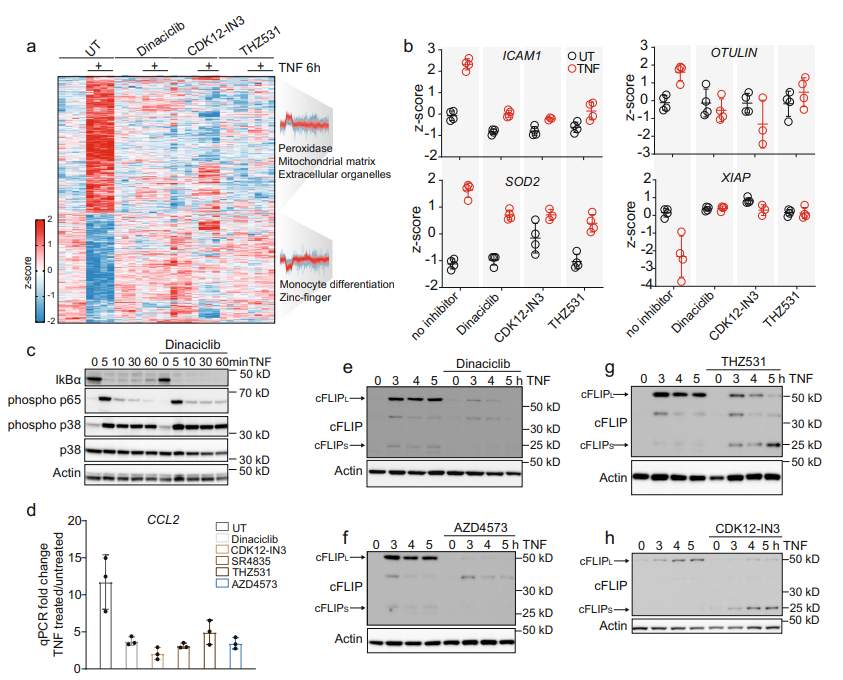
圖5 CDK9和CDK12/13抑制劑影響TNF靶基因的轉(zhuǎn)錄
本研究通過DIA磷酸化蛋白質(zhì)組學(xué)與亞細(xì)胞定位和激酶抑制劑分析相結(jié)合,深入分析了TNF受體下游的信號事件,闡明了數(shù)千個磷酸化事件的動力學(xué)、激酶底物關(guān)系和定位變化,提示了針對不同轉(zhuǎn)錄的CDKs的抑制劑可以作為抗炎劑或腫瘤細(xì)胞殺傷劑,深入全面的磷酸化水平的數(shù)據(jù)為后續(xù)研究提供了寶貴資源。

Nat Commun(IF 14.9)| 組學(xué)領(lǐng)軍大牛Matthias Mann利用DIA磷酸化組深度剖析促炎信號通路
作者:上海中科新生命生物科技有限公司 2021-12-30T18:51 (訪問量:4050)
上海中科新生命生物科技有限公司 商家主頁
地 址: 上海市園美路58號1號樓15-18樓
聯(lián)系人: 徐
電 話: 021-54665263
傳 真:
Email:marketing@aptbiotech.com
相關(guān)咨詢
會議邀請 | 第8屆全國植物蛋白質(zhì)研究大會暨首屆貴陽生命科學(xué)新高地科學(xué)家論壇 (2023-07-07T14:37 瀏覽數(shù):32748)
項(xiàng)目文章Cell(IF 64.5)| 中國科技大學(xué)探索食物過敏謎團(tuán) (2023-07-07T14:22 瀏覽數(shù):34099)
Gastroenterology(IF 29.4)| 基于機(jī)器學(xué)習(xí)算法開發(fā)的外泌體miRNA生物標(biāo)志物用于胰腺導(dǎo)管腺癌早期診斷 (2023-07-05T15:54 瀏覽數(shù):31401)
Cancer Letters(IF 9.7)|天津市環(huán)湖醫(yī)院利用Labelfree揭示超聲-替莫唑胺聯(lián)合誘導(dǎo)膠質(zhì)瘤細(xì)胞的凋亡機(jī)制 (2023-06-30T09:37 瀏覽數(shù):32389)
Excel表免費(fèi)下載 | 速來圍觀!2023年影響因子發(fā)布 (2023-06-29T09:35 瀏覽數(shù):27249)
外泌體多組學(xué)創(chuàng)新解決方案,精準(zhǔn)、前沿的疾病診斷生物標(biāo)志物 (2023-06-28T10:20 瀏覽數(shù):36723)
Immunity (IF=43.474)丨單細(xì)胞+空間聯(lián)合揭示肉芽腫形成的異常淋巴發(fā)育進(jìn)程 (2023-06-26T17:28 瀏覽數(shù):31076)
專家齊聚 亮點(diǎn)回顧 | 2023年海口·中醫(yī)藥創(chuàng)新多組學(xué)研究論壇圓滿落幕 (2023-06-25T10:10 瀏覽數(shù):35342)
項(xiàng)目文章Plant J(IF 7)| 杭州師范大學(xué)王慧中團(tuán)隊(duì)通過空間代謝+單細(xì)胞測序等揭示紅豆杉幼莖細(xì)胞特異的紫杉烷合成調(diào)控模式 (2023-06-25T09:42 瀏覽數(shù):33464)
項(xiàng)目文章Gut Microbes(IF 9.434)| 腸道微生物竟是導(dǎo)致膽囊切除術(shù)后患者腹瀉的元兇? (2023-06-14T16:35 瀏覽數(shù):30377)
