前言
腎臟衰竭、尤其是終末期腎病,依然是全球面臨的重大健康問(wèn)題,目前的主要治療方法是器官移植,但供體器官的短缺使得學(xué)界亟需尋找替代方案。類(lèi)器官是一類(lèi)使用干細(xì)胞、在體外培養(yǎng)而成的三維模型,可模擬原代器官(如腎臟)的組織結(jié)構(gòu)和生理功能,因此提供了腎臟再生的新可能。不過(guò),如何高效且穩(wěn)定地大規(guī)模生產(chǎn)并保證其結(jié)構(gòu)與功能的完備性,一直是該領(lǐng)域的核心挑戰(zhàn)之一。
2025年10月31日,西班牙巴塞羅那生物工程研究中心(IBEC)、CIBER-BBN、INIBIC、ONT、巴塞羅那大學(xué)(UB)及合作團(tuán)隊(duì)在期刊Nature Biomedical Engineering發(fā)表論文“Systematic production of human kidney organoids for transplantation in porcine kidneys during ex vivo machine perfusion”,開(kāi)發(fā)了一項(xiàng)生產(chǎn)人類(lèi)腎臟類(lèi)器官的可擴(kuò)展新方案。該方案能夠在可控且成本低廉的條件下規(guī)模化生產(chǎn)均一的腎臟類(lèi)器官。這些類(lèi)器官在通過(guò)體外機(jī)器灌注技術(shù)注入豬腎臟并移植回同一動(dòng)物體內(nèi)后,48小時(shí)內(nèi)觀(guān)測(cè)到與豬腎組織的整合。更為重要的是,移植的腎臟類(lèi)器官可正常運(yùn)作,未見(jiàn)損傷、毒性或免疫排斥,提示用于再生醫(yī)學(xué)的可行性。

總之,本研究是再生醫(yī)學(xué)和個(gè)性化醫(yī)學(xué)領(lǐng)域的一個(gè)重要里程碑,為利用人類(lèi)干細(xì)胞衍生的腎臟類(lèi)器官進(jìn)行細(xì)胞治療臨床試驗(yàn)鋪平了道路。
腎臟類(lèi)器官是一種體外自組織的三維結(jié)構(gòu),可在體外培養(yǎng)。圖片來(lái)源:IBEC
01 優(yōu)化腎臟類(lèi)器官培養(yǎng)方案
研究人員首先優(yōu)化了腎臟類(lèi)器官的培養(yǎng)條件。通過(guò)對(duì)不同的細(xì)胞聚集密度與培養(yǎng)微環(huán)境的系統(tǒng)測(cè)試,他們發(fā)現(xiàn),強(qiáng)化細(xì)胞間相互作用、誘導(dǎo)氧化磷酸化代謝并精確控制中間中胚層細(xì)胞分化節(jié)律,可以獲得更為均一且分化成熟的類(lèi)器官結(jié)構(gòu)。
表:優(yōu)化后的培養(yǎng)方案
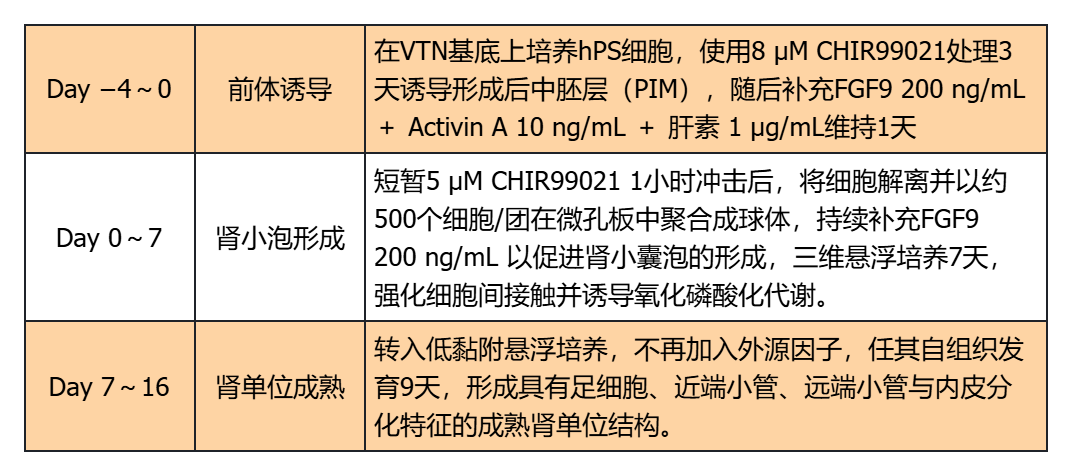
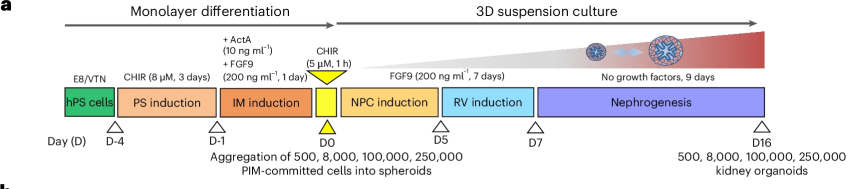
圖:優(yōu)化后的培養(yǎng)方案
值得注意的是,當(dāng)PIM定向的3D球狀體起始聚集量為500個(gè)時(shí),最終獲得腎臟類(lèi)器官表現(xiàn)出更高比例的腎單位結(jié)構(gòu)(如腎小球、近端小管、遠(yuǎn)端小管等),并具備更強(qiáng)的線(xiàn)粒體氧化代謝表型和成熟標(biāo)志基因表達(dá)(如PGC1A、SLC3A1、NPHS1等)。
由此,新方案為后續(xù)移植實(shí)驗(yàn)提供了標(biāo)準(zhǔn)化且可擴(kuò)增的類(lèi)器官來(lái)源。
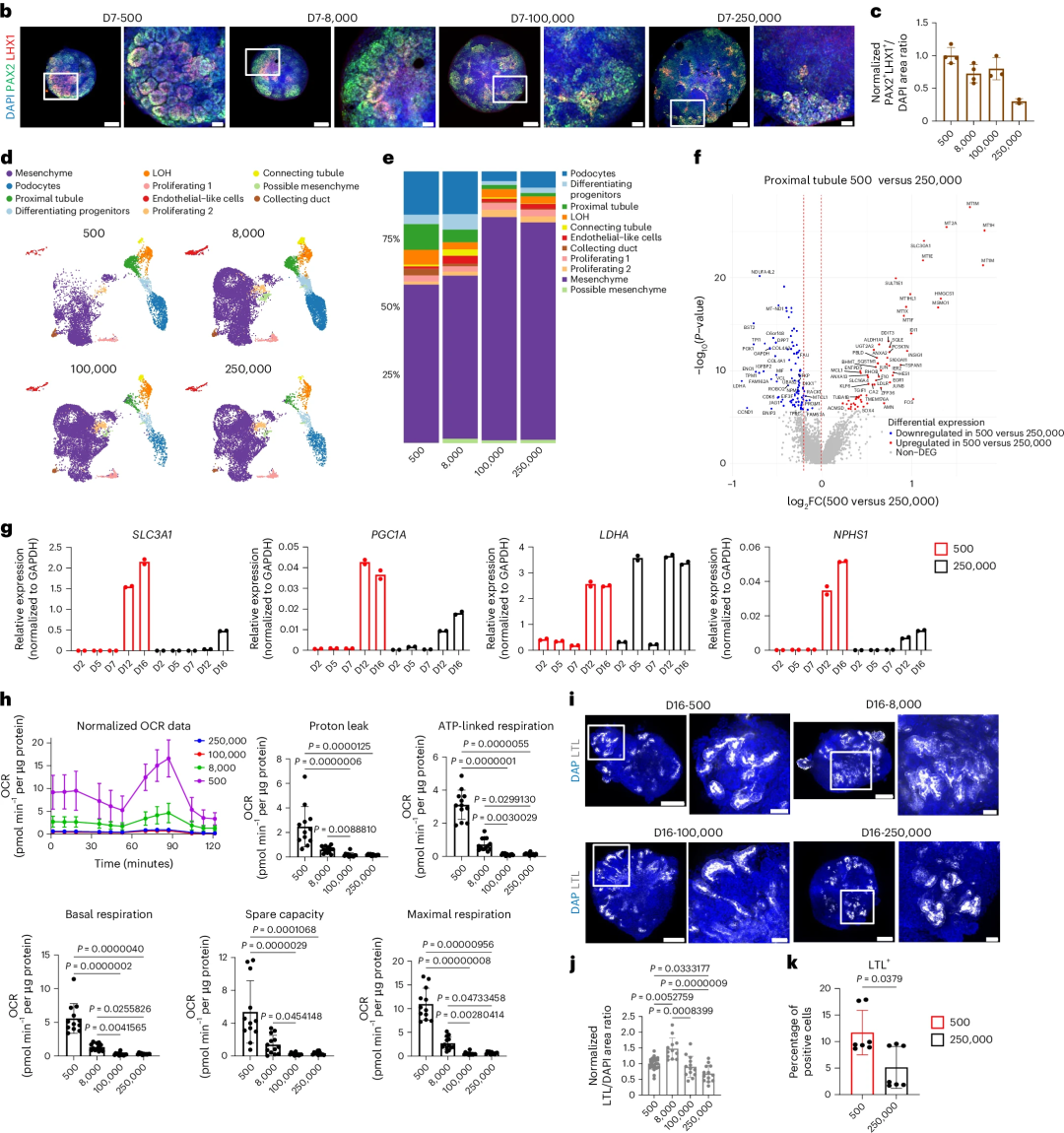
圖:懸浮培養(yǎng)中腎臟類(lèi)器官的生成
02 標(biāo)準(zhǔn)化腎臟類(lèi)器官生產(chǎn)體系的構(gòu)建:
微聚集法
當(dāng)確定了“500個(gè)細(xì)胞微團(tuán)+CHIR+FGF9+兩階段誘導(dǎo)+無(wú)因子成熟”的最優(yōu)方案后,研究團(tuán)隊(duì)試圖把它轉(zhuǎn)化為可規(guī)模化、可復(fù)現(xiàn)的生產(chǎn)系統(tǒng)。他們采用AggreWell微孔板精確控制每個(gè)微團(tuán)的起始細(xì)胞數(shù)(約500個(gè)),并通過(guò)離心聚合獲得均一球體,確保每個(gè)微團(tuán)都沿著三階段培養(yǎng)的節(jié)律發(fā)育,從而批量在每個(gè)24孔板上生成了約3萬(wàn)枚分化同步、結(jié)構(gòu)均一、在細(xì)胞組成、代謝狀態(tài)、基因表達(dá)上都高度可控的腎臟類(lèi)器官,且幾乎100%的類(lèi)器官都呈現(xiàn)出分節(jié)的腎單位樣結(jié)構(gòu),并表達(dá)腎單位和內(nèi)皮細(xì)胞標(biāo)志物。
此外,該方案也可用于人胚胎干細(xì)胞(hES細(xì)胞)和人誘導(dǎo)多能干細(xì)胞(iPS細(xì)胞)來(lái)源的類(lèi)器官培養(yǎng),具備可擴(kuò)展性,并顯著提升了生產(chǎn)效率與實(shí)驗(yàn)可重復(fù)性。接下來(lái),研究人員開(kāi)始探索下一步動(dòng)物試驗(yàn)階段。
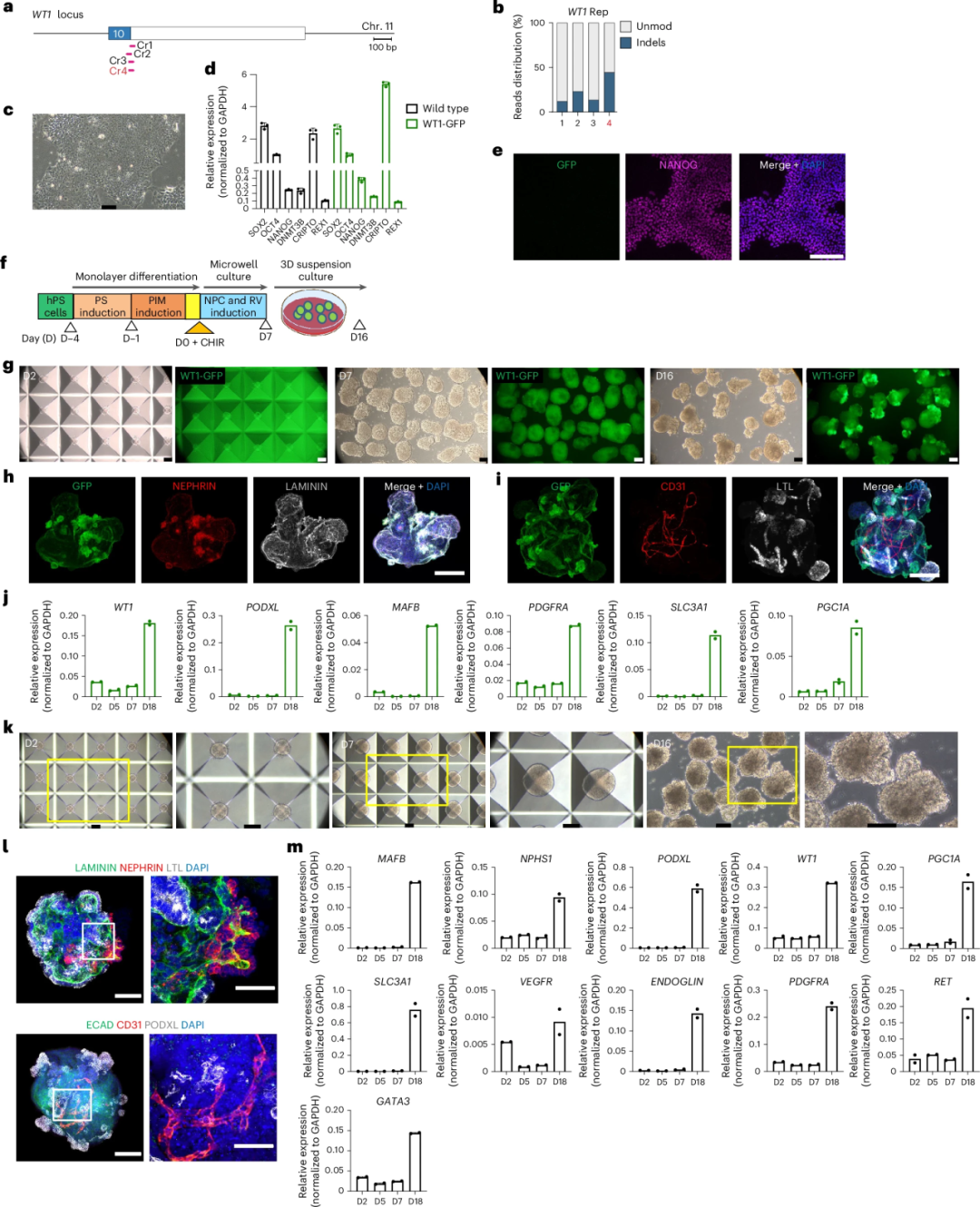
圖:通過(guò)微聚集實(shí)現(xiàn)均一腎臟類(lèi)器官的規(guī)模化生產(chǎn)
03 類(lèi)器官在豬腎中的存活與整合
豬腎結(jié)構(gòu)與人腎相似,是良好的動(dòng)物實(shí)驗(yàn)?zāi)P汀R虼耍芯繄F(tuán)隊(duì)首先將規(guī)模化生產(chǎn)的人腎臟類(lèi)器官通過(guò)標(biāo)準(zhǔn)的體外機(jī)器灌注(NMP)技術(shù)注入豬腎,模擬了腎臟移植前的處理過(guò)程,隨后將其移植回同一只動(dòng)物體內(nèi),持續(xù)觀(guān)察了48小時(shí)。
此處使用的NMP在手術(shù)室中常用于在移植前維持體外器官的活性和氧氣供應(yīng),因此能夠在移植前維持腎臟的生理功能,減少缺血-再灌注損傷,提高器官的耐受性。需要注意的是,此舉的目的并非在于直接“替代”腎臟,而是對(duì)人源類(lèi)器官在豬體內(nèi)的存活、整合和功能的驗(yàn)證,尤其是類(lèi)器官能否在免疫完整的宿主體內(nèi)長(zhǎng)期生存而不被急性排斥。
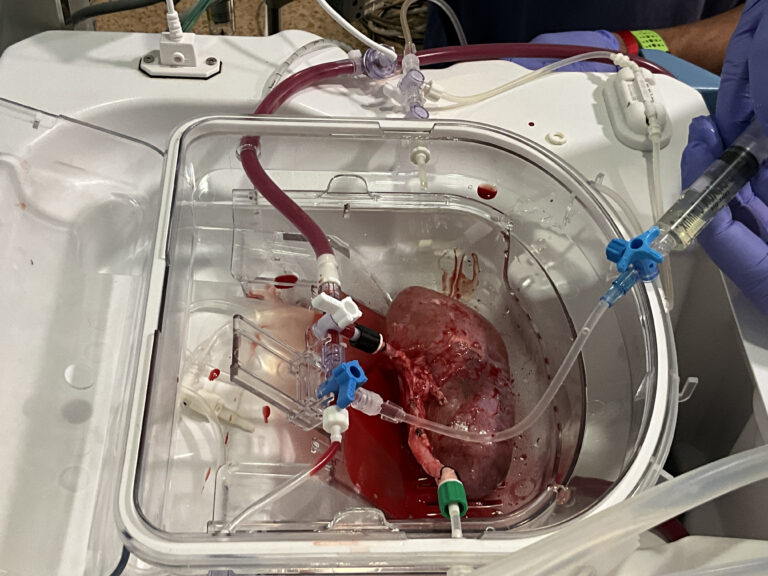
圖:豬腎連接至常溫灌注機(jī)。該裝置可使腎臟在體外保持活性并進(jìn)行氧合。圖片顯示的是將人腎臟類(lèi)器官注入豬腎的瞬間。
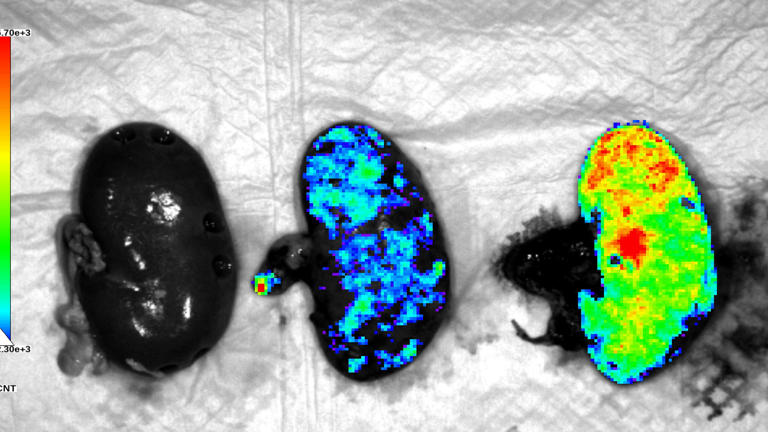
實(shí)驗(yàn)結(jié)果表明,注入豬腎的腎臟類(lèi)器官成功存活,并在48小時(shí)內(nèi)與豬腎組織實(shí)現(xiàn)初步整合并維持正常功能。研究人員通過(guò)體內(nèi)成像和流式細(xì)胞分析在腎皮質(zhì)及腎小管區(qū)域發(fā)現(xiàn)了人源細(xì)胞,其中部分細(xì)胞進(jìn)一步分化為上皮樣和腎小管樣結(jié)構(gòu),呈現(xiàn)活躍代謝和上皮極化信號(hào),提示其在宿主腎臟環(huán)境中可能持續(xù)生長(zhǎng)并發(fā)揮早期修復(fù)作用。
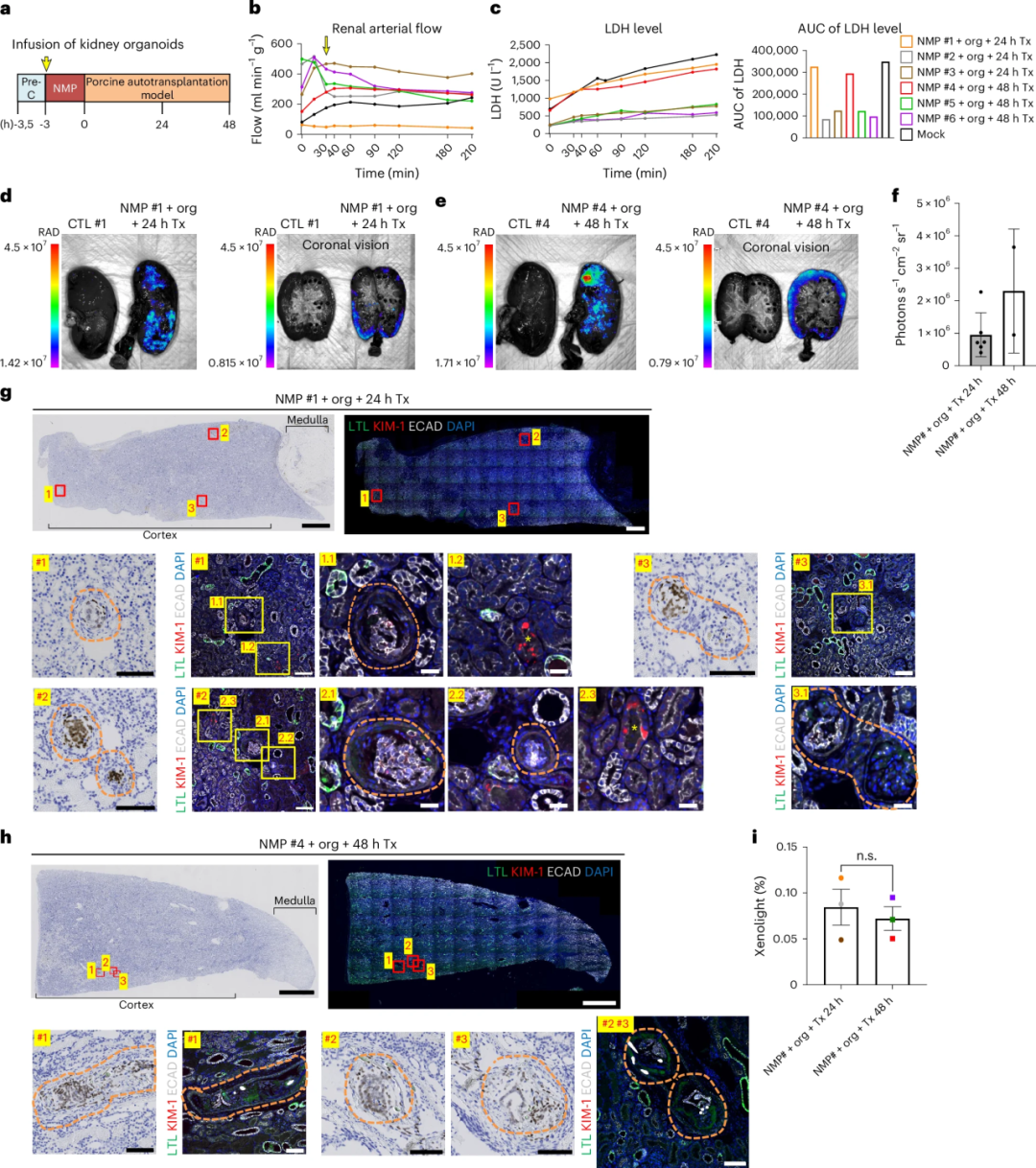
圖:將人類(lèi)腎臟類(lèi)器官注入豬腎臟進(jìn)行體內(nèi)移植
更重要的是,并未觀(guān)察到明顯的損傷、毒性或免疫排斥反應(yīng),這為類(lèi)器官移植提供了重要的免疫學(xué)依據(jù)。
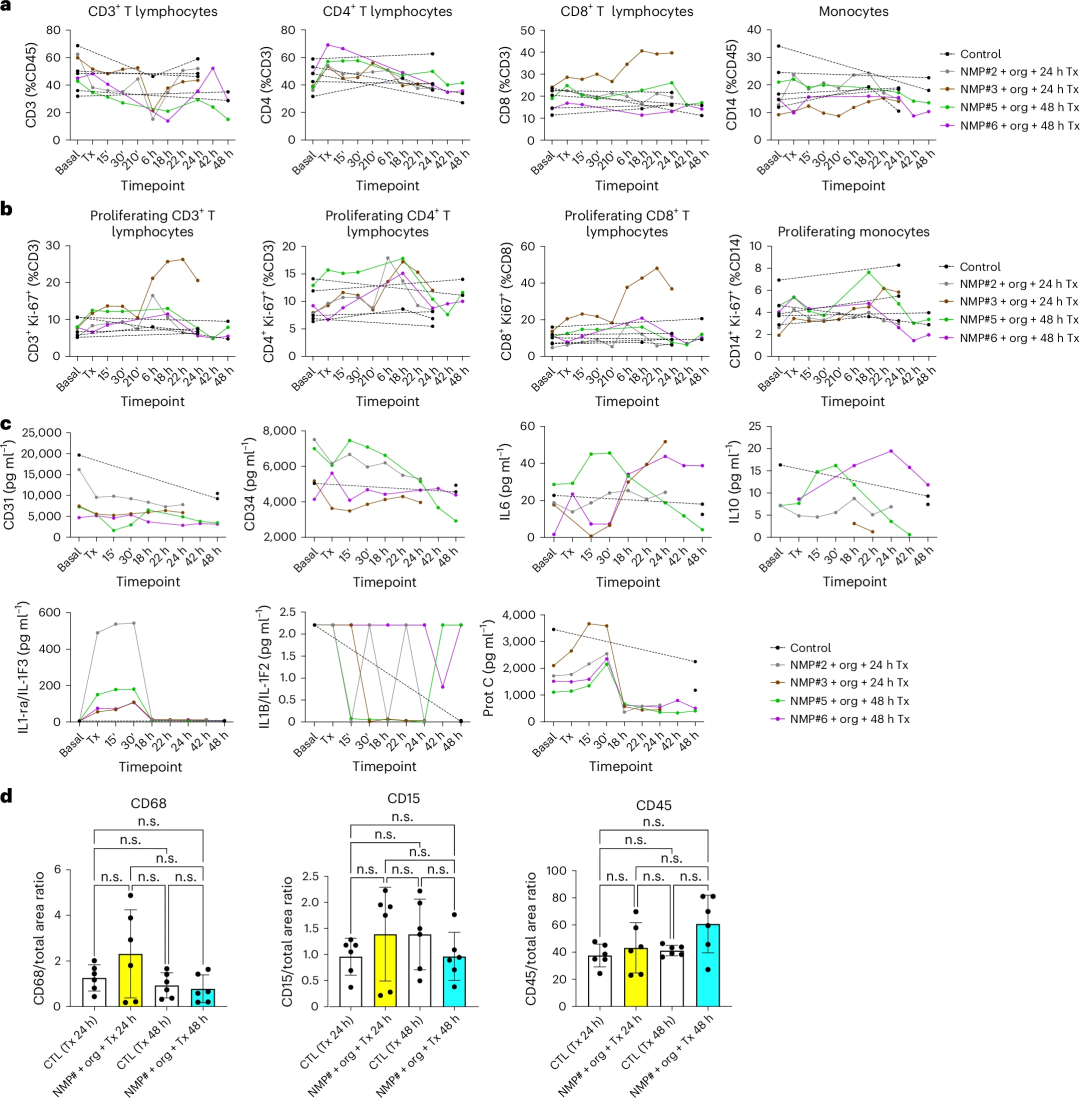
圖:體內(nèi)移植注入人類(lèi)腎臟類(lèi)器官的豬腎臟后全身和局部免疫反應(yīng)分析未見(jiàn)毒性或免疫排斥反應(yīng)
04 結(jié)論與展望
本研究通過(guò)改進(jìn)類(lèi)器官的生產(chǎn)技術(shù)和移植方法,研究人員展示了腎臟類(lèi)器官的移植不僅能夠在短期內(nèi)維持其功能,而且可能在臨床應(yīng)用中為腎臟再生治療提供新的解決方案。
需要注意的是,目前該項(xiàng)目組并不急于是直接“造一個(gè)完整人腎”,而是循序漸進(jìn)、力圖建立一個(gè)可修復(fù)、可增強(qiáng)、可重建的細(xì)胞治療模式。其臨床潛力體現(xiàn)在三個(gè)方向:
-
器官修復(fù):在邊緣性供體腎移植前,通過(guò)類(lèi)器官灌注修復(fù)受損腎小管或足細(xì)胞,提高移植存活率;
-
體外器官預(yù)活化:利用人源類(lèi)器官在動(dòng)物腎內(nèi)建立血管化、成熟的“人源化微腎單位”,為未來(lái)異種器官工程打基礎(chǔ);
-
細(xì)胞替代療法:以類(lèi)器官形式補(bǔ)充或替代受損腎功能區(qū)域,為慢性腎病提供細(xì)胞治療思路。
本文一作Garreta公開(kāi)表示,本研究開(kāi)發(fā)的類(lèi)器官技術(shù)能夠在可控條件下快速、精確地大規(guī)模生成腎臟類(lèi)器官,無(wú)需復(fù)雜的組件。“這為藥物篩選和疾病研究等應(yīng)用打開(kāi)了大門(mén),”她在新聞稿中總結(jié)道。“這種方法或許還能縮短慢性病患者的等待時(shí)間,并增加可用于移植的器官數(shù)量,從而幫助解決現(xiàn)代醫(yī)學(xué)面臨的最大挑戰(zhàn)之一。”
近岸蛋白相關(guān)產(chǎn)品
近岸蛋白提供多種類(lèi)器官體外培養(yǎng)全方案,包括基質(zhì)膠、培養(yǎng)基、相關(guān)細(xì)胞因子等:
經(jīng)類(lèi)器官培養(yǎng)驗(yàn)證的完全培養(yǎng)基
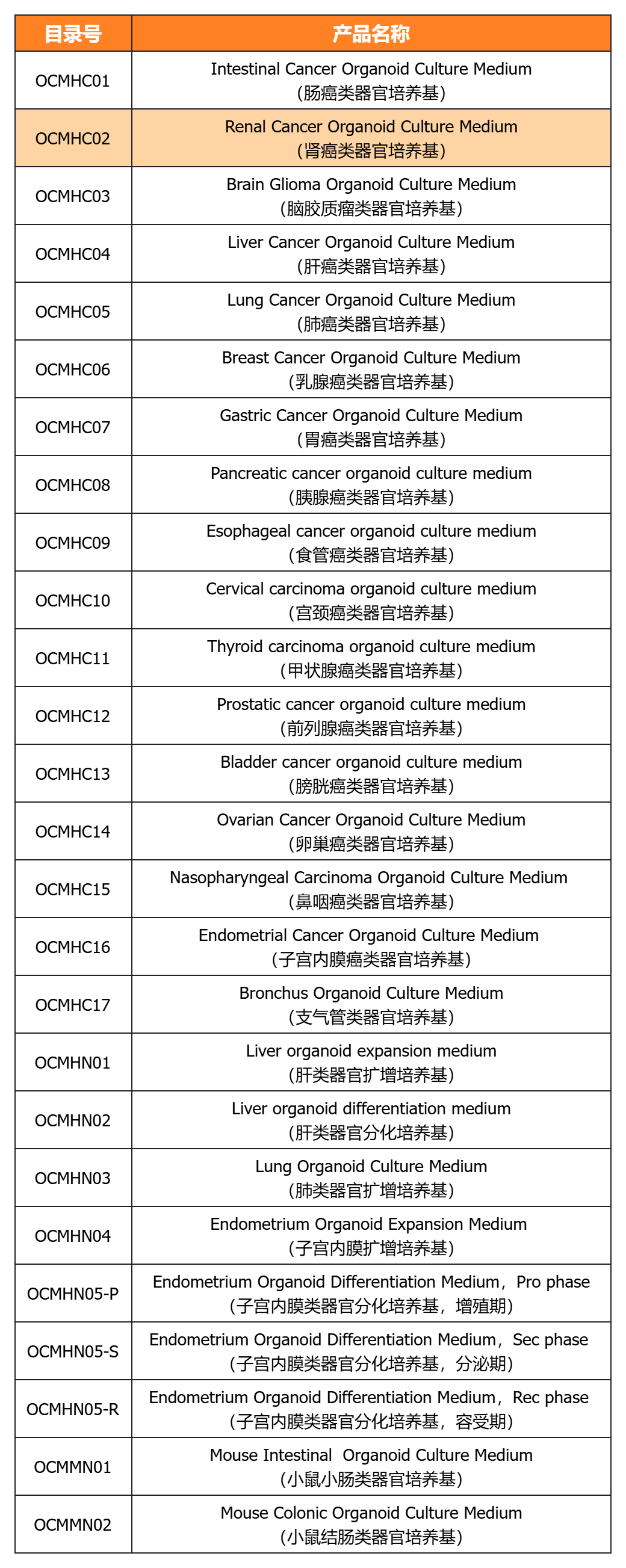
經(jīng)類(lèi)器官培養(yǎng)驗(yàn)證的細(xì)胞因子
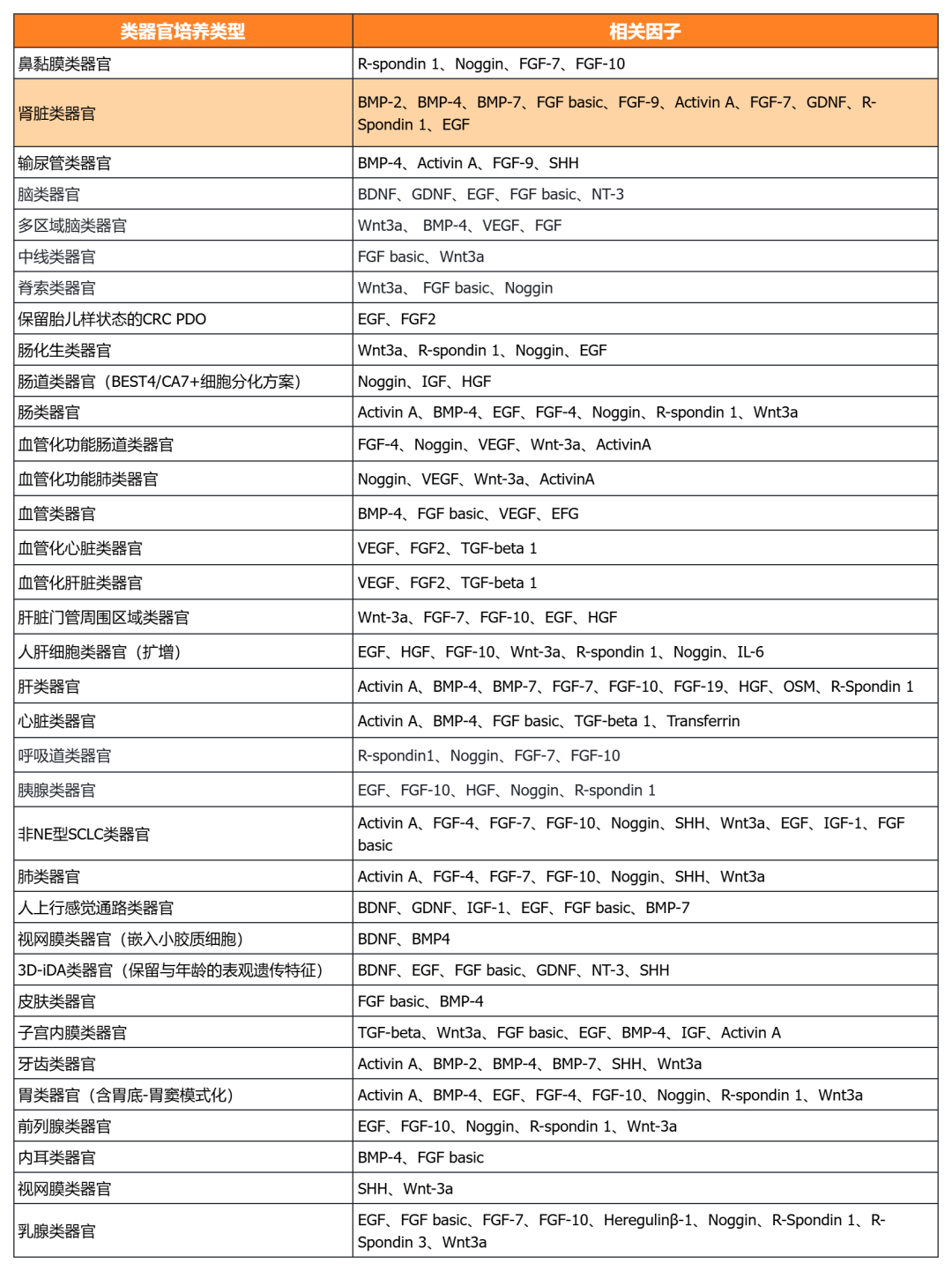
NovoMatrix 基質(zhì)膠
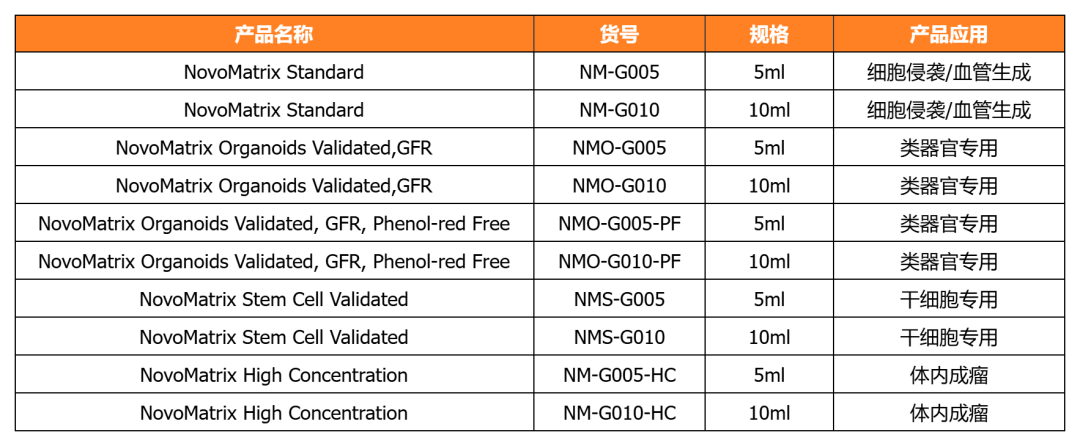
掃碼添加小編,加入類(lèi)器官培養(yǎng)交流群
技術(shù)支持答疑解惑,前沿進(jìn)展定期分享

??掃碼添加小編微信(請(qǐng)備注單位姓名)
參考資料
Garreta, E., Moya-Rull, D., Centeno, A. et al. Systematic production of human kidney organoids for transplantation in porcine kidneys during ex vivo machine perfusion. Nat. Biomed. Eng (2025).
