血管內(nèi)皮生長(zhǎng)因子(Vascular Endothelial Growth Factor , VEGF)在血管生成(angiogenesis)、血管通透性調(diào)節(jié)以及細(xì)胞增殖和存活中起關(guān)鍵作用,主要效應(yīng)細(xì)胞為內(nèi)皮細(xì)胞(ECs)[1]。VEGF家族包括VEGF-A/B/C/D/E、胎盤生長(zhǎng)因子(PIGF)共6個(gè)成員,根據(jù)其外顯子剪切的不同,主要分為5種亞型,再根據(jù)氨基酸的長(zhǎng)短依次命名為VEGF145、VEGF165、VEGF121、VEGF189、VEGF206,其中VEGF165是最常見且生物活性最強(qiáng)的亞型之一,也是內(nèi)皮細(xì)胞分泌最活躍且分布最廣泛的因子[2]。
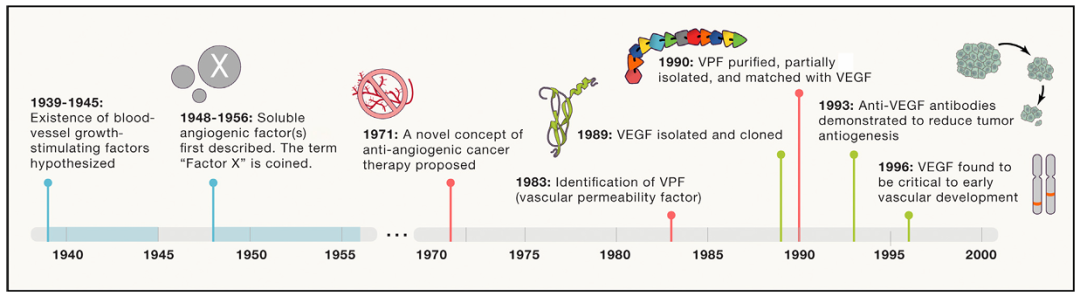
VEGF發(fā)現(xiàn)歷史[1]
VEGF165通過與細(xì)胞表面的受體(如VEGFR-1/23)結(jié)合,激活下游信號(hào)通路,在促進(jìn)血管生成、組織修復(fù)、胚胎發(fā)育過程中發(fā)揮重要作用。
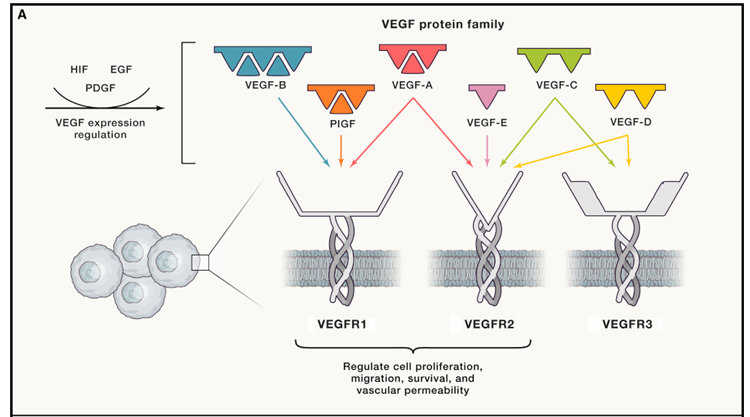
VEGF的激活和信號(hào)[1]
毛囊干細(xì)胞誘導(dǎo)分化血管內(nèi)皮細(xì)胞[2]
2017年,浙江中醫(yī)藥大學(xué)附屬江南醫(yī)院的研究者在J Cell Mol Med期刊上發(fā)表了一篇論文,該研究通過VEGF165誘導(dǎo)毛囊干細(xì)胞(rHFSC)分化為內(nèi)皮細(xì)胞,為了進(jìn)一步論述實(shí)驗(yàn)的可靠性,作者通過裸鼠體內(nèi)驗(yàn)證了新生血管的生成,設(shè)計(jì)了3組實(shí)驗(yàn)(PBS + Matrigel、VEGF165 + Matrigel、VEGF165 + rHFSCsGFP + Matrigel),結(jié)果證明PBS + Matrigel組幾乎沒有血管形成,VEGF165 + Matrigel組表現(xiàn)出形成血管的能力且有新生血管,VEGF165 + rHFSCsGFP + Matrigel)組具有明顯的新生血管網(wǎng)絡(luò)。總之,該研究改進(jìn)和優(yōu)化了rHFSC的分離、培養(yǎng)和純化方法,并建立了誘導(dǎo) rHFSCs分化為內(nèi)皮細(xì)胞的方法,并在體內(nèi)探究了體內(nèi)促血管生成的過程,為血管構(gòu)建、血管成形術(shù)和傷口早期血管形成提供了理論基礎(chǔ),并為使用組織工程皮膚臨床治療缺血性疾病提供了新的見解。
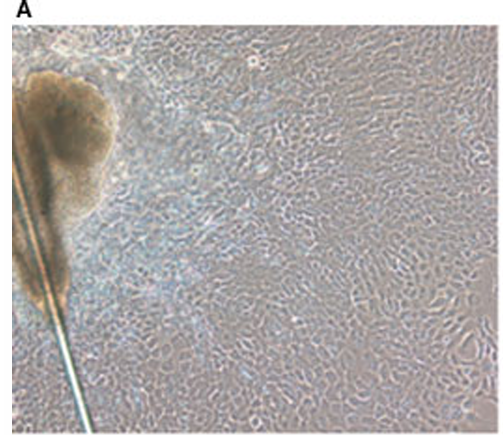
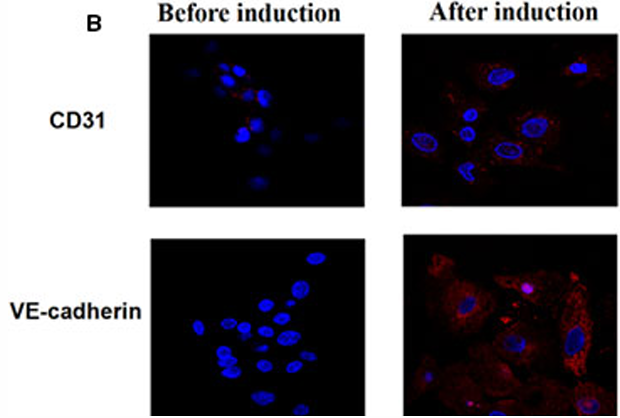
圖1 A-原代毛囊干細(xì)胞 B-VEGF165誘導(dǎo)后血管內(nèi)皮標(biāo)志物對(duì)比
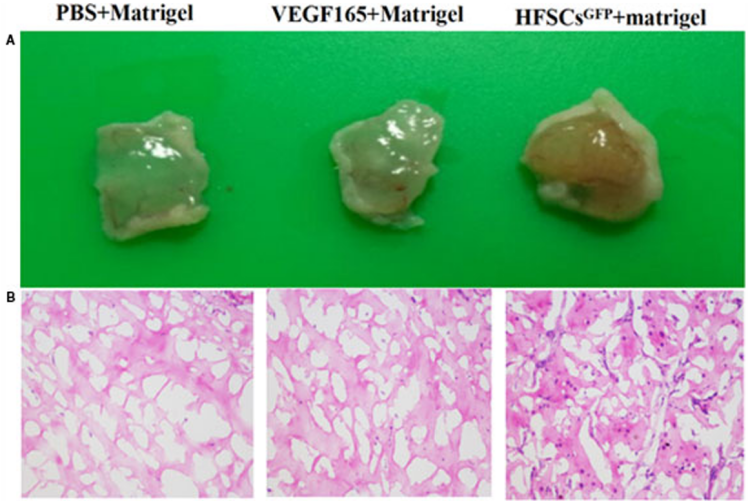
圖2 裸鼠體內(nèi)新生血管驗(yàn)證
iPSC誘導(dǎo)分化為血管內(nèi)皮細(xì)胞[3]
內(nèi)皮細(xì)胞(EC)排列在血管內(nèi)壁上,調(diào)節(jié)血管張力、結(jié)構(gòu)和炎癥。ECs對(duì)于維持血管穩(wěn)態(tài)至關(guān)重要,ECs功能障礙在驅(qū)動(dòng)動(dòng)脈粥樣硬化和高血壓等普遍的血管病變中起著關(guān)鍵作用。由于原代人ECs難以獲得,可塑性和增殖能力有限,因此相比之下,iPSC為各種應(yīng)用(包括疾病建模、細(xì)胞治療、組織移植血管化和微生理系統(tǒng))生成EC提供了潛在的無限來源。
2021年,國外一篇研究通過VEGF165誘導(dǎo)法建立了由iPSC生成血管內(nèi)皮(viEC)的方案,經(jīng)過7天的時(shí)間,將從350萬個(gè)人iPSC中分化多達(dá)5500萬個(gè)血管內(nèi)皮細(xì)胞(viEC),并對(duì)生理剪切力下的血管內(nèi)皮細(xì)胞的行為進(jìn)行了研究。該方案產(chǎn)生的viEC表現(xiàn)出內(nèi)皮細(xì)胞的多種特征功能,包括EC標(biāo)志物表達(dá)、流向?qū)R、敏感基因的上調(diào)等,生成的內(nèi)皮細(xì)胞可產(chǎn)生一氧化氮,響應(yīng)內(nèi)皮一氧化氮合酶 (NOS3) 反應(yīng),以維持血管穩(wěn)態(tài)。
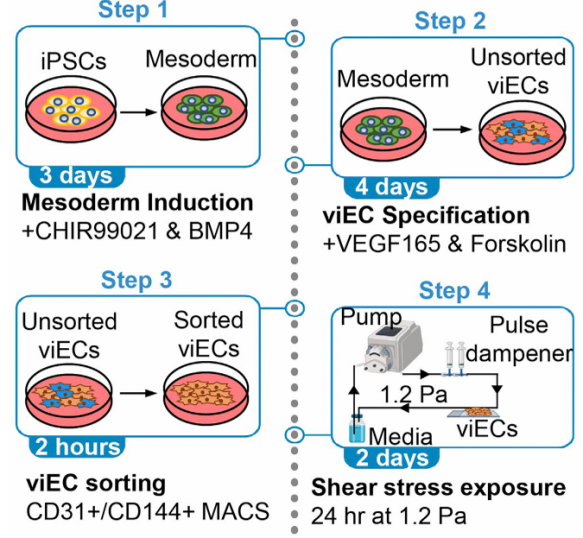
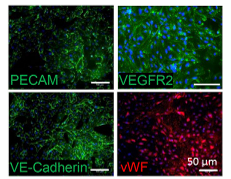
圖3 實(shí)驗(yàn)設(shè)計(jì)示意圖(左) ECs標(biāo)記物(右)
血管化前沿進(jìn)展

自2009年研究者對(duì)血管化技術(shù)的首次探索,經(jīng)過近20年的發(fā)展歷程,雖然已成功構(gòu)建多種血管化類器官模型,但通常缺乏清晰、完善的血管系統(tǒng),對(duì)自組織血管網(wǎng)絡(luò)形成的機(jī)制探究極為匱乏。
近日,國外專家于頂刊Science上發(fā)表了一篇重磅論文,該報(bào)道從人多能干細(xì)胞(hPSCs),在多種血管化誘導(dǎo)因子VEGF/FGF2/PDGF-BB/TGF-β1等的作用下,首次在體外構(gòu)建了與6.5周人類胚胎心臟發(fā)育階段相似的心臟血管類器官(具有心肌細(xì)胞、內(nèi)皮細(xì)胞和平滑肌細(xì)胞),精確模擬了人類胚胎發(fā)育早期心臟的血管形成過程[4]。
該研究不僅構(gòu)建了兼具血管功能和結(jié)構(gòu)的血管化類器官,也證明了血管生成機(jī)制可能是保守的,該研究結(jié)果不僅可用于體外心血管機(jī)制的深入探索,并且具有可預(yù)見的普適性,不僅對(duì)于類器官技術(shù)的發(fā)展具有關(guān)鍵推動(dòng)作用,也為發(fā)育生物學(xué)、先天缺陷疾病建模帶來新的突破。
內(nèi)皮細(xì)胞在血管生成、血管形成和分化過程中起著至關(guān)重要的作用,特別是在血管內(nèi)皮細(xì)胞分化和血管化類器官構(gòu)建中。VEGF165是誘導(dǎo)iPSC向血管內(nèi)皮細(xì)胞(Endothelial Cells, ECs)分化的關(guān)鍵因子,可以顯著提高iPSC分化的效率以及血管生成,因此,在心臟、肝臟、腎臟等器官的類器官培養(yǎng)中,VEGF165有助于類器官血管網(wǎng)絡(luò)的形成和功能成熟,為組織工程、再生醫(yī)學(xué)和疾病模型研究提供強(qiáng)有力的工具。
hPSC誘導(dǎo)類器官培養(yǎng)工具書,紙質(zhì)版免費(fèi)限時(shí)申領(lǐng)

-
9大hPSC來源類器官實(shí)驗(yàn)流程
-
提供經(jīng)驗(yàn)證的細(xì)胞因子種類和使用濃度
-
所需培養(yǎng)試劑組合推薦搭配
掃碼申請(qǐng)《hPSC誘導(dǎo)類器官白皮書》

近岸蛋白可提供高活性、高批間一致性的血管生成相關(guān)培養(yǎng)因子,包括VEGF165、FGF basic,、PDGF、 ANG、PGF、CXCL趨化因子等,覆蓋人屬、鼠屬,助力體外血管化技術(shù)的研究與發(fā)展。
VEGF165批間一致性數(shù)據(jù)
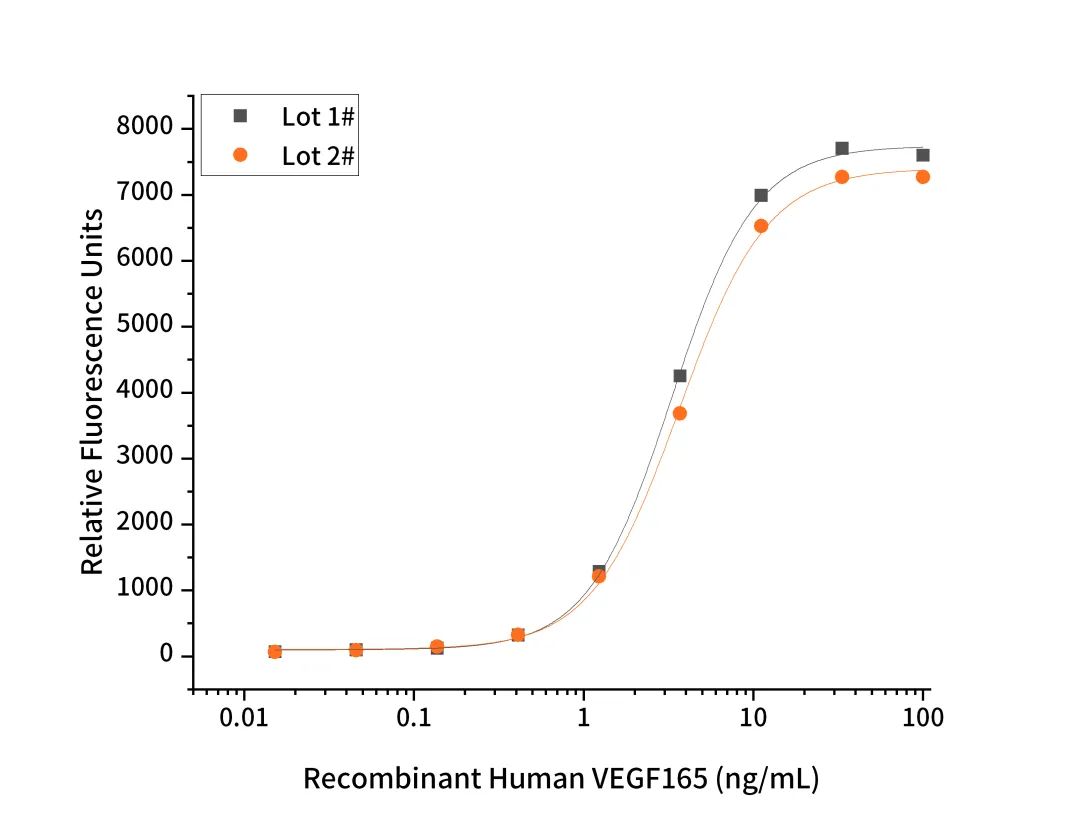
Measured by its ability to induce calcineurin- NFAT signaling in 293-VEGF Res cells. Two independent lots were tested for activity and plotted on the same graph to show lot-to-lot consistency of VEGF165.
血管生成相關(guān)細(xì)胞因子
|
|
|
|
|
|
|
|
|
GMP-CR96 |
Recombinant Human VEGF165 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
參考文獻(xiàn)
[1]Apte RS, Chen DS, Ferrara N.VEGF in Signaling and Disease: Beyond Discovery and Development.Cell. 2019;176(6):1248-1264. doi:10.1016/j.cell.2019.01.021.
[2]Quan R, Du W, Zheng X, Xu S, Li Q, Ji X, Wu X, Shao R, Yang D. VEGF165 induces differentiation of hair follicle stem cells into endothelial cells and plays a role in in vivo angiogenesis. J Cell Mol Med. 2017 Aug;21(8):1593-1604. doi: 10.1111/jcmm.13089.
[3]Abutaleb, & Truskey, G. A. (2021). Differentiation and characterization of human iPSC-derived vascular endothelial cells under physiological shear stress. STAR Protocols, 2(2), 100394.
[4]Abilez OJ, Yang H, Guan Y, et al. Gastruloids enable modeling of the earliest stages of human cardiac and hepatic vascularization. Science. 2025;388(6751):eadu9375. doi:10.1126/science.adu9375
