近期,廣州醫(yī)科大附屬第三醫(yī)院和美國得克薩斯大學(xué)西南醫(yī)學(xué)中心合作,利用基于質(zhì)譜的蛋白質(zhì)組學(xué)鑒定了參與鐵死亡的一個關(guān)鍵膜蛋白HPCAL1,并深入研究了其作用機制及潛在的靶向治療可能性。研究成果以“Identification of HPCAL1 as a specific autophagy receptor involved in ferroptosis”為題,發(fā)表在Autophagy(IF:13.391)上。

研究結(jié)果
?1.?HPCAL1?對鐵死亡是必須的
鐵死亡表現(xiàn)為細胞器和細胞膜的脂質(zhì)過氧化,但關(guān)鍵的膜調(diào)控蛋白仍然未知。研究者使用鐵死亡激活劑RSL3(一種谷胱甘肽過氧化物酶 4 (GPX4) 的抑制劑,誘導(dǎo)鐵死亡)分別處理人纖維肉瘤細胞HT-1080和人非小細胞肺癌細胞Calu-1,隨后分離細胞膜組分并進行基于質(zhì)譜的蛋白質(zhì)組學(xué)檢測,以期尋找關(guān)鍵的鐵死亡膜調(diào)控蛋白。
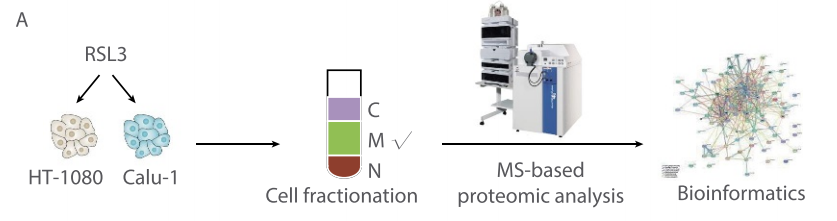
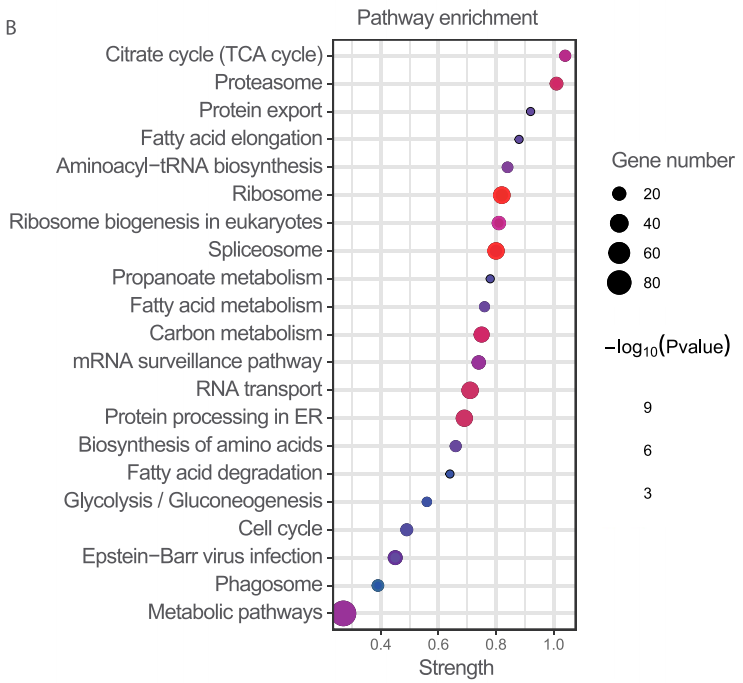
細胞膜組分的蛋白質(zhì)組學(xué)共鑒定了752個膜蛋白,這些膜蛋白的通路富集分析顯示,三羧酸循環(huán)代謝是鐵死亡中最受影響的通路,與此前報道的線粒體三羧酸循環(huán)和脂質(zhì)代謝參與鐵死亡的報道相一致。
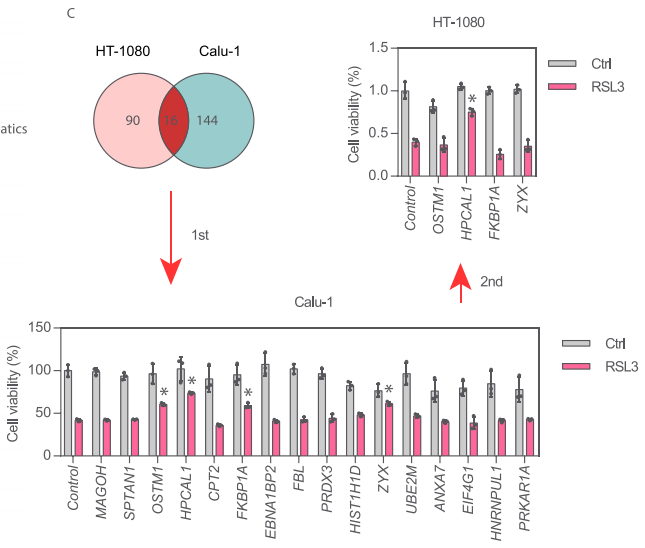
在鐵死亡激活劑RSL3處理后的HT-1080和Calu-1中有16個共有上調(diào)蛋白,包括MAGOH、SPTAN1、OSTM1、HPCAL1、CPT2、FKBP1A、EBNA1BP2、FBL、PRDX3、H1-3/HIST1H1D、ZYX、 UBE2M、ANXA7、EIF4G1、HNRNPUL1和PRKAR1A。隨后,研究者在兩輪實驗中分別使用靶向這些16個蛋白基因的siRNA處理HT-1080和Calu-1細胞,最終僅有HPCAL1 siRNA能同時降低RSL3誘導(dǎo)的細胞死亡。因此,研究者鎖定HPCAL1進行后續(xù)探索。
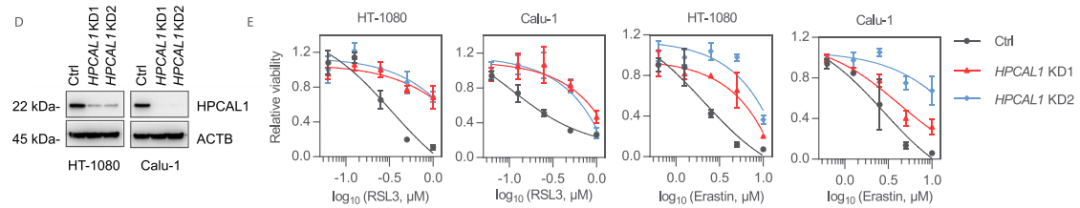
為了進一步確認HPCAL1在促進鐵死亡中的作用,研究者構(gòu)建了能穩(wěn)定敲低HPCAL1的兩個特異性shRNA。與HPCAL1 siRNA實驗結(jié)果一致,HPCAL1 shRNA抑制了RSL3或erastin(另一種鐵死亡誘導(dǎo)劑)誘導(dǎo)的HT-1080和Calu-1細胞生長抑制。
隨后的研究也表明,HPCAL1缺失不影響細胞膜的完整性。此外,HPCAL1缺失將顯著降低脂質(zhì)過氧化,因此HPCAL1可能是鐵死亡中脂質(zhì)過氧化的正調(diào)節(jié)劑。研究者繼續(xù)使用其他鐵死亡誘導(dǎo)劑,包括ML162、ML210、FIN56、FINO2和sulfasalazine處理HT-1080和Calu-1細胞,結(jié)果均證實了HPCAL1的促鐵死亡作用。而形成鮮明對比的是,細胞凋亡誘導(dǎo)劑staurosporine (STS)導(dǎo)致的細胞死亡并不受到HPCAL1敲低的影響。這一結(jié)果表明,HPCAL1是選擇性促進鐵死亡而非細胞凋亡。
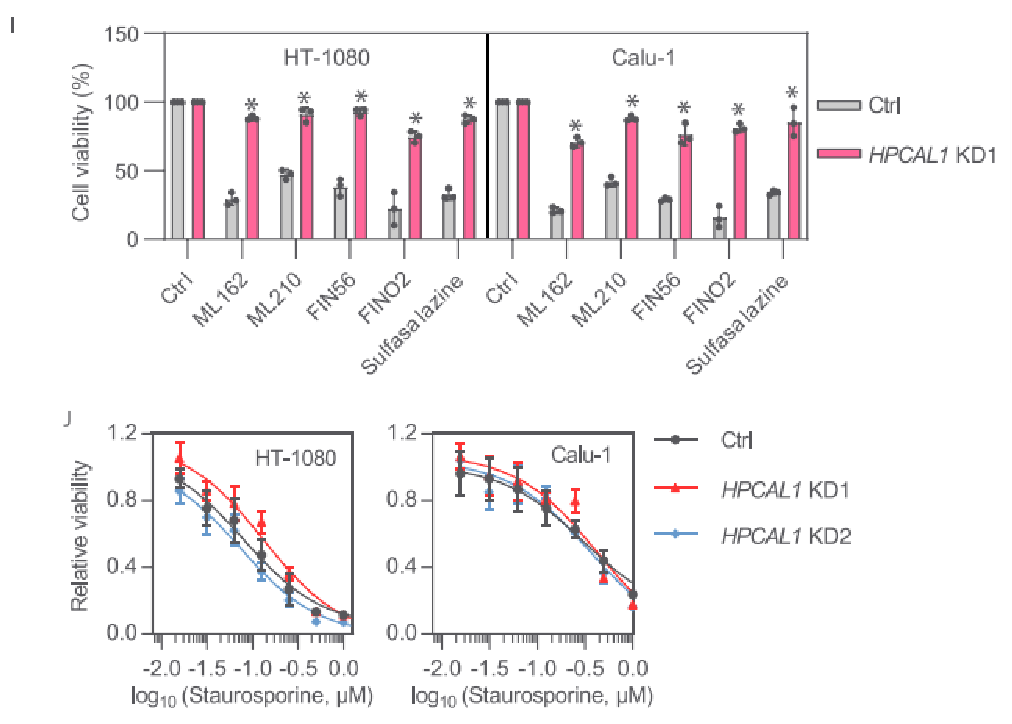
研究者隨后對HPCAL1進行過表達,過表達后細胞對鐵死亡誘導(dǎo)劑RSL3或erastin的處理更加敏感。此外,在HPCAL1敲低的細胞中重新穩(wěn)定過表達HPCAL1后,細胞恢復(fù)了對RSL3或erastin處理的敏感性,這種作用會被鐵死亡抑制劑liproxstatin-1抑制,而不受細胞凋亡抑制劑Z-VAD-FMK的影響。
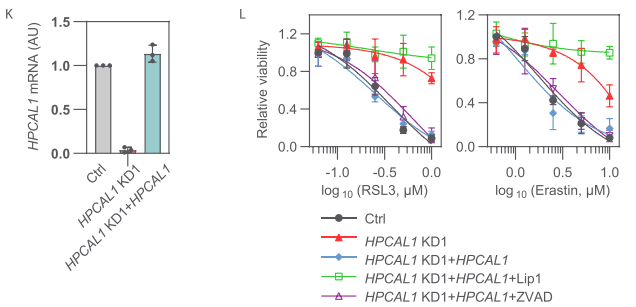
HPCAL1最開始是在視網(wǎng)膜和腦組織中被檢測到的,而該蛋白其實廣泛表達于各種組織和細胞中。研究者在其他種類的人癌細胞系中使用shRNA敲低HPCAL1,結(jié)果顯示HPCAL1敲低均可以抑制RSL3或erastin誘導(dǎo)的細胞死亡。綜合以上研究表明,HPCAL1介導(dǎo)廣泛的鐵死亡。
?2.?HPCAL1介導(dǎo)的CDH2抑制能促進鐵死亡
研究者進一步探索了HPCAL1促進鐵死亡的作用機制。首先,研究者通過實驗排除了鈣離子參與HPCAL1介導(dǎo)的鐵死亡以及HPCAL1在鐵死亡中催化脂質(zhì)通透性/氧化。隨后,研究者檢測HPCAL1是否與鐵死亡相關(guān)蛋白結(jié)合。通過HPCAL1的CO-IP MS實驗,共發(fā)現(xiàn)在RSL3處理和未處理的HT-1080和Calu-1細胞中,與HPCAL1結(jié)合的蛋白有600多個。GO功能富集分析顯示粘著斑和細胞-底物接合是最顯著富集的條目。
研究者關(guān)注其中一個在RSL3處理后與HPCAL1結(jié)合變化倍數(shù)最大的蛋白CDH2。隨后,研究者分別用RSL3(鐵死亡激活劑)和STS(細胞凋亡誘導(dǎo)劑)處理細胞,并進行CDH2的CO-IP。結(jié)果表明,在鐵死亡狀態(tài)下而非細胞凋亡狀態(tài)下,CDH2與HPCAL1的結(jié)合加強。該結(jié)果顯示了HPACAL1-CDH2復(fù)合體在鐵死亡中的特殊作用。
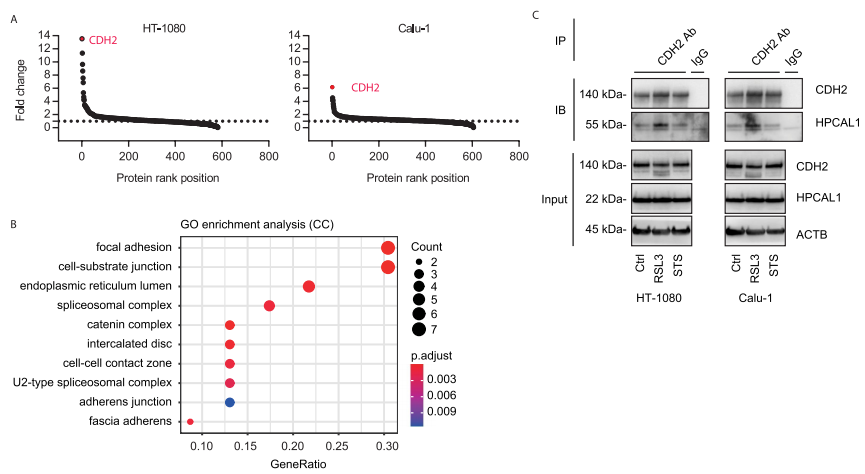
接下來的研究顯示,當(dāng)CDH2被敲低后,能恢復(fù)HPCAL1敲低細胞對RSL3或erastin的敏感性,而這種作用可以被鐵死亡抑制劑DFO而非細胞凋亡抑制劑Z-VAD-FMK逆轉(zhuǎn)。而在HPCAL1過表達的細胞中繼續(xù)過表達CDH2則會限制RSL3或erastin的細胞殺傷活性。綜合以上結(jié)果表明,HPCAL1通過劫持抗鐵死亡CDH2蛋白來促進鐵死亡。
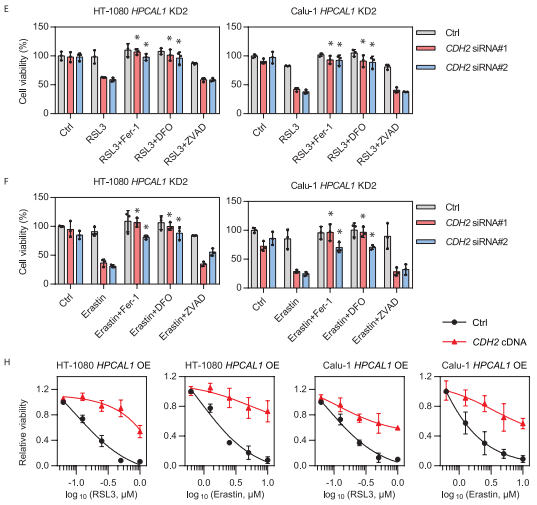
?3.?HPCAL1介導(dǎo)CDH2降解
緊接著研究者探究HPCAL1-CDH2復(fù)合體的形成是如何抑制CDH2的抗鐵死亡作用。首先發(fā)現(xiàn),在RSL3或erastin處理后,細胞中的CDH2蛋白表達顯著下調(diào),而細胞凋亡誘導(dǎo)劑STS則不影響CDH2的表達。研究者隨后明確,CDH2的降解是鐵死亡過程中的自噬介導(dǎo)的,在鐵死亡過程中自噬流增強。
自噬受體一般會將吞噬泡和自噬小體上的MAP1LC3B-II和要降解的目標分子進行連接,因此研究者檢測了HPCAL1和MAP1LC3B-II的膜脂質(zhì)定位。WB顯示在RSL3誘導(dǎo)的鐵死亡條件下,細胞膜組分中的HPCAL1和MAP1LC3B-II表達量均上升。HPCAL1可以與磷脂酰肌醇結(jié)合,這與此前報道的磷脂酰肌醇是自噬小體形成和成熟中關(guān)鍵的協(xié)調(diào)分子相一致。此外,CO-IP實驗也證實,在RSL3誘導(dǎo)的鐵死亡條件下,膜組分存在HPCAL1、CDH2和MAP1LC3B-II的結(jié)合。
下一步,研究者的實驗表明:(1)在鐵死亡中HPCAL1選擇性地介導(dǎo)CDH2蛋白的自噬降解。(2)HPCAL1上預(yù)測到的兩個LIR(LC3互作區(qū))motif :DEFFKKI (aa 46-51) 和AIYKMV (aa 127-132)。HPCAL1突變實驗表明, Δ127-132缺失不影響HPCAL1與LC3的結(jié)合,而Δ46-51缺失則影響HPCAL1與LC3的結(jié)合。此外,Δ46-51缺失抑制RSL3或erastin誘導(dǎo)的CDH2降解。
?4.?PRKCQ介導(dǎo)的HPCAL1磷酸化促進CDH2的降解
研究者繼續(xù)探索了HPCAL1磷酸化是否以及如何調(diào)控鐵死亡中的CDH2降解。研究者通過實驗初步確認PRKC(蛋白激酶C)的底物選擇性參與鐵死亡相關(guān)的自噬。隨后,研究者明確HPCAL1是PRKC的潛在底物。生信預(yù)測顯示,PRKC可能磷酸化HPCAL1 149位蘇氨酸(Thr)的磷酸化。功能實驗表明,過表達野生型HPCAL1(Thr149)增強CDH2降解,而過表達磷酸化突變(T149A,149位蘇氨酸突變?yōu)楸彼幔﹦t較少CDH2的降解。兩個PRKC抑制劑則抑制RSL3或erastin誘導(dǎo)的鐵死亡。以上結(jié)果表明,PRKC依賴的HPCAL1磷酸化介導(dǎo)了鐵死亡中CDH2的降解。此外,研究者的實驗表明,是PRKC家族中的PRKCQ Thr538的磷酸化使的PRKCQ激活,參與了鐵死亡。
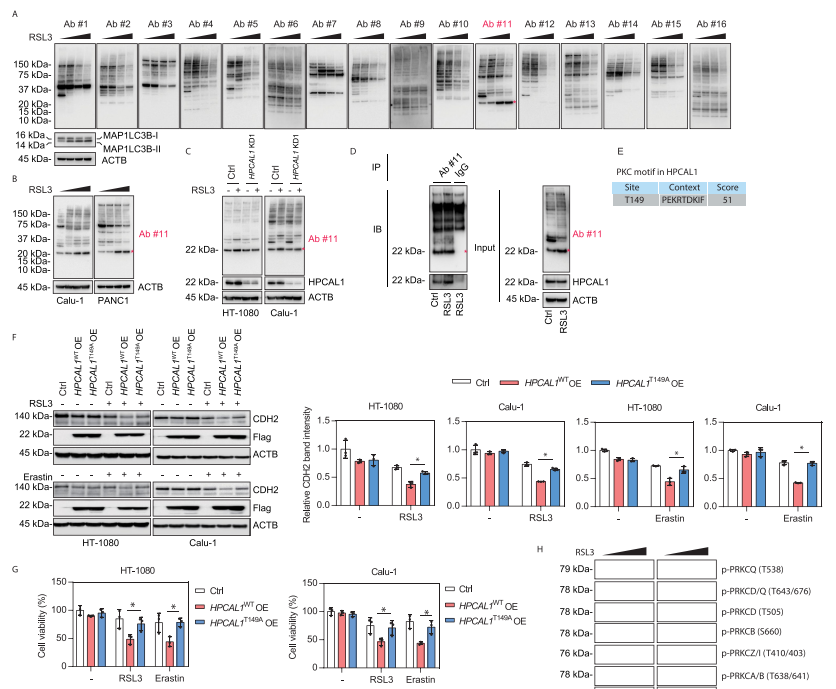
接下來,研究者檢測了PRKCQ在鐵死亡中的作用。結(jié)果表明,鐵死亡激活劑RSL3而非凋亡誘導(dǎo)劑STS能增強PRKCQ和HPCAL1的結(jié)合。PRKCQ敲低限制了RSL3或erastin誘導(dǎo)的癌細胞生長抑制。PRKCQ敲低保護細胞免受細胞死亡、脂質(zhì)過氧化和CDH2的自噬降解。此外,在細胞缺失HPCAL1和CDH2的情況下,敲低PRKCQ不影響細胞對鐵死亡敏感性。這表明,PRKCQ是鐵死亡的上游信號。
?5.?鑒定HPCAL1抑制劑(iHPCAL1)可作為鐵死亡的抑制劑
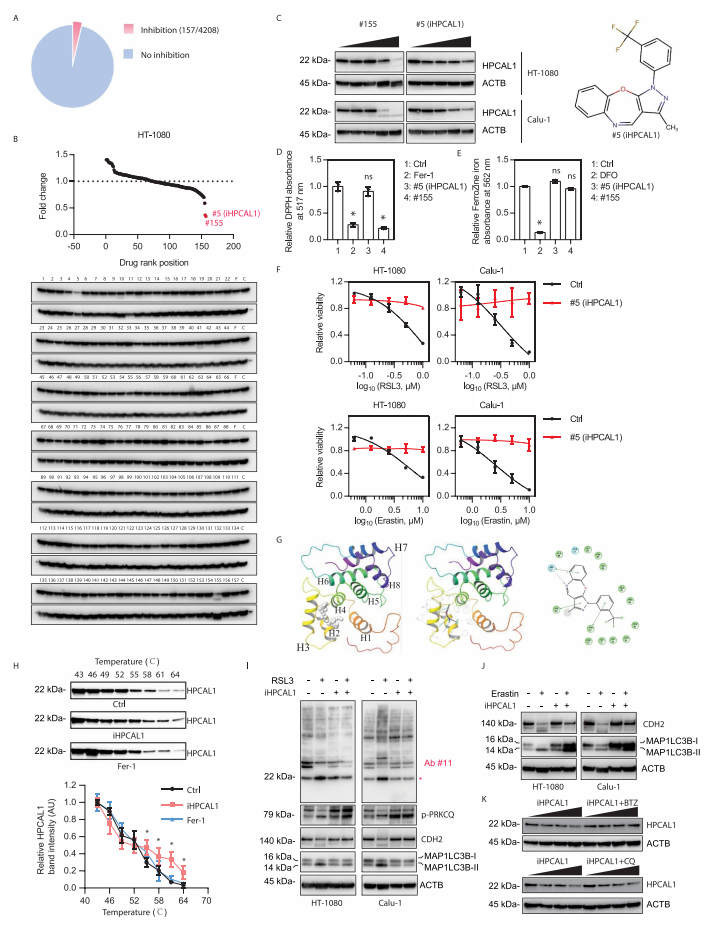
研究者從4208個無明確靶點的小分子中篩選新的HPCAL1抑制劑。實驗發(fā)現(xiàn),有157個化合物能抑制RSL3誘導(dǎo)的細胞死亡。接下來,研究者檢測這157個化合物中哪些可以降低HPCAL1的蛋白表達水平。結(jié)果發(fā)現(xiàn),#5和#155號化合物可以顯著抑制HPCAL1蛋白表達。隨后,研究者關(guān)注既不是抗氧化劑也無鐵螯合劑活性的#5號化合物,并將之命名為iHPCAL1。分子對接實驗(molecular docking assay)顯示iHPCAL1可以與HPCAL1結(jié)合。
細胞熱遷移分析(cellular thermal shift assay)證實iHPCAL1延緩熱誘導(dǎo)的HPCAL1蛋白降解,表明iHPCAL1直接與HPCAL1相互作用。功能分析表明iHPCAL1不能影響PRKCQ的磷酸化,但可以抑制HPCAL1的磷酸化以及RSL3或erastin誘導(dǎo)的CDH2的自噬降解。這些結(jié)果表明,iHPCAL1誘導(dǎo)的HPCAL1磷酸化和功能的抑制發(fā)生在PRKCQ 磷酸化的下游。隨后的研究表明硼替佐米(泛素-蛋白酶體抑制劑),而不是氯喹(自噬抑制劑),可以阻止iHPCAL1誘導(dǎo)的HPCAL1蛋白降解。這些結(jié)果表明iHPCAL1通過蛋白酶體途徑刺激HPCAL1的降解,從而限制了鐵死亡。
?6.?體內(nèi)實驗檢測HPCAL1介導(dǎo)的鐵死亡響應(yīng)
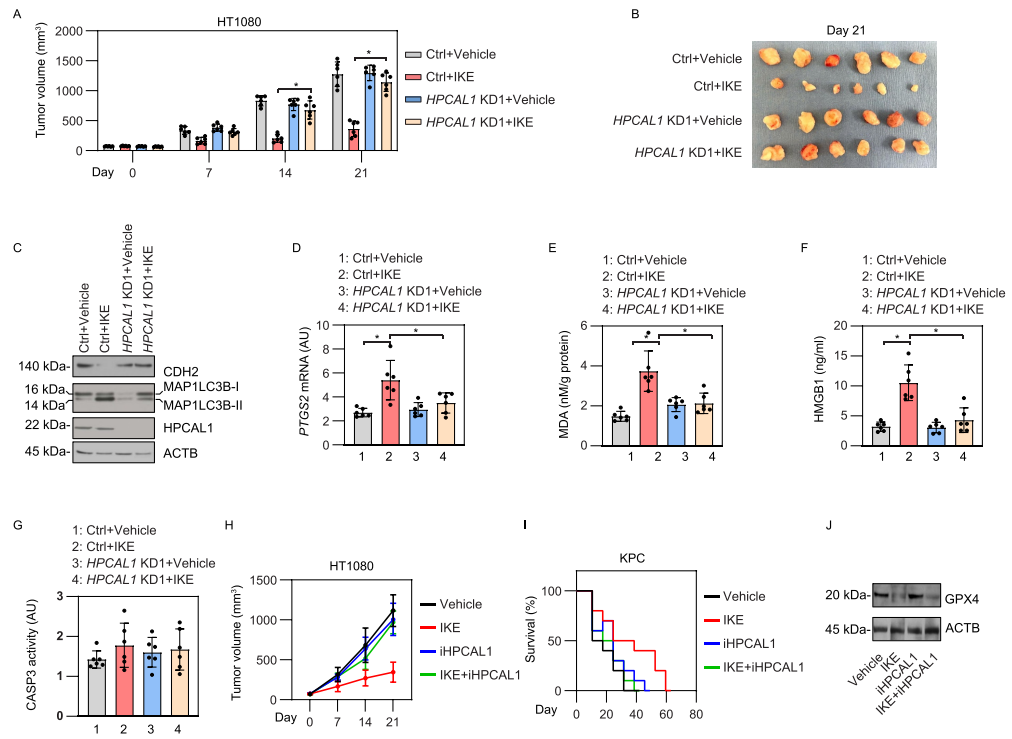
Imidazole ketone erastin (IKE)是一種具有更好效力和代謝穩(wěn)定性的erastin類似物,適用于在動物研究評估鐵死亡對腫瘤抑制的影響。研究者構(gòu)建了HPCAL1敲低的HT-1080癌細胞異種移植瘤裸鼠模型,并發(fā)現(xiàn)敲低HPCAL1限制了IKE的腫瘤抑制作用。HPCAL1敲低組與對照組相比,CDH2蛋白水平升高,而MAP1LC3B-II降低。鐵死亡生物標志物的定量結(jié)果以及血清中HMGB1的濃度進一步支持HPCAL1促進了IKE誘導(dǎo)的體內(nèi)鐵死亡的假設(shè)。同樣地,iHPCAL1在異種移植瘤模型中抑制IKE的抗癌活性,而對IKE誘導(dǎo)的GPX4降解無顯著影響。這些動物體內(nèi)研究與體外研究一致,表明HPCAL1是鐵死亡的正調(diào)節(jié)因子。
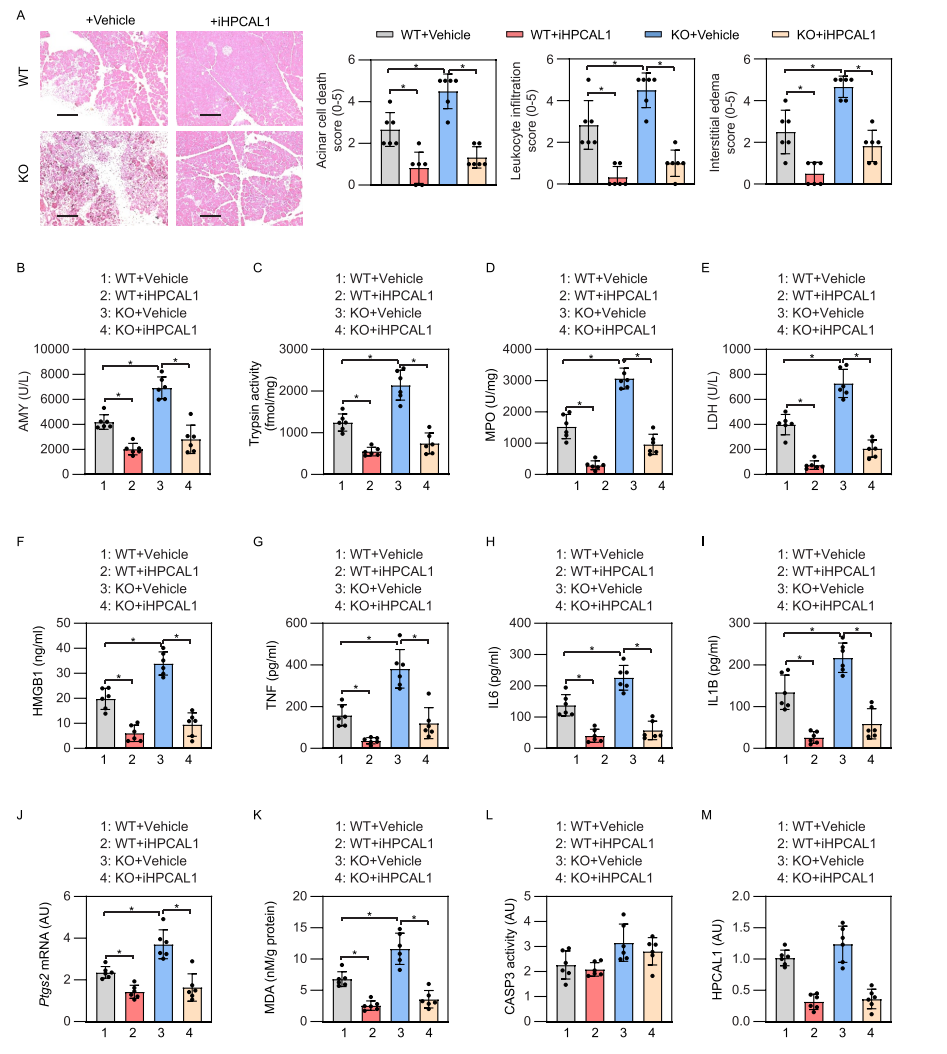
隨后,研究者利用蛙皮素(cerulein)誘導(dǎo)胰腺條件性敲除GPX4的小鼠發(fā)生急性胰腺炎,并檢測iHPCAL1是否有保護作用。結(jié)果顯示,iHPCAL1能很好地改善急性胰腺炎中的各項生化指標,具有顯著的保護作用。與預(yù)期一致,在使用iHPCAL1后,HPCAL1蛋白水平下調(diào)。綜合以上結(jié)果表明,HPCAL1參與了鐵死亡誘導(dǎo)的急性胰腺炎。
研究總結(jié)
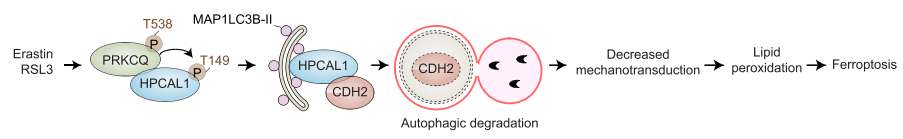
研究者利用定量蛋白質(zhì)組學(xué)篩選到了一個參與鐵死亡的膜蛋白HPCAL1。HPCAL1作為一種特異性自噬受體,在鐵死亡過程中選擇性降解CDH2(鈣粘蛋白2)。CDH2耗竭又進一步通過降低膜張力和促進脂質(zhì)過氧化而增加鐵死亡的易感性。深入的機制研究發(fā)現(xiàn),CDH2的自噬降解需要PRKCQ(蛋白激酶C theta)介導(dǎo)的HPCAL1在Thr149上的磷酸化,以及位于46-51位氨基酸之間的非經(jīng)典LC3互作區(qū)域motif。最后,研究者從4208個小分子化合物的藥物篩選中確定了一種抑制HPCAL1表達的鐵死亡抑制劑。在小鼠模型中,HPCAL1的抑制阻止了鐵死亡誘導(dǎo)的腫瘤抑制和胰腺炎。研究者的發(fā)現(xiàn)為自噬依賴細胞死亡的機制提供了見解,并為靶向HPCAL1以預(yù)防致病性鐵死亡提供了可能性。
吉凱基因憑借多年在靶標篩選及驗證服務(wù)領(lǐng)域的技術(shù)積累,建立的標準化 、工程化 、系統(tǒng)化的GRP平臺,為中國研究型醫(yī)生提供科研服務(wù),加快科研成果轉(zhuǎn)化。其中,多組學(xué)平臺包含蛋白質(zhì)組學(xué)平臺和高通量測序平臺:
·蛋白質(zhì)組學(xué)平臺擁有多臺timsTOF Pro、Exploris 480高精度質(zhì)譜儀,專業(yè)的Spectronaut Plusar、Mascot等分析軟件,提供專業(yè)的4D、DIA、TMT、PRM、磷酸化修飾組、olink蛋白質(zhì)組等檢測服務(wù),強大的機器學(xué)習(xí)算法、IPA分析、蛋白基因組分析服務(wù),系統(tǒng)的生物標志物、分子分型、藥物靶點、基因功能研究等解決方案,真正讓廣大研究型醫(yī)生的科研工作更省心、更省力、更高效;
·高通量測序平臺分為常規(guī)測序服務(wù)和單細胞測序服務(wù):單細胞測序擁有10x和BD兩個平臺,提供單細胞RNA-seq、單細胞核測序、單細胞混樣RNA-seq、單細胞TCR/BCR、單細胞(RNA+ATAC)、空間轉(zhuǎn)錄組測序等服務(wù);常規(guī)測序服務(wù)提供meRIP-seq(m6A/m1A/m7G/m5C 等RNA甲基化修飾測序)、acRIP-seq(ac4C RNA乙酰化修飾測序)、ATAC-seq、Ribo-seq(翻譯組測序) 、mRNA/miRNA/LncRNA/circRNA-seq、全轉(zhuǎn)錄組測序(兩文庫/三文庫)、外泌體miRNA/LncRNA-seq、WGS/WES、WGBS、RRBS、BSAS等服務(wù)。
