在作物研究、微生物學(xué)、藥物開發(fā)等場景的科研探索中,科研人員常常要解析DNA–蛋白質(zhì)的互作,以揭示基因調(diào)控網(wǎng)絡(luò)和表觀遺傳機制。然而,傳統(tǒng)DNA–蛋白質(zhì)互作技術(shù)總有“難以避免”的痛點:
1、ChIP-seq:耗時長,需要大量細胞樣本,且背景噪聲大,信噪比低,數(shù)據(jù)解析復(fù)雜。
2、傳統(tǒng)CUT&RUN:雖然靈敏度有所提升,但操作仍繁瑣,流程復(fù)雜,重復(fù)性和效率受限。
為了解決這些問題,近岸蛋白潛心研發(fā)出NEXT CUT&RUN(NovoNGS® NEXT CUT&RUN High-Sensitivity Kit (for Illumina®),Cat.No.: N359)——新一代精簡型CUT&RUN方案,讓DNA–蛋白互作分析更高效、更精準(zhǔn)、更輕松。
五大產(chǎn)品優(yōu)勢,專為高效科研設(shè)計
1、相比傳統(tǒng)CUT&RUN技術(shù),背景更低,信噪比大幅提升;
2、低至5000個細胞,操作簡單,僅需10 h;
3、融合pAG-Nuclease,一步實現(xiàn)靶標(biāo)識別和高效切割;
4、抗體單次實驗使用量低至0.1-0.5 μg,節(jié)省成本;
5、隨附建庫試劑,從靶標(biāo)捕獲到文庫構(gòu)建一套搞定。
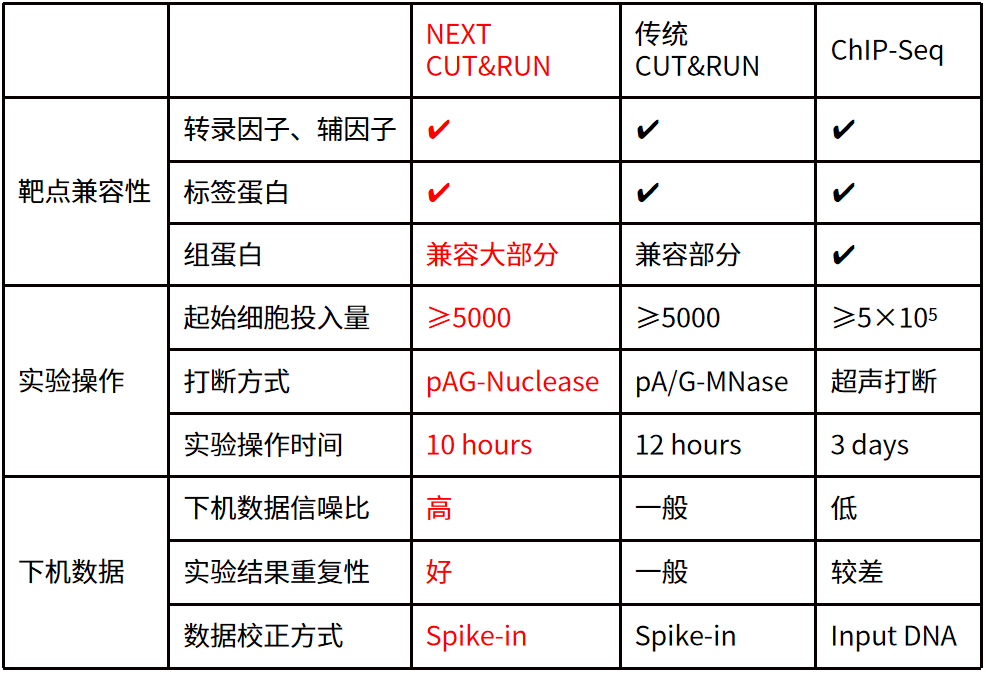
DNA/蛋白互作研究技術(shù)比對
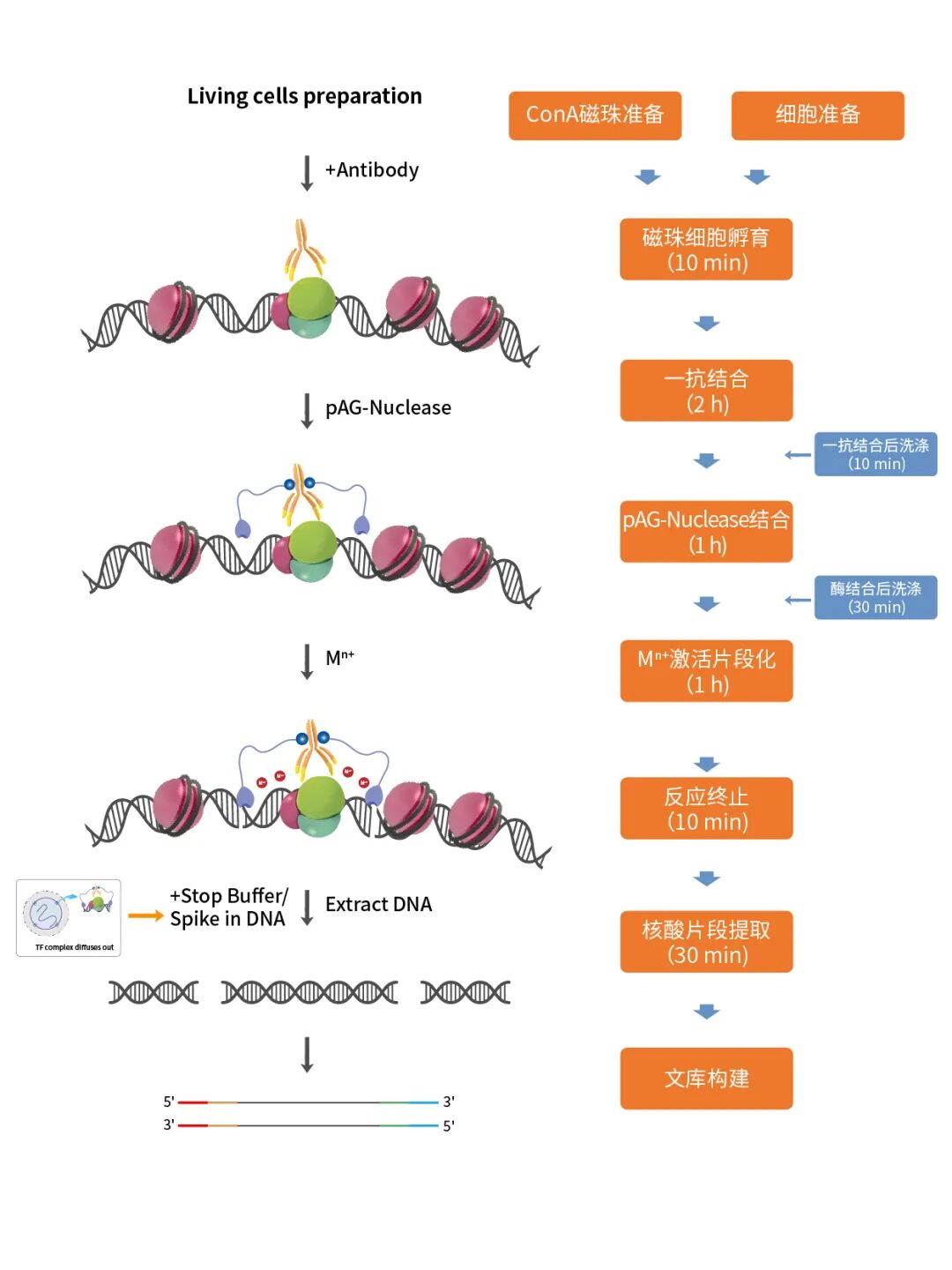
實驗流程圖
性能展示
1 NEXT CUT&RUN文庫構(gòu)建質(zhì)量高
轉(zhuǎn)錄因子研究:
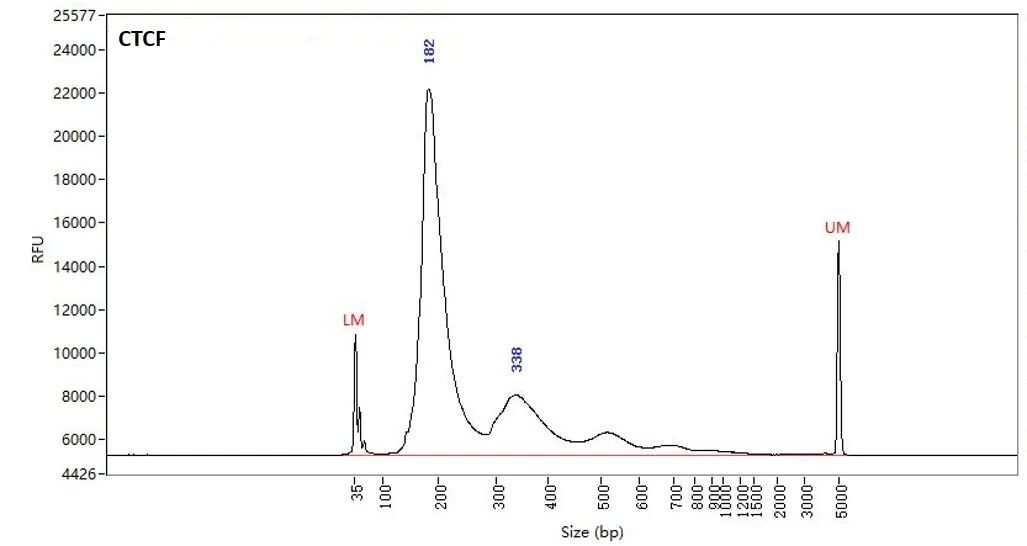
圖1. NEXT CUT&RUN試劑盒在100K K562細胞條件下進行CTCF CUT&RUN建庫。毛細管電泳結(jié)果顯示,文庫呈現(xiàn)典型的核小體周期分布,主峰180 bp以上,符合預(yù)期片段大小,表明文庫構(gòu)建成功且切割效率好,可用于后續(xù)高質(zhì)量測序分析。
組蛋白研究:
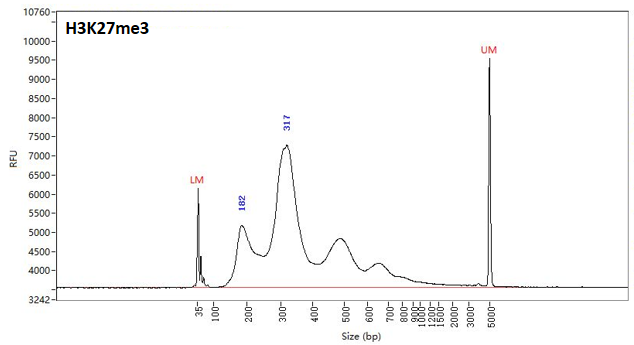
圖2. NEXT CUT&RUN試劑盒在100K K562細胞條件下進行H3K27me3 CUT&RUN建庫。文庫呈現(xiàn)典型的核小體周期分布,主峰約320 bp,符合預(yù)期片段大小,表明文庫構(gòu)建成功且切割效率好,可用于后續(xù)高質(zhì)量測序分析。
2 下機數(shù)據(jù)背景低,信噪比高
IGV數(shù)據(jù)分析:
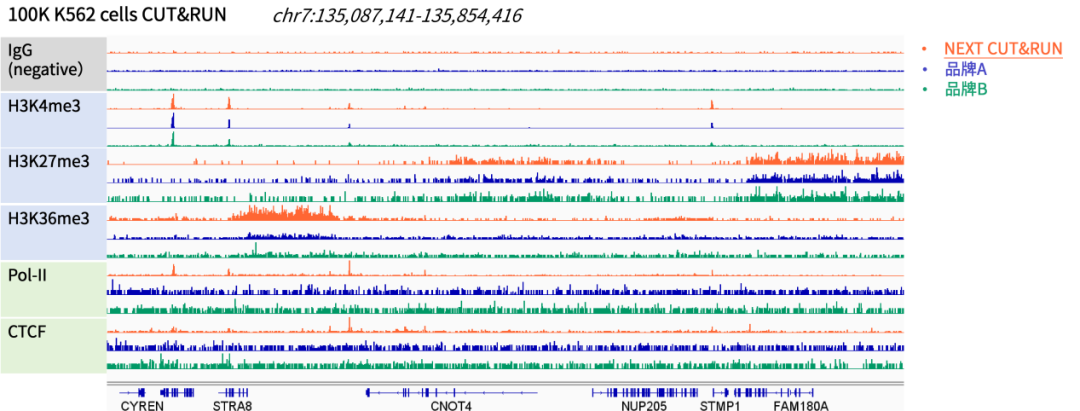
圖3. 以100K個K562細胞為樣本,使用不同品牌的CUT&RUN試劑盒對組蛋白修飾、DNA結(jié)合蛋白及轉(zhuǎn)錄因子進行檢測。IGV結(jié)果顯示,使用近岸蛋白NEXT CUT&RUN可在不同組蛋白、DNA結(jié)合蛋白和轉(zhuǎn)錄因子中獲得背景清晰,信噪比高的互作圖譜,且信噪比明顯優(yōu)于其他同類產(chǎn)品。
TSS富集分析:
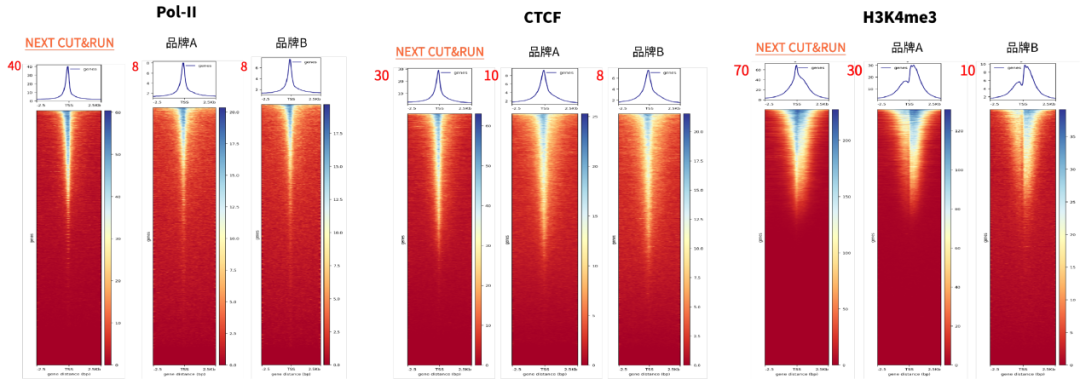
圖4. 以30K個K562細胞為樣本,使用不同品牌的CUT&RUN試劑盒對組蛋白修飾、DNA結(jié)合蛋白及轉(zhuǎn)錄因子進行檢測。通過TSS富集分析發(fā)現(xiàn),近岸蛋白NEXT CUT&RUN試劑盒獲得的TSS富集得分顯著高于其他同類產(chǎn)品,表現(xiàn)出更優(yōu)的信噪比。
3 NEXT CUT&RUN建庫所需樣本量少,僅需5000個細胞
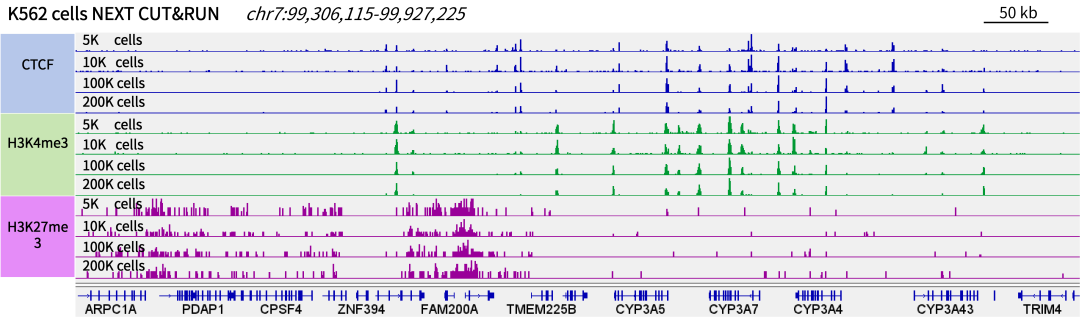
圖5. 以K562細胞為樣本,使用NEXT CUT&RUN在不同細胞數(shù)量條件下對組蛋白修飾及轉(zhuǎn)錄因子進行檢測。IGV結(jié)果顯示,僅需5000個細胞量也可獲得清晰、高質(zhì)量結(jié)果,且峰型與高細胞量條件保持一致。
4 NEXT CUT&RUN兼容不同類型細胞的互作研究
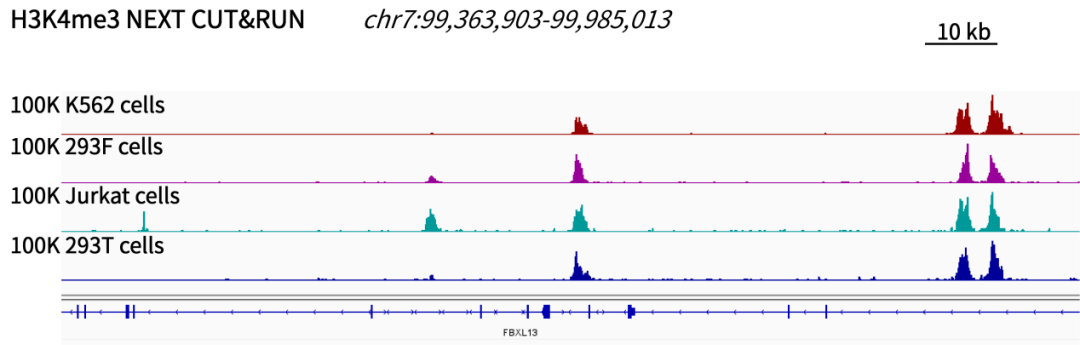
圖6. 使用NEXT CUT&RUN試劑盒對100K數(shù)量不同人源細胞進行H3K4me3抗體檢測,IGV結(jié)果顯示,四種不同來源的細胞均可以獲得高質(zhì)量的互作圖譜。
產(chǎn)品信息

如此高質(zhì)量的NEXT CUT&RUN試劑盒,你是否心動了?可以掃描下方二維碼申請樣品哦~數(shù)量有限,先到先得!

