126/science.1090521" style="color: rgb(0, 107, 180); text-decoration-line: none;">https://www.science.org/doi/10.1126/science.1090521
3. Biotechnology Industry Organization (BIO) analysis, 2012.
4. FDA, Innovation or stagnation: challenge and opportunity on the critical path to new medical technologies. March 2004.
5. Hellerstein, M.K. 2008. A critique of the molecular target-based drug discovery paradigm based on principles of metabolic control: advantages of pathway-based discovery. Metab Eng, 10(1), 1-9. https://doi.org/10.1016/j.ymben.2007.09.003
6. Hellerstein, M.K. 2003. In vivo measurement of fluxes through metabolic pathways: the missing link in functional genomics and pharmaceutical research. Annu Rev Nutr, 23, 379-402. https://doi.org/10.1146/annurev.nutr.23.011702.073045
7. Turner, S.M.; Hellerstein, M.K. 2005. Emerging applications of kinetic biomarkers in preclinical and clinical drug development. Curr Opin Drug Discov Devel, 8(1), 115-126. https://www.x-mol.com/paper/1212977911043006473?adv
8. Hellerstein, M.K. 2008. Exploiting complexity and the robustness of network architecture for drug discovery. J Pharmacol Exp Ther, 325(1), 1-9; https://doi.org/10.1124/jpet.107.131276
9. Shankaran, M.; King, C.; Lee, J.; et al. 2006. Discovery of novel hippocampal neurogenic agents by using an in vivo stable isotope labeling technique. J Pharmacol Exp Ther, 319(3), 1172-1181. https://doi.org/10.1124/jpet.106.110510
10. Fanara, P.; Wong, P.Y.; Husted, K.H.; et al. 2012. Cerebrospinal fluid-based kinetic biomarkers of axonal transport in monitoring neurodegeneration, J Clin Invest, 122(9), 3159-3169. https://www.jci.org/articles/view/64575
11. Potter, W.Z. 2012. Mining the secrets of the CSF: developing biomarkers of neurodegeneration. J Clin Invest, 122(9), 3051-3053. https://www.jci.org/articles/view/65309
12. Price, J.C.; Khambatta, C.F.; Li, K.W.; et al. 2012. The effect of long term calorie restriction on in vivo hepatic proteostatis: a novel combination of dynamic and quantitative proteomics. Mol Cell Proteomics, 11(12), 1801-1814. https://doi.org/10.1074/mcp.M112.021204
在新興的定制化醫(yī)療時(shí)代,穩(wěn)定同位素標(biāo)記與強(qiáng)大的質(zhì)譜分析技術(shù)的結(jié)合正在為藥物開(kāi)發(fā)和臨床診斷提供越來(lái)越重要的診斷工具。
問(wèn)題:當(dāng)代藥物開(kāi)發(fā)中的高流失率
雖然人們普遍認(rèn)為我們生活在一個(gè)新藥研發(fā)生產(chǎn)突破的黃金時(shí)代,但事實(shí)恰恰相反。近年來(lái),盡管制藥行業(yè)投資大幅增加,但新藥批準(zhǔn)率仍達(dá)到了一直以來(lái)的最低水平[1]。這些令人失望的情況適用于所有類別的疾病,但尤其令人擔(dān)憂的是日益流行的慢性疾病,如阿爾茨海默病、糖尿病、骨關(guān)節(jié)炎和肥胖相關(guān)疾病。這個(gè)問(wèn)題的出現(xiàn)不在于缺乏分子靶點(diǎn)或候選藥物。基于分子靶點(diǎn)的藥物發(fā)現(xiàn)方法在過(guò)去20年的藥物研究中占據(jù)主導(dǎo)地位,它產(chǎn)生了大量的基因、蛋白質(zhì)和潛在的藥物療法。問(wèn)題是藥物線索的減損率變得更糟,而不是更好,現(xiàn)在98%的線索由于療效或安全性原因而失效,包括人體試驗(yàn)中90%的失敗率[2,3]。這種減損在很大程度上導(dǎo)致了最終批準(zhǔn)的每一種成功藥物的高成本。
藥物復(fù)雜網(wǎng)絡(luò)中的難以預(yù)測(cè)性
藥物線索的減損,其主要原因是由生命系統(tǒng)組成的復(fù)雜網(wǎng)絡(luò)的不可預(yù)測(cè)性組成的,而這些網(wǎng)絡(luò)是對(duì)特定節(jié)點(diǎn)的針對(duì)性干預(yù)措施做出反應(yīng)的[2],在這些系統(tǒng)中,有針對(duì)性的干預(yù)措施會(huì)帶來(lái)意想不到的功能后果(可能是有害或者是有益的),這是非常常見(jiàn)的情況而非特例(圖1)。每種疾病中個(gè)體之間的致病異質(zhì)性放大了這一問(wèn)題,因此需要針對(duì)不同患者亞群采取不同的干預(yù)策略。后一個(gè)問(wèn)題體現(xiàn)在私人定制化醫(yī)療的理念上。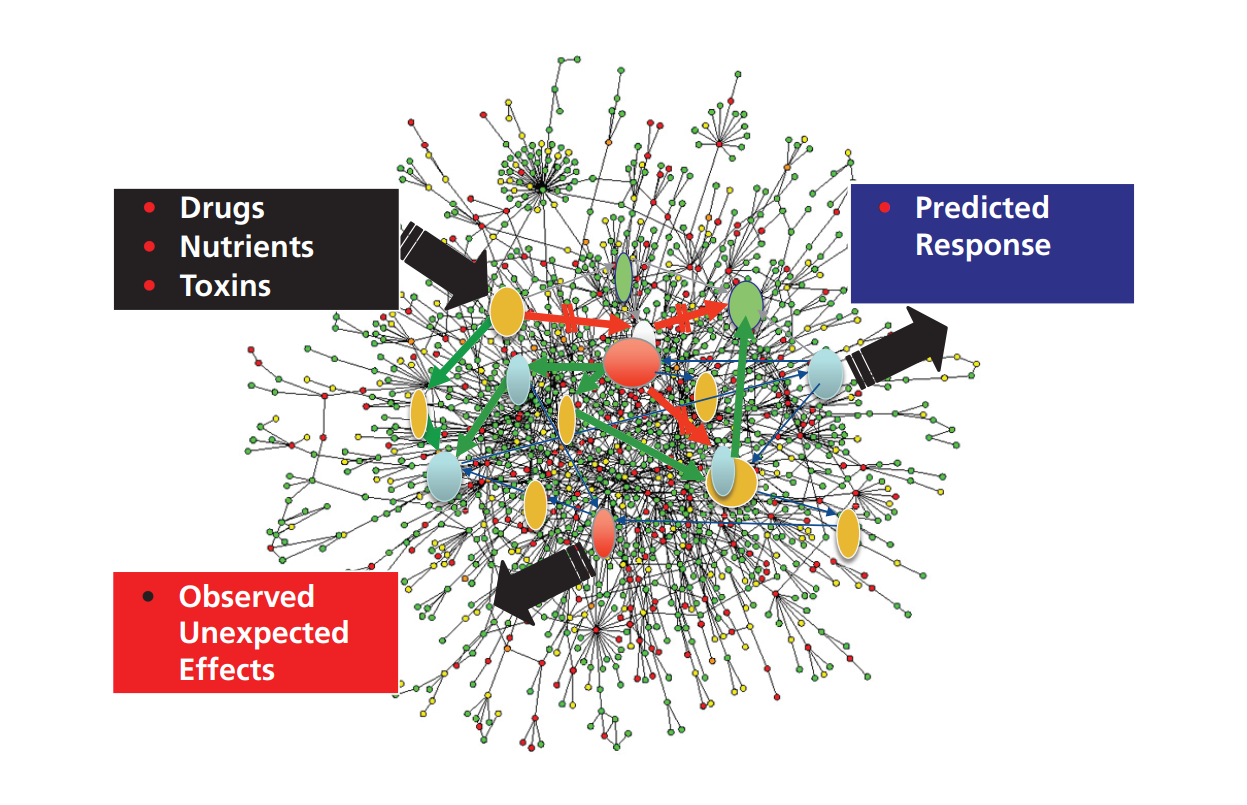
圖1:藥物復(fù)雜網(wǎng)絡(luò)中的難以預(yù)測(cè)性。
缺失的一環(huán):探索疾病復(fù)雜生物學(xué)的指標(biāo)
在了解疾病的復(fù)雜生物學(xué)過(guò)程中,關(guān)鍵缺失的因素是指導(dǎo)藥物研發(fā)人員朝著安全有效結(jié)局目標(biāo)前進(jìn)的客觀指標(biāo)[4]。這些指標(biāo)被稱為生物標(biāo)記物,必須能夠預(yù)測(cè)臨床結(jié)局,并且可以從臨床前模型轉(zhuǎn)化到人類。實(shí)現(xiàn)這些目標(biāo)的最可靠方法是捕獲驅(qū)動(dòng)每種疾病的基礎(chǔ)生物學(xué)過(guò)程(即疾病修飾通路或基礎(chǔ)發(fā)病機(jī)制)。這類指標(biāo)可用于指導(dǎo)合理的藥物發(fā)現(xiàn)和開(kāi)發(fā),并用于監(jiān)測(cè)臨床應(yīng)答情況。
“定制化醫(yī)學(xué)”領(lǐng)域?qū)δ苄畔⑸飿?biāo)記物的需求最大,即正確的患者、正確的藥物、正確的時(shí)間和正確的劑量。伴隨診斷檢查是這一趨勢(shì)的價(jià)值極高的例子。
穩(wěn)定性同位素對(duì)于一類新型生物標(biāo)記物至關(guān)重要:通過(guò)揭示基礎(chǔ)疾病過(guò)程的功能可解讀信息來(lái)預(yù)測(cè)臨床檢測(cè)的結(jié)果
我們需要能夠預(yù)測(cè)臨床結(jié)果的一類新型生物標(biāo)記物[4,5]。構(gòu)成慢性疾病基礎(chǔ)的生物學(xué)通路(負(fù)責(zé)疾病啟動(dòng)、進(jìn)展、嚴(yán)重程度和治療逆轉(zhuǎn)的因果過(guò)程)通常涉及分子流動(dòng),而這一通路本身復(fù)雜,且受到許多因素的影響(圖2)[5-8]。穩(wěn)定同位素技術(shù)已使所有這些因果通路在高等生物中可測(cè)量。
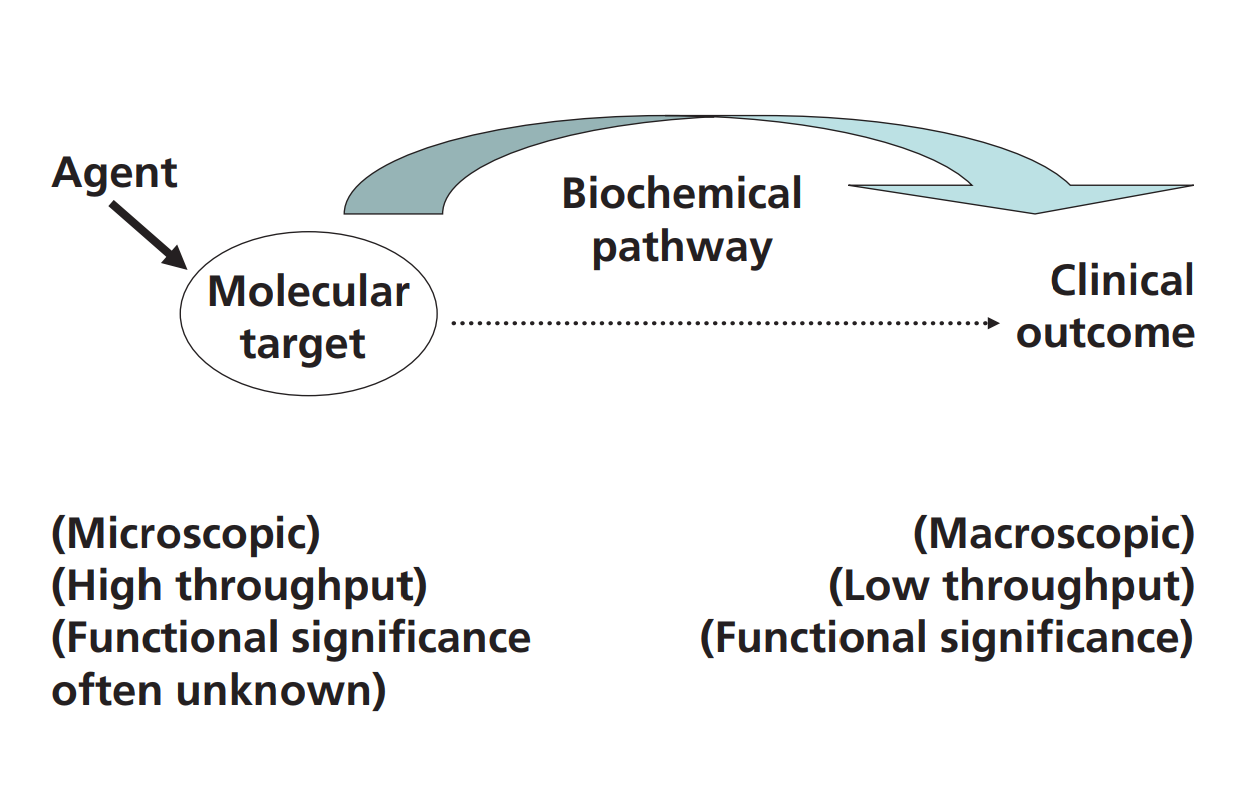
圖2:通路通量作為分子靶點(diǎn)和臨床結(jié)果之間的聯(lián)系。穩(wěn)定同位素為診斷生物標(biāo)記物帶來(lái)了什么
穩(wěn)定同位素允許測(cè)量通過(guò)代謝途徑的通量和全球生化網(wǎng)絡(luò)的動(dòng)態(tài),且無(wú)毒性,通常無(wú)創(chuàng),原因有二:第一,穩(wěn)定同位素的實(shí)驗(yàn)性施用在時(shí)間維度上引入了“不對(duì)稱”(本身沒(méi)有標(biāo)記,隨后加入標(biāo)記),這使得動(dòng)態(tài)過(guò)程耗費(fèi)的時(shí)間可以被測(cè)量;其次,過(guò)去一個(gè)世紀(jì)的生化研究已經(jīng)建立了連接細(xì)胞和生物體分子的途徑,使得標(biāo)記底物在體內(nèi)的運(yùn)動(dòng)行為得以被追蹤。
重要的是,穩(wěn)定同位素已經(jīng)在人類和實(shí)驗(yàn)動(dòng)物中使用了70多年,幾乎沒(méi)有已知的毒性。FDA對(duì)穩(wěn)定同位素標(biāo)記產(chǎn)品的政策是明確的,并且?guī)资陙?lái)一直是一致的:除了管理其天然豐度同系物(無(wú)菌性、無(wú)熱原性等)所需的審批之外,管理穩(wěn)定同位素標(biāo)記的化合物不需要任何監(jiān)管批準(zhǔn)。需要注意的是,穩(wěn)定同位素質(zhì)譜生物標(biāo)記物不是放射成像技術(shù),但需要來(lái)自身體的樣本(血液、尿液、腦脊液、組織、唾液)。
兩大類基于穩(wěn)定同位素的可用動(dòng)力學(xué)生物標(biāo)記物
有兩大類基于穩(wěn)定同位素的生物標(biāo)記物,它們?cè)谒幬镩_(kāi)發(fā)和診斷中是最有用的:(1)靶向因果途徑的動(dòng)力學(xué),以及(2)網(wǎng)絡(luò)動(dòng)力學(xué)的研究,以無(wú)偏倚地發(fā)現(xiàn)動(dòng)力學(xué)特征和其無(wú)法被預(yù)測(cè)的因果途徑。這兩種類型在藥物發(fā)現(xiàn)和開(kāi)發(fā)中都是有效的[5-15]。
作為藥物發(fā)現(xiàn)和開(kāi)發(fā)生物標(biāo)記物的靶向因果通路動(dòng)力學(xué)
表1列出了疾病致病途徑的一些常見(jiàn)例子。其中包括:纖維化疾病中膠原和細(xì)胞外基質(zhì)的合成;多發(fā)性硬化的髓鞘合成和代謝;阿爾茨海默病中淀粉樣斑塊的周轉(zhuǎn)和淀粉樣β1-42的合成;肌少癥患者肌肉肌球蛋白合成及線粒體生物發(fā)生的研究腫瘤血管生成與腫瘤細(xì)胞增殖和死亡;在神經(jīng)退行性疾病中通過(guò)軸突運(yùn)送分子;亨廷頓病、帕金森病和其他以蛋白質(zhì)聚集為特征的疾病中的自噬流;血栓栓塞性疾病中的凝塊形成和溶解;胰島素抵抗?fàn)顟B(tài)下胰島素介導(dǎo)的葡萄糖攝取與胰島β細(xì)胞增殖肥胖時(shí)脂肪組織脂質(zhì)動(dòng)力學(xué)及重塑;動(dòng)脈粥樣硬化中的膽固醇逆向轉(zhuǎn)運(yùn);炎癥狀態(tài)下補(bǔ)體級(jí)聯(lián)的激活;艾滋病患者的HIV復(fù)制和CD4+ T細(xì)胞的轉(zhuǎn)換等其他案例。
測(cè)量被認(rèn)為在疾病中起因果作用的任何功能相關(guān)過(guò)程的活動(dòng)的能力,對(duì)這些領(lǐng)域的藥物發(fā)現(xiàn)和開(kāi)發(fā)具有潛在的變革作用(如帕金森病)[10,11]。
A) 神經(jīng)生物學(xué) |
通過(guò)軸突進(jìn)行的遞送 | 淀粉樣β蛋白合成和斑塊周轉(zhuǎn) | 神經(jīng)發(fā)生 |
髓鞘形成/髓鞘再生 | 神經(jīng)遞質(zhì)釋放和周轉(zhuǎn) | 神經(jīng)元線粒體生物發(fā)生 |
神經(jīng)炎癥,小膠質(zhì)細(xì)胞的活化 | 細(xì)胞因子釋放 | 亨廷頓蛋白周轉(zhuǎn) |
朊病毒的周轉(zhuǎn) | 突觸可塑性 | |
B) 肥胖/II型糖尿病 |
胰腺β細(xì)胞增殖 | 胰島素介導(dǎo)的葡萄糖攝取 | 肝葡萄糖的生成 |
脂肪生成和TG沉積 | 脂肪組織重塑 | 脂肪組織脂肪酸氧化/棕色脂肪轉(zhuǎn)化 |
動(dòng)脈粥樣硬化、膽固醇清除和沉積 | 脂肪組織巨噬細(xì)胞增殖和活化 | 肌肉線粒體β-氧化和生物發(fā)生 |
肝臟TG的合成與釋放 | | |
C) 癌癥/腫瘤形成 |
腫瘤細(xì)胞增殖和死亡率 | 血管新生 | 淋巴管生成/轉(zhuǎn)移擴(kuò)散 |
DNA甲基化/脫甲基 | 核糖核苷酸還原酶活性 | 組蛋白去乙酰化 |
癌前進(jìn)化到侵襲性表型 | 腫瘤特異性T細(xì)胞增殖 | 細(xì)胞外基質(zhì)轉(zhuǎn)換 |
表1:因果途徑的例子
網(wǎng)絡(luò)動(dòng)力學(xué)探究
也許近年來(lái)穩(wěn)定同位素生物標(biāo)記最令人興奮的進(jìn)展是“網(wǎng)絡(luò)動(dòng)力學(xué)”的出現(xiàn):對(duì)構(gòu)成生命系統(tǒng)的復(fù)雜生化網(wǎng)絡(luò)的動(dòng)態(tài)行為進(jìn)行全面的探究。這已經(jīng)成功地應(yīng)用于臨床前模型和人類的全球蛋白質(zhì)組動(dòng)力學(xué)或動(dòng)態(tài)蛋白質(zhì)組學(xué)[12,13]。這提供了一種新型的系統(tǒng)生物學(xué),作為生物標(biāo)記物發(fā)現(xiàn)的無(wú)偏倚篩選工具具有巨大的潛力。
動(dòng)態(tài)蛋白質(zhì)組學(xué)代表了“組學(xué)”技術(shù)中功能上最可解釋的技術(shù),不僅提供熱圖或信息學(xué),而且提供功能上可解釋的系統(tǒng)生物學(xué)信息。圖3顯示了測(cè)量蛋白質(zhì)組動(dòng)態(tài)的操作流程圖。該方法已成功應(yīng)用于以下場(chǎng)景,如熱量限制對(duì)細(xì)胞蛋白穩(wěn)態(tài)的影響,包括線粒體生物發(fā)生和線粒體自噬;慢性淋巴細(xì)胞白血病腫瘤細(xì)胞不良預(yù)后的蛋白質(zhì)組動(dòng)力學(xué)特征區(qū)分成功補(bǔ)償肥胖動(dòng)物胰島素抵抗的胰島和衰竭并變得“疲憊”的胰島;運(yùn)動(dòng)對(duì)肌肉蛋白質(zhì)組轉(zhuǎn)換的影響神經(jīng)炎癥對(duì)腦脊液蛋白質(zhì)組周轉(zhuǎn)的影響;血脂異常狀態(tài)下高密度脂蛋白(HDL)蛋白質(zhì)組的動(dòng)態(tài)變化;以及生理學(xué)和病理生理學(xué)中的其他問(wèn)題。
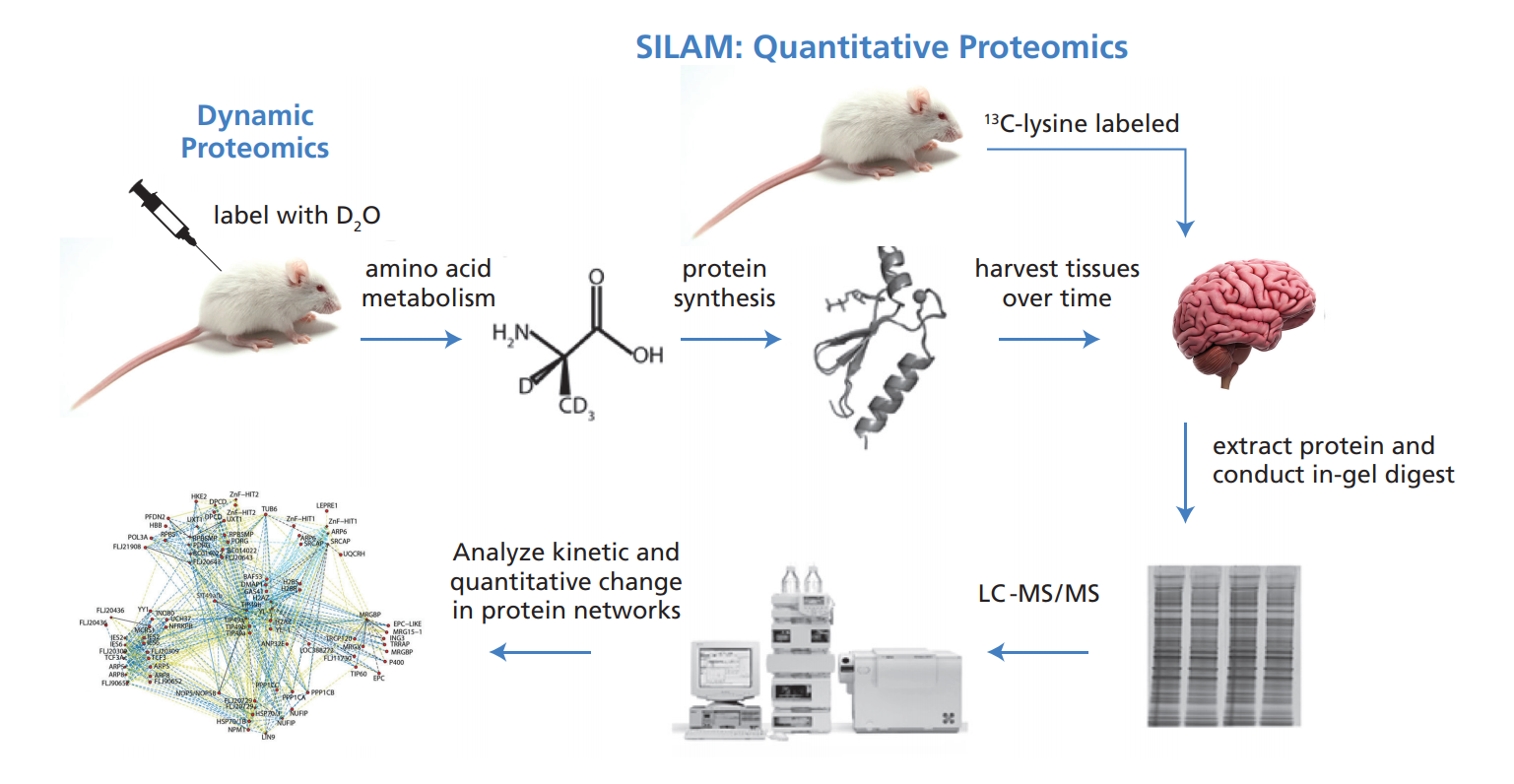
圖3:動(dòng)態(tài)蛋白質(zhì)組學(xué):在體內(nèi)通過(guò)穩(wěn)定同位素標(biāo)記測(cè)量蛋白質(zhì)組動(dòng)力學(xué)和濃度。
用于細(xì)胞內(nèi)通路非侵入性生物標(biāo)記物的“虛擬活檢”方法
組織中蛋白質(zhì)組動(dòng)力學(xué)的無(wú)偏篩選也可以導(dǎo)致發(fā)現(xiàn)可在體液中采樣的靶向蛋白質(zhì)生物標(biāo)記物。被稱為“虛擬活檢”技術(shù)(圖4),這是一種強(qiáng)大的方法,用于測(cè)量難以接近的原始組織(如骨骼肌、心臟、大腦、腎臟、肝臟或癌癥組織)中蛋白質(zhì)合成或蛋白質(zhì)分解的速率,通過(guò)測(cè)量可接近的體液(如血液、腦脊液、唾液或尿液)。該方法包括給藥穩(wěn)定同位素示蹤劑(例如,氧化氘(D, 70%);L-亮氨酸(13C6, 99%);甘氨酸(15N, 98%);螺旋藻全細(xì)胞(凍干粉)(U-15N, 98%),代謝并入新合成的蛋白質(zhì)。然后這些蛋白質(zhì)逃逸到可接觸的體液中,從中分離并分析同位素含量或模式。所測(cè)量的逃逸蛋白的替換率反映了蛋白質(zhì)在原始組織中的合成或分解率。因此,可以稱作是對(duì)原始組織進(jìn)行了“虛擬活檢”。
虛擬活檢方法可用于發(fā)現(xiàn)和驗(yàn)證生物標(biāo)記物,用于藥物發(fā)現(xiàn)和開(kāi)發(fā)、識(shí)別個(gè)性化醫(yī)療中的疾病子集,以及患者的臨床診斷和管理。這種方法已被開(kāi)發(fā)并應(yīng)用于基于血液的組織纖維化和骨骼肌蛋白合成測(cè)量,以及基于CSF的軸突運(yùn)輸和神經(jīng)炎癥測(cè)量[10]。一個(gè)例子是血漿肌酸激酶MM(來(lái)源于骨骼肌),用于從血液測(cè)試中測(cè)量骨骼肌蛋白合成代謝。還有許多其他的應(yīng)用可以設(shè)想。
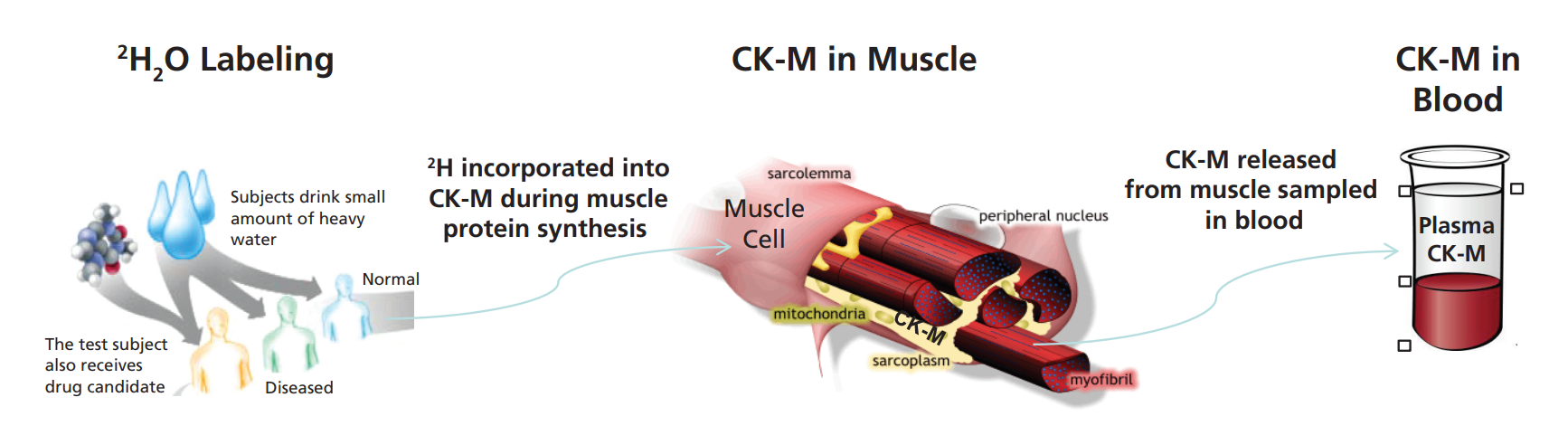
圖4:動(dòng)態(tài)生物標(biāo)記物的“虛擬活檢”技術(shù)。從血漿肌酸激酶M型(CK-M)合成骨骼肌蛋白的案例
原位動(dòng)力學(xué)組織化學(xué):結(jié)合組織病理學(xué)與穩(wěn)定同位素和質(zhì)譜
現(xiàn)在也有可能在組織病理學(xué)標(biāo)本中,在空間上可視化感興趣的目標(biāo)分子的動(dòng)力學(xué)[14]。將空間組織學(xué)信息與分子通量率聯(lián)系起來(lái),為病理診斷和疾病監(jiān)測(cè)提供了一個(gè)顯著的新維度,這可以通過(guò)激光顯微解剖或物理顯微切片來(lái)實(shí)現(xiàn)(圖5)。在前列腺癌中引入穩(wěn)定同位素后組織顯微解剖的例子已經(jīng)發(fā)表。例如,前列腺細(xì)胞的增殖梯度已被證明與前列腺癌患者活檢標(biāo)本的組織
學(xué)分級(jí)密切相關(guān),并通過(guò)從精液中分離的前列腺上皮細(xì)胞的增殖率反映出來(lái),作為一種潛在的非侵入性生物標(biāo)記物[14]。
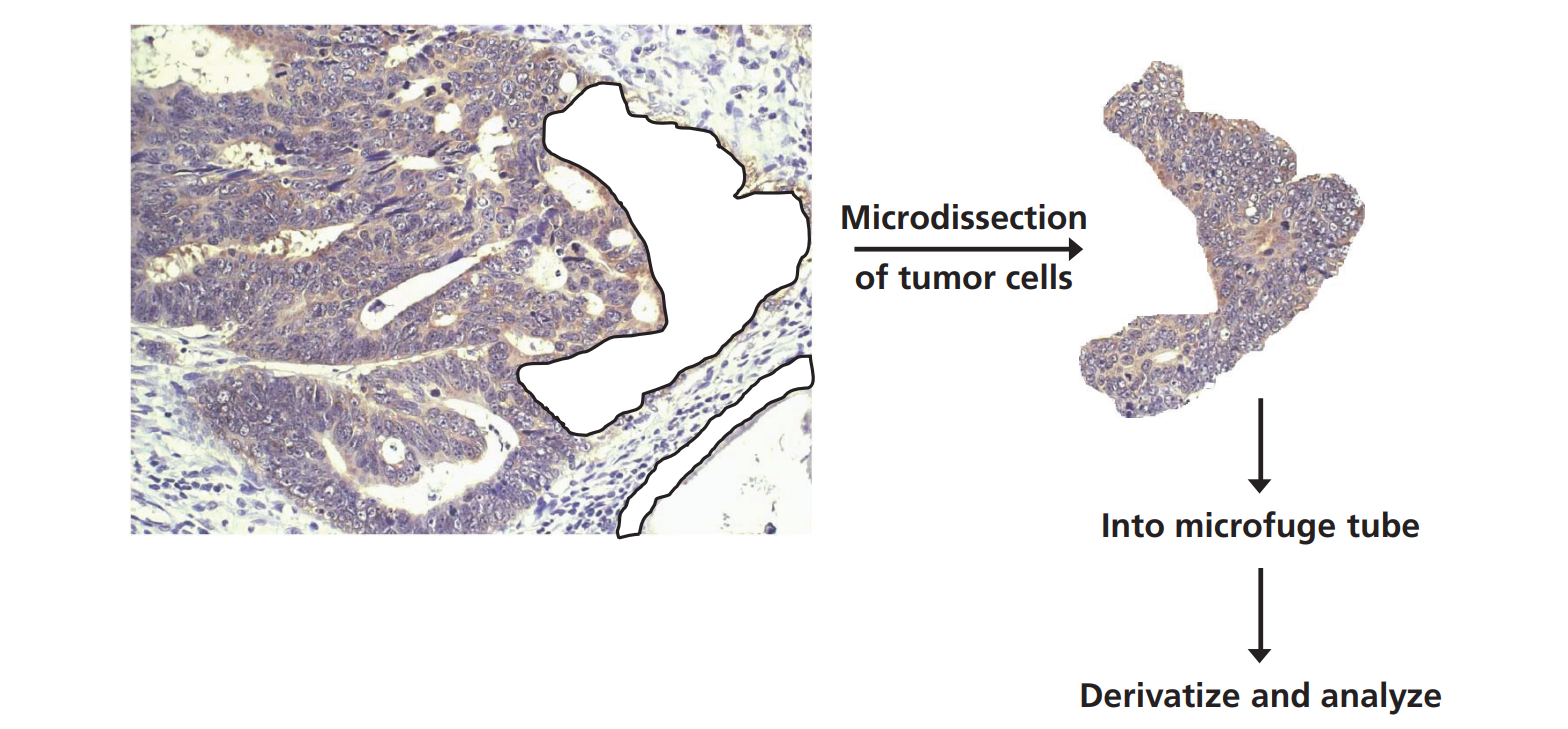
圖5:用于質(zhì)譜動(dòng)力學(xué)分析的正常和腫瘤組織的顯微解剖。
組織樣本的動(dòng)力學(xué)成像
通過(guò)將穩(wěn)定同位素標(biāo)記與組織質(zhì)譜成像相結(jié)合,通過(guò)基于NIMS或MALDI的組織切片空間可視化,現(xiàn)在可以實(shí)現(xiàn)動(dòng)力學(xué)或代謝通量成像。腫瘤模型中空間定義的動(dòng)力學(xué)脂質(zhì)組學(xué)揭示了小鼠乳腺癌模型中與體內(nèi)侵襲性相關(guān)的腫瘤行為的解剖學(xué)差異[15]。
穩(wěn)定同位素生物標(biāo)記物在藥物開(kāi)發(fā)中的實(shí)際應(yīng)用
基于同位素的穩(wěn)定生物標(biāo)記物在藥物發(fā)現(xiàn)和開(kāi)發(fā)中有許多用途(表2)。將臨床前研究結(jié)果迅速轉(zhuǎn)化進(jìn)行人體實(shí)驗(yàn);“快速殺傷”的代理或類對(duì)目標(biāo)路徑的活性差;確定適當(dāng)?shù)幕颊邅喨哼M(jìn)行治療;確定最佳劑量、狀態(tài)、測(cè)量終點(diǎn)和受試者間反應(yīng)變異性;醫(yī)療個(gè)性化(伴隨診斷);通過(guò)調(diào)整劑量來(lái)預(yù)測(cè)毒性或避免毒性。可預(yù)測(cè)疾病結(jié)果的轉(zhuǎn)譯標(biāo)記物還允許選擇最能反映人類疾病的動(dòng)物模型,或者從藥物開(kāi)發(fā)過(guò)程中減少甚至逐漸消除動(dòng)物模型。
減少推測(cè)過(guò)程: |
1. 選擇目標(biāo); |
2. 選擇化學(xué)類別及類別中最佳化合物; |
3. 確定合適的受試者(排除有毒性風(fēng)險(xiǎn)的無(wú)反應(yīng)亞群); |
4. 為臨床試驗(yàn)尋找最佳劑量和方案; |
5. 在患者中選擇終點(diǎn)進(jìn)行測(cè)量和預(yù)期的變異性; |
6. 給藥以最大限度地減少毒性; |
7. 測(cè)試個(gè)性化調(diào)整是否能改善反應(yīng); |
8. 決定是否提前退出(快速殺傷)。 |
表2:因果路徑指標(biāo)的應(yīng)用
基于穩(wěn)定同位素的動(dòng)態(tài)生物標(biāo)記物與靜態(tài)生物標(biāo)記物相比具有優(yōu)勢(shì),同時(shí)具有補(bǔ)充作用
傳統(tǒng)的靜態(tài)生物標(biāo)記提供了有關(guān)生命系統(tǒng)中分子的濃度、存在或結(jié)構(gòu)的信息。相比之下,動(dòng)力學(xué)生物標(biāo)記物揭示了通向和離開(kāi)這些分子的途徑的動(dòng)態(tài)行為。例如,組織中膠原蛋白的數(shù)量并不能顯示在疾病環(huán)境中或開(kāi)始治療干預(yù)后膠原蛋白合成(成纖維)的速度。線粒體蛋白質(zhì)的含量也沒(méi)有告訴我們線粒體生物發(fā)生或線粒體自噬是由干預(yù)引起的程度。同樣,腦脊液中蛋白質(zhì)的濃度也能告訴我們大腦神經(jīng)元將這種分子通過(guò)軸突運(yùn)送到神經(jīng)末梢的效率。后一種過(guò)程的核心都是分子通過(guò)復(fù)雜的途徑和網(wǎng)絡(luò)流動(dòng)。
這些致病過(guò)程或疾病途徑的活性原則上是與疾病的發(fā)生、嚴(yán)重程度、進(jìn)展和治療逆轉(zhuǎn)最密切相關(guān)的指標(biāo)。如上所述,測(cè)量分子通量速率的唯一方法是引入同位素標(biāo)簽。雖然靜態(tài)參數(shù)可以提供關(guān)鍵的補(bǔ)充信息,如池大小和分子組分的凈增益或損失,但只能通過(guò)動(dòng)力學(xué)測(cè)量來(lái)揭示潛在致病過(guò)程的功能活性。
與靜態(tài)“組學(xué)”生物標(biāo)記物相比,同樣的考慮適用于“網(wǎng)絡(luò)動(dòng)力學(xué)”,如動(dòng)態(tài)蛋白質(zhì)組學(xué),但有一個(gè)額外的點(diǎn)值得注意。蛋白質(zhì)的合成和分解速率通常代表細(xì)胞或有機(jī)體的主動(dòng)決定,在健康或疾病的背景下,這種決定在功能上是可解釋的。以蛋白質(zhì)為例,基于泛素蛋白組的去除,轉(zhuǎn)錄因子刺激的合成,細(xì)胞器生物發(fā)生過(guò)程中的組裝,囊泡中的包裝和分泌,通過(guò)未折疊蛋白反應(yīng)的調(diào)節(jié),作為細(xì)胞外基質(zhì)的沉積,作為蛋白質(zhì)信號(hào)級(jí)聯(lián)的一部分的誘導(dǎo)等等,這些都可以被生理學(xué)家、毒理學(xué)家和臨床醫(yī)生從功能角度考慮。對(duì)于蛋白質(zhì)的簡(jiǎn)單存在或濃度并不總是如此。由于內(nèi)在功能意義和廣泛、無(wú)假設(shè)篩選之間的結(jié)合,動(dòng)態(tài)蛋白質(zhì)組學(xué)是一種特別強(qiáng)大的生物標(biāo)記物和靶標(biāo)發(fā)現(xiàn)技術(shù)。
小結(jié)
總之,將基于穩(wěn)定同位素的生物標(biāo)記物添加到診斷庫(kù)中,為藥物開(kāi)發(fā)帶來(lái)了一個(gè)新的和迅速擴(kuò)大的維度。這些生物標(biāo)記物提供了關(guān)于疾病基礎(chǔ)生物學(xué)的功能可解釋的決策相關(guān)信息,捕捉了驅(qū)動(dòng)疾病和治療的因果途徑的活動(dòng)。因此,動(dòng)力學(xué)生物標(biāo)記物可預(yù)測(cè)臨床應(yīng)答及其與靶點(diǎn)接觸或臨床治療方案效果的關(guān)系。穩(wěn)定的基于同位素的動(dòng)力學(xué)生物標(biāo)記物在個(gè)性化醫(yī)學(xué)的新興時(shí)代是特別強(qiáng)大的補(bǔ)充。參考文獻(xiàn)
1. Swann, J.P. 2011. Summary of NDA Approvals & Receipts, 1938 to the present, FDA History Office, http://www.fda.gov/AboutFDA/WhatWeDo/History.
2. Duyk, G. 2003. Attrition and translation. Science, 302(5645), 603-605.
地 址: 上海市新金橋路36號(hào)財(cái)富中心16樓
聯(lián)系人: 阿博士
電 話: 400-620-6333
傳 真: 021-50323701
Email:market@aladdin-e.com






