雖然代謝最初被認(rèn)為在細(xì)胞生物學(xué)中起被動(dòng)作用,通過產(chǎn)生ATP來(lái)滿足生物能量需求,除產(chǎn)生ATP外,代謝為磷脂、氨基酸和核苷酸合成提供碳前體以維持細(xì)胞分裂,最近研究還證實(shí)代謝在新物質(zhì)生成和為組蛋白和DNA表觀遺傳修飾提供專屬性底物方面具有關(guān)鍵作用。本綜述詳細(xì)介紹了糖酵解和三羧酸循環(huán)產(chǎn)生的代謝物是如何被成體干細(xì)胞用來(lái)維持細(xì)胞增殖,及成體干細(xì)胞如何整合外部代謝和內(nèi)在代謝機(jī)制來(lái)調(diào)節(jié)細(xì)胞命運(yùn),相關(guān)成果發(fā)表于《Cell Metabolism》。
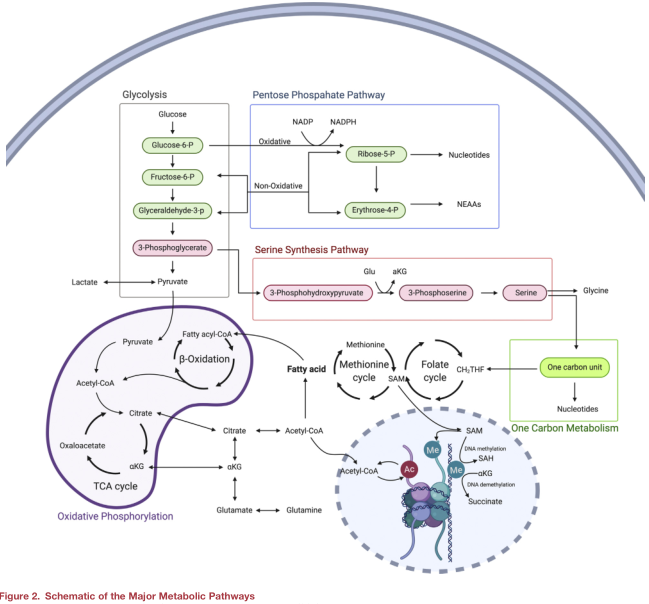
細(xì)胞中ATP的兩個(gè)主要來(lái)源是糖酵解和氧化磷酸化(OxPhos)。糖酵解是一個(gè)快速的過程,可以將單個(gè)葡萄糖分子轉(zhuǎn)化為兩分子丙酮酸,凈獲得兩個(gè)ATP。糖酵解產(chǎn)生的丙酮酸會(huì)以兩種方式進(jìn)一步代謝,一種方式是丙酮酸轉(zhuǎn)化為乳酸并從細(xì)胞中排出,另一種方式是在氧氣充足的條件下,丙酮酸運(yùn)輸?shù)骄€粒體中并被氧化成乙酰輔酶A進(jìn)入三羧酸(TCA)循環(huán)和驅(qū)動(dòng)OxPhos。除了葡萄糖生成的丙酮酸發(fā)揮作用外,乙酰輔酶A可以通過脂肪酰輔酶A的β氧化提供豐富但緩慢的ATP。盡管OxPhos能量效率較高,但許多高度增殖的細(xì)胞類型如癌細(xì)胞都優(yōu)先利用糖酵解。這種對(duì)糖酵解的偏好最早由Otto Warburg教授發(fā)現(xiàn),并提出腫瘤發(fā)生是由線粒體功能缺陷導(dǎo)致對(duì)糖酵解的依賴增加而誘導(dǎo)的。但這種被稱為需氧糖酵解方式后來(lái)被證明不是由于OxPhos缺陷引起的,而是細(xì)胞對(duì)新的生物量如磷脂、核苷酸和氨基酸的需要所驅(qū)動(dòng)。重要的是,這種生物量大部分是通過糖酵解及其相互連接的旁路途徑即磷酸戊糖途徑和絲氨酸生物合成途徑產(chǎn)生。
磷酸戊糖途徑(PPP)是一個(gè)完整的系列反應(yīng),在生物合成和氧化還原反應(yīng)中起重要作用。PPP又分為氧化途徑和非氧化途徑,氧化途徑負(fù)責(zé)將6-磷酸葡萄糖(G6P)分解為二氧化碳、5-磷酸核酮糖和兩分子NADPH。生成的NADPH是維持細(xì)胞氧化還原狀態(tài)的強(qiáng)還原劑。非氧化途徑中,6-磷酸-果糖(F6P)和3-磷酸-甘油(G3P)被代謝成5-磷酸-核糖和4-磷酸-赤蘚糖。4-磷酸赤蘚糖可作為芳香族氨基酸(如組氨酸)合成前體。重要的是,PPP分支中產(chǎn)生的5-磷酸-核糖是用于合成嘌呤和嘧啶核苷酸的糖主體。有趣的是,PPP氧化途徑產(chǎn)生的5-磷酸-核酮糖也可以通過核糖-5-磷酸異構(gòu)酶(RPI)轉(zhuǎn)化為5-磷酸核糖進(jìn)入非氧化途徑。通過這種方式,PPP的兩個(gè)途徑都可以為核苷酸和非必需氨基酸(NEAAs)從頭合成提供所需的碳。
第二個(gè)關(guān)鍵旁路途徑是絲氨酸合成途徑(SSP)。雖然細(xì)胞通常從細(xì)胞外環(huán)境獲取絲氨酸, 但大量證據(jù)表明SSP對(duì)高度增殖細(xì)胞群(如致癌細(xì)胞)提供絲氨酸至關(guān)重要。SSP將糖酵解生成的3-磷酸甘油酸在磷酸甘油酸脫氫酶(PHGDH)、磷酸絲氨酸氨基轉(zhuǎn)移酶(PSAT)和磷酸絲氨酸磷酸酶(PSPH)作用下逐步代謝為絲氨酸。值得注意的是,PSAT介導(dǎo)3-磷酸羥基丙酮酸(PHP)轉(zhuǎn)化為3-磷酸絲氨酸需要消耗谷氨酸并產(chǎn)生α-酮戊二酸(αKG),αKG是TCA循環(huán)關(guān)鍵中間代謝物,也是DNA和組蛋白去甲基化的必需底物。在其合成之后,絲氨酸作為許多促進(jìn)細(xì)胞增殖的生物分子的重要前體,如同源NEAAs、半胱氨酸和甘氨酸的合成,甘氨酸隨后用于嘌呤核苷酸和抗氧化劑谷胱甘肽的生成。絲氨酸還可以通過生成鞘氨醇(合成鞘磷脂所必需的物質(zhì))并可作為磷脂頭基團(tuán)的前體維持新細(xì)胞膜的生成。除了用于磷脂和NEAAs合成外,SSP途徑通過絲氨酸羥甲基轉(zhuǎn)移酶(SHMT)生成甘氨酸為一碳代謝提供碳源。一碳代謝途徑可結(jié)合葉酸和蛋氨酸循環(huán),有助于核苷酸合成、脂質(zhì)代謝及維持細(xì)胞氧化還原平衡。更重要的是,一碳代謝對(duì)S-腺苷蛋氨酸(SAM)的生成至關(guān)重要,而SAM是組蛋白和DNA甲基化專屬性代謝物。
線粒體不單是“細(xì)胞的動(dòng)力源”
當(dāng)氧氣充足時(shí),來(lái)自脂肪酸氧化(FAO)或糖酵解的乙酰輔酶A在線粒體中與草酰乙酸結(jié)合生成檸檬酸。檸檬酸首先轉(zhuǎn)化為異檸檬酸,然后轉(zhuǎn)化為αKG,產(chǎn)生CO2, H+和NADH。然后αKG經(jīng)脫羧作用形成琥珀酰輔酶A,并生成NADH和H+。磷酸化的琥珀酰輔酶A可以產(chǎn)生琥珀酸,其通過氧化和水合過程再生成草酰乙酸和NADH和H+。TCA循環(huán)的總體結(jié)果是乙酰輔酶A脫羧生成CO2、NADH和H+。所產(chǎn)生的NADH和H+可以被電子傳遞鏈(ETC)利用形成化學(xué)滲透質(zhì)子梯度產(chǎn)生ATP。幾十年來(lái),線粒體研究的主要焦點(diǎn)一直與它在ATP生成中的作用有關(guān),但這種簡(jiǎn)單化的觀點(diǎn)正在迅速改變,TCA循環(huán)已經(jīng)成為了NEAA合成、DNA和組蛋白翻譯后修飾所必需的代謝物生成的關(guān)鍵調(diào)控因子。例如,檸檬酸可以從線粒體輸出到細(xì)胞質(zhì)中,并被ATP檸檬酸裂解酶(ACLY)轉(zhuǎn)化為乙酰輔酶A,用于組蛋白或非組蛋白的乙酰化,或用于脂肪酸的生物合成。同樣,線粒體αKG是由異檸檬酸脫羧產(chǎn)生,也可由谷氨酸脫氨基產(chǎn)生。考慮到它在DNA和組蛋白去甲基化中的作用,該代謝物調(diào)節(jié)細(xì)胞命運(yùn)的作用得到重點(diǎn)關(guān)注也不足為奇。
細(xì)胞代謝調(diào)節(jié)表觀遺傳特征
細(xì)胞代謝為蛋白質(zhì)、組蛋白和DNA翻譯后修飾酶提供專屬性底物或輔助因子。組蛋白和DNA的磷酸化、巴豆酰化、琥珀酰化、丁酰化、乙酰化和甲基化對(duì)染色質(zhì)可及性和轉(zhuǎn)錄都有顯著影響,并且都受代謝物可用性調(diào)控,而這些關(guān)鍵的表觀調(diào)控代謝物的主要來(lái)源是三羧酸循環(huán)。
組蛋白乙酰化和其他酰化作用
組蛋白乙酰化可增加轉(zhuǎn)錄因子結(jié)合染色質(zhì)的可及性,從而增加基因轉(zhuǎn)錄。有趣的是,雖然乙酰輔酶A可以從FAO、氨基酸分解和糖酵解得到,但研究人員發(fā)現(xiàn),細(xì)胞主要依賴糖酵解中丙酮酸的氧化脫羧作用來(lái)實(shí)現(xiàn)組蛋白乙酰化,而葡萄糖來(lái)源的乙酰輔酶A的缺失會(huì)顯著損害組蛋白乙酰化。最近研究發(fā)現(xiàn),在乙酰輔酶A合成酶短鏈家族成員2 (ACSS2)的催化作用下,乙酸可以用于合成胞質(zhì)乙酰輔酶A。檸檬酸來(lái)源的乙酰輔酶A耗盡后(通過ACL基因敲除實(shí)現(xiàn)),細(xì)胞通過ACSS2的代償性上調(diào)維持細(xì)胞活力和從頭合成脂質(zhì)。然而,ACSS2只能部分恢復(fù)ACL敲除后組蛋白乙酰化水平,表明檸檬酸來(lái)源的乙酰輔酶A是組蛋白乙酰化的主要底物。細(xì)胞的代謝狀態(tài)也可能通過組蛋白乙酰化對(duì)轉(zhuǎn)錄活性產(chǎn)生負(fù)面影響。乙酰輔酶A能自發(fā)地乙酰化或去乙酰化賴氨酸殘基主要取決于局部乙酰輔酶A濃度。通過這種方式,整體的基因表達(dá)可以被代謝物的可用性被動(dòng)的調(diào)節(jié),也表明了代謝通量的作用。此外,組蛋白酰基化可由酰基輔酶A可用性進(jìn)行調(diào)節(jié),因此它被認(rèn)為是細(xì)胞代謝狀態(tài)的一個(gè)重要整合者。研究表明,線粒體代謝通過TCA循環(huán)(乙酰化和琥珀酰化)和β-氧化(巴豆酰化和丁酰化)產(chǎn)生的酰基部分調(diào)節(jié)染色質(zhì)可及性方面起著重要作用。
組蛋白和DNA甲基化
組蛋白甲基化也與轉(zhuǎn)錄激活/抑制相關(guān),而DNA甲基化通常導(dǎo)致轉(zhuǎn)錄抑制。在組蛋白和DNA甲基化中,甲基供體主要是由蛋氨酸和ATP縮合產(chǎn)生的SAM提供。SAM生成所需的碳來(lái)自蘇氨酸、甘氨酸、絲氨酸參與的葉酸代謝途徑。值得注意的是,甲基化四氫葉酸(N5-MTHF)也可以提供甲基,但在大多數(shù)情況甲基來(lái)自SAM。組蛋白和DNA去甲基化過程需要消耗αKG并釋放琥珀酸,說明去甲基化與細(xì)胞代謝、細(xì)胞內(nèi)αKG的可用性直接相關(guān)。反過來(lái),富馬酸和琥珀酸可作為αKG拮抗劑抑制αKG依賴性雙加氧酶的活性。所以組蛋白和DNA甲基化可通過改變代謝中間體的水平進(jìn)行調(diào)控。
組蛋白磷酸化
組蛋白磷酸化發(fā)揮多種生物學(xué)效應(yīng),包括DNA損傷和修復(fù)、細(xì)胞分裂中染色質(zhì)壓實(shí)以及誘導(dǎo)細(xì)胞凋亡。不同于組蛋白乙酰化明確的性質(zhì),同一位點(diǎn)的磷酸化會(huì)根據(jù)細(xì)胞環(huán)境導(dǎo)致明顯的分化作用。例如,在有絲分裂和減數(shù)分裂期間H3S10p和H3S28p殘基的磷酸化參與染色質(zhì)壓實(shí),但在染色質(zhì)松弛階段則激活轉(zhuǎn)錄。代謝可通過啟動(dòng)激酶激活的信號(hào)級(jí)聯(lián)反應(yīng)間接影響組蛋白磷酸化,但是否能直接改變磷酸基團(tuán)的可用性仍有待確定。
細(xì)胞營(yíng)養(yǎng)感知
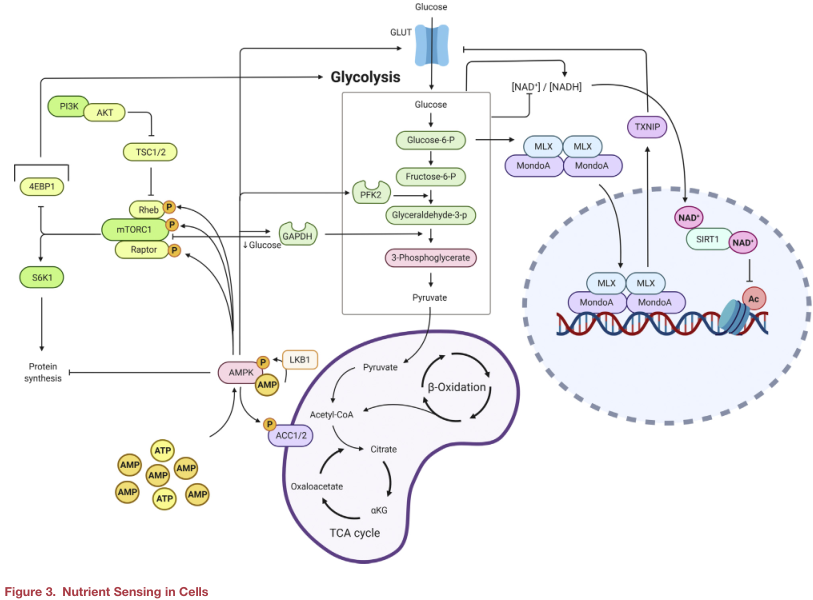
生態(tài)代謝環(huán)境在維持成體干細(xì)胞命運(yùn)的體內(nèi)平衡中發(fā)揮怎樣的作用?此外,損傷或創(chuàng)傷通常會(huì)導(dǎo)致生態(tài)位代謝環(huán)境的破壞,干細(xì)胞暴露在新的代謝環(huán)境中,是否會(huì)影響細(xì)胞的命運(yùn)也是一個(gè)問題。局部代謝環(huán)境變化和細(xì)胞命運(yùn)之間的溝通是通過幾個(gè)關(guān)鍵的營(yíng)養(yǎng)傳感器,它們將細(xì)胞外環(huán)境的變化轉(zhuǎn)化為細(xì)胞的固有信號(hào)(或信號(hào)),如TXNIP、mTOR、AMPK和組蛋白去乙酰化酶的sirtuin家族。
硫氧還蛋白相互作用蛋白--葡萄糖利用看門人
硫氧還蛋白相互作用蛋白(TXNIP)是一種α-抑制蛋白,具有調(diào)節(jié)糖酵解、氧化應(yīng)激和細(xì)胞增殖等多種生物學(xué)功能。TXNIP與硫氧還蛋白(TRX) 1和2相互作用并結(jié)合,抑制TRX的抗氧化特性,導(dǎo)致細(xì)胞內(nèi)氧化應(yīng)激增加。TXNIP也通過抑制GLUT1活性和轉(zhuǎn)錄抑制糖酵解通量。細(xì)胞內(nèi)葡萄糖和G6P升高可促進(jìn)Txnip轉(zhuǎn)錄,進(jìn)而導(dǎo)致TXNIP介導(dǎo)的葡萄糖攝取減少。因此,TXNIP與G6P在負(fù)反饋回路中調(diào)節(jié)葡萄糖攝取。此外,TXNIP在調(diào)節(jié)細(xì)胞增殖方面也具有重要作用。
雷帕霉素:生長(zhǎng)與營(yíng)養(yǎng)的交點(diǎn)
雷帕霉素(mTOR)由兩個(gè)復(fù)合物(mTORC1和mTORC2)組成,它們的作用既有重疊又有不同。兩種復(fù)合物都會(huì)對(duì)刺激物(胰島素和IGF-1)、氨基酸和葡萄糖水平、能量狀態(tài)和細(xì)胞氧水平做出反應(yīng)。特別是營(yíng)養(yǎng)成分和氨基酸是mTORC1通路有效激活劑,可對(duì)下游靶點(diǎn)4EBP1和S6K1磷酸化,從而啟動(dòng)mRNA翻譯、糖酵解和生物合成。mTORC活性由其上游調(diào)節(jié)劑控制,包括負(fù)調(diào)節(jié)劑TSC1/2。TSC1/2活性缺失導(dǎo)致GTP結(jié)合的Rheb出現(xiàn)積累和mTORC1的活化。重要的是,mTORC1信號(hào)的改變?cè)诩?xì)胞命運(yùn)中起著重要的作用。MuSCs靜止?fàn)顟B(tài)下發(fā)現(xiàn)了一個(gè)不同的G0期,在靜止G0期和激活啟動(dòng)狀態(tài)之間過渡,稱為GAlert期。這兩種細(xì)胞狀態(tài)之間的轉(zhuǎn)換受到mTORC1信號(hào)調(diào)控,這可能與靜止?fàn)顟B(tài)下環(huán)境營(yíng)養(yǎng)可獲得性有關(guān)。
AMPK
5'AMP活化蛋白激酶(AMPK)是細(xì)胞中最具特征的能量傳感器。鑒于AMPK對(duì)磷酸化腺苷核苷酸水平的敏感性,AMPK在細(xì)胞感知營(yíng)養(yǎng)利用率和對(duì)變化作出反應(yīng)的能力中具有至關(guān)重要的作用,活化的AMPK通過促進(jìn)葡萄糖轉(zhuǎn)運(yùn)蛋白的表達(dá)和活化直接影響葡萄糖穩(wěn)態(tài),通過磷酸化6-磷酸果糖-2-激酶促進(jìn)果糖2-6二磷酸生成并激活糖酵解。AMPK還可以通過乙酰輔酶A羧化酶1/2 (ACC1/2)的磷酸化調(diào)控脂質(zhì)代謝。AMPK除了調(diào)節(jié)代謝和生長(zhǎng)外,還參與啟動(dòng)適應(yīng)性代謝重編程反應(yīng)。在這種能力下,AMPK磷酸化并調(diào)節(jié)參與細(xì)胞表觀遺傳的轉(zhuǎn)錄因子、輔酶因子活性,包括HAT p300, HDACs,甚至組蛋白本身。雖然研究已經(jīng)揭示了AMPK在表觀基因組中的調(diào)控作用,但其如何影響細(xì)胞生長(zhǎng)和細(xì)胞命運(yùn)仍有待探索。
Sirtuins蛋白
Sirtuins是由7種組蛋白/蛋白去乙酰化酶(SIRT1-7)組成,其活性主要依賴于NAD+的可用性,在功能上將其活性與營(yíng)養(yǎng)物質(zhì)的可用性和先天細(xì)胞代謝聯(lián)系起來(lái)。Sirtuins介導(dǎo)組蛋白和非組蛋白的乙酰化狀態(tài)來(lái)調(diào)控細(xì)胞增殖、存活和衰老。不過相關(guān)研究結(jié)果顯示SIRT1介導(dǎo)調(diào)控細(xì)胞命運(yùn)具有一定復(fù)雜性,提示其作用可能取決于特定的代謝微環(huán)境。
小結(jié)
本文對(duì)細(xì)胞命運(yùn)與代謝的聯(lián)系進(jìn)行系統(tǒng)總結(jié),線粒體既是能量發(fā)生器,又是體細(xì)胞和多能細(xì)胞雙向轉(zhuǎn)換的推動(dòng)者,為發(fā)育生物學(xué)開辟了新的研究視野。代謝中活性小分子可誘導(dǎo)代謝重編程和影響干細(xì)胞功能。一種值得注意的方法是將關(guān)鍵代謝物或小分子微粒直接注射到組織或損傷部位以促進(jìn)再生,如在耳廓損傷后局部給予2-脫氧-D-葡萄糖(2-DG),證實(shí)可增強(qiáng)耳朵再生。也有研究已經(jīng)證明靶向代謝(熱量限制)可增強(qiáng)移植后干細(xì)胞的移植。此外,干細(xì)胞的激活狀態(tài)和代謝狀態(tài)的顯著變化相關(guān)。目前對(duì)于改變代謝狀態(tài)控制干細(xì)胞在體外狀態(tài)和功能仍知之甚少,且干細(xì)胞群體存在巨大異質(zhì)性,因此研究干細(xì)胞代謝前仍需建立更為成熟的單細(xì)胞水平代謝檢測(cè)平臺(tái)和技術(shù)。
參考文獻(xiàn)
Ly C H , et al. A Metabolic Roadmap for Somatic Stem Cell Fate. Cell Metabolism, 2020, 31(6).
原文閱讀,請(qǐng)長(zhǎng)按識(shí)別下方二維碼

精彩推薦
1. Nature reviews Molecular cell Biology | 小分子代謝物如何調(diào)控上游大分子
3. 最新綜述 | 腸道菌群調(diào)節(jié)能量代謝機(jī)制
4. 綜述 | 腸道菌群的營(yíng)養(yǎng)代謝及其代謝產(chǎn)物
5. NCB | 葡萄糖饑餓誘導(dǎo)的細(xì)胞死亡:胱氨酸調(diào)控戊糖磷酸途徑依賴和二硫化物脅迫
6. 繪譜學(xué)堂 | 7月腫瘤代謝組學(xué)專題班 · 揭曉
7. 引領(lǐng)行業(yè) │ 聚焦麥特繪譜代謝組學(xué)整體解決方案
8. 618狂歡 | 繪譜學(xué)堂14場(chǎng)精品課程免!費(fèi)!送!

