間充質干細胞(MSC)是來源于胚胎發育早期中胚層的一種具備自我更新、多向分化潛能且經體外規模化擴增仍能保持其生物學特性的成體干細胞,最早由Friedenstein等從骨髓中分離發現,具有貼壁性,呈纖維狀,MSC具有來源豐富、制備簡單、多向分化潛能、低免疫源性和低致瘤性等特點受到科研的親睞,特別是MSC向成骨,成脂肪分化一直是實驗制作的熱點,MSC向成骨,成脂分化的操作步驟,記得收藏,實驗用時不迷路。
準備材料:
1.MSC細胞(啟達生物可提供人,大鼠,小鼠,新西蘭大白兔,牛,豬來源MSC細胞,詳見公司網站)
2. MSCM培養基(啟達生物:P2001)
3. 誘導成骨分化培養基/Osteogenic differentiation medium(啟達生物,貨號:P1301)
4. 成脂分化培養基-adipogenic Culture Medium(啟達生物,貨號:P1302)
5. 24孔板


一.MSC細胞成骨/成脂分化:
在加入MSCM培養基的24孔板中,每孔板50000-60000個MSC細胞。
1.第二天或當它們達到匯合時(通常在24-48小時內),將培養基轉換為分化培養基。若細胞太稀,則不會分化,因此在加入間充質干細胞分化培養基前必須確保MSC細胞至少80%-90%融合。
2.每2-3天換液,注意:成骨分化容易使細胞卷起,成骨分化時應使用包被液包被細胞培養板,可使用多聚賴氨酸溶液或者細胞包被液(貨號:SD0044)進行細胞包被。
3.每隔1-2天更換新鮮的間充質干細胞分化培養基;
注意:換液時請注意,對24孔板要輕拿輕放,換液的培養基需要預熱,換液時沿孔壁慢慢滴入,為防止成骨細胞脫落,建議成骨過程中出現大量鈣結節之后,換液形式變為每天一次半量換液。
4. 誘導14-21天期間,視細胞的形態變化及生長情況進行染色。
二.細胞染色:
1.MSC誘導的成骨分化染色:
1.誘導成骨分化結束后,吸掉6孔板中的成骨分化培養基,用PBS沖洗1-2次。每孔加入1 mL細胞固定液,固定10~30 min;
2. 吸掉細胞固定液,PBS沖洗2次。每孔加入1 mL成骨檢測染液,在室溫下在黑暗中培養30分鐘,并檢查顏色發展
3.吸掉成骨檢測染液,用PBS沖洗2-3次;
4.將培養板置于顯微鏡下觀察成骨染色效果;
2.茜素紅S染色檢測礦化
茜素紅S是一種鈣敏感染料。分化的成骨細胞沉積大量的細胞外鈣(礦化的標志),可以通過與茜素紅S絡合來檢測。鈣沉積呈現為亮橙紅色染色區域,在對堿性磷酸酶染色的板拍照后,通過用1x PBS洗滌染色的板兩次來進行茜素紅S染色。
1.先PBS的pH值用0.1%NH4OH調節至4.2。
2.吸取PBS并加入足夠的茜素紅S染色溶液以覆蓋細胞單層。將平板在室溫下在黑暗中培養45分鐘。
3.小心地吸取茜素紅S溶液,用蒸餾水清洗板子四次。
4. 細胞外鈣沉積物表現為顏色鮮艷的橙紅色區域。
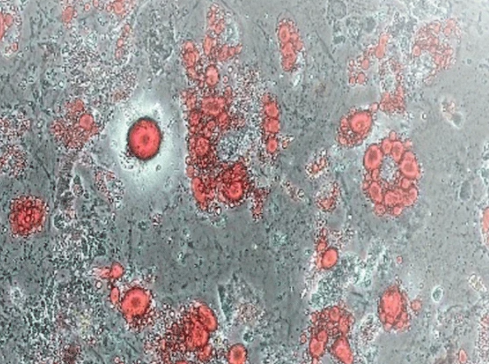
骨髓間充質干細胞誘導(Day12)
3.油紅O染色法測定脂肪分化
這種染色測定基于親脂性染料油紅O保留在顯微鏡下可見的脂肪細胞脂肪球中的原理,操作步驟如下:
1.吸盡培養基并在PBS中洗滌細胞一次。
2.在室溫下將細胞固定在4%PFA中15分鐘。
3.用ddH2O洗滌兩次,持續2 x 5分鐘。
4.在室溫下用Oil-Red-O工作溶液染色15分鐘。
5.用1x PBS或ddH2O洗滌3 x 5分鐘。
6.室溫下用50%異丙醇沖洗細胞一次。
7.用1x PBS或ddH2O沖洗細胞。
8.紅色染色的脂滴可以通過光學顯微鏡觀察到。脂肪細胞也很容易在正常顯微鏡下通過其圓形形態和顯著增強的較大脂滴的光反射來觀察。
9.為了計數總細胞,用Mayer HemTox染色劑在RT下染色15分鐘,并用dd水洗滌2次。
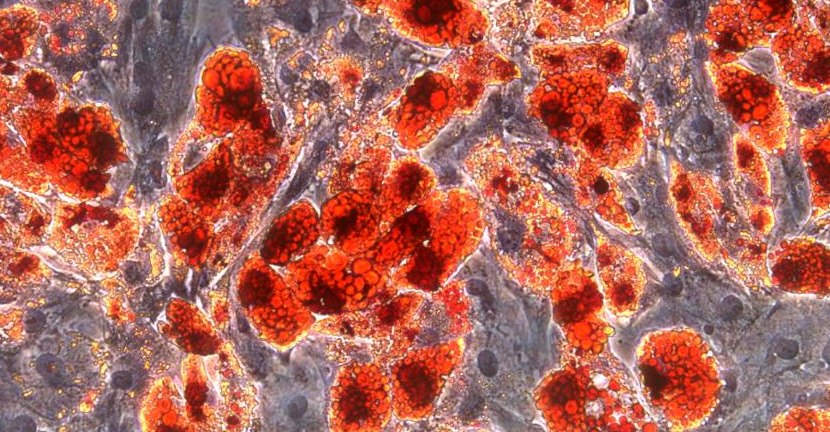
間充質干細胞脂肪誘導(Day10)
