編者按 2021年8月25日,來(lái)自美國(guó)Wistar研究所等研究人員在Science Advances(IF:14.136)在線發(fā)表題為" A cancer ubiquitome landscape identifies metabolic reprogramming as target of Parkin tumor suppression"的研究成果。該研究通過(guò)蛋白質(zhì)組學(xué)和泛素化修飾組篩選,發(fā)現(xiàn)了通用腫瘤抑制機(jī)制:E3泛素連接酶Parkin,可以作為腫瘤抑制途徑的關(guān)鍵以及應(yīng)激激活效應(yīng)物,通過(guò)干擾癌細(xì)胞重新編程其代謝的能力來(lái)拮抗惡性細(xì)胞增殖和轉(zhuǎn)移能力。 【研究材料】 PC3、LN229、MCF10A等多種癌細(xì)胞、癌組織 【技術(shù)方法】 蛋白組學(xué)、泛素化修飾蛋白組學(xué)、免疫組化、western blot等 【方法流程】 1. Parkin不影響癌細(xì)胞中的線粒體自噬 將Parkin在前列腺癌PC3細(xì)胞中過(guò)表達(dá),未引起線粒體外膜蛋白的丟失(圖1A),也未引起線粒體質(zhì)量的改變(圖1B)。溶酶體LAMP1蛋白與線粒體自噬時(shí)的標(biāo)志蛋白TOMM20的共定位也未受PC3的影響(圖1C和圖1D),線粒體結(jié)構(gòu)和活性也均未受影響(圖1E和圖1F)。 圖1 Parkin不影響癌細(xì)胞中的線粒體自噬 2. Parkin抑制腫瘤細(xì)胞的運(yùn)動(dòng)和侵襲 Parkin在惡性膠質(zhì)瘤LN229細(xì)胞中過(guò)表達(dá)減少了黏合斑的面積(圖2A)、長(zhǎng)度(圖2B)及其組裝和解體(圖2C),抑制了腫瘤的細(xì)胞運(yùn)動(dòng)(圖2D和圖2E)。傷口閉合實(shí)驗(yàn)中顯示Parkin抑制了細(xì)胞的定向遷移(圖2F),多種癌細(xì)胞的侵襲也被Parkin阻斷(圖2G)。 圖2 Parkin抑制腫瘤細(xì)胞的運(yùn)動(dòng)和侵襲 3. Parkin抑制原發(fā)性腫瘤和轉(zhuǎn)移性腫瘤的生長(zhǎng) 為了驗(yàn)證Parkin在腫瘤生長(zhǎng)中的作用,作者進(jìn)行了體內(nèi)實(shí)驗(yàn)。將Parkin過(guò)表達(dá)的PC3細(xì)胞皮下接種至NOD-SCID免疫缺陷小鼠中,發(fā)現(xiàn)Parkin抑制了腫瘤的肺轉(zhuǎn)移(圖3A-3C),將PC3細(xì)胞直接接種至脾臟,結(jié)果發(fā)現(xiàn)Parkin也抑制了腫瘤轉(zhuǎn)移至肝臟(圖3D和3E)。組織芯片實(shí)驗(yàn)也證實(shí)腫瘤病人組織中的Parkin表達(dá)量較正常組織中少。 圖3 Parkin抑制原發(fā)性腫瘤和轉(zhuǎn)移性腫瘤的生長(zhǎng) 4. Parkin抑制腫瘤細(xì)胞運(yùn)動(dòng)是通過(guò)其E3連接酶活性實(shí)現(xiàn)的 對(duì)Parkin進(jìn)行點(diǎn)突變(S65A或C431S),使其失去E3連接酶活性,轉(zhuǎn)染入前列腺癌PC3細(xì)胞中發(fā)現(xiàn)Parkin丟失了抑制腫瘤細(xì)胞的運(yùn)動(dòng)和侵襲的能力(圖4A-4D)。 圖4 Parkin抑制腫瘤細(xì)胞運(yùn)動(dòng)是通過(guò)其E3連接酶活性實(shí)現(xiàn)的 5. Parkin在癌癥中的功能分子分析 為驗(yàn)證Parkin在癌癥中的具體作用,作者開(kāi)展了蛋白組學(xué)和泛素化修飾蛋白組學(xué)。蛋白組學(xué)實(shí)驗(yàn)中共鑒定到5557個(gè)蛋白,對(duì)顯著性差異蛋白(Parkin過(guò)表達(dá)vs Vector)的生信分析發(fā)現(xiàn)Parkin影響了細(xì)胞運(yùn)動(dòng)通路、抑制了MAPK信號(hào)通路、下調(diào)了癌基因信號(hào)通路等通路(圖5A-5D)。5557個(gè)總鑒定蛋白中的741個(gè)蛋白屬于線粒體蛋白,該部分蛋白參與的呼吸鏈復(fù)合體(MTND1等)、內(nèi)源性抗氧化、蛋白翻譯等多個(gè)通路中的多個(gè)蛋白均受Parkin影響(圖5E和5F)。 圖5 蛋白組學(xué)和泛素化修飾蛋白組學(xué)結(jié)果 泛素化修飾組學(xué)結(jié)果中,受Parkin顯著調(diào)控的泛素化蛋白主要參與了細(xì)胞死亡(如HK1蛋白)、線粒體動(dòng)態(tài)變化(如MFN2、RHOT1等蛋白)、非氧化的磷酸戊糖途徑(如TKT、TALDO1蛋白)等信號(hào)通路(圖6A)。 Western blot實(shí)驗(yàn)驗(yàn)證了Parkin下游蛋白MFN2和TKT的泛素化水平(圖6B和6C)以及Parkin對(duì)MFN2、TKT蛋白的降解和對(duì)FAK、Src的磷酸化(細(xì)胞運(yùn)動(dòng)所需)水平的下調(diào)(圖6D和6H),且自噬抑制劑BafA不影響Parkin對(duì)MFN2和TKT的降解(圖6E)。 圖6 泛素化修飾蛋白組學(xué)結(jié)果及驗(yàn)證 6. Parkin通過(guò)調(diào)節(jié)線粒體的動(dòng)態(tài)變化從而抑制腫瘤的運(yùn)動(dòng) 泛素化修飾蛋白組學(xué)結(jié)果中顯示MFN2和RHOT1參與了線粒體動(dòng)態(tài)變化信號(hào)通路,Parkin通過(guò)降解MFN2和RHOT1,從而抑制了線粒體的動(dòng)態(tài)變化,在過(guò)表達(dá)Parkin的細(xì)胞中過(guò)表達(dá)MFN2則恢復(fù)了線粒體的動(dòng)態(tài)變化、線粒體的融合和裂變及線粒體運(yùn)動(dòng)。RHOT1的過(guò)表達(dá)也發(fā)揮了與MFN2相同的作用(圖7A-7F)。RHOT1點(diǎn)突變實(shí)驗(yàn)驗(yàn)證了Parkin是通過(guò)特異性調(diào)節(jié)線粒體的動(dòng)態(tài)變化從而抑制腫瘤運(yùn)動(dòng)的(圖7G和7H)。 圖7 Parkin通過(guò)調(diào)節(jié)線粒體的動(dòng)態(tài)變化抑制腫瘤運(yùn)動(dòng) 7. Parkin通過(guò)調(diào)節(jié)磷酸戊糖信號(hào)通路影響氧化應(yīng)激從而調(diào)控腫瘤細(xì)胞的運(yùn)動(dòng) 泛素化修飾蛋白組學(xué)結(jié)果顯示Parkin靶向了磷酸戊糖途徑(PPP),作者隨即驗(yàn)證了該信號(hào)通路對(duì)腫瘤的影響。Parkin抑制了磷酸戊糖途徑中的TKT的活性(圖8A),這導(dǎo)致了PPP通量的減少(圖8B和8C)。Parkin還抑制了葡萄糖的攝入和乳酸的形成,最終導(dǎo)致了細(xì)胞饑餓。Parkin對(duì)TKT的抑制還降低了NADPH的水平、提高了線粒體活性氧(ROS)的增加(圖8D-8F),由此產(chǎn)生的氧化應(yīng)激可以抑制線粒體運(yùn)輸和腫瘤細(xì)胞運(yùn)動(dòng)。在Parkin過(guò)表達(dá)細(xì)胞中過(guò)表達(dá)TKT恢復(fù)了線粒體的運(yùn)動(dòng)(圖8I)、TKT的siRNA沉默抑制了腫瘤的侵襲(圖8K)以及TKT K499R的突變而未被Parkin降解進(jìn)而促進(jìn)了細(xì)胞遷移,上述均證明了PPP在Parkin抑制腫瘤細(xì)胞運(yùn)動(dòng)中的特異性。 小結(jié) 中科優(yōu)品推薦 基于新一代離子淌度質(zhì)譜平臺(tái),4D-修飾產(chǎn)品實(shí)現(xiàn)檢測(cè)性能全面突破: ?? 高深度——鑒定深度提升超20%~100%,挖掘更多生物信息 ?? 更微量——樣本用量降低2/3,為珍貴、微量分析節(jié)省樣本 ?? 更精準(zhǔn)——精準(zhǔn)定位相近修飾位點(diǎn),提高后續(xù)位點(diǎn)驗(yàn)證概率 ?? 更可靠——金標(biāo)抗體富集修飾肽段,操作可靠有保障
腫瘤作為人類健康的"頭號(hào)殺手",通過(guò)重組細(xì)胞代謝適應(yīng)不利微環(huán)境從而促進(jìn)疾病的發(fā)展。Parkin是一種E3泛素連接酶,它可能在調(diào)節(jié)癌細(xì)胞代謝和抑制腫瘤生長(zhǎng)方面發(fā)揮作用,但具體作用機(jī)制仍不清楚。

研究結(jié)果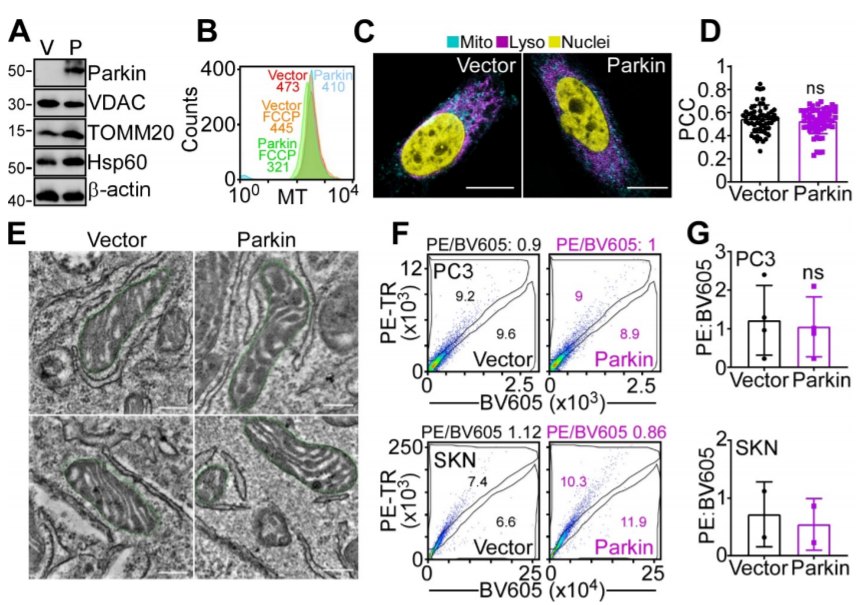
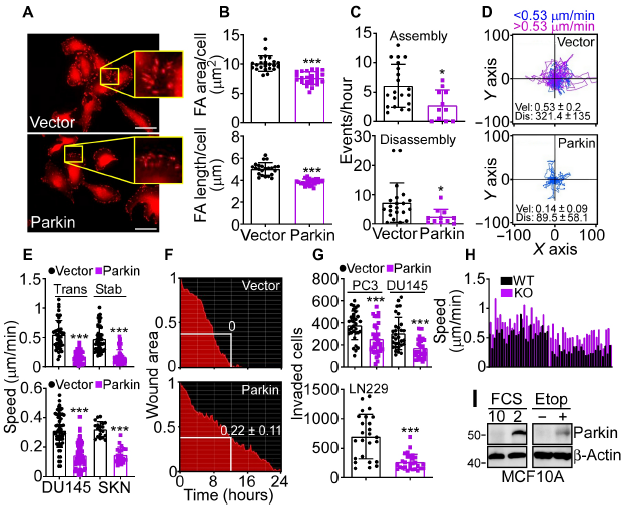
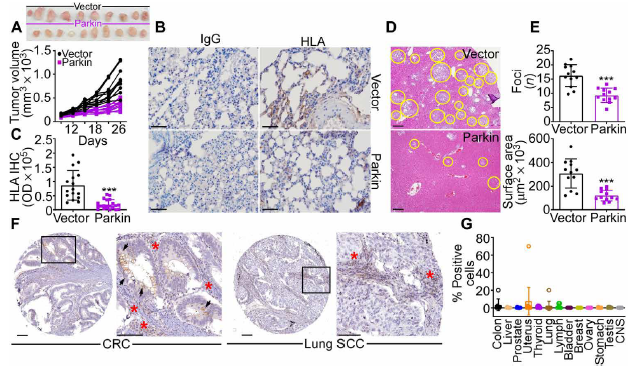
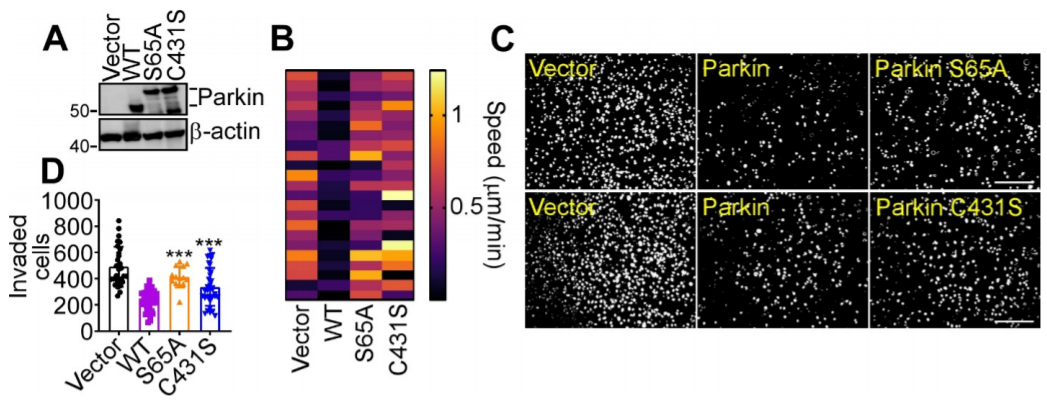
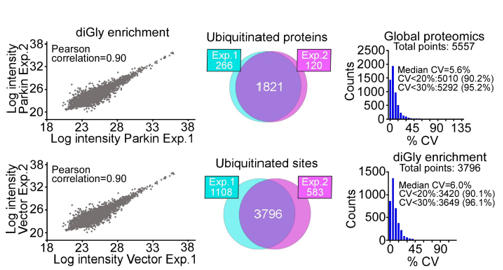
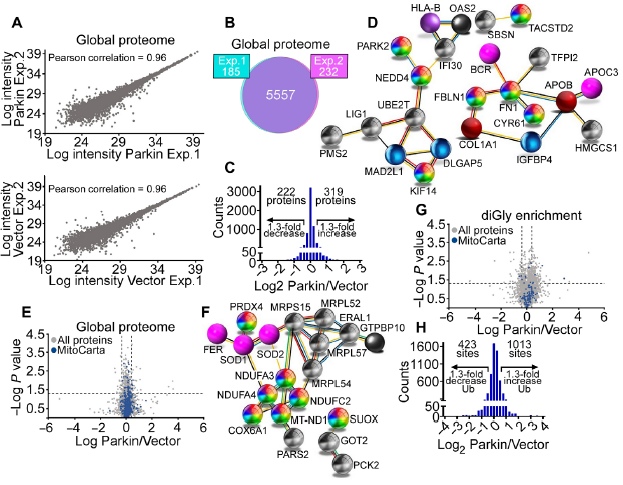
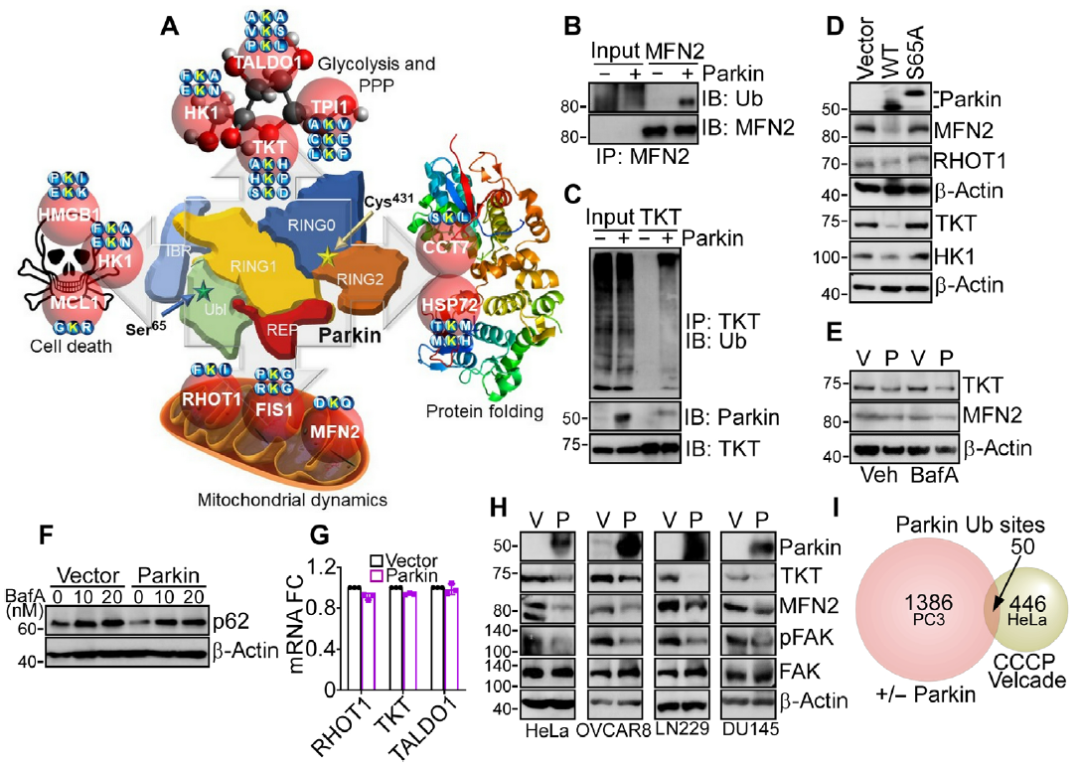
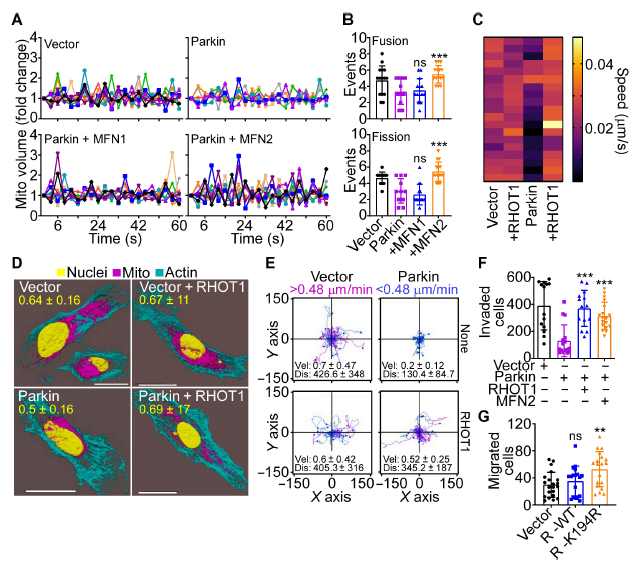
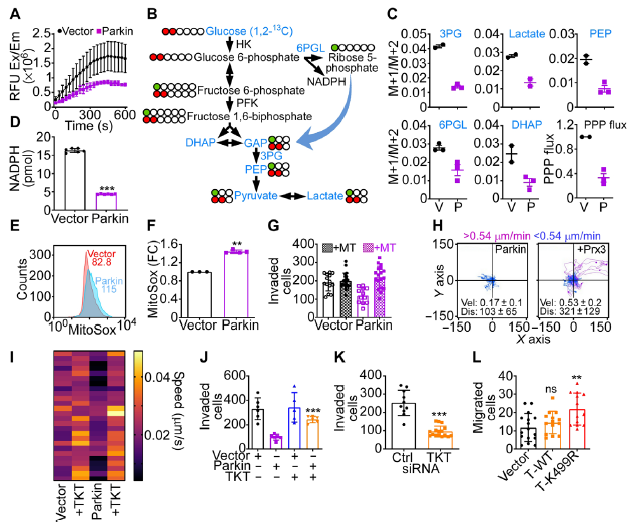
圖8 Parkin通過(guò)調(diào)節(jié)磷酸戊糖信號(hào)通路調(diào)控氧化應(yīng)激從而調(diào)控腫瘤細(xì)胞的運(yùn)動(dòng)
在這項(xiàng)研究中,作者證明了Parkin靶向糖酵解和線粒體網(wǎng)絡(luò)來(lái)拮抗腫瘤生長(zhǎng)。該途徑獨(dú)立于線粒體損傷或線粒體自噬激活,需要Parkin E3連接酶活性來(lái)降解線粒體動(dòng)力學(xué)效應(yīng)物(MFN2和RHOT1)和PPP的非氧化階段(TKT)。這造成了急性代謝和氧化應(yīng)激,抑制亞細(xì)胞線粒體運(yùn)輸,抑制細(xì)胞運(yùn)動(dòng)激酶、FAK和Src的磷酸化,并阻止腫瘤細(xì)胞運(yùn)動(dòng),從而極大地抑制體內(nèi)原發(fā)和轉(zhuǎn)移性腫瘤的生長(zhǎng)。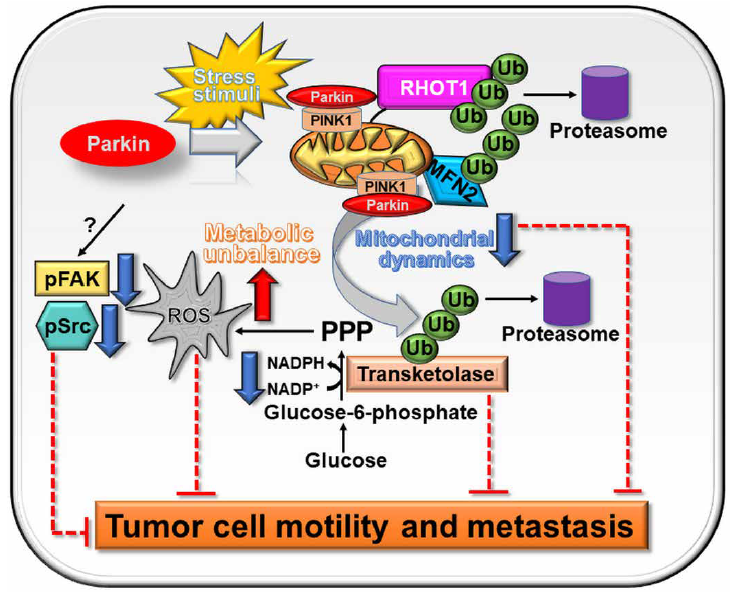
中科新生命攜全新一代4D-修飾蛋白質(zhì)組,開(kāi)展千萬(wàn)級(jí)補(bǔ)貼優(yōu)惠活動(dòng),單個(gè)樣品優(yōu)惠上千元。歡迎感興趣的老師前來(lái)咨詢!
Sci Adv (IF 14.136)|腫瘤“一網(wǎng)打盡”! 泛素化修飾組揭示廣譜抑制腫瘤生長(zhǎng)的新機(jī)制
作者:上海中科新生命生物科技有限公司 2021-12-23T19:30 (訪問(wèn)量:4837)
上海中科新生命生物科技有限公司 商家主頁(yè)
地 址: 上海市園美路58號(hào)1號(hào)樓15-18樓
聯(lián)系人: 徐
電 話: 021-54665263
傳 真:
Email:marketing@aptbiotech.com
相關(guān)咨詢
會(huì)議邀請(qǐng) | 第8屆全國(guó)植物蛋白質(zhì)研究大會(huì)暨首屆貴陽(yáng)生命科學(xué)新高地科學(xué)家論壇 (2023-07-07T14:37 瀏覽數(shù):32748)
項(xiàng)目文章Cell(IF 64.5)| 中國(guó)科技大學(xué)探索食物過(guò)敏謎團(tuán) (2023-07-07T14:22 瀏覽數(shù):34102)
Gastroenterology(IF 29.4)| 基于機(jī)器學(xué)習(xí)算法開(kāi)發(fā)的外泌體miRNA生物標(biāo)志物用于胰腺導(dǎo)管腺癌早期診斷 (2023-07-05T15:54 瀏覽數(shù):31402)
Cancer Letters(IF 9.7)|天津市環(huán)湖醫(yī)院利用Labelfree揭示超聲-替莫唑胺聯(lián)合誘導(dǎo)膠質(zhì)瘤細(xì)胞的凋亡機(jī)制 (2023-06-30T09:37 瀏覽數(shù):32390)
Excel表免費(fèi)下載 | 速來(lái)圍觀!2023年影響因子發(fā)布 (2023-06-29T09:35 瀏覽數(shù):27249)
外泌體多組學(xué)創(chuàng)新解決方案,精準(zhǔn)、前沿的疾病診斷生物標(biāo)志物 (2023-06-28T10:20 瀏覽數(shù):36725)
Immunity (IF=43.474)丨單細(xì)胞+空間聯(lián)合揭示肉芽腫形成的異常淋巴發(fā)育進(jìn)程 (2023-06-26T17:28 瀏覽數(shù):31076)
專家齊聚 亮點(diǎn)回顧 | 2023年海口·中醫(yī)藥創(chuàng)新多組學(xué)研究論壇圓滿落幕 (2023-06-25T10:10 瀏覽數(shù):35343)
項(xiàng)目文章Plant J(IF 7)| 杭州師范大學(xué)王慧中團(tuán)隊(duì)通過(guò)空間代謝+單細(xì)胞測(cè)序等揭示紅豆杉幼莖細(xì)胞特異的紫杉烷合成調(diào)控模式 (2023-06-25T09:42 瀏覽數(shù):33465)
項(xiàng)目文章Gut Microbes(IF 9.434)| 腸道微生物竟是導(dǎo)致膽囊切除術(shù)后患者腹瀉的元兇? (2023-06-14T16:35 瀏覽數(shù):30377)
