01
概 述
bFGF(basic Fibroblast Growth Factor,即堿性成纖維細(xì)胞生長(zhǎng)因子),也稱為 FGF-2(成纖維細(xì)胞生長(zhǎng)因子-2),屬于 FGF家族成員之一,該家族包含至少22種結(jié)構(gòu)相關(guān)的蛋白。FGF家族成員具有廣泛的促有絲分裂和細(xì)胞存活活性,并參與多種生物學(xué)過(guò)程,包括胚胎發(fā)育、細(xì)胞生長(zhǎng)、形態(tài)發(fā)生、組織修復(fù)、腫瘤生長(zhǎng)和侵襲。FGF-2是一種非糖基化、肝素結(jié)合的生長(zhǎng)因子,能與細(xì)胞表面的硫酸乙酰肝素蛋白聚糖(HSPG)結(jié)合。FGF-2在多種組織中表達(dá),包括大腦、垂體、腎臟、視網(wǎng)膜、骨骼、睪丸、腎上腺、肝臟、單核細(xì)胞、上皮細(xì)胞和內(nèi)皮細(xì)胞。
02
bFGF結(jié)構(gòu)
01
基本結(jié)構(gòu)特征
蛋白類型:單鏈多肽,屬于FGF家族(FGF-2)。
氨基酸數(shù)量:標(biāo)準(zhǔn)形式由 155個(gè)氨基酸 組成(人源),分子量約 17-18 kDa。
二硫鍵:含有3個(gè)保守的二硫鍵(Cys78-Cys96, Cys33-Cys101, Cys68-Cys129),維持三維結(jié)構(gòu)穩(wěn)定性。
02
三維結(jié)構(gòu)
bFGF核心結(jié)構(gòu):由β-折疊主導(dǎo)。
肝素結(jié)合域:表面富含帶正電荷的氨基酸(如Arg、Lys),與肝素/硫酸乙酰肝素(HSPG)結(jié)合,增強(qiáng)其穩(wěn)定性和受體激活能力。關(guān)鍵肝素結(jié)合位點(diǎn):Lys128、Arg129、Lys135 等。
受體結(jié)合位點(diǎn):與 FGFR, 結(jié)合的區(qū)域包括:N端(β1-β2環(huán)區(qū))、C端(β10-β12環(huán)區(qū))。需肝素作為共受體,形成 bFGF-FGFR-HSPG三元復(fù)合物 才能激活下游信號(hào)。
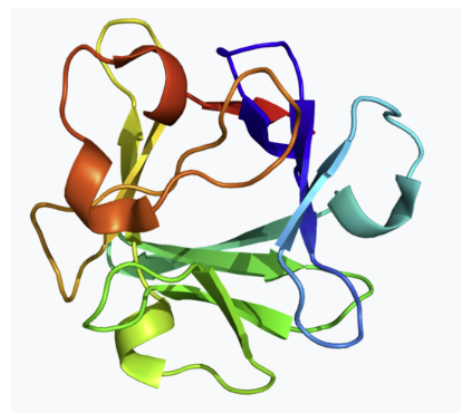
圖1.bFGF蛋白結(jié)構(gòu)(來(lái)源于WiKipedia)
03
bFGF生物學(xué)功能
不同信號(hào)通路的激活會(huì)導(dǎo)致不同的細(xì)胞反應(yīng):
01
促進(jìn)細(xì)胞增殖(如干細(xì)胞、成纖維細(xì)胞)
MAPK/ERK通路激活 → 上調(diào)Cyclin D1/CDK4/6 → 促進(jìn)G1/S期轉(zhuǎn)換。
PI3K/AKT 抑制凋亡(如減少BAX、增加BCL-2)。
02
維持干細(xì)胞多能性(如ESC/iPSC)
ERK與Nanog/OCT4/SOX2協(xié)同 → 抑制分化,維持未分化狀態(tài)。
03
促進(jìn)分化(如神經(jīng)、成骨、血管分化)
與BMP、WNT、VEGF等信號(hào)協(xié)同,調(diào)控譜系特異性基因(如RUNX2成骨、PAX6神經(jīng))。
04
促進(jìn)血管生成
激活內(nèi)皮細(xì)胞遷移、增殖(與VEGF協(xié)同)。上調(diào)MMP(基質(zhì)金屬蛋白酶),促進(jìn)ECM重塑。
04
bFGF的作用機(jī)制
bFGF通過(guò)結(jié)合其受體(FGFR)并激活下游信號(hào)通路,調(diào)控細(xì)胞的增殖、分化、遷移和存活。其作用機(jī)制可分為以下幾個(gè)關(guān)鍵步驟:
01
bFGF與受體結(jié)合
受體類型
bFGF主要結(jié)合成纖維細(xì)胞生長(zhǎng)因子受體(FGFR),F(xiàn)GFR屬于酪氨酸激酶受體(RTK)家族,包括四種亞型:FGFR1、FGFR2、FGFR3、FGFR4(不同亞型在不同細(xì)胞中表達(dá)不同)。
肝素/硫酸乙酰肝素(HSPG)的輔助作用
bFGF本身具有肝素結(jié)合域,需與細(xì)胞表面的肝素硫酸蛋白聚糖(HSPG)結(jié)合,才能穩(wěn)定構(gòu)象并促進(jìn)FGFR二聚化。HSPG可防止bFGF被降解,并增強(qiáng)其與FGFR的親和力。
02
受體二聚化與激活
bFGF結(jié)合FGFR后,誘導(dǎo)FGFR二聚化,觸發(fā)胞內(nèi)酪氨酸激酶結(jié)構(gòu)域自磷酸化。
磷酸化的FGFR招募銜接蛋白(如FRS2、PLCγ),進(jìn)而激活下游信號(hào)通路。
03
主要下游信號(hào)通路
bFGF-FGFR信號(hào)通過(guò)以下關(guān)鍵通路發(fā)揮作用:
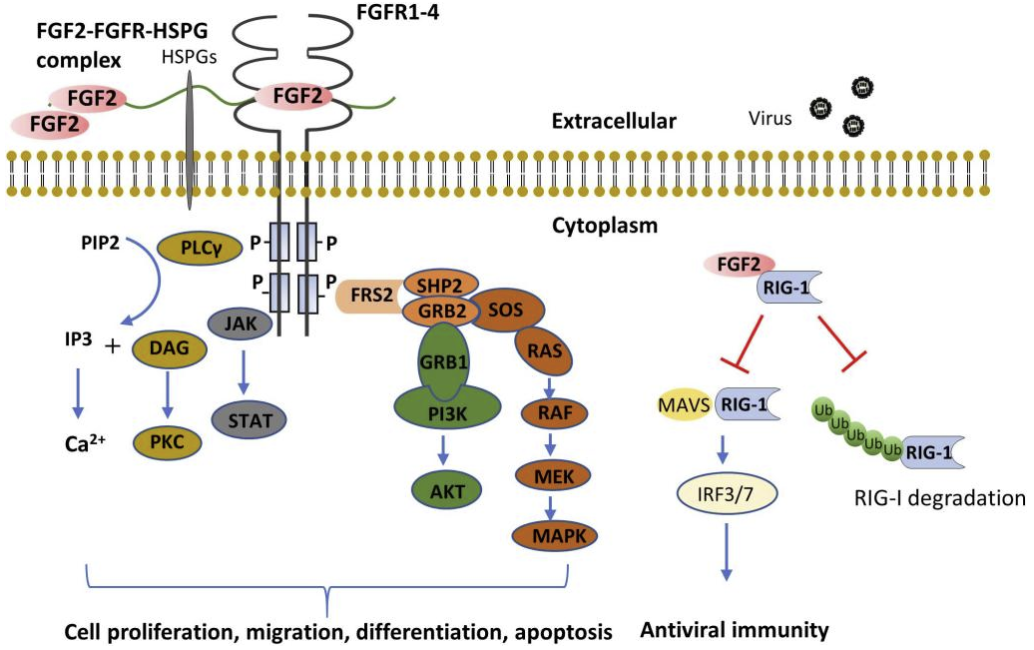
圖2.bFGF信號(hào)轉(zhuǎn)導(dǎo)[1]
05
bFGF在干細(xì)胞領(lǐng)域的應(yīng)用
01
維持胚胎干細(xì)胞(ESCs)與誘導(dǎo)多能干細(xì)胞(iPSCs)的未分化狀態(tài)
在干細(xì)胞治療中,bFGF是維持ESC/iPSC未分化狀態(tài)的關(guān)鍵因子,常與TGF-β/Nodal信號(hào)協(xié)同使用。bFGF通過(guò)激活MAPK/ERK和PI3K/AKT通路,促進(jìn)干細(xì)胞增殖并抑制自發(fā)分化。
hESCs/iPSCs培養(yǎng):常用濃度為4-20 ng/mL,需每日補(bǔ)加以維持活性(因bFGF在37℃下易降解)。
02
促進(jìn)間充質(zhì)干細(xì)胞(MSCs)的增值
bFGF增強(qiáng)MSCs的增殖能力,延緩衰老,維持其多向分化潛能(如骨髓、脂肪、臍帶來(lái)源MSCs)。
03
促進(jìn)干細(xì)胞定向分化
bFGF可與其他因子協(xié)同,誘導(dǎo)干細(xì)胞向特定譜系分化:
神經(jīng)干細(xì)胞(NSCs)
bFGF能夠刺激神經(jīng)干細(xì)胞的增殖,并與其他生長(zhǎng)因子如胰島素樣生長(zhǎng)因子(IGF)和血小板衍生生長(zhǎng)因子(PDGF)協(xié)同作用,共同調(diào)節(jié)神經(jīng)干細(xì)胞的增殖。此外,F(xiàn)GF-2 在神經(jīng)細(xì)胞培養(yǎng)中可能具有促進(jìn)神經(jīng)再生和修復(fù)的功能。
成骨/軟骨分化
早期添加bFGF可增強(qiáng)MSCs的成骨分化能力(與BMP-2協(xié)同)。在軟骨組織工程中,bFGF可促進(jìn)軟骨細(xì)胞增殖(如關(guān)節(jié)修復(fù))。
血管/內(nèi)皮分化
bFGF與VEGF聯(lián)用,可誘導(dǎo)干細(xì)胞分化為血管內(nèi)皮細(xì)胞,用于血管再生治療。
04
3D培養(yǎng)與類器官構(gòu)建
類器官培養(yǎng)(如腸道、腦、肝類器官):bFGF常作為基礎(chǔ)生長(zhǎng)因子,維持干細(xì)胞增殖并促進(jìn)3D結(jié)構(gòu)形成。
05
優(yōu)化培養(yǎng)體系
無(wú)血清培養(yǎng)基: bFGF是無(wú)血清/低血清培養(yǎng)的核心成分。
提高克隆形成率:在單細(xì)胞克隆培養(yǎng)中,bFGF可減少細(xì)胞凋亡,提高克隆形成效率。
06
注意事項(xiàng)
穩(wěn)定性:在37℃下易降解,細(xì)胞培養(yǎng)時(shí)需每1-2天補(bǔ)充。
濃度優(yōu)化:不同細(xì)胞類型需求不同(通常4-100 ng/mL)。
06
翌圣GMP級(jí)重組人FGF2/bFGF蛋白
GMP級(jí)重組人bFGF蛋白是干細(xì)胞治療藥物的關(guān)鍵原料,YEASEN專注細(xì)胞治療上游GMP級(jí)原料試劑研發(fā)。YEASEN的GMP級(jí)重組人Human bFGF蛋白,使用大腸桿菌表達(dá),高活性、高純度、無(wú)動(dòng)物源性污染。
01
產(chǎn)品質(zhì)控指標(biāo)

02
GMP級(jí)細(xì)胞因子質(zhì)量管理體系

03
產(chǎn)品優(yōu)勢(shì)
·
無(wú)動(dòng)物源性:無(wú)動(dòng)物病毒、無(wú)致病物質(zhì)、無(wú)外源因子污染,安全性高。
·
質(zhì)量穩(wěn)定:可保證連續(xù)穩(wěn)定的批量生產(chǎn),批間差異小。
·
文件合規(guī):生產(chǎn)設(shè)備和生產(chǎn)環(huán)境符合相關(guān)法規(guī)要求,符合GMP指導(dǎo)原則。
·
藥典標(biāo)準(zhǔn)放行
04
產(chǎn)品數(shù)據(jù)
高純度
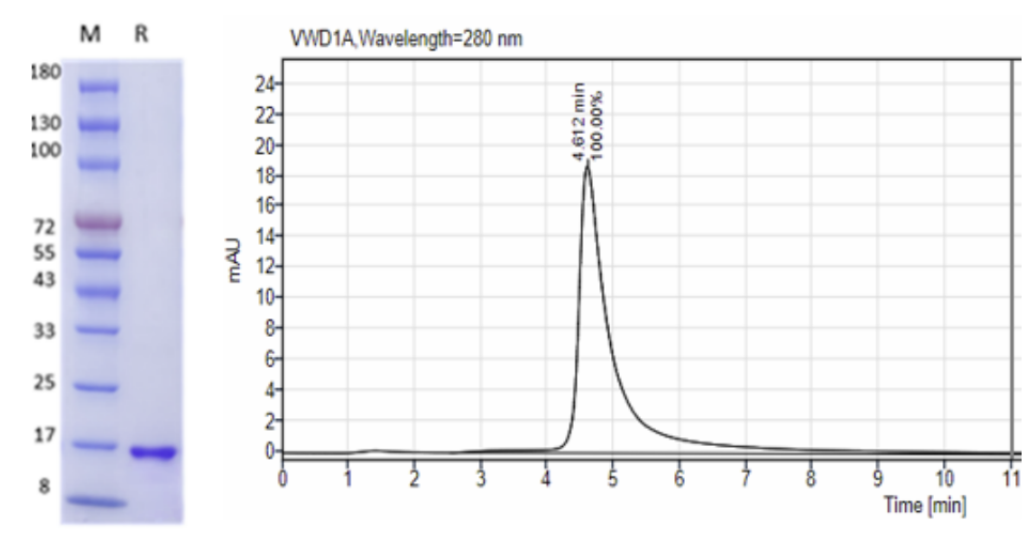
圖 3. SDS-PAGE和HPLC鑒定Human bFGF蛋白純度:純度>95%,未見雜蛋白
高生物活性
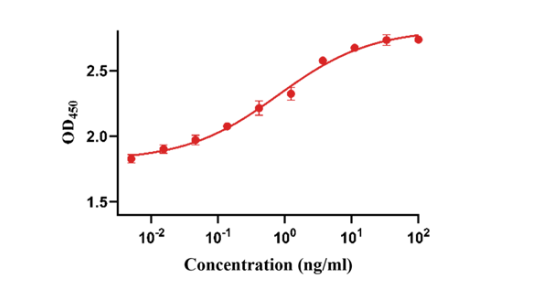
圖4.用balb/c 3T3細(xì)胞進(jìn)行細(xì)胞增殖測(cè)定,細(xì)胞活性為≥5.0×10^6 IU/mg
07
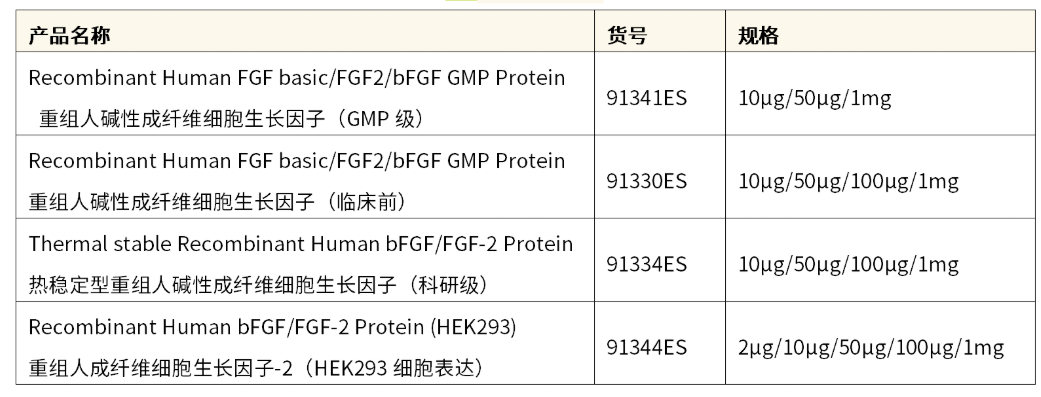
相關(guān)產(chǎn)品信息
08
參考文獻(xiàn)
[1].Yuanyang T, Yongkang Q, Zhuanggui C, et al. FGF2, an Immunomodulatory Factor in Asthma and Chronic Obstructive Pulmonary Disease (COPD).Front. Cell Dev. Biol., 02 April 2020,Volume 8 - 2020.
