
肥胖的代謝性炎癥特征就是促炎性巨噬細(xì)胞浸潤(rùn)脂肪組織。在肥胖組織中,M1巨噬細(xì)胞可能占總脂肪細(xì)胞的50%,會(huì)引起胰島素抵抗、代謝功能障礙以及全身炎癥(元炎癥)狀態(tài)。
真核生物翻譯起始因子5A(elF5A)是目前已知的唯一一種在保守賴氨酸殘基處進(jìn)行翻譯后修飾生成罕見(jiàn)氨基酸Hyp的蛋白。DHPS(deoxyhypusine synthase)催化eIF5A生成的eIF5AHyp可以控制參與炎癥的mRNA的翻譯,但DHPS及eIF5AHyp在肥胖代謝炎癥發(fā)生過(guò)程中的作用仍未闡明。
2021年9月,來(lái)自美國(guó)印第安納大學(xué)的Carmella Evans-Molina團(tuán)隊(duì)和芝加哥大學(xué)的Raghavendra G. Mirmira團(tuán)隊(duì)合作在Cell Metabolism(IF 27.3)上發(fā)表題為“Deoxyhypusine synthase promotes a pro-inflammatory macrophage phenotype”的研究文章,該研究借助蛋白質(zhì)組學(xué)和轉(zhuǎn)錄組學(xué)揭示了DHPS通過(guò)eIF5AHyp參與巨噬細(xì)胞中炎癥調(diào)控和趨化性的mRNA亞群的轉(zhuǎn)錄后調(diào)控,阻斷DHPS可減少炎癥,改善胰島素敏感性和葡萄糖穩(wěn)態(tài)。

研究材料
C57BL/6J小鼠的骨髓衍生巨噬細(xì)胞 (BMDM)
骨髓特異性Dhps敲除小鼠
RAW 264.7小鼠巨噬細(xì)胞系
斑馬魚(yú)
技術(shù)路線
步驟1:肥胖小鼠脂肪組織中DHPS和eIF5AHyp水平檢測(cè);
步驟2:研究DHPS和eIF5AHyp對(duì)促炎型巨噬細(xì)胞M1的調(diào)控作用;
步驟3:蛋白組學(xué)分析:探討DHPS對(duì)M1巨噬細(xì)胞炎癥信號(hào)的轉(zhuǎn)錄后調(diào)控;
步驟4:轉(zhuǎn)錄組學(xué)分析:揭示DHPS 對(duì)M1巨噬細(xì)胞轉(zhuǎn)錄水平的影響;
步驟5:DHPS對(duì)M1巨噬細(xì)胞在炎癥過(guò)程中浸潤(rùn)到脂肪組織中的調(diào)控作用。
研究結(jié)果
1. 肥胖小鼠脂肪組織巨噬細(xì)胞中DHPS和eIF5AHyp水平升高
為了評(píng)估DHPS和eIF5AHyp水平的變化是否與肥胖和脂肪組織炎癥相關(guān),研究人員從低脂飲食(LFD)或高脂飲食(HFD)的C57BL/6J小鼠附睪脂肪組織的基質(zhì)血管部分(SVF)中分離出免疫細(xì)胞,通過(guò)多色流式細(xì)胞術(shù)和免疫印跡分析發(fā)現(xiàn)高脂飲食會(huì)增加SVF中促炎(M1樣)巨噬細(xì)胞的占比,以及巨噬細(xì)胞中eIF5AHyp的含量。為了闡明DHPS在巨噬細(xì)胞表型中的作用,作者使用來(lái)自C57BL/6J小鼠的骨髓衍生巨噬細(xì)胞(BMDM)進(jìn)行了體外研究。結(jié)果顯示,BMDM的 M1巨噬細(xì)胞極化后,DHPS和eIF5AHyp水平增加。而DHPS的小分子抑制劑Gc7處理卻可導(dǎo)致促炎巨噬細(xì)胞的劑量依賴性降低,eIF5AHyp水平也同樣降低。
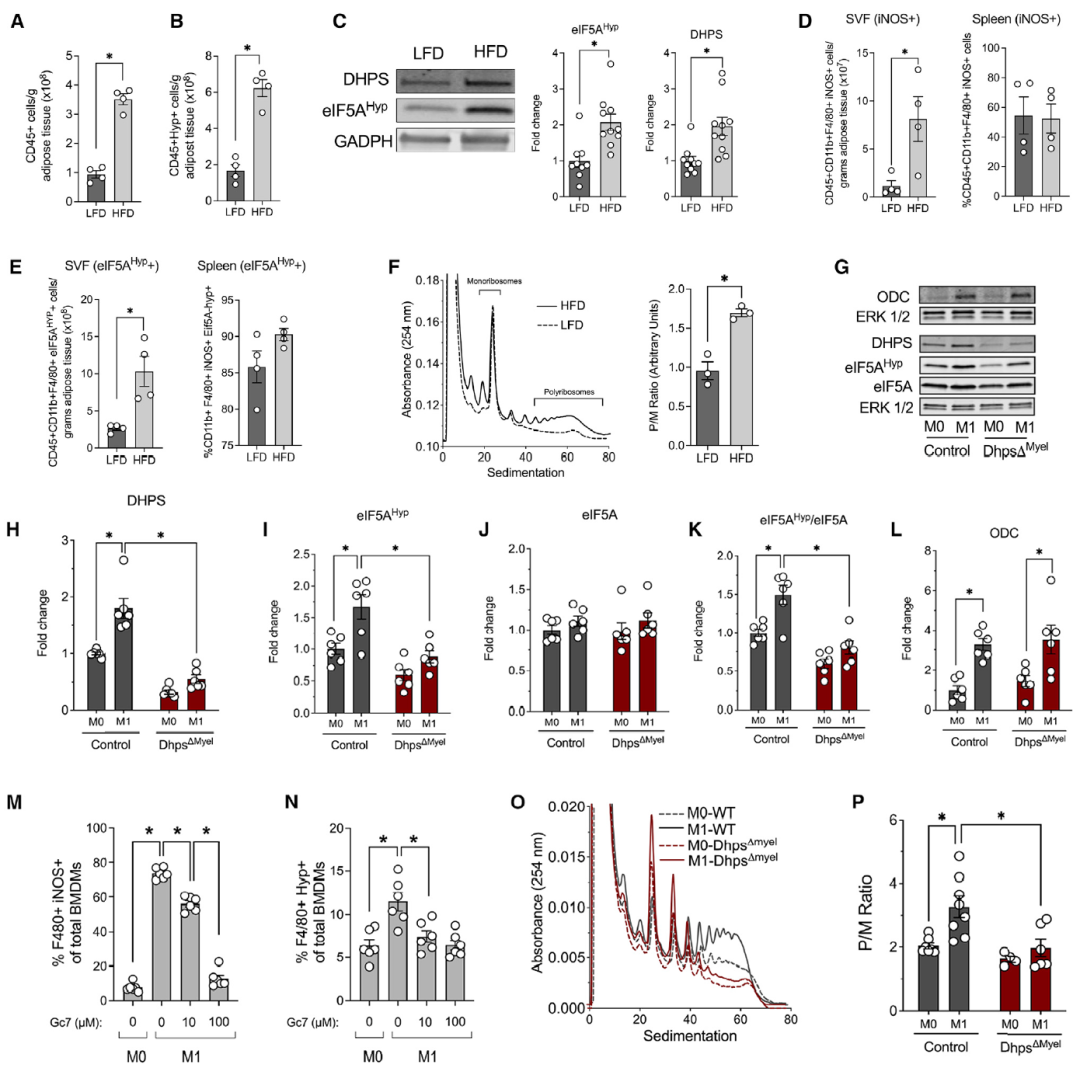
圖1 促炎性M1樣巨噬細(xì)胞表型依賴于DHPS
2. DHPS 控制巨噬細(xì)胞的mRNA翻譯和細(xì)胞遷移
在髓系特異性Dhps敲除小鼠(DhpsΔMyel) BMDM中,DHPS和eIF5AHyp水平降低。通過(guò)多聚核糖體分析,觀察到DHPS不足會(huì)導(dǎo)致與M1極化的BMDM多聚核糖體相關(guān)聯(lián)的總RNA降低,mRNA翻譯起始減少,表明DHPS不足會(huì)引發(fā)翻譯起始阻滯。作者在斑馬魚(yú)中進(jìn)行了尾鰭損傷試驗(yàn),尾鰭損傷導(dǎo)致巨噬細(xì)胞6小時(shí)內(nèi)遷移到損傷部位增加,用DHPS抑制劑處理則會(huì)導(dǎo)致遷移到損傷部位的巨噬細(xì)胞數(shù)量顯著減少。這些結(jié)果表明抑制DHPS會(huì)較少巨噬細(xì)胞遷移。
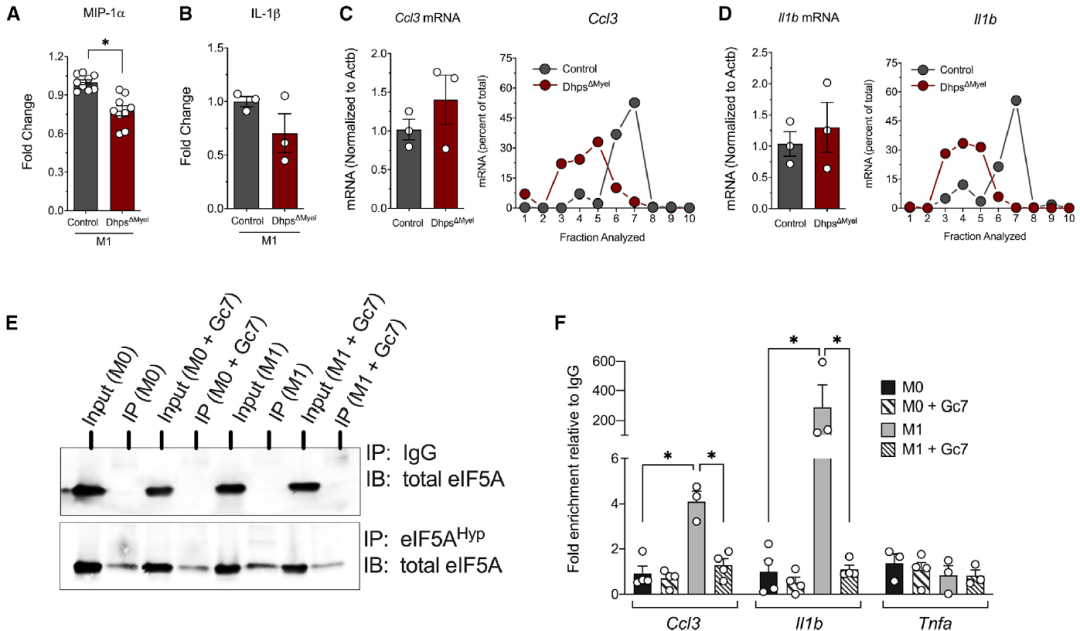
圖2 eIF5AHyp調(diào)控mRNA翻譯起始
3. DHPS促進(jìn)M1巨噬細(xì)胞炎癥信號(hào)的轉(zhuǎn)錄后調(diào)控
研究者對(duì)Control小鼠和Dhps敲除小鼠的骨髓源性巨噬細(xì)胞 (BMDM) M0、M1、M2進(jìn)行TMT蛋白質(zhì)組學(xué)分析,發(fā)現(xiàn)在DhpsΔMyel巨噬細(xì)胞中顯著變化的有111種蛋白質(zhì)。KEGG 通路分析表明,差異蛋白聚集在一氧化氮信號(hào) (cGMP-PKG)通路中、感染/炎癥通路和代謝炎癥(脂肪細(xì)胞因子信號(hào))通路,這些途徑都與DHPS促進(jìn)M1巨噬細(xì)胞極化的作用相關(guān)。
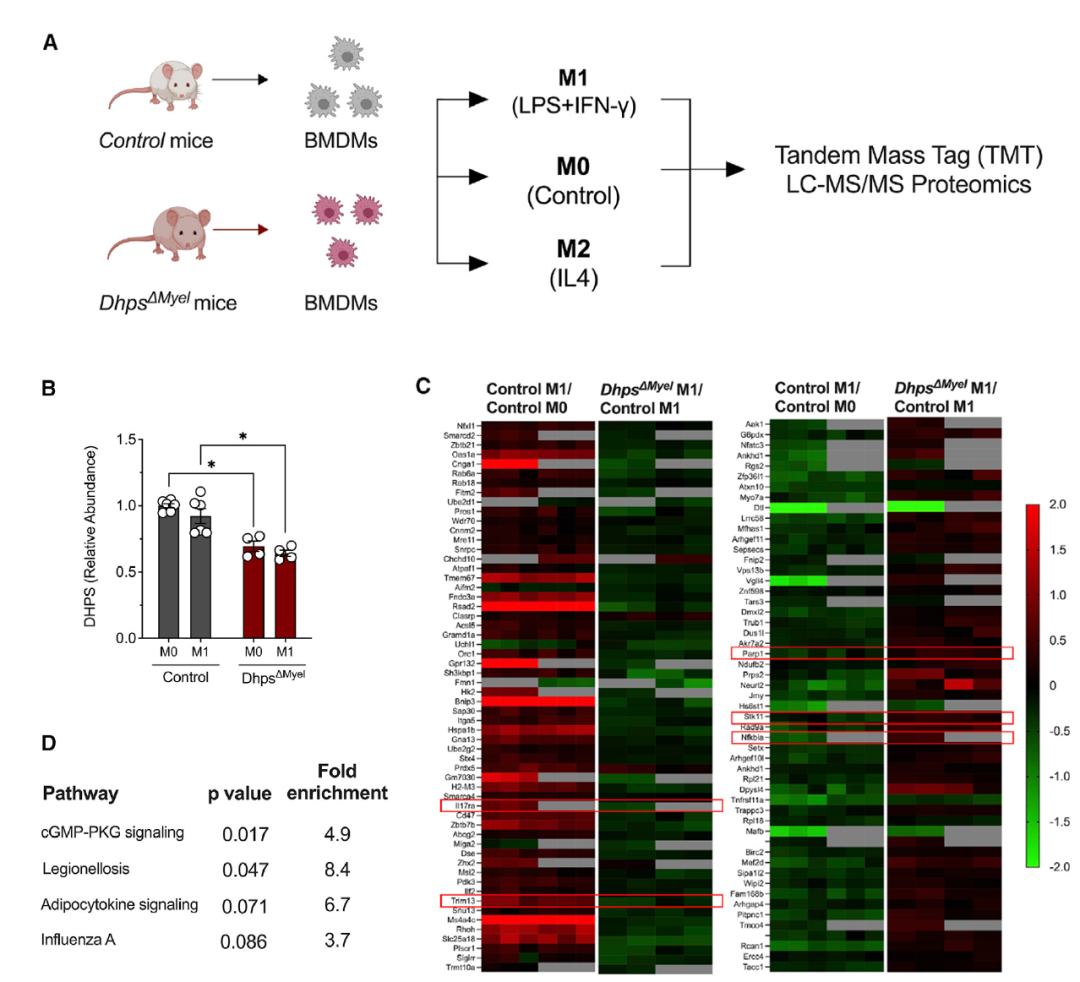
圖3 Dhps缺失的M1巨噬細(xì)胞蛋白質(zhì)組學(xué)特征
4. DHPS 影響M1巨噬細(xì)胞炎癥信號(hào)的轉(zhuǎn)錄
進(jìn)一步通過(guò)轉(zhuǎn)錄組學(xué)分析發(fā)現(xiàn),Dhps缺乏導(dǎo)致M1巨噬細(xì)胞NF-κB 靶標(biāo)基因Tlr2、Fcgr3、Il-27、Ccl2、Fcgr1、Cxcl1和Ptges的表達(dá)降低,誘導(dǎo)了與抗炎和組織修復(fù)反應(yīng)相關(guān)的基因Col1a2、Timp3和Fstl1的表達(dá)。上述結(jié)果表明,DhpsΔMyel BMDMs 在M1 極化條件下基因表達(dá)譜發(fā)生改變,傾向于下調(diào) NF-κB 靶標(biāo)和上調(diào)抗炎特征。此外,轉(zhuǎn)錄組和蛋白組學(xué)聯(lián)合分析發(fā)現(xiàn)僅有7個(gè)基因在轉(zhuǎn)錄和蛋白層面變化一致,這些數(shù)據(jù)顯示DhpsΔMyel巨噬細(xì)胞蛋白質(zhì)的改變可能發(fā)生在轉(zhuǎn)錄水平改變后。
5. DHPS 調(diào)控M1巨噬細(xì)胞浸潤(rùn)脂肪組織
為了測(cè)試DHPS在肥胖誘導(dǎo)的代謝炎癥和葡萄糖耐受不良中的作用,對(duì)DhpsΔMyel小鼠和同窩對(duì)照小鼠喂食LFD或HFD 5周。與喂食LFD的小鼠相比,喂食HFD的DhpsΔMyel小鼠脂肪組織中的巨噬細(xì)胞總數(shù)沒(méi)有差異,但M1巨噬細(xì)胞比例顯著降低,在腹腔注射葡萄糖后也表現(xiàn)更好的葡萄糖耐受性。
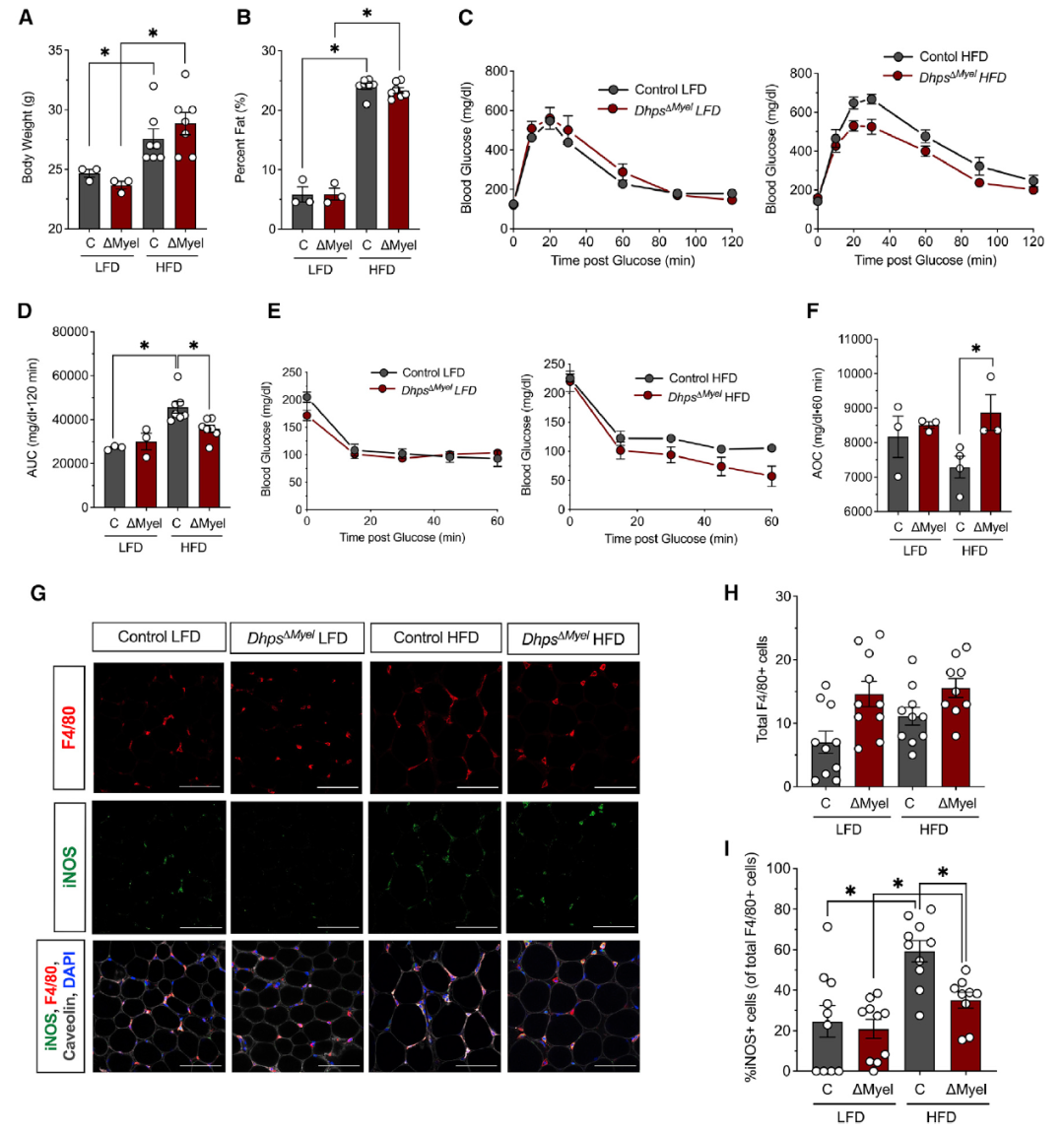
圖4 Dhps缺失會(huì)減少脂肪組織中M1巨噬細(xì)胞的積累并改善葡萄糖耐受性
小結(jié)
本研究借助蛋白質(zhì)組學(xué)和轉(zhuǎn)錄組學(xué),揭示了肥胖中DHPS通過(guò)修飾翻譯因子eIF5AHyp促進(jìn)巨噬細(xì)胞中控制炎癥的mRNA的轉(zhuǎn)錄后調(diào)節(jié),進(jìn)而通過(guò)NF-kB信號(hào)促進(jìn)促炎癥表型M1的極化,最后實(shí)現(xiàn)脂肪組織代謝性炎癥減輕、調(diào)控葡萄糖穩(wěn)態(tài)的目的。本研究加深了我們對(duì)于肥胖過(guò)程中巨噬細(xì)胞調(diào)控炎癥發(fā)生過(guò)程的理解,揭示了調(diào)控巨噬細(xì)胞活化的關(guān)鍵靶點(diǎn)——DHPS/eIF5AHyp。
中科優(yōu)品推薦
【中科新生命】建立了完整的多組學(xué)服務(wù)平臺(tái),幫助老師從基因組、轉(zhuǎn)錄組、蛋白組、修飾組、代謝組等多組學(xué)角度系統(tǒng)地解析數(shù)據(jù),挖掘關(guān)鍵生物學(xué)信息。歡迎感興趣的老師前來(lái)咨詢。


