編者按
創(chuàng)傷性腦損傷(TBI)是神經(jīng)退行性疾病的主要環(huán)境風(fēng)險(xiǎn)因素,每年估計(jì)發(fā)生超過(guò)6000萬(wàn)例。最近的研究表明TBI與神經(jīng)毒性蛋白tau、TDP-43和β淀粉樣蛋白的病理性積聚有關(guān),導(dǎo)致慢性創(chuàng)傷性腦病(CTE)、肌萎縮側(cè)索硬化(ALS)、阿爾茨海默病和其他癡呆癥等進(jìn)行性神經(jīng)退行性疾病。一次中度至重度的TBI會(huì)使患老年癡呆的風(fēng)險(xiǎn)增加4倍。
今天我們來(lái)分享一篇2024年4月4日由南加州大學(xué)凱克醫(yī)學(xué)院Justin K. Ichida團(tuán)隊(duì)發(fā)表在Cell Stem Cell雜志(IF=23.9)上的一項(xiàng)最新研究——《KCNJ2 inhibition mitigates mechanical injury in a human brain organoid model of traumatic brain injury》,該研究開(kāi)發(fā)了一種高強(qiáng)度超聲平臺(tái)來(lái)實(shí)施機(jī)械損傷,并利用腦類器官,揭示了神經(jīng)元亞型在損傷易感性上的關(guān)鍵差異,并建立了一個(gè)監(jiān)測(cè)不同人類遺傳背景下?lián)p傷反應(yīng)的方法。抑制KCNJ2可能有助于減輕腦損傷后早期神經(jīng)元死亡。
文章題目
KCNJ2 inhibition mitigates mechanical injury in a human brain organoid model of traumatic brain injury
雜志:《Cell Stem Cell》(IF=23.9)
發(fā)表時(shí)間:2024年4月4日
作者:Justin K. Ichida團(tuán)隊(duì)
單位:南加州大學(xué)凱克醫(yī)學(xué)院
01、皮層類器官損傷與TBI相關(guān)的標(biāo)志物
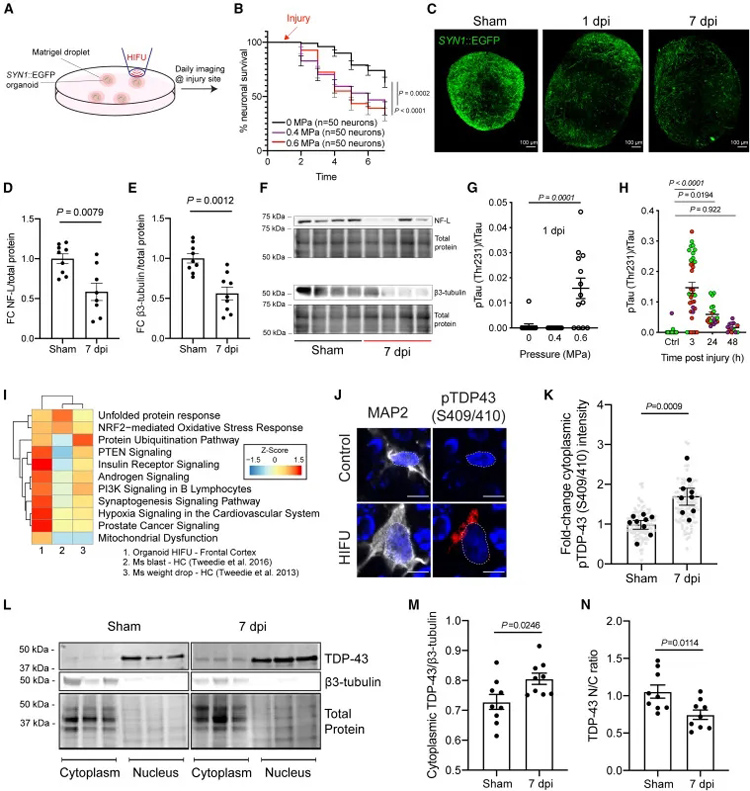
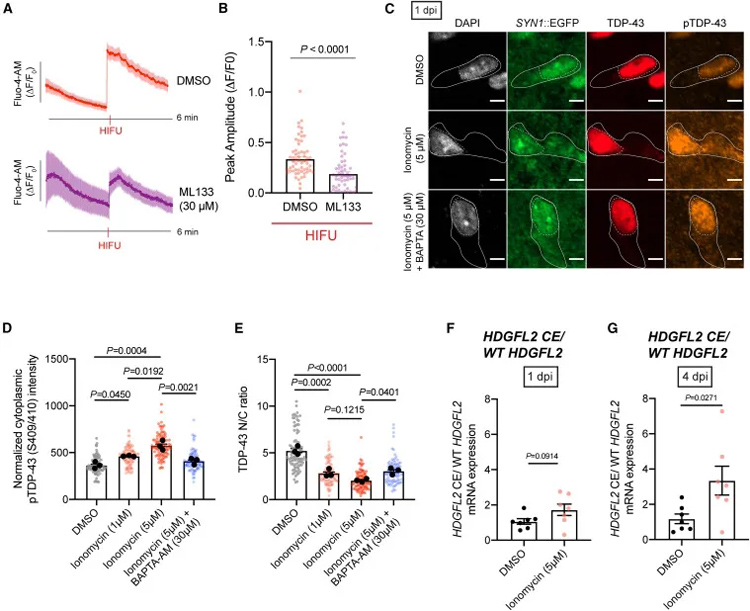
研究團(tuán)隊(duì)首先使用高強(qiáng)度聚焦超聲波(HIFU)技術(shù)對(duì)誘導(dǎo)多能干細(xì)胞(iPSC)來(lái)源的腦類器官進(jìn)行機(jī)械損傷,通過(guò)慢病毒轉(zhuǎn)染(SYN1::eGFP)標(biāo)記興奮性神經(jīng)元,成功模擬了TBI的關(guān)鍵病理特征,包括神經(jīng)元死亡、tau蛋白磷酸化和TDP-43核輸出。
在對(duì)TBI的生物標(biāo)志物進(jìn)行檢測(cè)后,研究人員發(fā)現(xiàn)在受傷的皮層類器官中,磷酸化tau蛋白水平增加、神經(jīng)元死亡,神經(jīng)元的胞質(zhì)中顯著聚集磷酸化的TDP-43。RNA測(cè)序結(jié)果和活細(xì)胞成像也驗(yàn)證了,類器官出現(xiàn)與TBI一致的變化特征。
這些結(jié)果表明,通過(guò)HIFU損傷皮層皮層類器官,可以模擬TBI相關(guān)的生物標(biāo)志物和疾病機(jī)制。
02、深層神經(jīng)元損傷后表現(xiàn)出增強(qiáng)的TDP-43功能障礙
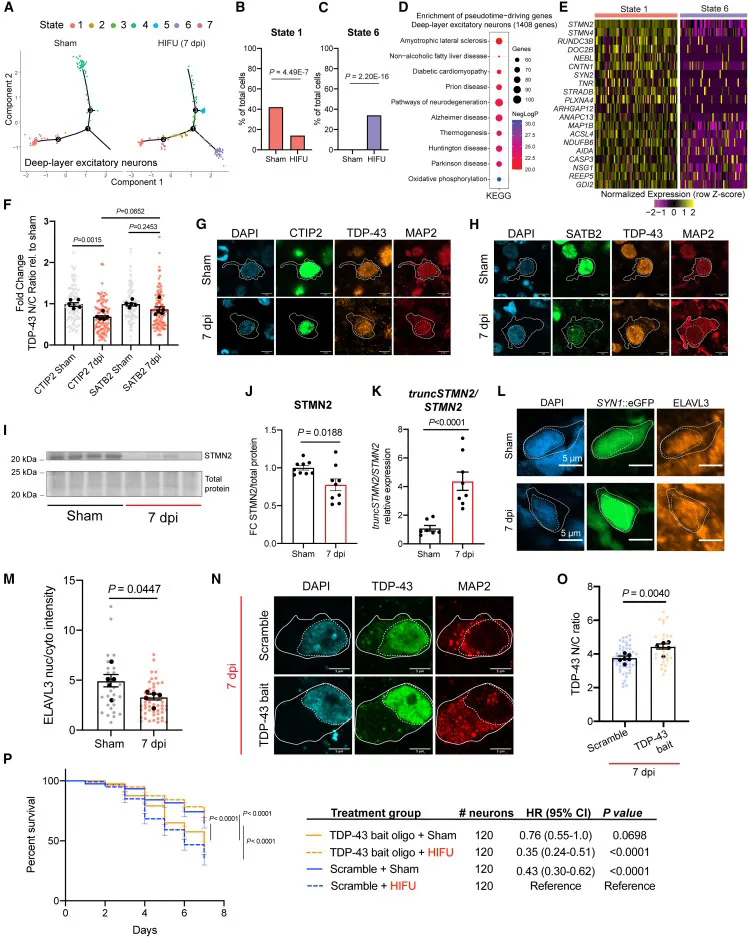
隨后,研究人員對(duì)2,530個(gè)類器官細(xì)胞進(jìn)行單細(xì)胞RNA測(cè)序發(fā)現(xiàn),未接受損傷和深層損傷的神經(jīng)元間差異表達(dá)的基因富集多種神經(jīng)退行性疾病,最顯著的是肌萎縮性側(cè)索硬化癥。
利用人類iPSC腦類器官模型研究表明,在深層神經(jīng)元中發(fā)生的TDP-43功能障礙,是神經(jīng)元死亡的主要驅(qū)動(dòng)因素,并且在肌萎縮側(cè)索硬化癥(ALS)和額顳葉癡呆(FTD)神經(jīng)元中更為明顯。TDP-43功能喪失,導(dǎo)致深層興奮性神經(jīng)元中許多潛在的TDP-43靶基因表達(dá)下調(diào),這可能是機(jī)械損傷后TDP-43功能喪失的標(biāo)志。
進(jìn)一步分析發(fā)現(xiàn),受損的深層興奮性神經(jīng)元中,許多TDP-43靶向的基因出現(xiàn)明顯下調(diào),提示機(jī)械損傷破壞了TDP-43的功能,隨后的免疫染色、mRNA以及蛋白結(jié)果驗(yàn)證了這一點(diǎn)。在沒(méi)有損傷的情況下,用誘餌寡核苷酸治療誘導(dǎo)神經(jīng)元死亡。該誘餌基于 TDP-43 的充分表征的高親和力核酸序列。在沒(méi)有損傷且細(xì)胞質(zhì)TDP-43 升高的情況下,高濃度的這些寡核苷酸可能會(huì)進(jìn)入細(xì)胞核,在那里它們可能會(huì)競(jìng)爭(zhēng)性取代TDP-43偏離其正常目標(biāo),通過(guò)新生轉(zhuǎn)錄的剪接失調(diào)導(dǎo)致靶向毒性。
結(jié)果顯示,這一操作顯著提升了損傷后神經(jīng)元TDP-43的核質(zhì)比。這說(shuō)明TDP-43功能障礙在損傷誘導(dǎo)的神經(jīng)元死亡中起著重要作用,且其傾向于影響深層神經(jīng)元。
03、抑制KCNJ2可減輕HIFU誘導(dǎo)的神經(jīng)元死亡
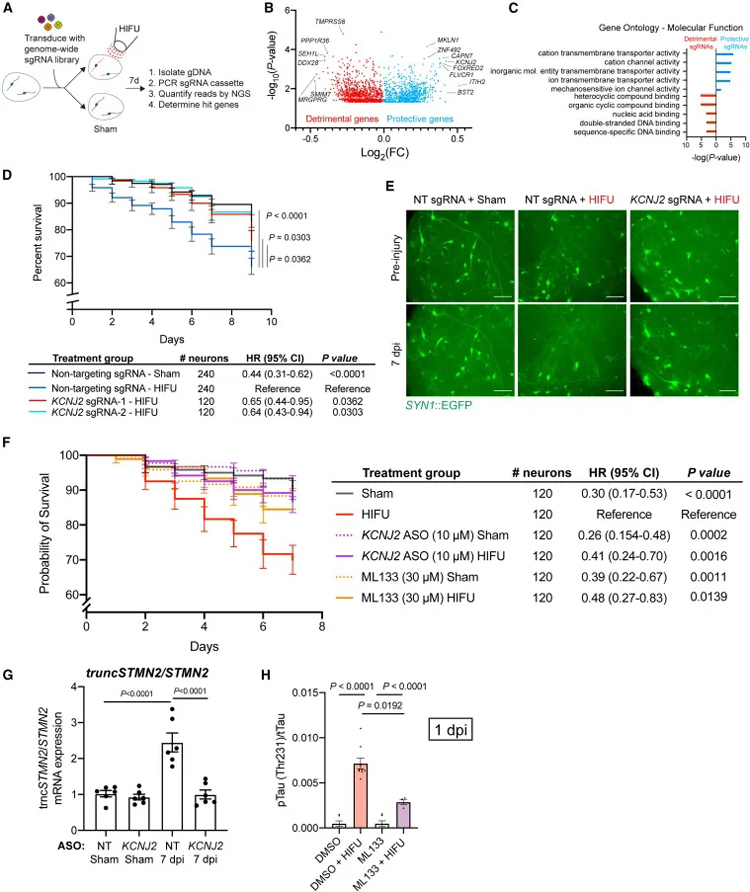
利用全基因組CRISPR干擾篩選,作者鑒定了最佳的靶點(diǎn)KCNJ2。KCNJ2的遺傳敲除和小分子抑制均顯示出維持受損皮層類器官中神經(jīng)元存活的效果。研究表明,抑制KCNJ2可以減輕HIFU引起的神經(jīng)元死亡,降低p-Tau與總Tau比率。
KCNJ2通過(guò)調(diào)節(jié)Ca2+通量導(dǎo)致TDP-43功能障礙,而KCNJ2的抑制可以減輕這些過(guò)程,顯示了其在神經(jīng)保護(hù)中的潛在作用。
對(duì)其作為治療的潛力至關(guān)重要的是,損傷后 1 小時(shí)對(duì)KCNJ2的小分子抑制足以改善神經(jīng)元存活。這與當(dāng)前藥物干預(yù)措施的治療窗一致,例如巴比妥類藥物,通常在人類TBI后 1-2 小時(shí)內(nèi)給藥。KCNJ2抑制也可被視為對(duì)TBI急性風(fēng)險(xiǎn)較高的個(gè)體的預(yù)防性治療。
此外,通過(guò)在小鼠模型中進(jìn)行控制皮層撞擊(CCI)實(shí)驗(yàn),研究人員驗(yàn)證了KCNJ2抑制對(duì)TBI的保護(hù)作用。
研究發(fā)現(xiàn),在小鼠腦損傷模型中,使用Kcnj2 反義寡核苷酸治療可顯著減少神經(jīng)元TDP-43核質(zhì)比和細(xì)胞質(zhì)TDP-43在損傷部位的聚集。Kcnj2 反義寡核苷酸治療還降低了細(xì)胞死亡和星形膠質(zhì)增多,減少了細(xì)胞質(zhì)中的磷化TDP-43水平。
Kcnj2 反義寡核苷酸還減少了損傷部位附近的細(xì)胞死亡和星形膠質(zhì)增多。研究顯示,Kcnj2抑制顯著減少了腦損傷后的TDP-43損傷和退行性反應(yīng)。
這不僅揭示了TBI后大腦病理學(xué)的分子機(jī)制,而且還為開(kāi)發(fā)新的治療策略提供了潛在的靶點(diǎn)——KCNJ2,這對(duì)于未來(lái)治療TBI及其相關(guān)神經(jīng)退行性疾病具有重要意義。通過(guò)深入了解TBI如何與神經(jīng)退行性疾病相互關(guān)聯(lián),這項(xiàng)工作為未來(lái)的神經(jīng)保護(hù)和修復(fù)策略提供了重要的科學(xué)基礎(chǔ)。
04、編者點(diǎn)評(píng)
總體而言,這篇文章介紹了一個(gè)用于發(fā)現(xiàn)和驗(yàn)證機(jī)械損傷修飾劑的人體類器官平臺(tái)。該損傷模型旨在彌合傳統(tǒng)體外系統(tǒng)和復(fù)雜高等生物之間的差距,提供可擴(kuò)展且遺傳靈活的系統(tǒng),以確定TBI急性和慢性影響的潛在疾病機(jī)制和治療方法。
研究人員發(fā)現(xiàn) TDP-43 功能障礙是機(jī)械損傷后神經(jīng)元死亡的關(guān)鍵驅(qū)動(dòng)因素,并確定了深層興奮性神經(jīng)元對(duì) TDP-43 功能障礙的內(nèi)在脆弱性。最后,在已建立的TBI小鼠模型以及攜帶導(dǎo)致ALS/FTD的突變的健康和患病類器官中,KCNJ2抑制可有效減輕損傷誘發(fā)的疾病過(guò)程,部分是通過(guò)損傷后胞質(zhì) Ca2+ 的神經(jīng)保護(hù)性減少。
作為健康美麗產(chǎn)業(yè)CRO服務(wù)開(kāi)拓者與引領(lǐng)者、斑馬魚生物技術(shù)的全球領(lǐng)導(dǎo)者,環(huán)特生物搭建了“斑馬魚、類器官、哺乳動(dòng)物、人體”四位一體的綜合技術(shù)服務(wù)體系,開(kāi)展健康美麗CRO服務(wù)、科研服務(wù)、智慧實(shí)驗(yàn)室搭建三大業(yè)務(wù)。目前,環(huán)特已建立200多種斑馬魚模型及腦類器官、心臟類器官及各種腫瘤類器官培養(yǎng)平臺(tái),歡迎有需要的讀者垂詢!
參考文獻(xiàn)
SKCNJ2 inhibition mitigates mechanical injury in a human brain organoid model of traumatic brain injury: Cell Stem Cell
