膽汁酸(BAs)除了促進(jìn)脂類消化吸收外,還可作為信號分子調(diào)控代謝和免疫等多種生理功能。細(xì)胞表面的Takeda G蛋白偶聯(lián)受體5(TGR5,又稱GPBAR1)是BAs的主要受體,它們在腸道、腎臟、肝臟以及中樞神經(jīng)系統(tǒng)等部位均有表達(dá)。近些年有報道顯示,大腦中存在BAs,并與循環(huán)BAs水平高度相關(guān),可通過被動擴(kuò)散到達(dá)中樞神經(jīng)系統(tǒng)(CNS),但人們對BAs在CNS中的生理作用卻知之甚少。來自瑞士洛桑理工學(xué)院的Kristina Schoonjans團(tuán)隊(duì)發(fā)現(xiàn),小鼠生理進(jìn)食后BAs到達(dá)下丘腦,使下丘腦BAs濃度短時上調(diào),特異性激活A(yù)gRP/NPY神經(jīng)元膜受體TGR5的表達(dá),進(jìn)而調(diào)控小鼠食欲,揭示了BA-TGR5信號在中樞神經(jīng)系統(tǒng)中介導(dǎo)的生理反饋?zhàn)饔谩_@一發(fā)現(xiàn)給肥胖治療提供了新思路。相關(guān)成果發(fā)表在《Nature Metabolism》。
中樞神經(jīng)系統(tǒng)BA-TGR5信號可調(diào)控小鼠進(jìn)食行為
作者首先發(fā)現(xiàn)野生型小鼠生理進(jìn)食后,BAs進(jìn)入到下丘腦,幾種內(nèi)源性BAs(主要是牛磺酸結(jié)合型)濃度短時升高。給小鼠口服混合BAs后,小鼠全天食物攝入量減少,表明CNS中由飲食介導(dǎo)的BAs增加可能通過激活BA受體在禁食-進(jìn)食過渡期間觸發(fā)飽腹感。利用RNAscope腦表達(dá)譜發(fā)現(xiàn)內(nèi)源Gpbar1 mRNA在控制食欲的下丘腦弓狀核(ARC)區(qū)高表達(dá)。給小鼠灌胃TGR5特異性半合成BA INT-777,發(fā)現(xiàn)INT-777與內(nèi)源BA一樣在下丘腦迅速積累。并可在10-100 mg /kg劑量范圍內(nèi)減少食物攝入,在最高劑量下,INT-777 到達(dá)下丘腦的濃度與餐后內(nèi)源性BA 的濃度相當(dāng),概括了BA介導(dǎo)的攝食行為反饋調(diào)節(jié)所需的中樞生理濃度。在參與攝食調(diào)節(jié)的不同神經(jīng)元群體中,促食欲AgRP/NPY神經(jīng)元和抑食欲POMC神經(jīng)元位于ARC中,靠近有孔的血腦屏障,可促進(jìn)與血液的交換。ARC內(nèi)神經(jīng)肽表達(dá)顯示,小鼠口服或靜脈注射TGR5激動劑1 h后,Agrp和Npy mRNA水平降低,而Pomc水平不受影響。
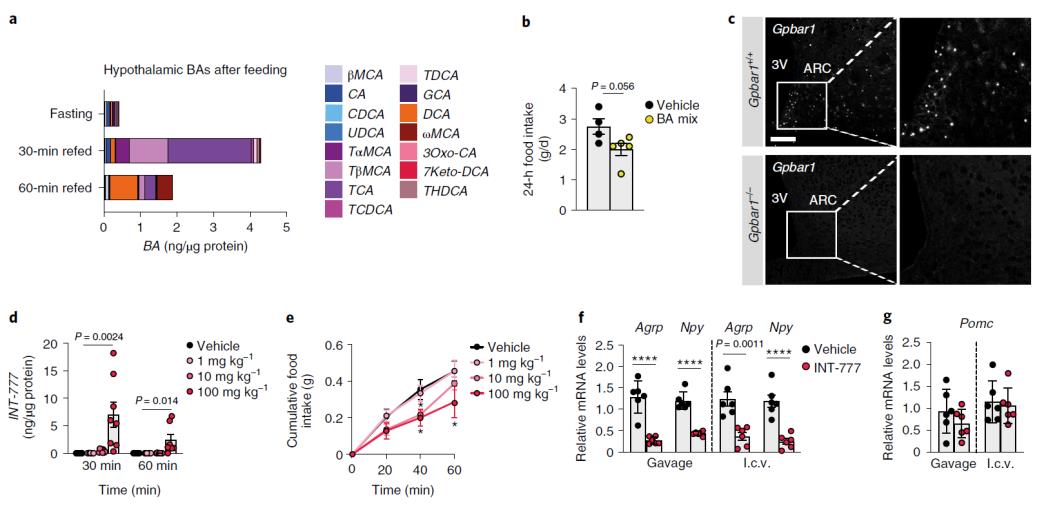
圖1 生理喂養(yǎng)過程中BAs到達(dá)下丘腦,并通過TGR5抑制進(jìn)食
分析野生型(Gpbar1+/+)和TGR5完全敲除型(Gpbar1?/?)小鼠的表型發(fā)現(xiàn),Gpbar1?/?小鼠總進(jìn)食量顯著增加、夜間進(jìn)食量顯著增加,并且不能抑制Agrp和Npy –促食欲神經(jīng)肽的表達(dá),而抑食欲神經(jīng)肽Pomc的表達(dá)不受影響,表明在喂食狀態(tài)下TGR5可能通過抑制AgRP/NPY而不是刺激POMC神經(jīng)元來協(xié)調(diào)飽腹感。進(jìn)一步分析TGR5在大腦不同細(xì)胞類型中的分布,免疫熒光分析顯示,TGR5存在于下丘腦神經(jīng)元以及其他腦細(xì)胞中,包括神經(jīng)膠質(zhì)細(xì)胞和星形膠質(zhì)細(xì)胞。用神經(jīng)元特異性TGR5敲除小鼠重復(fù)該實(shí)驗(yàn)發(fā)現(xiàn),小鼠的總進(jìn)食量和促食欲神經(jīng)肽分泌量也顯著增加。
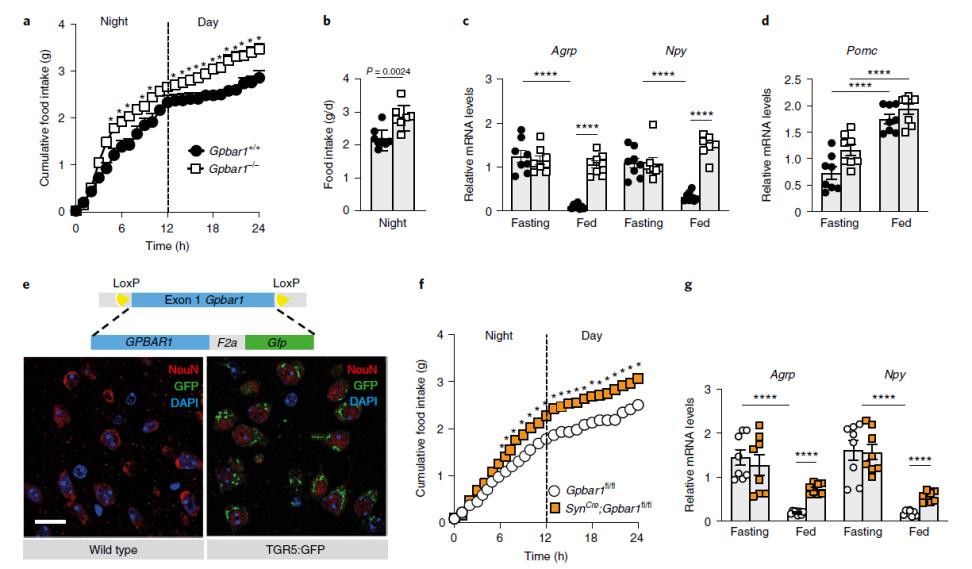
圖2 神經(jīng)元中TGR5的表達(dá),其缺失會促進(jìn)食物攝入
TGR5通過抑制下丘腦AgRP/NPY神經(jīng)元來抑制食物攝入
為了進(jìn)一步證實(shí)上述結(jié)論,作者分別構(gòu)建了AgRP和POMC神經(jīng)元特異性敲除Gpbar1的小鼠模型,和野生型小鼠相比,AgRP突變小鼠在夜間進(jìn)食量顯著增加,而POMC突變小鼠的進(jìn)食量無變化。此外,口服INT-777后,POMC突變小鼠和野生型小鼠產(chǎn)生厭食反應(yīng),而這種效應(yīng)在AgRP突變小鼠中顯著減弱,表明TGR5通過AgRP/NPY神經(jīng)元,而不是POMC神經(jīng)元來控制食物攝入。在 TGR5:GFP 小鼠中使用 Agrp RNAscope 探針和 GFP 免疫熒光共染色實(shí)驗(yàn),結(jié)果顯示,TGR5在AgRP /NPY神經(jīng)元中表達(dá)。免疫熒光實(shí)驗(yàn)表明,禁食動物中 INT-777 介導(dǎo)的 TGR5 激活顯著降低了Fos陽性AgRP/NPY神經(jīng)元的百分比。這些結(jié)果表明BA-TGR5信號通過抑制下丘腦AgRP/NPY神經(jīng)元中神經(jīng)肽的表達(dá)來抑制進(jìn)食行為。
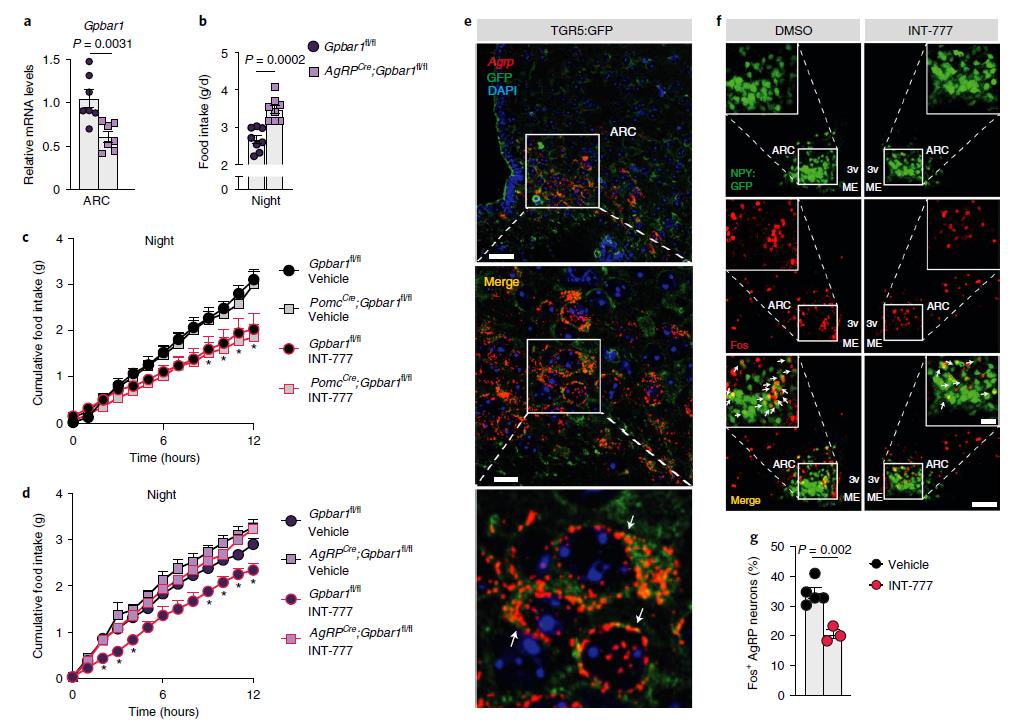
圖3 AgRP/NPY中的TGR5選擇性缺失可消除BA衍生物誘導(dǎo)的飽腹感
機(jī)制探究:TGR5能瞬時性地阻斷AgRP/ NPY神經(jīng)元神經(jīng)肽的釋放
由于TGR5能介導(dǎo)快速神經(jīng)元的反應(yīng),作者推斷TGR5除了抑制促食欲基因表達(dá),還可能參與阻斷神經(jīng)肽的分泌。下丘腦外植體離體實(shí)驗(yàn)表明,禁食后,用INT-777激活TGR5可迅速抑制Gpbar1+/+的AgRP/NPY神經(jīng)元中AgRP和NPY的釋放,但在Gpbar1-/-中無該效應(yīng)。這些結(jié)果表明進(jìn)食后BA-TGR5信號的生理厭食作用是通過選擇性減少AgRP/NPY分泌來實(shí)現(xiàn)的。
進(jìn)一步探究其分子機(jī)制,作者用AgRP/ NPY陽性且表達(dá)TGR5的小鼠胚胎下丘腦細(xì)胞系mHypoE-N41 (N41)進(jìn)行了一系列實(shí)驗(yàn),與體內(nèi)和離體研究結(jié)果一致, INT-777處理能快速降低N41細(xì)胞中Agrp和Npy的表達(dá),并短時阻斷了Agrp的釋放。
已有證據(jù)表明,在致密核心囊泡(DCVs)動員的早期階段,皮質(zhì)肌動蛋白絲是分泌囊泡和質(zhì)膜之間的主要物理屏障,肌動蛋白網(wǎng)絡(luò)重塑可限制不同類型細(xì)胞(包括神經(jīng)元)的肽分泌。肌動蛋白的解聚合和穩(wěn)定性可通過Rho–ROCK信號通路來調(diào)節(jié)。那么,TGR5是否通過Rho–ROCK–肌動蛋白軸瞬時調(diào)節(jié)神經(jīng)肽的分泌?通過評估INT-777 處理后的 AgRP 和 NPY 分泌以及同時使用thiazovivin 抑制ROCK。ROCK的抑制消除了TGR5對AgRP和NPY分泌抑制。此外,用INT-777或BA混合物短期刺激TGR5可調(diào)節(jié)細(xì)胞骨架,有利于肌動蛋白纖維的穩(wěn)定和聚合。與以上研究結(jié)果一致,用INT-777或BA混合物急性激活TGR5后,N41細(xì)胞內(nèi)NPY小泡的積累增加、釋放明顯減少;機(jī)制上,BA-TGR5信號可以促進(jìn)ROCK下游蛋白MLC和COFILIN的瞬時磷酸化進(jìn)而促進(jìn)肌動蛋白的穩(wěn)定和聚合。這些結(jié)果表明BA-TGR5信號可以降低AgRP/NPY mRNA的豐度,并暫時阻斷AgRP/ NPY神經(jīng)元中神經(jīng)肽的釋放,進(jìn)而抑制進(jìn)食行為。
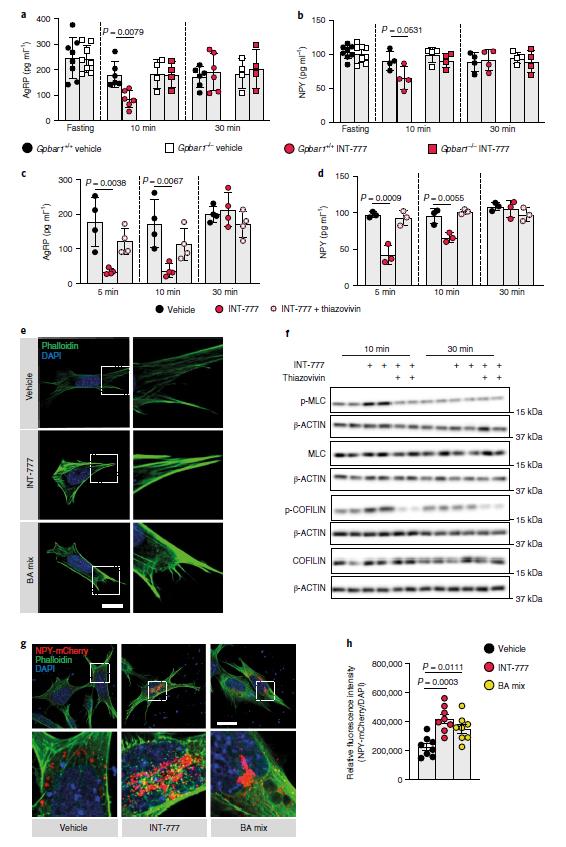
圖4 TGR5通過Rho–ROCK信號通路的短暫激活調(diào)控促食欲神經(jīng)肽的釋放
小結(jié)
BAs作為多功能信號分子,調(diào)節(jié)肝腸和外周代謝器官之間的交流,近些年研究表明BAs在全身代謝和免疫調(diào)節(jié)方面具有重要作用。本研究發(fā)現(xiàn)BA-TGR5信號軸不僅在疾病中起重要作用,而且在進(jìn)食行為的生理控制中也起著重要作用。BAs在下丘腦中通過結(jié)合AgRP/NPY神經(jīng)元上的TGR5受體抑制AgRP/NPY mRNA表達(dá)和神經(jīng)肽釋放,從而抑制進(jìn)食行為,揭示了BAs在神經(jīng)調(diào)節(jié)方面的新功能。
繪譜幫你測
腸腦軸研究中一般關(guān)注較多的代謝物有神經(jīng)遞質(zhì)、短鏈脂肪酸、激素等,而本研究發(fā)現(xiàn)膽汁酸及其受體在腸腦軸調(diào)控食欲方面具有重要作用。針對膽汁酸代謝,麥特繪譜可絕對定量檢測65種膽汁酸,此外,我們可提供代謝組學(xué)一站式整體解決方案,獨(dú)家的檢測技術(shù)、全面的數(shù)據(jù)報告以及專業(yè)的售后探討,助力您的科研探索之路不斷創(chuàng)新和突破。歡迎聯(lián)系獲取詳細(xì)資料!
參考文獻(xiàn)
Alessia Perino, et al. Central anorexigenic actions of bile acids are mediated by TGR5. Nature Metabolism, VOL 3 , MAY 2021 ,595–603.
原文閱讀,請長按識別下方二維碼

精彩推薦
2. 膽汁酸或?qū)⒊蔀榘柎暮D⌒碌纳飿?biāo)志物
3. 膽汁酸-腸道菌之間對話出錯推動消化道腫瘤的發(fā)生
4. Protein&Cell | 膽汁酸替代合成途徑與代謝性疾病
5. Cell Metabolism | 腸道菌群相關(guān)代謝物--膽汁酸生物學(xué)功能
6. Nature Medicine│膽汁酸-腸道菌群調(diào)控多囊卵巢綜合征的新機(jī)制
7. Cell Host & Microbe | 石膽酸通過重塑腸肝軸改善減肥手術(shù)后糖尿病
8. 引領(lǐng)行業(yè) | 聚焦麥特繪譜代謝組學(xué)整體解決方案

