長(zhǎng)久以來(lái),腫瘤被認(rèn)為是孤立的腫塊,獨(dú)立存在于器官特定的部位。在過(guò)去的數(shù)十年中,通過(guò)使用靶向治療和聯(lián)合用藥方案,腫瘤治療領(lǐng)域取得了長(zhǎng)足的進(jìn)步。但這些治療方案中的絕大多數(shù)患者最終都無(wú)法完全治愈,甚至有些患者在用藥初期療效顯著,最終卻復(fù)發(fā)為耐藥腫瘤。這是由于腫瘤組織還包括多種類型的基質(zhì)細(xì)胞(成纖維細(xì)胞、淋巴細(xì)胞、巨噬細(xì)胞和內(nèi)皮細(xì)胞)、免疫細(xì)胞(T和B淋巴細(xì)胞等)和細(xì)胞外成分(細(xì)胞因子、生長(zhǎng)因子、激素、細(xì)胞外基質(zhì)ECM等),它們圍繞著腫瘤細(xì)胞,并由血管系統(tǒng)滋養(yǎng),構(gòu)成了腫瘤微環(huán)境(tumor microenvironment, TME)【1】。腫瘤微環(huán)境 (TME)為腫瘤提供良好的生長(zhǎng)環(huán)境及營(yíng)養(yǎng)物質(zhì),促進(jìn)腫瘤的進(jìn)展和轉(zhuǎn)移,這些特征導(dǎo)致了個(gè)體患者中許多常規(guī)治療的失敗。?腫瘤類器官是一種可以在體外模擬病人腫瘤微組織的模型,其樣本來(lái)源是原代腫瘤組織。類器官結(jié)構(gòu)包含多種特異性細(xì)胞類型,空間結(jié)構(gòu)與其對(duì)應(yīng)腫瘤組織相似。目前已有多種類型腫瘤建立了類器官培養(yǎng)方案,如:胃癌、肝癌、胰腺癌、結(jié)腸癌、卵巢癌等類器官培養(yǎng)方案已日趨成熟。隨著生理學(xué)上建模方式的精確和完善,類器官培養(yǎng)技術(shù)可以與體外腫瘤微環(huán)境(TME)技術(shù)相結(jié)合,并維持其多樣化的細(xì)胞群體。?
?
用于模擬腫瘤免疫微環(huán)境的類器官培養(yǎng)系統(tǒng)
?
?模擬腫瘤免疫微環(huán)境的腫瘤類器官培養(yǎng)可以通過(guò)三種途徑實(shí)現(xiàn):
?
I?將腫瘤組織經(jīng)過(guò)物理或酶解分離后,在細(xì)胞外基質(zhì)(Matrigel或BME)中進(jìn)行類器官培養(yǎng);同時(shí)分離外源性免疫細(xì)胞(通常來(lái)源于自體外周血或腫瘤組織),隨后與生長(zhǎng)的類器官進(jìn)行共培養(yǎng)。這種將類器官完全浸沒(méi)的培養(yǎng)方式適用于富集上皮類型腫瘤細(xì)胞,但不能保留間質(zhì)細(xì)胞,因此需要外源性添加免疫細(xì)胞來(lái)構(gòu)建腫瘤微環(huán)境【2】;
?
II?將腫瘤消化后形成的球狀組織與膠原蛋白混合,并接種到微流體培養(yǎng)裝置中,即腫瘤細(xì)胞與樣本中的固有免疫微環(huán)境共同培養(yǎng),形成天然TME模型。這種裝置的中心部分是用來(lái)培養(yǎng)腫瘤微球體的3D凝膠,培養(yǎng)基由兩側(cè)的孔隙進(jìn)行流通,可以實(shí)時(shí)地、持續(xù)地調(diào)節(jié)腫瘤類器官所處的液體環(huán)境,并且也可以模擬在體內(nèi)依靠血液自然流動(dòng)的藥物遞送方式【3】;
?
III?將含有免疫細(xì)胞的腫瘤組織物理切割成組織碎片,在包被膠原蛋白凝膠的transwell小室中進(jìn)行培養(yǎng)。凝膠的頂部暴露在空氣中,同時(shí)外皿中的培養(yǎng)基通過(guò)可滲透的transwell擴(kuò)散到內(nèi)皿中,形成氣-液交互界面(air–liquid interface, ALI)。與普通的凝膠培養(yǎng)方式不同,ALI法不僅保留了原始腫瘤的基本特征,還保留了TME復(fù)雜的細(xì)胞組成和結(jié)構(gòu)【4】。目前黑色素瘤、腎細(xì)胞癌(RCC)、非小細(xì)胞肺癌(NSCLC)都已經(jīng)實(shí)現(xiàn)ALI法構(gòu)建腫瘤類器官-TME。
?
?
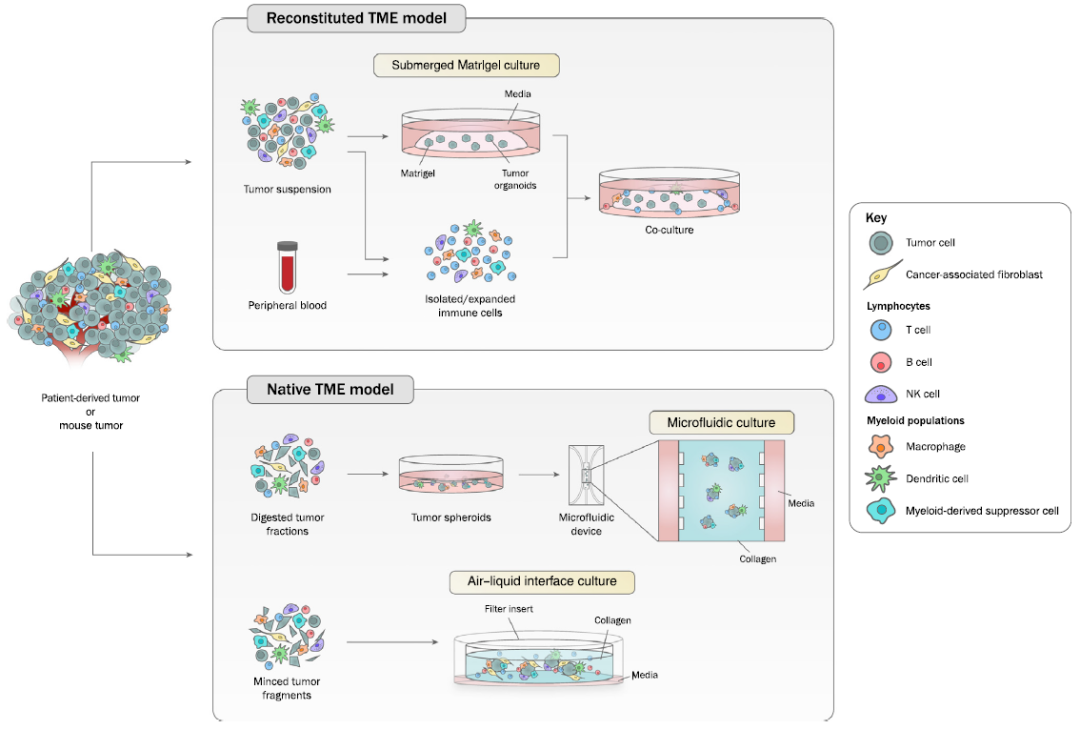
圖1. 用于模擬腫瘤免疫微環(huán)境的類器官培養(yǎng)系統(tǒng)【5】?
?
?
類器官作為一種研究模型,在發(fā)育生物學(xué)、疾病病理學(xué)、細(xì)胞生物學(xué)、再生機(jī)制、精準(zhǔn)醫(yī)療以及藥物毒性和藥效試驗(yàn)等方面均顯示出巨大的應(yīng)用潛力。為了更好地挖掘類器官技術(shù)的應(yīng)用價(jià)值,近岸蛋白特邀類器官研究領(lǐng)域的研究專家和行業(yè)大咖共同探討類器官技術(shù)在疾病研究以及轉(zhuǎn)化醫(yī)學(xué)中的應(yīng)用。報(bào)名通道已開(kāi)啟,歡迎報(bào)名參加,獲取更多關(guān)于類器官研究的前沿動(dòng)態(tài)。
?
時(shí)間
?
2022年6月16日,19:00-21:00
?
?
直播日程
?
?

?
?
腫瘤類器官-TME在研究中的應(yīng)用
?
1、用于評(píng)估免疫檢查點(diǎn)抑制劑的效果
?
通過(guò)對(duì)腫瘤患者的臨床研究表明,免疫檢查點(diǎn)受體信號(hào)抑制劑(immune checkpoint inhibitors,ICI)對(duì)于治療腫瘤有一定的協(xié)同作用。通過(guò)對(duì)其安全性和有效性的綜合考量,目前有七種單克隆抗體包括一種阻斷細(xì)胞毒性T淋巴細(xì)胞相關(guān)抗原4 (CTLA-4),六種阻斷程序性細(xì)胞死亡蛋白1 (PD-1)或其配體(PD-L1)已被FDA批準(zhǔn)用于治療包括黑色素瘤、皮膚鱗狀細(xì)胞癌、頭頸癌在內(nèi)的多種晚期癌癥,許多其他抗體也在臨床測(cè)試中【6】。?
2、擴(kuò)大免疫療法的治療范圍
?
迄今為止,研究人員寄希望于多種免疫療法,但絕大部分效果被其內(nèi)源性或獲得性耐藥機(jī)制抵消了;此外,一些腫瘤組織似乎對(duì)ICI不敏感。腫瘤類器官-TME作為一種潛在的免疫研究模型,可以用于優(yōu)化現(xiàn)有免疫療法的療效,并且對(duì)新方法進(jìn)行功能評(píng)估。?臨床免疫治療越來(lái)越多地探索聯(lián)合用藥方法,即利用多個(gè)免疫檢查點(diǎn)(如PD-1、CTLA-4、LAG-3、TIM-3、VISTA)的抑制劑與免疫抑制細(xì)胞群(如Treg、MDSC)的獨(dú)特生物學(xué)特性進(jìn)行聯(lián)合治療,免疫檢查點(diǎn)和TME內(nèi)局部作用的旁分泌途徑(如TGFβ)或趨化因子受體(如CCR4和CXCR4)共同阻斷的研究正在進(jìn)行中。免疫治療組合的其他潛在靶點(diǎn)(包括JAK-STAT、MAPK、Wnt/β-catenin、NF-κB信號(hào)通路等)都可以使用腫瘤類器官-TME模型來(lái)進(jìn)行效果驗(yàn)證。?
3、精準(zhǔn)醫(yī)學(xué)與免疫治療效果預(yù)測(cè)
?
與TME相結(jié)合的患者來(lái)源腫瘤類器官(patient-derived organoid, PDO)可以通過(guò)記錄不同治療方法(包括化療和免疫療法,以及小分子或蛋白質(zhì)治療)的抗腫瘤效果,實(shí)現(xiàn)在體外預(yù)測(cè)病人治療后的反應(yīng)。在保留腫瘤細(xì)胞和自體免疫成分的微流控培養(yǎng)PDO-T體系中,通過(guò)監(jiān)測(cè)T細(xì)胞對(duì)腫瘤的細(xì)胞毒性,有助于預(yù)測(cè)或評(píng)估患者對(duì)ICI治療的反應(yīng)【7】;或者通過(guò)流式細(xì)胞術(shù)、免疫熒光染色的檢測(cè)方式,由ALI-PDO中多種內(nèi)源性免疫元件來(lái)模擬體內(nèi)腫瘤對(duì)ICI的反應(yīng)【8】。這些預(yù)測(cè)方法都需要具有前期大量相關(guān)的臨床結(jié)果支持,但通過(guò)我們對(duì)免疫療法效果的篩選,為臨床轉(zhuǎn)化治療提供了方向。?盡管已經(jīng)建立了許多類型的腫瘤類器官-TME體系,但仍然需要為罕見(jiàn)的腫瘤建立模型以擴(kuò)大其適用性。體外腫瘤類器官-TME的培養(yǎng)通常需要添加不同于生理?xiàng)l件的細(xì)胞因子,如:腎癌類器官培養(yǎng)體系中需要添加R-spondin 1、EGF、FGF-10;而乳腺癌類器官則需要額外添加Neuregulin 1、FGF-7、Noggin。這些添加在培養(yǎng)基中的生長(zhǎng)因子水平異常,可能會(huì)導(dǎo)致類器官中不準(zhǔn)確的生長(zhǎng)曲線和異常的藥物反應(yīng)【9】。
?近岸蛋白自主研發(fā)生產(chǎn)的低內(nèi)毒素Activin A、FGF系列、HGF、R-Spondin 1、Noggin和Wnt3a等細(xì)胞因子,內(nèi)毒素低至<10EU/mg,具有高活性、高純度、高批間一致性,為類器官培養(yǎng)設(shè)計(jì),已獲得市場(chǎng)認(rèn)可,讓您研究放心!??
?
推薦產(chǎn)品
?
??
參考文獻(xiàn)
?
【1】MAO, Xiaoqi, et al. Crosstalk between cancer-associated fibroblasts and immune cells in the tumor microenvironment: new findings and future perspectives. Molecular cancer, 2021, 20.1: 1-30.
?
【2】SATO, Toshiro, et al. Single Lgr5 stem cells build crypt-villus structures in vitro without a mesenchymal niche.?Nature, 2009, 459.7244: 262-265
?
【3】AREF, Amir R., et al. 3D microfluidic ex vivo culture of organotypic tumor spheroids to model immune checkpoint blockade.?Lab on a Chip, 2018, 18.20: 3129-3143.
?
【4】NEAL, James T., et al. Organoid modeling of the tumor immune microenvironment. Cell, 2018, 175.7: 1972-1988. e16.
?
【5】YUKI, Kanako, et al. Organoid models of tumor immunology.?Trends in immunology, 2020, 41.8: 652-664.
?
【6】VADDEPALLY, Raju K., et al. Review of indications of FDA-approved immune checkpoint inhibitors per NCCN guidelines with the level of evidence.?Cancers, 2020, 12.3: 738.
?
【7】JENKINS, Russell W., et al. Ex vivo profiling of PD-1 blockade using organotypic tumor spheroids.?Cancer discovery, 2018, 8.2: 196-215.
?
【8】KONG, Joseph Cherng Huei, et al. Tumor-infiltrating lymphocyte function predicts response to neoadjuvant chemoradiotherapy in locally advanced rectal cancer.?JCO Precision oncology, 2018, 2: 1-15.
?
【9】LUO, Zhimin, et al. Reconstructing the tumor architecture into organoids.?Advanced Drug Delivery Reviews, 2021, 176: 113839.
?
蘇州近岸蛋白質(zhì)科技股份有限公司,是一家專注于重組蛋白應(yīng)用解決方案的高新技術(shù)企業(yè),主營(yíng)業(yè)務(wù)為靶點(diǎn)及細(xì)胞因子類蛋白、重組抗體、酶及試劑的研發(fā)、生產(chǎn)和銷售,并提供相關(guān)技術(shù)服務(wù)。公司定位為醫(yī)療健康與生命科學(xué)領(lǐng)域原料與技術(shù)解決方案的上游供應(yīng)商,致力于為下游客戶提供及時(shí)、穩(wěn)定、優(yōu)質(zhì)的產(chǎn)品及服務(wù),助力全球生物醫(yī)藥企業(yè)和研究機(jī)構(gòu)的技術(shù)與產(chǎn)品創(chuàng)新升級(jí)。
詳詢www.novoprotein.com.cn或致電400-600-0940。
?
?
?
?
