本期將帶您深入基因編輯正史的核心:一把源自細(xì)菌與病毒30億年攻防戰(zhàn)的"分子剪刀"——CRISPR/Cas9技術(shù),它正以納米級精度重寫生命密碼。這場顛覆生物醫(yī)學(xué)領(lǐng)域的革命,其開端竟隱藏在一次被忽視的實驗室意外中!
從“垃圾序列”到基因魔剪的蛻變
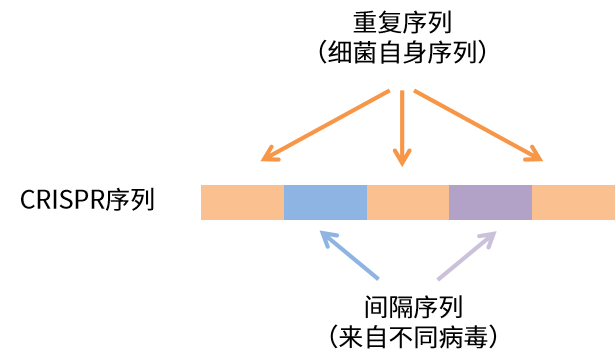
1987年,日本科學(xué)家石野良純在解析大腸桿菌基因組中某些酶功能時,意外地在某個片段中發(fā)現(xiàn)了一些神秘的重復(fù)序列(即后來的CRISPR序列),但他并未深究這些看似無規(guī)律但又極具規(guī)律的片段,僅留下“值得深入探討”幾個字,因此這些奇特的序列在隨后的十八年里一直沉睡于科學(xué)文獻(xiàn)中。

神秘的重復(fù)序列(來自 Ishino, Y , et al. 1987)
此后,西班牙和荷蘭等各地科學(xué)家也陸續(xù)在細(xì)菌和古細(xì)菌中發(fā)現(xiàn)新的重復(fù)序列,并發(fā)現(xiàn)這些重復(fù)序列和間隔序列的排列方式、重復(fù)序列重復(fù)出現(xiàn)的次數(shù)都可以表現(xiàn)出很大差異。因此Ruud Jansen在2002年將具有以上特征的DNA片段命名為CRISPR(Clustered Regularly Interspaced Short Palindromic Repeats,成簇規(guī)律性間隔短回文重復(fù)序列),但依舊無法解釋它的作用。
直到2005年,西班牙微生物學(xué)家Francisco Mojica發(fā)表的文章才揭開了這些序列的真實身份:他證實CRISPR間隔序列匹配噬菌體DNA,提出其作為細(xì)菌“免疫記憶庫”的假說。細(xì)菌通過將病毒DNA片段嵌入自身基因組,形成“分子通緝令”,當(dāng)相同病毒再次來襲時,便能精準(zhǔn)識別并摧毀入侵者。這一發(fā)現(xiàn)開啟了基因編輯的新紀(jì)元!
2011年,Emmanuelle Charpentier團(tuán)隊發(fā)現(xiàn)CRISPR/Cas9系統(tǒng)的核心組分:crRNA(由CRISPR轉(zhuǎn)錄而來)與tracrRNA(反式激活crRNA)結(jié)合,指導(dǎo)Cas9蛋白切割目標(biāo)DNA。
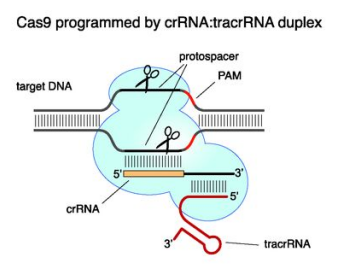
CRISPR/Cas9系統(tǒng)(來自Emmanuelle Charpentier,2012)
2012年,Jennifer Doudna與Emmanuelle Charpentier在《Science》發(fā)表載入基因編輯史冊的里程碑研究:她們將復(fù)雜的CRISPR系統(tǒng)簡化為Cas9蛋白+sgRNA 的二元組合,開發(fā)了第三代基因編輯工具——CRISPR/Cas9技術(shù)。只需修改sgRNA的20個堿基序列,就能引導(dǎo)Cas9精準(zhǔn)切割任意DNA靶點。更因此獲得了2020年的諾貝爾化學(xué)獎!

(來自諾貝爾獎官網(wǎng))
次年,張鋒發(fā)表了利用CRISPR技術(shù)實現(xiàn)哺乳動物細(xì)胞基因編輯的文章,標(biāo)志著CRISPR技術(shù)從理論到實踐的一大飛躍。后續(xù)科學(xué)家們的不斷深入探索研究,CRISPR技術(shù)逐漸完善,正朝著基因編輯的時代邁進(jìn)。
細(xì)菌免疫系統(tǒng)如何變身基因魔剪?
CRISPR系統(tǒng)的本質(zhì)是RNA引導(dǎo)的DNA切割引擎,其納米級精準(zhǔn)性源于三大核心組件的精密協(xié)作:
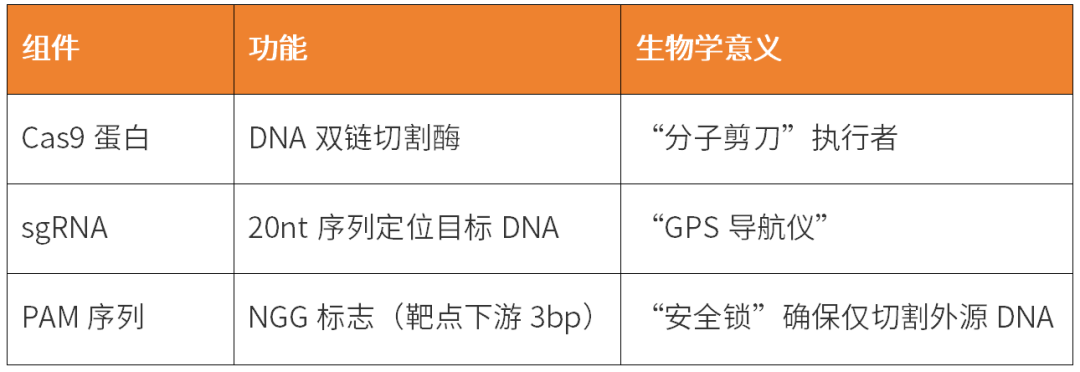
當(dāng)這些組件協(xié)同工作時,將啟動四步精密機制:
1.組裝:Cas9與sgRNA結(jié)合形成核糖核蛋白復(fù)合體(RNP);
2.掃描:sgRNA通過堿基互補配對在基因組中搜尋目標(biāo);
3.解鎖:Cas9識別PAM序列(NGG)后解旋DNA雙鏈;
4.切割:Cas9蛋白的HNH結(jié)構(gòu)域切斷互補鏈,RuvC結(jié)構(gòu)域切斷非互補鏈。獲得斷裂的雙鏈DNA(DSB)。
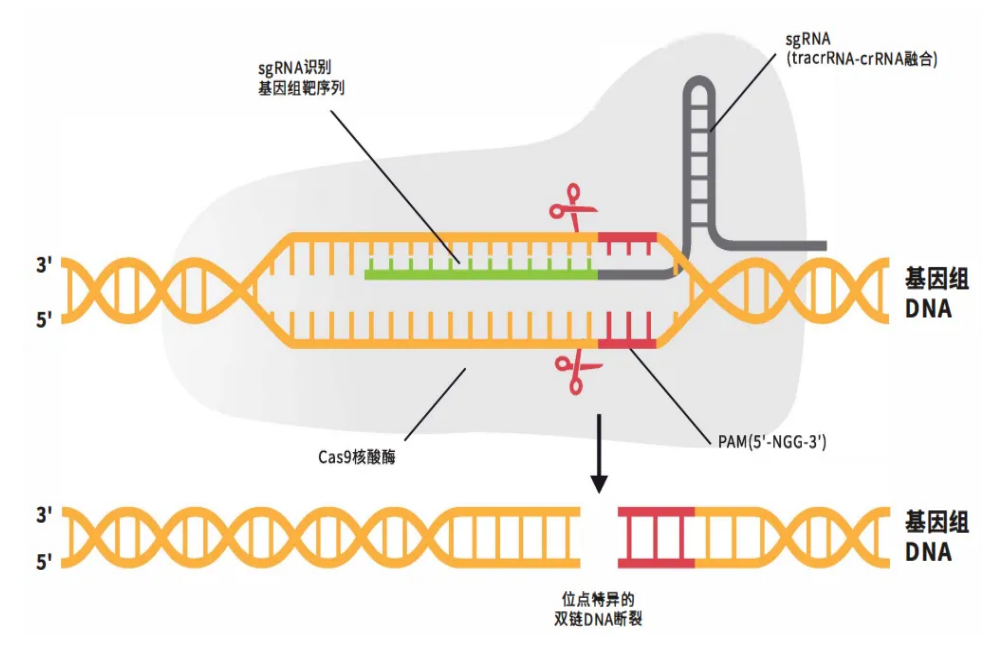
CRISPR/Cas9技術(shù)原理
切割后的DNA修復(fù)路徑如下:
路徑1:非同源末端連接(NHEJ),生物體內(nèi)自發(fā)的SOS修復(fù),修復(fù)期間會導(dǎo)致片段的插入或缺失。
路徑2:同源定向修復(fù)(HDR),引入高度同源的DNA修復(fù)模板時會啟動,實現(xiàn)片段的定向插入。
第三代技術(shù)相比于ZFNs和TALENs前兩代技術(shù)更有優(yōu)勢,實驗設(shè)計難度降低、操作流程簡便、脫靶率低,細(xì)胞毒性低(如使用純蛋白RNP體系進(jìn)行基因編輯)。但依舊有脫靶風(fēng)險,當(dāng)sgRNA與非目標(biāo)序列部分匹配時,Cas9可能誤切關(guān)鍵基因(如癌癥相關(guān)基因)。不過基因編輯研發(fā)并未止步,2023年,CRISPR基因編輯藥物Casgevy上市,據(jù)2025年5月數(shù)據(jù)顯示90%以上的鐮狀細(xì)胞病患者實現(xiàn)“功能性治愈”;2024年,中國科學(xué)家更發(fā)現(xiàn)VII型CRISPR系統(tǒng)(Cas14),首次實現(xiàn)僅靶向RNA而不改變DNA序列的精準(zhǔn)編輯,為基因治療開辟更安全的路徑。相信在未來CRISPR技術(shù)將更加精進(jìn),運用于個性化的精準(zhǔn)醫(yī)療,造福人類。
隨著CRISPR技術(shù)從實驗室走向產(chǎn)業(yè)化,標(biāo)準(zhǔn)化工具鏈的完善成為推動臨床與農(nóng)業(yè)應(yīng)用的關(guān)鍵。針對基因編輯全流程的痛點——從Cas蛋白、sgRNA設(shè)計、Cas蛋白遞送到脫靶驗證,近岸蛋白已開發(fā)出覆蓋全鏈條的解決方案:
01 純蛋白編輯工具:Cas9(Cat.No.:E365)蛋白及其突變體,同時包含GMP級別的Cas9蛋白(Cat.No.:GMP-1701)、0脫靶的AaCas12bMax、enCas12Ultra等蛋白;
02 通用型一步法sgRNA制備:sgRNA體外轉(zhuǎn)錄試劑盒(Cat.No.:E399)在20μl體系下sgRNA產(chǎn)量可達(dá)10-30μg;
03 高效RNP遞送系統(tǒng):首先在體外將sgRNA和Cas9蛋白混合成為sgRNA和Cas9的復(fù)合效應(yīng)物,然后通過瞬時轉(zhuǎn)染技術(shù)(脂質(zhì)體或電轉(zhuǎn)等)將復(fù)合效應(yīng)物遞送到細(xì)胞內(nèi),進(jìn)而實現(xiàn)對靶基因的編輯(相關(guān)實驗操作可后臺咨詢近岸蛋白公眾號);
04 脫靶驗證:T7核酸內(nèi)切酶I有效檢測基因編輯之后形成的突變體,識別切割效率高。
三代基因編輯技術(shù)性能比對

以上便是基因編輯技術(shù)從ZFNs、TALENs到CRISPR/Cas9三代技術(shù)的進(jìn)化史詩。而CRISPR革命的核心引擎——Cas蛋白家族,實則暗藏更精妙的分子江湖:下期我們將帶您深入CRISPR武器庫,解析不同Cas蛋白的PAM偏好、切割特性與應(yīng)用場景,助您精準(zhǔn)匹配研究需求。
作為深耕基因編輯領(lǐng)域的專業(yè)解決方案提供者,近岸蛋白將持續(xù)推出技術(shù)解析、實操指南與定制化工具,陪伴每一位科研工作者探索生命密碼的無限可能。敬請期待,下期再會!
相關(guān)產(chǎn)品推薦
CRISPR/Cas9相關(guān)產(chǎn)品
| 產(chǎn)品類型 | 優(yōu)勢 | 目錄號 | 產(chǎn)品名稱 |
| RNA體外轉(zhuǎn)錄 | 通用型體外轉(zhuǎn)錄sgRNA | E399 | Universal sgRNA In Vitro one-step Transcription Kit |
| 一步法體外轉(zhuǎn)錄sgRNA | E369 | sgRNA In Vitro one-step Transcription Kit | |
| T7 RNA聚合酶轉(zhuǎn)錄 | E131 | T7 High Yield RNA Transcription kit | |
| SpCas9 | 通用型及突變體型 | GMP-1701 | Recombinant Cas9 Nuclease, GMP Grade |
| E365 | NLS-Cas9 Nuclease | ||
| E376 | NLS-Cas9 (D10A) Nickase | ||
| E377 | NLS-Cas9 (H840A) Nickase | ||
| E378 | NLS-Cas9 (D10A, H840A) Nuclease | ||
| E379 | NLS-Cas9-EGFP Nuclease | ||
| MR019 | Cas9 mRNA (N1-Me-Pseudo UTP) | ||
| MR107 | Cas9 mRNA | ||
|
AaCas12bMax |
零脫靶 | GMP-E375 | AaCas12bMax Enhanced, GMP Grade |
| E375 | AaCas12bMax Enhanced | ||
| MR205 | AaCas12bMax Enhanced mRNA (N1-Me-Pseudo UTP) | ||
| GR002 | AaCas12bMax Human TRAC sgRNA | ||
| GR003 | AaCas12bMax Human CIITA sgRNA | ||
| enCas12Ultra | 高編輯效率 | GMP-E393 | enCas12Ultra, GMP Grade |
| E393 | enCas12Ultra | ||
| MR208 | enCas12Ultra mRNA (N1-Me-Pseudo UTP) | ||
| piggyBac轉(zhuǎn)座子mRNA | 適用于動物和人細(xì)胞的轉(zhuǎn)座 | MR005 | piggyBac mRNA |
| 基因編輯效率檢測 | 80倍高保真性 | E035 | 2×Fast Pfu Master Mix |
| T7核酸內(nèi)切酶I | M017 | T7 Endonuclease I | |
| DNA/RNA純化 | DNA純化磁珠 | N240 | NovoNGS® DNA Clean Beads |
| RNA純化磁珠 | N243 | RNA Clean Beads | |
| 病毒純化 | GMP級 | GMP-1707 | BenzoNuclease®, GMP Grade |
| GMP-1709 | BenzoNuclease® (Tag-free), GMP Grade | ||
| GMP-1711 | High Salt Active BenzoNuclease® (HSAB), GMP Grade |
